问题导向下发展学科核心素养的教学设计*
——以“氮气及氮的氧化物”为例
2024-01-12吴相华
许 艳 吴相华
(云南师范大学化学化工学院 云南 昆明 650500)
《普通高中化学课程标准(2017年版2020年修订》(以下简称“新课标”)颁布实施,新课标要求普通高中学生在学习完普通高中化学课程以后具备五个化学学科核心素养。在科学教育领域中教师扮演着重要的角色。教师不仅是科学知识的传播者,还是科学精神的传播者、科学思想的倡导者和科学方法的实践者。为实现化学课程目标,教师在教学设计中要注重培养学生的科学素养和科学精神,使学生具备未来发展需要的正确价值观、必备品格和关键能力。本文以“氮气及其氧化物”为例,以问题为导向,提出具有启发性和探究性的问题,教学通过解决这些问题,达到学生知识构建和能力培养的目的。
一、普通高中化学课程目标与核心素养
课程目标是指课程在实施之后达到的预期结果。化学课程目标和核心素养如下表所示。

表1 普通高中化学课程目标与核心素养[1]
二、问题导向下发展化学学科核心素养的教学模式
问题导向是由英文Problem-Based Learning 翻译来的,字面意思就是基于问题的学习。问题导向下发展化学学科核心素养的教学模式是指教师在课堂教学中,基于化学学科的核心素养,通过提问、设问、导问等方式,激发学生学习的欲望,引导学生开展思考、讨论、探究等活动,引导学生解决问题。化学教学中坚持问题导向,对培养学生的化学发散性思维非常有利。
本节课通过“氮在自然界中是如何循环的?”“N2、NO、NO2三者是如何转化的?”“如何减少酸雨的形成?”三个核心问题来组织该节的知识点。在学生课前预习的基础上,通过核心问题的引导,使学科的基本概念变得清晰、深刻和富有逻辑性。问题可以促使学生积极地思考,教师以知识为载体,通过连续的“问题链”[2],在情境中形成对这个知识点的深刻理解。在教学过程中还需要注意帮助学生建立结构决定性质等化学观念和元素及其化合物的认知模型。
三、问题导向下发展化学学科核心素养的教学设计
1.教材分析
“氮气及氮的氧化物”位于人教版高中化学必修第二册第五章第二节氮及其化合物,内容包括氮气与氮的固定、一氧化氮和二氧化氮。在教材这一节的序言中介绍了氮元素在元素周期表中的位置、氮原子的结构以及氮元素在自然界的存在形式,以“自然界是怎样通过氮的循环为生物体提供氮元素的呢?”为核心问题展开。关于氮气与氮的固定,教材首先介绍了氮原子之间形成的氮氮三键性质稳定,不易与其他物质发生反应,但在高温、放电等条件下能与一些金属或非金属发生反应。其次以正文的形式介绍了人工固氮和自然固氮两种方式。随后以图片展示了自然界中氮的循环,图片展示了大气中的氮通过自然固氮和人工固氮的途径形成各种含氮物质,这些含氮物质又通过细菌分解转化成大气中的氮。然后以科学史话的栏目形式介绍了合成氨的历史,让学生了解到合成氨的发展历史以及体会化学的发展对社会的进步与发展的作用。在课本上以正文的形式介绍了一氧化氮与二氧化氮的物理性质以及它们跟水的反应,然后以探究实验展示了二氧化氮溶于水的实验,通过实验说明一氧化氮与二氧化氮的物理化学性质。
2.课标分析
2017年版普通高中化学课程标准明确规定,利用真实情境通过学生身边的事物,提出问题让学生带着问题去探究,在探究中学习,以培养学生的科学精神和创新精神。本节课在教学内容上以氮气的组成和结构为切入点,引导学生学习氮气的主要性质。宏观性质是化学教学的重难点,宏观性质的学习必须基于微观结构的认识。因此,在教学中可以通过对分子微观结构的探究,为学生提供宏观性质认识的基础,进而培养学生宏观辨识与微观探析的学科素养。氮气的性质主要取决于氮分子的微观结构,从这个角度来培养学生“结构决定性质,性质决定用途”的观念,培养证据推理与模型认知的学科素养。通过“氮的循环”引导学生了解和认识氮的固定与循环过程,从元素守恒的角度认识氮循环中的变化与平衡,培养变化观念与平衡思想的学科素养。在氮的循环中能从物质类别、元素价态等维度,利用离子反应和氧化还原反应原理,预测、探究氮及其氧化物的主要化学性质[3],通过探究实验形成实验探究氮的氧化物主要性质的基本思路,培养学生科学探究与创新意识的学科素养。最后能够认识到氮的氧化物的危害,用所学的相关知识参与到社会性议题的讨论中[4],采取能力范围内的有效防治措施,养成保护环境的可持续发展意识,培养科学态度与社会责任的学科素养。分析氮及其化合物的内容要求可知,主题2 和主题5 中都与氮气及氮的化合物相关,新课标不仅关注化学知识的学习,也关注学生素养能力的培养。
3.学情分析
(1)前在状态
在之前的学习中已经学过了其他的元素及其化合物。又学习过氧化还原反应,能够进行反应产物的分析与判断,能够依据一定的标准对物质进行分类,对于简单的实验能够进行设计并独立操作。
(2)潜在状态
在本课时的学习过程中,学生可能出现以下问题:学生对物质结构和性质的联系理解不透彻,会出现对不同氮的氧化物性质的记忆不清、混淆的情况;认识物质的角度还不明确[5];利用氧化还原反应的规律判断产物的方法还不够熟练;对含氮物质的离子反应产物判断还不够清晰。
4.教学目标
(1)通过分析氮的原子结构示意图,掌握氮气的物理性质和化学性质,并正确运用化学方程式表示,认识微观结构对物质化学性质的影响,发展素养1。
(2)分析NO、NO2中氮元素的化合价,通过实验探究,掌握利用氧化还原原理判断NO2的氧化还原性,并用化学方程式表示其性质;掌握氮的氧化物的特性及其应用,建立物质性质和用途之间的关系,发展素养1和素养3。
(3)通过分析酸雨的形成原因并能用化学方程式表示,了解酸雨的危害及治理办法,发展绿色化学观念,养成环境保护意识。发展素养5。
5.设计思路
“氮气及其氧化物”的课堂教学设计包含知识和素养两条主线。知识主线从氮原子的结构入手,从氮气的组成和结构探究氮气的性质,从氮的循环和氮的固定引出氮的主要氧化物——一氧化氮与二氧化氮,通过实验探究认识二者的性质,从绿色环保的角度认识氮的主要氧化物的危害以及防治措施。下图1展示了本节课教学设计的主要思路。主要围绕三个核心问题展开,分别对应不同的教学内容,通过不同的主题情境展开,每一个教学内容对应多个学习任务,需要设计相应的教学活动对学生进行知识的传授和能力的培养。素养线主要从氮在元素周期表中的位置入手,分析氮气的结构,推测可能具有的性质,建立微观结构与宏观性质之间的关系。然后从氮循环的角度认识自然界中氮的存在形态、固定方法以及氮循环的过程,建立变化观与平衡观。建构氮气及其氧化物的价类二维图,建立元素及其化合物的一般认知模型。最后从实验探究的角度认识一氧化氮、二氧化氮的主要性质,实验探究培养学生的探究精神和创新精神。认识到氮的氧化物对环境的危害,上升到学生科学态度与社会责任的培养。
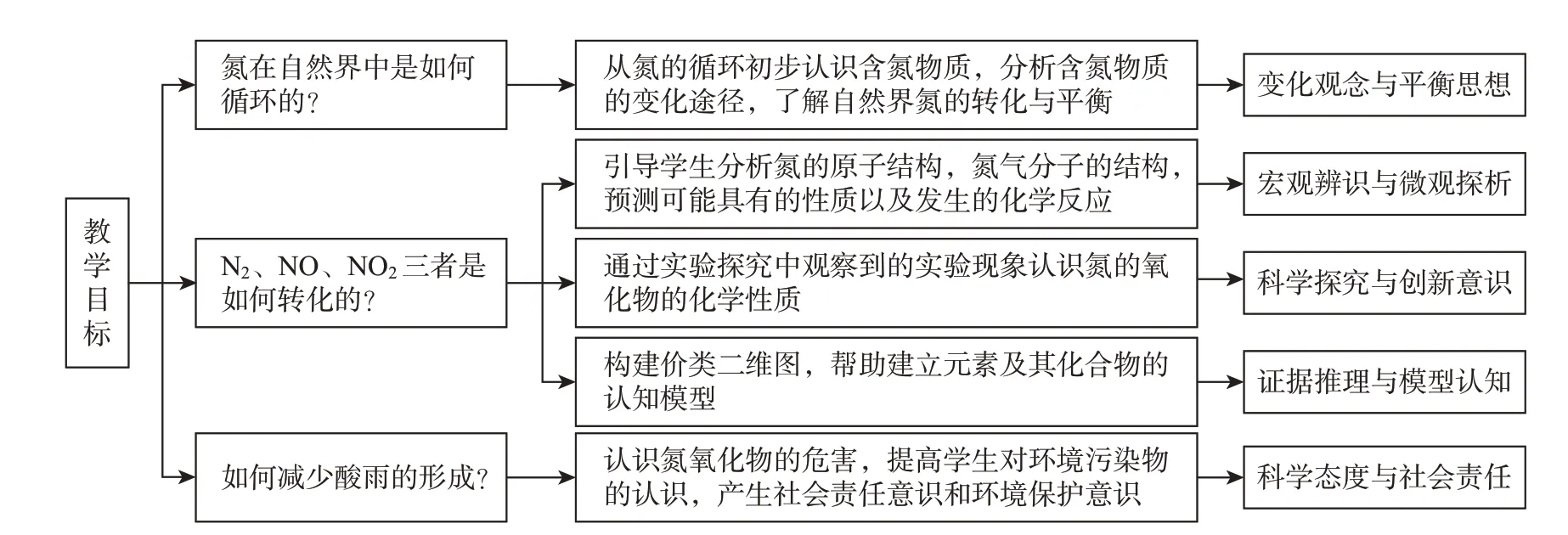
图1 教学设计的主要思路
6.教学设计
氮气及氮的氧化物教学设计
[导入]氮元素是生物体内不可或缺的基本元素之一,氮元素广泛存在于蛋白质、核酸、叶绿素中。氮的循环和碳的循环、水的循环一起构成了地球生态系统的重要循环系统。本节课我们就通过氮的循环认识氮气及其常见的氧化物。
[学生活动]认识氮循环过程及在生产生活中的重要作用,初步认识氮及其化合物的种类,从自然界的氮循环入手,展开“氮气及氮的氧化物”性质的学习。
[设计意图]在生活情境中引入氮元素的学习,氮的循环过程涉及氮的不同化合物之间的转化,学生能够认识到氮的循环对生产生活的重要作用,同时也要考虑社会的可持续性,从而发展素养5。
[提问]我们都说“雷雨发庄稼”,这是为什么呢?
[多媒体展示图片]氮在自然界中的循环示意图(图2)。
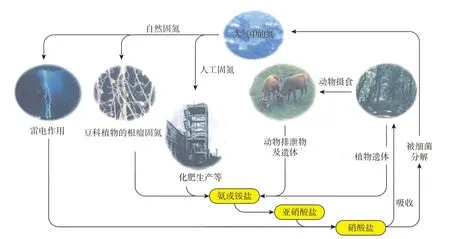
图2 氮在自然界中的循环示意图
[设计意图]了解氮循环的过程,认识氮循环对维持生态系统平衡的重要作用。发展素养5。
[提问]自然界的哪些地方有氮元素?
[回答]大气中、动植物体内、土壤中、水体中。
[追问]自然界的氮元素存在形态有哪些?
[回答]游离态和化合态。
游离态主要是大气中的氮气,化合态主要是动植物体内、土壤中、水体中的含氮化合物。那你能不能尝试描述氮元素在自然界中的循环过程呢?
[学生1回答]一种是氮气在雷雨天在电作用下生成NO,另一种是在植物体内,如在豆科植物的根中,存在着与根瘤菌共生的豆荚蛋白产生系统,系统会产生植物蛋白,还有人工合成氨,以及汽车排放的尾气。
[评价]刚刚这位同学说的是自然界中的氮元素的转化,还没有涉及到循环,氮循环是不是围绕着这些箭头反复循环?哪位同学再来试着描述下。
[学生2回答]大气中的氮通过自然固氮和人工固氮转化成含氮的化合物,如铵盐、硝酸盐等,这些物质被动植物体吸收,通过遗体及排泄物又回到了大气中,或者被细菌分解回到大气中。
[师生总结]氮的循环过程。
[引导]我们重点来看大气中的氮如何变成含氮化合物?我们把这个转化过程叫做氮的固定,根据刚才同学们所说,氮的固定有哪几种方法?
[学生]思考,交流,做好笔记。回答人工固氮和自然固氮的定义。
[解释]自然固氮和人工固氮过程。
[引导]请同学们从元素周期表中找出N的位置,画出氮原子的结构,根据原子结构可以推测它有哪些性质?结合硫及其化合物的学习方法推测氮的主要化合价有哪些?
[思考]氮元素位于第二周期第VA 族,并写出氮的原子结构。
[回答]N 是第7 号元素,原子结构的最外层有5 个电子,在形成化合物时,为了达到稳定结构,氮原子可以得到3个电子。所以可能在化合物中显-3价。
[设计意图]基于原子结构认识氮气的化学性质,让学生建立“位-构-性”三者之间的关系,发展素养3。
[板书]氮元素的原子结构(图3)
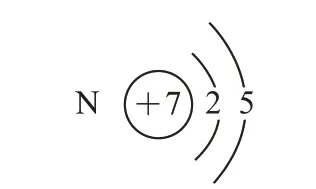
图3 氮元素的原子结构示意图
[补充]还有0 价的N2、+2 价的NO、+4 价的NO2。我们首先以0 价的N 也就是N2为例,探究氮气的性质。请同学们思考氮气的化学式、电子式、结构式是如何书写的?
[思考并书写]
[板书]
化学式:N2
电子式:∶N N∶
结构式:N≡N
[提问]从原子结构的角度思考为什么会这样书写呢?
[回答]因为氮的最外层有五个电子,要达到八电子稳定结构还需要三个电子,两个氮在一起形成三个共用电子对,从而形成稳定的N2分子。
[小结]氮气分子中的两个氮原子以氮氮三键结合,相比于单键或者双键,要断开三键需要很高的能量,所以氮气的化学性质非常稳定,通常情况下N2难以与其他物质发生反应。但是如果在获得了足够的能量的情况下,氮气也是会发生反应的,氮气发生反应的条件是非常苛刻的,一般是高温或者放电。
[思考]氮气化学性质稳定的原因:氮气分子中的三键不容易断裂。
[布置任务]写出氮气与Mg、H2、O2反应的化学方程式。
[写化学方程式]写出化学方程式并认真听讲。
分析在三个反应中N的化合价的变化
[提问]由氮气生成含氮化合物,氮元素的化合价一定升高吗?
[回答]不一定,氮气与镁发生反应化合价由0降低为-3,与氢气发生反应化合价由0 降低为-3,与氧气发生反应化合价由0 升高为+2,化合价不一定升高,既体现氮气的氧化性又体现氮气的还原性。
[设计意图]从氧化还原的角度认识氮气,帮助学生建立氧化还原的认知模型,发展素养2和3。
[引导]我们在初中学过空气中氮气的含量在78%左右,你能根据生活常识归纳出氮气的物理性质吗?
[回答]氮气是一种无色无味、难溶于水、密度比空气略小的气体。
[总结用途]由于氮气的化学性质比较稳定,在生活中用途很多,例如液氮可以用于医疗手术,可以制造氮肥,用作灯泡中的填充气,用作粮食瓜果的保护气等。所以氮气在各领域都发挥着非常重要的作用。
[认真听讲]认识氮气的用途。
[PPT 展示]新闻:某矿井地下炸药库因违章吸烟导致爆炸造成人员氮氧化物中毒,死亡7人,重度中毒2人,轻度中毒66人。
[提问]请同学们猜测引起中毒的含氮的物质是什么?
[设计意图]在主题情境中,从氮的氧化物能够引起中毒的问题,学生能够认识到在人类发展的同时也要考虑发展过程中的安全问题而发展素养5。
[回答]可能是一氧化氮和二氧化氮。
[布置任务]请同学们阅读课本的第13页,完成导学案中NO和NO2的物理性质的比较。
合作交流完成。
[板书]NO:无色无味的有毒气体,不溶于水,密度比空气小。
NO2:红棕色有刺激性气味的有毒气体,易溶于水,密度比空气大。
[提问]请同学们思考:如何收集NO 和NO2?归纳原因。
[回答]NO 用排水法收集,二氧化氮用向上排空气法收集。原因是NO不溶于水,NO2密度比空气大。
[演示实验]在一支20 mL 的注射器中冲入8 mL的NO,后吸入2 mL 的水,用乳胶管和弹簧夹封住管口,震荡注射器。
[设计意图]学生通过化学演示实验认识NO 与O2NO2与水的反应过程,并认识到化学实验是获得知识的有效途径,避免被动地接受知识,发展素养4。
[提问]此时有什么实验现象,你能得出什么实验结论?
观察思考,无明显现象,说明NO不溶于水。
[演示实验]打开弹簧夹,迅速吸入5 mL 空气后夹上弹簧夹,此时又有什么现象,你能得出什么结论?
[回答]无色气体变为红棕色,注射器活塞向右移动,说明NO与空气中的氧气发生了反应,生成了红棕色的NO2。
[实验演示]震荡注射器,观察实验现象。
[回答]红棕色的气体变成了无色,注射器的活塞向右移动。
[提问]为什么会出现这种现象?
思考
[演示]打开弹簧夹吸入空气,我们可以看到无色气体又变红了,说明刚刚的无色气体是?
[回答]一氧化氮。
[提问]非常好,那你能用化学方程式表示这一过程吗?
思考、交流、书写化学方程式。
[设计意图]帮助学生建立“宏-微-符”三重化学表征,发展素养。
[讲授]分析反应间化合价的变化。NO2与水的反应是氮元素自身发生氧化还原反应。通过这个反应我们可以知道NO、NO2可以相互转化,简单提一下这也是我们后面要学习的工业制取硝酸的一个主要原理。
[布置任务]刚刚我们讲了N2、NO、NO2主要的物理性质和化学性质,你能尝试建立三者的价类二维图吗?
思考交流,解决问题,建立价类二维图(图4)。
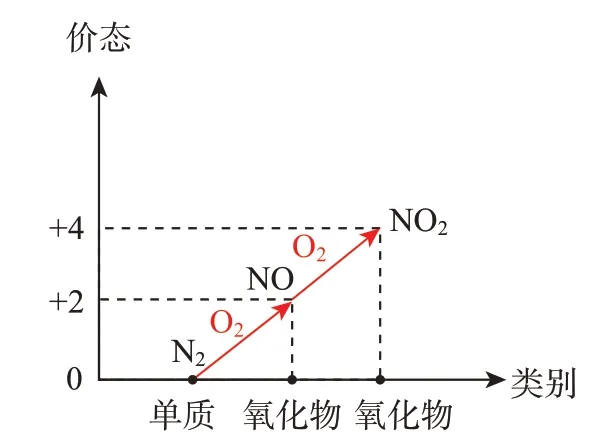
图4 三者的价类二维图
[归纳总结]价类二维图,后面我们会学到更多的关于氮的化合物,对价类二维图进行完善。
[设计意图]帮助学生建立认识元素及其化合物的一般方法,建立认知模型,发展素养2。
[讲授]我们都知道事物都具有两面性。氮及其化合物对我们的生产生活产生了巨大的影响,但同时也造成了很多负面影响。
[视频呈现]氮氧化物:毒与火的炼狱。
根据视频所讲归纳氮氧化物带来的环境问题有哪些?
[设计意图]能够认识到化学知识在实际生活中的应用,尊重科学伦理道德并逐步形成绿色化学、环境保护等观念,发展素养5。
观看视频,归纳
[归纳]光化学污染:氮氧化合物在紫外线的作用下发生光化学反应,产生有毒的烟雾。
破坏臭氧层:导致地面紫外线辐射增强。
酸雨:NO2排入大气与水反应生成硝酸、亚硝酸,随雨雪降落到地面,对动植物、建筑物造成破坏。
[布置任务]在硫及其化合物中我们学习了硫酸型酸雨的形成,根据我们上面所学的化学方程式,分析硝酸型酸雨的形成。
[回答]会发生如下反应:
[引导]学生归纳氮的循环过程以及本节课的学习内容。
[学生]归纳总结
[设计意图]强化巩固,突出重难点。
[布置作业]
四、教学反思
以问题为导向的教学,可以引发学生的积极思考,有利于学生的思维拓展。通过“氮的循环”“N2、NO、NO2的性质和转化”与“酸雨的形成与危害”三个教学内容的学习,使学生认识了氮气及其常见的氧化物的性质;通过对氮气与其氧化物之间相互转化的学习,学生认识了物质之间的转化与平衡,以及它们的性质与用途,培养了学生的科学探究能力;通过对元素及其化合物认知模型的学习,培养学生分析问题、解决问题的能力及归纳、概括、推理能力。学生能够学以致用,将所学知识应用到实际生产生活中去;同时也培养了学生热爱科学,关心环境友好型社会建设等社会责任感。本文以氮元素为例,对元素性质、化学反应、工业生产、生活应用等方面进行知识和技能的介绍,旨在引导学生了解元素性质与其相关物质的联系,进一步领悟化学在生活中的价值和意义。化学知识是人类社会文明发展的重要基础,化学也帮助人们认识自然、改造自然。因此,教师在教学过程中要加强化学知识与社会、自然以及人与人之间关系的联系,引导学生提高对化学知识和科学的价值理解,培养学生热爱祖国、关心社会和关注环境的情怀。在新课程中,教师应以培养学生的学科素养为前提充分发挥教学活动中的主导作用,通过引导学生主动参与教学活动,让他们在参与过程中形成一定的能力和掌握相应知识,促进个体的发展。
