二氧化硫性质的实验改进*
2024-01-12王爱华
王爱华
(江苏省宝应中学 江苏 扬州 225899)
一、设计的意图
化学实验是化学教师教学的灵魂,力求在核心素养导向下,以二氧化硫的四个化学性质(如图1)为线索,改进实验,设计学生可操作的微型实验,使学生由过去被动“等待”和“接受式”的学习方式,变为“主动”和“探索式”的学习方式;使多年来提倡的“启发式”“学生为主体、教师为主导”的教学方法得以实现[1];力求在核心素养导向下,利用微型实验,通过亲手做实验,帮助学生理解和形成化学概念,培养观察和实验能力,同时有效地激发学生学习化学的兴趣,发展学生思维[2],培养学生动手操作、设计实验的能力,为化学教学改革和学生素质的全面发展起积极的推动作用。
图1 二氧化硫的主要化学性质
医用三通阀是一种医疗领域输送道中常用的连接工具(如图2),主要用于输送液体,一般使用螺口注射器进行兑药操作,将其应用于二氧化硫性质的小组微型化实验探究,教学成效显著。
图2 医用三通阀
二、设计的方案
1.酸性:二氧化硫与水反应的实验
(一)实验原理
(二)实验用品
2个三通阀、3个100 mL的螺口注射器、紫色石蕊溶液、SO2、蒸馏水。
(三)实验装置
新设计的实验装置如图3。
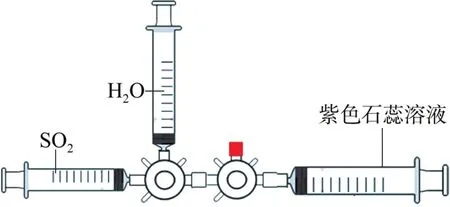
图3 在注射器里做二氧化硫与水反应的实验
(四)实验步骤
(1)三个100 mL 的注射器分别抽取SO2气体、蒸馏水和紫色石蕊溶液,按照图示方式安装好。
(2)旋转第一个三通阀的旋塞,将注射器里的蒸馏水挤入充有SO2气体的注射器,关闭旋塞,可以看到注射器的活塞芯杆慢慢向前移动,气体的体积不断的减少。实验说明二氧化硫是极易溶于水的。
(3)旋转第二个三通阀的旋塞,将SO2的水溶液挤入紫色石蕊溶液中,发现溶液变红。
(五)实验结论:二氧化硫的水溶液具有酸性。
[设计意图]苏教版高中化学教科书中明确强调二氧化硫的水溶液呈酸性是学生必做实验。利用三通阀和螺口注射器组装的实验装置不仅避免了二氧化硫的危害和空气的干扰,而且放大了实验现象,增添了实验的趣味性,培养学生动手操作的能力,还增强学生环境保护的意识。
2.漂白性:二氧化硫的漂白性
(一)实验原理
二氧化硫溶于水后生成的亚硫酸跟有机色质直接结合成无色的化合物。
(二)实验用品
三通阀、2个100 mL的螺口注射器、品红、SO2、酒精灯、试管、试管夹。
(三)实验装置
新设计的实验装置如图4。
(四)实验步骤
(1)2 个100 mL 的注射器分别抽取SO2气体、品红,按照图示的方式安装好。
(2)旋转三通阀的旋塞,将注射器里的SO2挤入充有品红的注射器,关闭旋塞,现象是品红褪色。
(3)将液体挤入试管中,把气球套在试管的尾部,然后给试管加热,红色又恢复。冷却下来后,红色又消失,继续加热,红色又恢复。
(五)实验结论
二氧化硫具有漂白性,并且这个漂白性是暂时的,还可以再恢复。
[设计意图]通过图4的设计,不但可以降低二氧化硫的污染,还可以通过加热、冷却反复地看到红色褪去,红色恢复。由此可以让学生掌握二氧化硫与氯水的漂白原理的差异;因为这种现象的独一无二,因此也可以得出二氧化硫的检验方法;可以比对后面二氧化硫能使高锰酸钾和碘的淀粉溶液褪色,为二氧化硫的还原性也能使部分的物质褪色做铺垫。
3.还原性:二氧化硫水溶液与KMnO4溶液的反应
(一)实验原理
(二)实验用品
2个三通阀、3个100 mL的螺口注射器、KMnO4溶液、SO2、BaCl2溶液。
(三)实验装置
新设计的实验装置如图5。
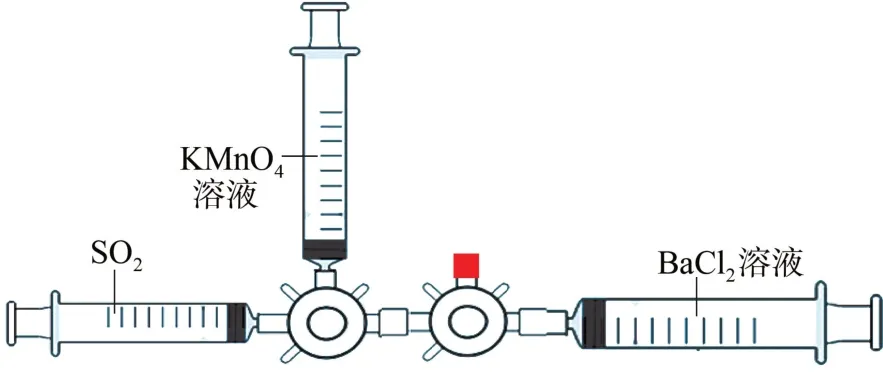
图5 在注射器里做二氧化硫与KMnO4溶液的反应的实验
(四)实验步骤
(1)三个100 mL 的注射器分别抽取SO2气体、KMnO4溶液和BaCl2溶液,按照图示的方式安装好。
(2)旋转三通阀的旋塞,将注射器里的KMnO4溶液挤入充有SO2气体的注射器,关闭旋塞。可以看到紫红色的KMnO4溶液褪色。
(3)旋转三通阀的旋塞,将BaCl2溶液挤入之前的溶液中,发现立即有白色沉淀生成。
(4)改变药品加入的顺序,先将注射器里的BaCl2溶液挤入充有SO2气体的注射器,没有明显的现象,再将无色溶液挤入KMnO4溶液中,可以看到KMnO4溶液褪色,并且产生白色沉淀。
(五)实验结论
二氧化硫与BaCl2溶液本质上不反应,高锰酸钾将二氧化硫氧化成硫酸根,硫酸根结合了Ba2+,从而产生了白色沉淀,体现了二氧化硫的还原性。
【设计意图】通过图5的设计,改变药品加入的顺序,可以将一个验证性的实验转化成一个探究性的实验。从褪色的表象去引导学生思考是不是与SO2的漂白性有关;从白色沉淀的现象让学生推断白色沉淀可能的成分;从硫酸根产生的角度再去分析KMnO4褪色的本质,引导学生得出二氧化硫的还原性。
4.还原性:二氧化硫水溶液与碘的淀粉溶液的反应
(一)反应原理
(二)实验用品
三通阀、3 个100 mL 的螺口注射器、碘的淀粉溶液、SO2、BaCl2溶液。
(三)实验装置
新设计的实验装置如图6。
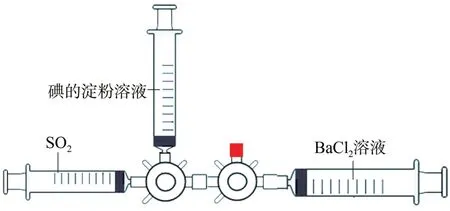
图6 在注射器里做二氧化硫与碘的淀粉溶液反应的实验
(四)实验步骤
(1)三个100 mL 的注射器分别抽取SO2气体、碘的淀粉溶液、BaCl2溶液,按照图示的方式安装好。
(2)旋转三通阀的旋塞,将SO2气体挤入碘的淀粉溶液的注射器,关闭旋塞。可以看到蓝色的溶液褪色。引导学生分析溶液褪色的原因,是利用了SO2的漂白性还是还原性?如何验证自己的猜想。
(3)旋转三角阀的旋塞,将BaCl2溶液挤入之前的溶液中,发现立即有白色沉淀生成。
(五)实验结论
二氧化硫具有还原性。
【设计意图】如果说二氧化硫使高锰酸钾褪色的本质体现了二氧化硫的还原性,追加的二氧化硫使得碘的淀粉溶液褪色的这个实验的设计可以有效的体现学生的分析能力,自主探究的能力。通过药品加入顺序的变更,再通过实验现象去验证自己的推理。达到了学以致用的高度,升华了这节课的高度。
5.氧化性:二氧化硫与硫化氢气体的反应
(一)实验原理
(二)实验用品
三通阀、2个100 mL的螺口注射器、H2S、SO2。
(三)实验装置
新设计的实验装置如图7。

图7 在注射器里做SO2与H2S反应的实验
(四)实验步骤
(1)2 个100 mL 的注射器分别抽取SO2气体、H2S气体,按照图示的方式安装好。
(2)旋转三通阀的旋塞,将注射器里H2S挤入充有SO2气体的注射器,关闭旋塞。挤压活塞增大体系的压强,可以看到注射器里产生水雾并且有淡黄色的固体生成。
(五)实验的结论
从化合价变化的角度分析二氧化硫具有氧化性。
【设计意图】二氧化硫与硫化氢的反应不是相遇了就立即反应的,短时间内要看到明显的实验现象,需要增大反应体系的压强,这套简易装置通过挤压活塞轻松实现压强的增大,从而呈现明显的实验现象;二氧化硫和硫化氢都是有毒的气体,通过这个装置降低了它的空气污染,简化了实验。
6.二氧化硫性质的一体化设计
(一)实验原理
(二)实验用品
6 个三通阀、7 个100 mL 螺口注射器、H2S、SO2、KMnO4、碘的淀粉溶液、品红、BaCl2溶液。
(三)实验装置
如图8。
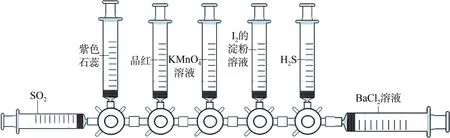
图8 二氧化硫性质的一体化设计
(四)实验步骤
(1)打开活塞,将SO2气体挤入紫色石蕊溶液。
(2)打开活塞,将SO2气体挤入品红溶液。
(3)打开活塞,将SO2气体挤入KMnO4溶液。
(4)打开活塞,将SO2气体挤入碘的淀粉溶液。
(5)打开活塞,将SO2气体挤入H2S气体中。
(6)打开活塞,将BaCl2溶液挤入褪色的KMnO4溶液中。
(7)打开活塞,将BaCl2溶液挤入褪色的碘的淀粉溶液中。
(五)实验结论
二氧化硫的水溶液具有酸性,二氧化硫具有漂白性、氧化性和还原性。
【设计意图】一体化的性质设计,可以同时体现二氧化硫的四个性质;实验现象的明显对比,增加了实验的趣味性,给学生非常强烈的视觉效果;实验现象层次性地出现,更加利于学生对知识的消耗理解;封闭体系的微型实验便于学生的操作,增强了学生环保的意识和学习化学的热情。
三、设计的意图与应用:探究硫酸型酸雨形成的原理
(一)反应原理
(二)实验用品
两个三通阀、3 个100 mL 的螺口注射器、O2、SO2、BaCl2溶液。
(三)实验装置
新设计的实验装置如图9。
(四)实验步骤
(1)三个100 mL 的注射器分别抽取SO2气体、O2、BaCl2溶液,按照图示的方式安装好。
(2)旋转三角阀的旋塞,将注射器里的BaCl2溶液挤入充有SO2气体的注射器,关闭旋塞。
(3)旋转三角阀的旋塞,将O2挤入之前的溶液中,立即有白色沉淀生成。
(五)实验结论
氧气可以将亚硫酸氧化成硫酸。
【设计意图】通过图9的设计,成功模拟了酸雨形成的真实情景,从而揭示硫酸型酸雨形成的本质。通过二氧化硫性质的验证和探究的实验设计,让学生从实验中掌握物质的性质和使用时的注意事项,并且应用物质的性质揭示自然现象的本质,引导学生建立科学的思维模式,激发学生的创新能力,培训学生分析判断的能力,从而体现学以致用的育人价值。
四、反思和感悟
2017年版的普通高中化学课程标准中强调:“化学实验是进行科学探究的主要方式,他的功能是其他教学手段所无法替代的[3],微型化学实验有利于培养学生的创新精神和实践能力,尤其是在有限的教学时间内让学生具备这种能力成为了一种可能。从推进学生素质教育的角度而言,中学化学实验的微型化实验提高了学生乐于动手动脑的能力,培养了学生勤于实践的意识和习惯;从培养适应21世纪需要的高素质人才的高度看,认识推广微型化学实验的意义更加深远[4]。教育专家指出,微型实验已经被称为21世纪最引人注目的重大变革之一。随着中学化学课程改革的不断深入,中学实验的微型化将具有更加广阔的前景[5]。这就要求我们在日常的教学中要勤于创新,开发多样的微型化学实验,打造高质量的课堂教学模式。
