安乐阴洗剂微生物限度检查方法学的研究
2024-01-12郑域茹高丹玲廖燕萍
郑域茹 朱 铮 郑 挺 高丹玲 廖燕萍
福建省食品药品质量检验研究院,福建福州 350001
医院制剂是由医疗机构根据临床需要自行配制且经药品监督管理部门审核批准后,按固定处方使用的制剂[1]。它能有效弥补市场药物供应不足,具有便捷、疗效显著且价格低廉等优势,是临床用药不可或缺的组成部分[2]。安乐阴洗剂是一种临床常用的治疗妇科疾病的医院制剂,其处方由多种中草药组成,具有清热、解毒、燥湿、止痒的功效[3]。文献报道,该洗液配方中的一枝黄花能明显抑制大肠杆菌、枯草芽孢杆菌及酿酒酵母[4];制剂中的黄柏能抑制金黄色葡萄球菌、破伤风杆菌及其他人体内常见的致病菌[5];蛇床子、绵马贯众、百部和花椒对细菌和真菌同样具有一定程度的体外抑菌作用[6-7]。此外,该制剂还添加了各种防腐剂,如苯甲酸钠和羟苯乙酯,这些防腐剂还具有很强的防腐作用。因此,安乐阴洗剂微生物限度检查法的建立需要采用适当的方法消除抑菌活性之后,其检查结果才能够有效地反映其实际污染情况[8]。本研究应用常规法、稀释法、中和法、薄膜过滤法及中和-薄膜过滤法等摸索出消除安乐阴洗剂自身抑菌性的方法,以期建立合适的微生物限度检验方法,为该制剂的药品质量检验起到一定的借鉴作用,进而保障患者用药安全。
1 仪器与材料
1.1 主要仪器设备
TX2202L 电子天平(日本岛津)、HVA-110 高压蒸汽灭菌器(日本雅马哈)、MSC1.8A2 生物安全柜(赛默飞世尔科技)、HTY-306A 过滤系统(浙江泰林)、IQ822C 培养箱(日本雅马拓)和VITEK2 COMPACT 全自动微生物鉴定仪(梅里埃)等。
1.2 菌种
金黄色葡萄球菌[CMCC(B)26003]、枯草芽孢杆菌[CMCC(B)63501]、铜绿假单胞菌[CMCC(B)10104]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003]、生孢梭菌[CMCC(B)64941]均购自中国食品药品检定研究院,传代次数为第3 代。
1.3 培养基
胰酪大豆胨液体培养基(tryptic soy agar,TSA)、胰酪大豆胨琼脂培养基(tryptic soy broth,TSB)和沙氏葡萄糖琼脂培养基(Sabouraud dextrose agar,SDA)等均购于北京三药科技有限公司,哥伦比亚琼脂培养基和梭菌增菌液体培养基购自中国食品药品检定研究院。
1.4 稀释剂与冲洗液
TSB;含4%聚山梨酯80 和0.5%大豆卵磷脂[9]的TSB;pH 7.0 无菌氯化钠-蛋白胨缓冲液。
1.5 供试品
安乐阴洗剂3 批(批号分别为221010、221014 和221020),均来源于福建中医药大学附属人民医院。
2 方法
2.1 试验用菌液的制备
按照《中国药典》2020 年版[10]规定制备适宜浓度的铜绿假单胞菌、金黄色葡萄球菌、枯草芽孢杆菌、白色念珠菌、黑曲霉菌悬液和梭菌的菌悬液。
2.2 需氧菌总数计数检查方法的建立与验证
方法A:1 ∶10 常规法。无菌量取安乐阴洗剂10 ml,加90 ml TSB,混匀,作为1 ∶10 供试液。分装该供试液,取5 支无菌的试管,每支分装9.9 ml,分别加入适宜浓度的菌悬液,控制最终每支试管中每毫升菌含量低于100 cfu,将此作为试验组。将上述混合液2 ml 分别无菌吸取到直径为90 mm 的无菌平皿中(1 ml/皿),然后注入TSA 培养基,置于30 ~35℃培养2 ~3 d,点计平板上的菌落数。以稀释液替代菌液,其余操作方法与试验组相同,作为供试品对照组;取稀释液替代供试品溶液,其余操作方法与试验组相同,作为菌液对照组。计算安乐阴洗剂中5 株试验菌的回收率,回收率=(试验组菌落数- 供试品对照组菌落数)/ 菌液对照组菌落数×100%。
方法B:1 ∶20 稀释法。取方法A 项下的供试液50 ml,加入50 ml TSB,混匀,作为方法B 的供试液。其余操作同方法A。
方法C:1 ∶50 稀释法。取方法A 项下的供试液20 ml,加入80 ml TSB,混匀,作为方法C 的供试液。其余操作同方法A。
方法D:中和法(1 ∶10)。将方法A 项下TSB稀释液替换为含4%聚山梨酯80 和0.5%大豆卵磷脂的TSB,混匀,作为方法D 的供试液。用含4%聚山梨酯80 和0.5%大豆卵磷脂的TSB 代替TSB,作为中和剂对照组。其余操作同方法A。
2.3 霉菌和酵母菌计数检查方法的建立与验证
方法E:原液薄膜过滤法。取1 ml 供试品原液,加入100 ml pH 7.0 氯化钠-蛋白胨缓冲液,混匀,加入1 ml 含菌量不大于100 cfu 的白色念珠菌菌悬液,采用HTY-306A 过滤系统过滤,随后用pH 7.0氯化钠-蛋白胨缓冲液冲洗3 次,每次100 ml,滤干后将膜贴于SDA 平板后,置20 ~25℃培养3 d,点计滤膜上的菌落数。黑曲霉依照此法操作,最后对试验菌的回收率进行计算。
方法F:薄膜过滤法。将方法E 项下1 ml 供试品原液替换为2.2 项下方法A 中以TSB 为稀释剂的1 ∶10 供试液10 ml,其余操作参考方法E。
方法G:中和剂- 薄膜过滤法。将方法E 项下1 ml 供试品原液替换为2.2 项下方法D 中含有中和剂的1 ∶10 供试液10 ml,其余操作参考方法E。
2.4 控制菌检查方法的建立与验证
2.4.1 常规法 以TSB 为稀释剂,制备1 ∶10 的供试液。金黄色葡萄球菌:取10 ml 供试液接种到TSB 增菌液(100 ml)中,同时接种的1 ml 金黄色葡萄球菌菌悬液(菌含量不超过100 cfu),混合均匀,按药典规定培养观察;铜绿假单胞菌:取10 ml 接种到TSB 增菌液(100 ml)中,同时接种1 ml 铜绿假单胞菌菌悬液(菌含量不超过100 cfu),混合均匀,按药典规定培养观察;白色念珠菌:取10 ml,接种到沙氏液体培养基(100 ml)中,同时接种1 ml白色念珠菌菌悬液(菌含量不超过100 cfu),混合均匀,按药典规定的白色念珠菌检查法培养观察;梭菌:取10 ml,接种到梭菌增菌液(100 ml)中,同时接种1 ml 梭菌菌悬液(菌含量不超过100 cfu),混合均匀,按药典规定的梭菌检查法培养观察。以不加菌悬液作为供试品对照组,以不加供试液作为阳性对照组,以稀释液代替供试液且不加菌悬液作为阴性对照组。4 个控制菌方法适用性试验中有疑似或典型菌落生长时,均采用微生物鉴定仪进行鉴定确认,根据鉴定结果确定试验菌株是否检出,并据此判断方法适用性试验是否可行。
2.4.2 中和法 将常规法中1 ∶10 供试液替换为2.2 项下方法D 制备的含中和剂的1 ∶10 供试液,其余操作参照2.4.1 的常规法。
3 结果
3.1 需氧菌总数计数预实验
以批号为221010 的安乐阴洗剂开展预实验,以TSB 作为稀释剂的常规法(方法A),白色念珠菌的回收率为26%,枯草芽孢杆菌和金黄色葡萄球菌分别为39%和28%,均未达到50%,不符合药典规定;方法B 将供试液稀释倍数提高为1 ∶20,枯草芽孢杆菌和金黄色葡萄球菌的回收率有所提高,分别为51%和50%,但是白色念珠菌的回收率仅为47%,仍未达到50%;方法C 将供试液按1 ∶50 的比例进一步稀释,各试验菌回收率在50%~200%,满足适用性试验回收率要求,但是白色念珠菌回收率仍偏低(仅为54%),显然白色念珠对安乐阴洗剂最敏感;方法D 在稀释剂TSB 中添加4%聚山梨酯80 和0.5%大豆卵磷脂制备1 ∶10 供试液后,白色念珠菌的回收率菌达79%,而其他各试验菌的回收率均在90%~110%,表明供试液的抑菌性已基本消除。见表1。
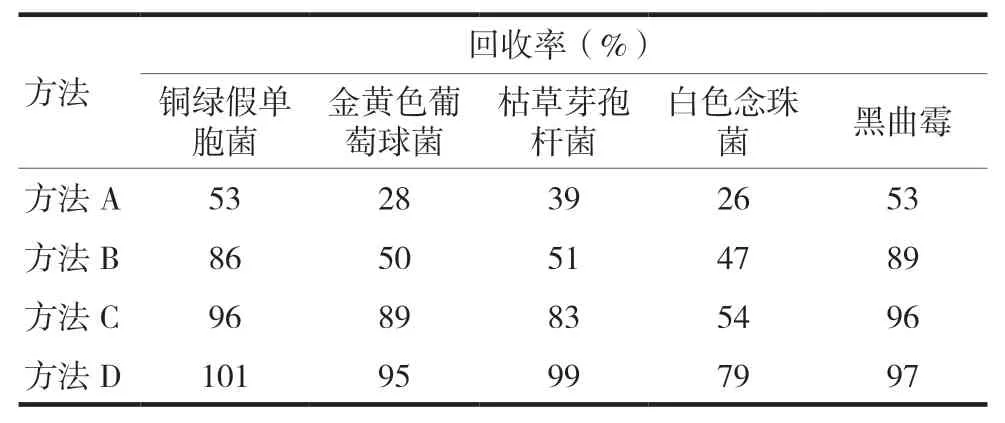
表1 需氧菌总数计数预试验结果
本研究采用稀释法和中和法各试验菌的回收率均符合《中国药典》2020 年版[10]的规定。其中稀释法需采用1 ∶50 的供试液,而中和法的供试液则为1 ∶10,依据《中国药典》2020 年版[10]规定宜优先选择稀释级更小的中和法对安乐阴洗剂需氧菌总数计数方法适用性试验。
3.2 需氧菌总数计数检查方法适用性结果
基于3.1 的试验结果,用中和法验证三批供试品需氧菌总数计数的方法,三批样品的5 种试验菌回收率均符合《中国药典》2020 年版[10]的规定(表2)。因此安乐阴洗剂的需氧菌总数计数法:以含有4%聚山梨酯80 和0.5%大豆卵磷脂的TSB作为稀释剂制备1∶10供试液,采用平皿法(1 ml/皿)进行计数。
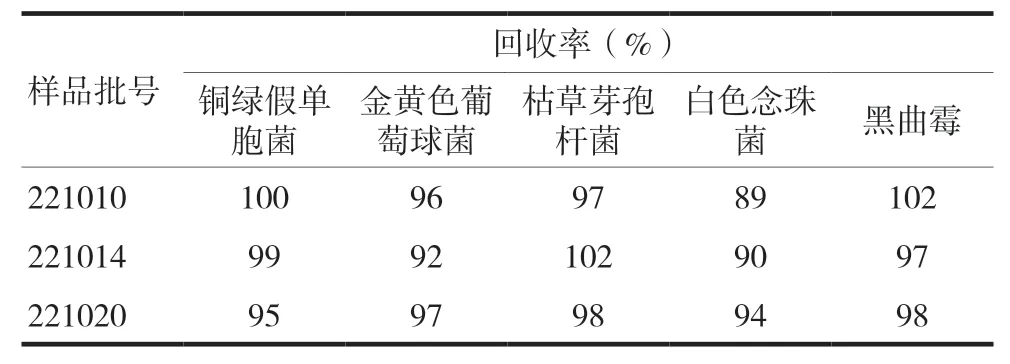
表2 需氧菌总数计数检查方法适用性结果
3.3 霉菌和酵母菌总数计数检查方法适用性结果
在取供试品原液1 ml 薄膜过滤(方法E)试验中,由于安乐阴洗剂原药液中存在较多细小易散的沉淀,薄膜堵塞,无法进行试验;而取TSB 为稀释剂的1 ∶10 供试液10 ml 进行过滤(方法F),供试液中仍可见较多细小不溶物,薄膜过滤速度极为缓慢,难以进行试验。方法G 中,以添加了4%聚山梨酯80 和0.5% 大豆卵磷脂的TSB 为稀释剂,制备1 ∶10 试液,供试液变得肉眼可见澄清,取10 ml 进行薄膜过滤,堵膜现象明显缓解,过滤速度大幅提高,pH 7.0 氯化钠- 蛋白胨缓冲液冲洗3 次(100 ml/次),三批样品的白色念珠菌和黑曲霉回收率均90%以上,符合《中国药典》2020 年版[10]的规定。因此安乐阴洗剂的霉菌和酵母菌总数计数方法:含4%聚山梨酯80 和0.5%大豆卵磷脂的TSB为稀释剂制备1 ∶10 供试液,取10 ml 薄膜过滤,冲洗量300 ml/膜。见表3。
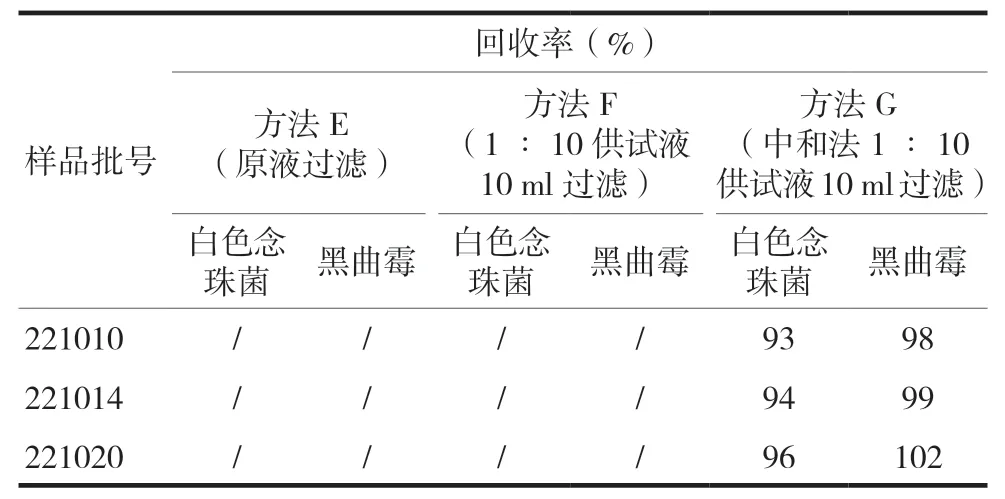
表3 霉菌和酵母菌总数计数方法适用性结果
3.4 控制菌检查方法适用性结果
4 种控制菌的检查主要采用常规法和中和法进行考察(表4)。采用常规法对金黄色葡萄球菌、白色念珠菌和梭菌进行适用性试验时,批号为221010的样品试验组的白色念珠菌和梭菌均未检出,批号为221014 的样品试验组的金黄色葡萄球菌未检出;当供试液中添加中和剂后,3 批样品试验组的金黄色葡萄球菌、白色念珠菌和梭菌均生长良好,因此中和法适用于金黄色葡萄球菌、白色念珠菌和梭菌的检查。采用常规法和中和法对铜绿假单胞菌进行适用性试验时,阳性对照组和3 批样品试验组的试验菌均生长良好,阴性对照组无菌落生长,因此两种方法均可用于铜绿假单胞菌的检查。本研究中为了供试液制备的方便,铜绿假单胞菌检查采用中和法进行。
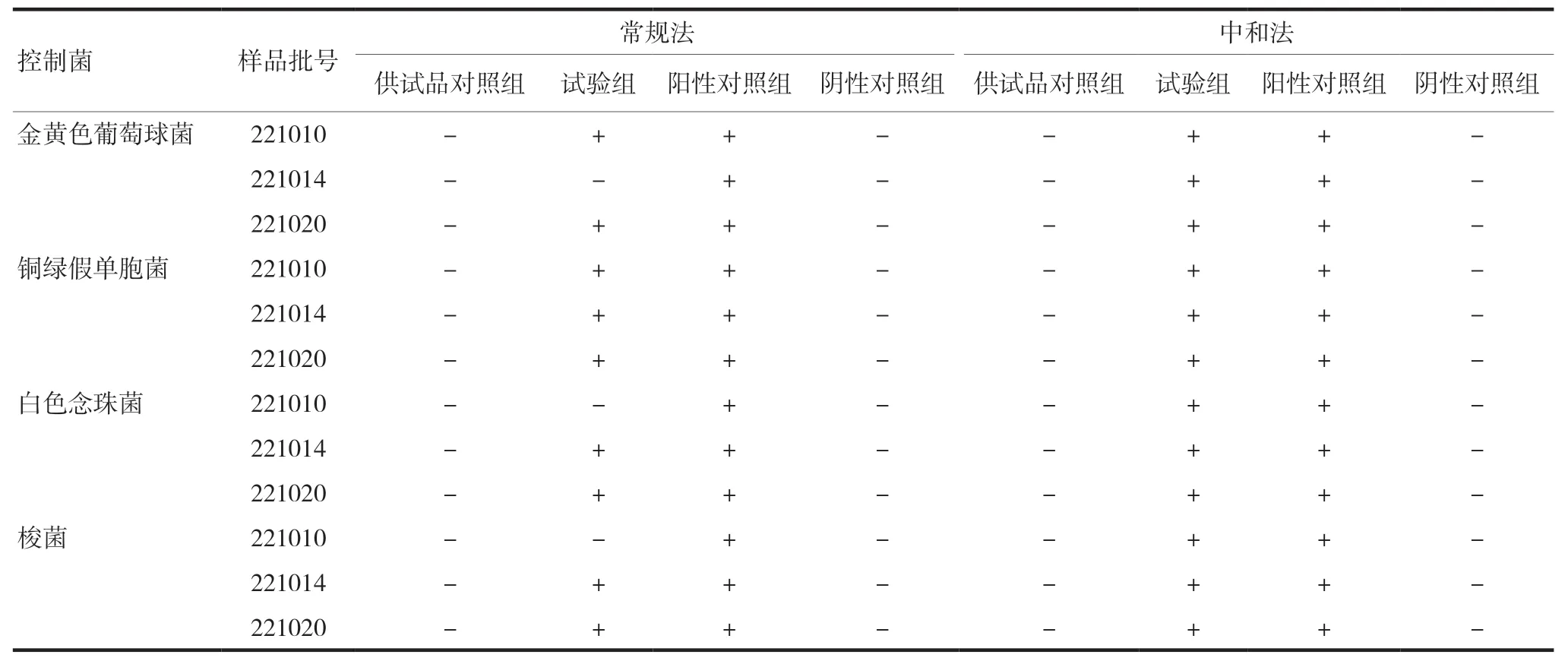
表4 控制菌检查方法适用性结果
综上所述,安乐阴洗剂控制菌检查方法:采用添加4%聚山梨酯80 和0.5%大豆卵磷脂的TSB为稀释液制备1 ∶10 供试液,取10 ml 依相应检查法对金黄色葡萄球菌、铜绿假单胞菌、白色念珠菌和梭菌进行检查。
4 讨论
中药复方制剂,内含多种对微生物具有抑制作用的成分,使用常规的微生物限度检查法往往不适用,通常需要通过降低或去除样品中抑菌作用,从而减少对检验结果的干扰,最大限度的避免漏检、误检的情况[11-12]。本研究结果表明,安乐阴洗剂对枯草芽孢杆菌、金黄色葡萄球菌和白色念珠菌具有不同程度的抑菌活性,故要建立可靠、稳定的微生物限度检查法必须排除该制剂的抑菌性,以保证检验结果真实有效[13-15]。
本研究采用稀释法、中和法对安乐阴洗剂需氧菌总数计数进行方法优化,稀释法和中和法的5 株试验菌的回收率均符合我国药典要求,但是中和法能有效降低供试液稀释级别。聚山梨酯80 和卵磷脂均为中国药典收载的中和剂,分别为非离子型和两性离子表面活性剂,可保护微生物的细胞膜,降低酚、醛、对羟基苯甲酸类等引起的抑菌作用。张光华等[16]曾报道,3%吐温80 和0.3%蛋黄卵磷脂联用降低化学药品的抑菌性,但蛋黄卵磷脂较难溶解。本研究选用较易溶解的大豆卵磷脂,添加4%聚山梨酯80 和0.5%大豆卵磷脂作为中和剂,同样能有效降低供试液中药材对试验菌的抑制作用。在进行霉菌和酵母菌总数计数检查方法适用性试验中,添加中和剂能有效增加样品的溶解性,改善样品的薄膜堵塞情况,提高薄膜过滤的工作效率。因此,开展对有抑菌作用中药液体制剂微生物限度检验方法的适用性验证是非常必要的,选用适当的中和剂能迅速除去样品抑菌性,提高方法适用性试验准确度,提高检验效率。
在建立药品微生物限度检查法的过程中,在确保检验方法操作简便快捷的同时,还需充分了解其受微生物限度标准的限制。本品根据《中国药典》2020 年版[10]的规定,霉菌和酵母菌总数限度标准为101cfu,本品若采用1 ∶10 供试液1 ml 进行检验,可能影响结果有效性的判断。因此对本品霉菌和酵母菌总数计数检查方法适用性研究中,主要采用原液1 ml 和1 ∶10 供试液10 ml 薄膜过滤法进行验证。考虑到本品自身的抑菌性(白色念珠菌是一种敏感菌株),本验证采用中和法和薄膜过滤法相结合进行测定,各试验菌的回收率与我国药典规定一致,方法可行。
本研究是根据《中国药典》2020 年版[10]四部通则中规定的微生物限度检查法进行检查,该方法能有效去除药物自身的抑菌性,简便易行,确保微生物限度检查法科学准确,为药品常规监管检验工作提供技术支撑。同时,本研究试验过程和思路可为其他相似的中药制剂建立微生物限度检查方法提供参考。
