真实世界吡咯替尼治疗HER2 阳性晚期乳腺癌的安全性分析
2024-01-10朱仲玲郑禹史业辉
朱仲玲,郑禹,史业辉
(天津医科大学肿瘤医院药物临床试验机构办公室,国家恶性肿瘤临床医学研究中心,天津市恶性肿瘤临床医学研究中心,天津市肿瘤防治重点实验室,天津 300060)
真实世界研究(real-world study,RWS)是针对预设的临床问题,在真实世界环境下收集及分析现实的医疗实践数据,以获得真实世界证据(realworld evidence,RWE)的研究过程[1]。近年来,RWS 受到药物研发领域的广泛关注[2-5],国家药品监督管理局药品审评中心已连续发布多项指导原则[6-8],用于规范真实世界数据的方法学、明确RWE 的适用范围。高质量的RWS 不仅可用于支持新药注册上市和已上市药品的说明书变更,还可用于指导临床试验设计和精准定位目标人群[1]。标准化临床科研大数据平台是开展RWS 的重要支持工具[9],可以提供规范、动态、实时的多源数据,保证数据的准确性和时效性。
马来酸吡咯替尼是我国自主研发的小分子酪氨酸激酶抑制剂[10],2018 年8 月在国内上市,与卡培他滨联合用于治疗表皮生长因子受体2(human epidermal growth factor receptor 2,HER2)阳性、既往未接受或接受过曲妥珠单克隆抗体(单抗)的复发或转移性乳腺癌患者,或与曲妥珠单抗和多西他赛联合用于HER2 阳性晚期乳腺癌的一线治疗[11]。本研究在医院电子病历系统的基础上构建了适合RWS的临床科研大数据平台、乳腺癌专病库以及吡咯替尼用药分析科研课题库,并探讨了真实世界中吡咯替尼治疗HER2 阳性晚期乳腺癌患者的安全性。
1 对象与方法
1.1 临床科研大数据平台构建 临床科研大数据平台分为数据湖、全院科研大数据中心、专病数据库和科研课题数据库4 个层次。临床业务数据首先汇聚到原始数据湖,基于临床知识图谱和医学自然语言处理方法,并结合人工智能(artificial intelligence,AI)技术对医院原始数据进行数据清洗、治理和融合,实现数据的分层提取、转换、存储和应用,构建适合RWS 的患者全生命周期标准化数据集,见图1。

图1 基于AI 的原始数据处理流程图Fig.1 Flow chart of raw data processing based on AI
1.1.1 基础架构 使用虚拟化技术Docker 集成微服务架构体系,以面向服务的架构作为基础性支撑平台,在平台提供的技术以及业务组件上,开发多个管理、检索、计算和处理医学大数据的应用系统。为了保证数据库的先进性及数据的可扩展性,使用Elasticsearch 大数据分布式存储数据库进行混合部署,其基于集群实现分布式存储,具有很好的容灾性,在需要实时读写、随机访问超大规模数据集时,能够保持性能稳定。
1.1.2 自适应模式识别和自然语言处理 基于深度学习方法以端到端的学习方式求解序列标注问题,即将“原始数据”输入模型后,模型自动完成特征学习和标签预测任务。深度学习模型包含嵌入层、编码层和解码层,嵌入层用于获取文本序列的嵌入表示;编码层用于文本特征提取和标签预测,如双向长短期记忆神经网络、双向编码器表征等神经网络模型;解码层用于解析最优标签序列。根据“嵌入层-编码层”实现方式的不同,可将深度学习模型分为基于特征和基于微调两种。
1.1.3 自适应关系网络 将传统的机器学习方法——条件随机场和支持向量机结合,建立实体关系网络,通过实体链接和消歧将抽取出的实体链接到已有的知识库实体,逐层迭代构建实体网络。通过标注三元组逻辑关系,形成网状拓扑结构,更好地挖掘疾病进展的规律。利用自然语言处理肿瘤治疗指南如《中国抗癌协会肿瘤诊治指南》,初建实体概念。对特定类型肿瘤的诊断、分期、手术、放疗、化疗、靶向治疗、免疫治疗等,利用自适应关系网络链接关系构建医疗知识图谱。
1.1.4 针对肿瘤精准细分设定纳排条件 根据肿瘤细分的适应证,对病历库设定纳排条件,进行实时的智能化检索,获得病历库中对应的病历,同时设置观察指标和展现形式,得到对病历中观测指标的基线统计或者医疗事件的规律统计结果。
1.2 研究对象纳入标准 从乳腺癌专病库中筛选符合纳入标准的患者组成吡咯替尼用药分析科研课题库。患者纳入标准为:(1)年龄≥18 岁的女性。(2)经组织病理学证实为HER2 阳性的晚期乳腺癌患者。(3)美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)体能状况评分0~2 分。(4)病历资料完整,且具有吡咯替尼治疗期间血常规、肝肾功能等检验记录。
1.3 临床资料收集 收集医院乳腺肿瘤中心2022 年1 月至2023 年4 月经吡咯替尼治疗并符合纳入标准的HER2 阳性乳腺癌患者60 例,中位年龄55.5 岁(35~76 岁)。所有患者经组织病理学证实为HER2 阳性乳腺癌。所有数据收集截至2023 年6 月30日。
1.4 治疗方法 马来酸吡咯替尼片(商品名艾瑞妮,江苏恒瑞医药股份有限公司),规格为80 mg。患者按照医嘱服用吡咯替尼片进行治疗,每日1 次,由医生根据乳腺癌治疗指南或共识选择联用药物,治疗直至患者疾病进展或无法耐受。
1.5 不良反应评估 参照美国国立癌症研究所不良事件通用术语标准5.0 版[12](National Cancer Institute Common Terminology Criteria for Adverse Events v5.0,CTCAE v5.0)评估吡咯替尼治疗期间发生的不良事件程度,不良反应分为5 级。
1.6 统计学处理 采用SPSS 16.0 软件进行数据分析,纳入患者的临床特征和不良事件情况采用描述性分析,计数资料用构成比表示。
2 结果
2.1 临床科研大数据平台的构建 第1 层:数据湖。获取医院信息系统、电子病历等临床诊疗数据,做镜像库实时同步,同时创建并接入科研所需数据相关视图,并保留原始数据集。第2 层:全院科研大数据中心。收集临床患者数据后,将以患者为中心的数据集成入搜索引擎中,以倒排索引算法,生成患者词条。数据治理着重非关系型数据,以自然语言后结构化为核心,建立医学词条与患者的映射。第3 层:专病数据库。以检索条件组、专病标签、治疗组等初筛条件形成肿瘤专病库,每日执行筛选条件增量入组。第4 层:科研课题数据库。以课题研究目的为核心创建病例报告表表单,自动抓取患者临床数据与自然语言分析后的病历、病理、检验、检查等文本内容作为研究变量,并提供数据统计分析的工具支撑。临床科研大数据平台架构图详见图2。
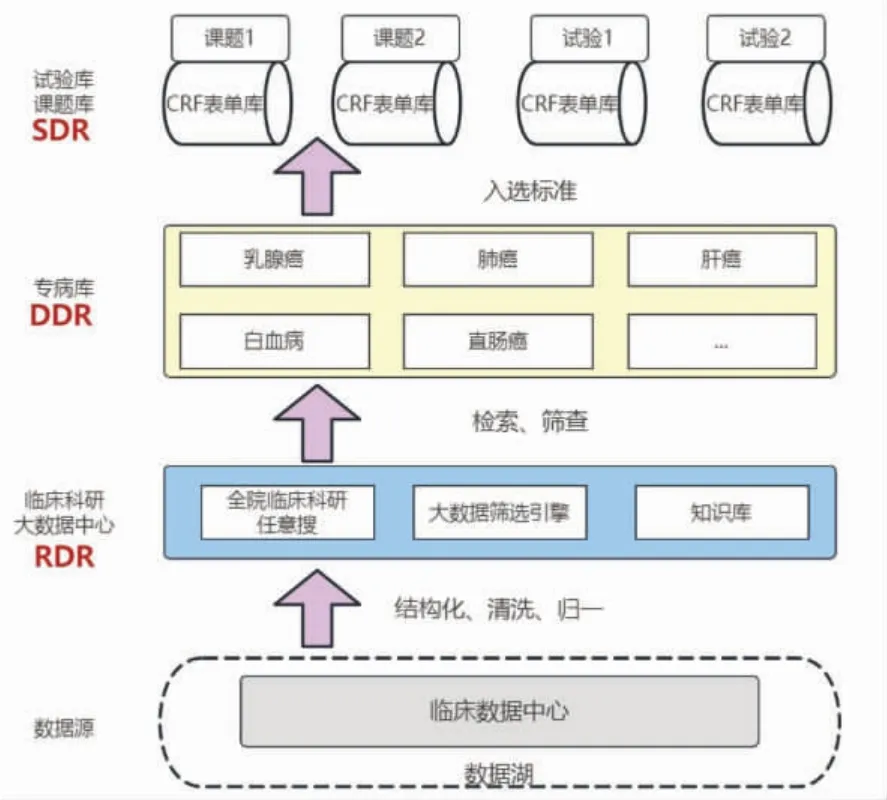
图2 临床科研大数据平台架构图Fig.2 Architecture diagram of clinical research big data platform
2.2 患者临床特征 共计60 例患者符合纳入标准进入吡咯替尼用药分析的研究,均为晚期乳腺癌患者。中位年龄55.5 岁(35~76 岁)。96.7%为浸润性导管癌患者。雌激素受体(ER)和(或)孕激素受体(PR)阳性患者38 例,ER 且PR 阴性患者22 例。75%的患者初次诊断时临床分期是Ⅰ~Ⅲ期(表1)。

表1 60 例患者的临床特征[n(%)]Tab.1 Clinical characteristics of 60 patients[n(%)]
2.3 吡咯替尼治疗情况 51 例(85%)患者初始治疗剂量为400 mg,9 例(15%)为320 mg。具体方案:(1)吡咯替尼+化疗30 例(50%),化疗方案包括:卡培他滨18 例,长春瑞滨3 例,紫杉醇(白蛋白结合型)2 例,艾立布林2 例,依托泊苷2 例,T-DM1 1例,卡培他滨+长春瑞滨1 例,卡培他滨+艾立布林1例。(2)双靶+化疗:吡咯替尼联合曲妥珠单抗/伊尼妥单抗+化疗23 例(38.3%),化疗方案包括:紫杉醇(白蛋白结合型)9 例,卡培他滨5 例,长春瑞滨3例,紫杉醇脂质体3 例,多西他赛2 例,多西他赛+顺铂1 例。(3)吡咯替尼联合内分泌治疗2 例,方案包括:氟维司群2 例。(4)吡咯替尼联合曲妥珠单抗4 例。(5)吡咯替尼单药1 例。
2.4 实验室检查相关不良事件发生情况 在真实世界临床诊疗中,对于用药后患者发生的症状性不良事件(如腹泻、皮疹、疲劳等),医师大多仅对其进行描述,不明确不良事件的具体级别,故本文仅收集实验室检查相关的不良事件,并依据CTCAE 标准进行级别判定。
常见实验室检查相关不良事件(发生率高于10%)依次为:淋巴细胞减少、谷丙转氨酶/谷草转氨酶升高、贫血、白细胞减少、低钾、中性粒细胞减少、尿酸升高、高血糖、高甘油三酯血症。发生率低于10%的不良事件包括低密度脂蛋白升高、低钙、高胆固醇血症、血小板减少、碱性磷酸酶升高和白蛋白减少,以上均为1、2 级不良事件(表2)。
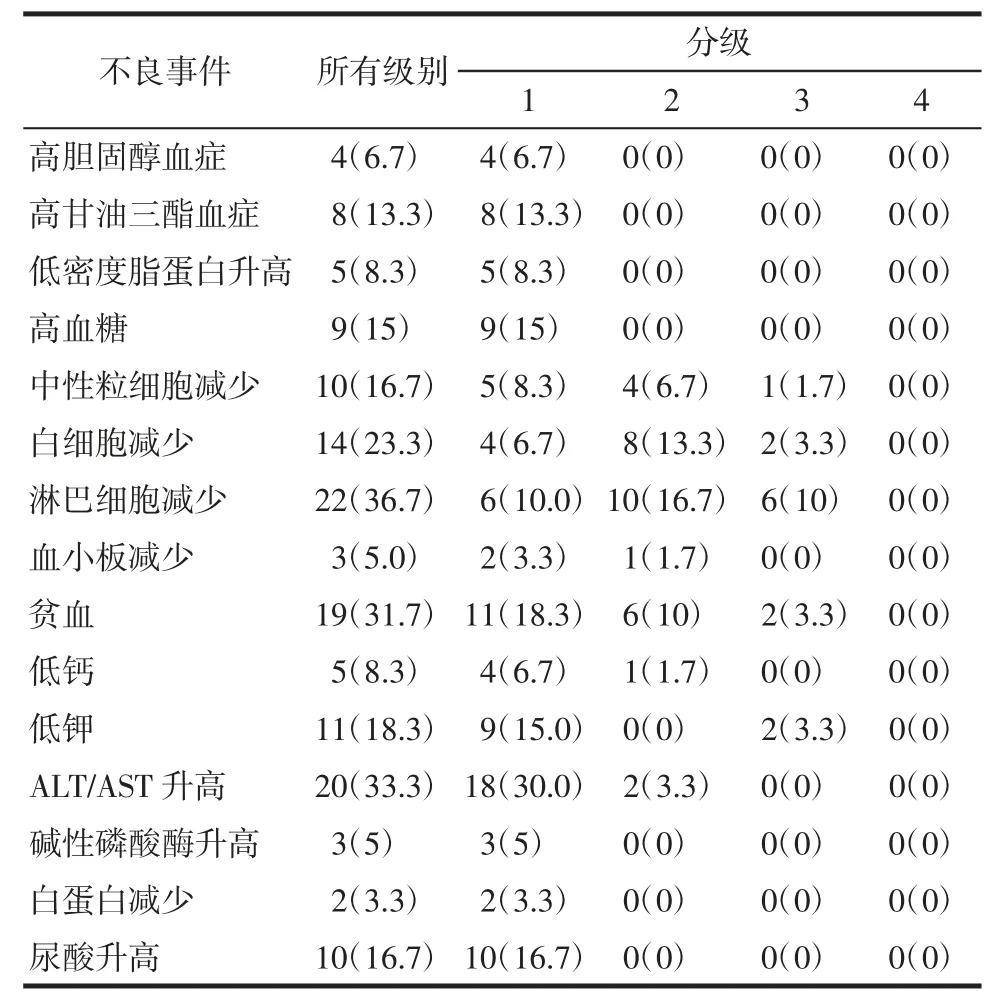
表2 60 例患者实验室检查相关不良事件发生情况[n(%)]Tab.2 Incidence of laboratory adverse events of 60 patients[n(%)]
3 讨论
标准化临床科研大数据平台可实现对临床数据、医院管理数据以及科研数据的标准化组织存储与治理,还支持对原始医院数据模型、数据治理报告、数据资产等的管理工作。数据平台利用AI 技术对海量医疗数据进行筛选、校验,对非结构化数据进行归一、建模[13-14],并支持快速检索出符合研究课题基础条件的患者集合,科研人员可以根据初筛的患者规模初步评估课题可行性。若初筛患者规模符合课题研究要求,可以在平台上建立对应课题的研究项目,并将符合课题要求的患者导入到对应的研究项目中,科研人员可以在项目中根据课题要求对患者集合执行精准纳排、数据提取以及统计分析。
在临床科研大数据平台的基础上,笔者建立了吡咯替尼治疗HER2 阳性晚期乳腺癌安全性分析的科研课题库,抽样50%患者进行临床数据的溯源验证,传输正确率为100%。科研课题库覆盖患者360°全息视图,包含新增患者集、删除患者集、患者分组、支持自定义纳排条件组等设置,可根据项目要求和纳排条件建立、删除、更改患者数据集,导入相应科研项目,并支持患者集手动批量移除。基于强大的字段处理和分析能力,该平台可仅将吡咯替尼用药期间异常的实验室检查结果抓取到科研课题库,大大提高了数据获取和分析的效率。
在乳腺癌真实世界诊疗中,吡咯替尼联合用药方案多样[15-16]。本研究显示,吡咯替尼联合化疗占比最多(50%),联合的化疗药物除了卡培他滨,还可见强效抗微管类药物(如紫杉醇、长春瑞滨和艾立布林)以及抗体药物耦联物类药物T-DM1。38.3%的患者使用了吡咯替尼联合曲妥珠单抗/伊尼妥单抗的双靶方案,联合的化疗药物多为紫杉类药物,少数患者使用了卡培他滨或长春瑞滨。
本研究安全性分析显示,以吡咯替尼为基础的治疗方案常见的实验室相关不良事件为淋巴细胞减少、贫血、白细胞减少、中性粒细胞减少等血液学毒性和肝肾毒性。此外,低钾、高血糖、高甘油三酯血症等不良事件也较为常见。以上实验室检查相关不良事件多为1、2 级,3 级不良事件发生率仅为21.7%,主要为血液学毒性,未见4 级不良事件,与既往文献报道基本一致[16]。以上结果显示,真实世界中以吡咯替尼为基础的治疗方案不良反应可耐受。
