ICU病人耐碳青霉烯类肺炎克雷伯菌血流感染的危险因素与预后分析(附81例报告)
2024-01-09戴赟麒谭若铭刘嘉琳顾飞飞陈尔真王晓丽瞿洪平邱毓祯
刘 萌,徐 文,戴赟麒,谭若铭,刘嘉琳,顾飞飞,陈尔真,王晓丽,瞿洪平,邱毓祯
(上海交通大学医学院附属瑞金医院 a.重症医学科,b.老年医学科,c.微生物科,d.急诊科,上海 200025)
关键字:耐碳青霉烯类肺炎克雷伯菌; 血流感染; 重症病人
近年来,细菌耐药已引起全球关注。作为世界卫生组织分类中具威胁性和耐药性严重的耐碳青霉烯类肠杆菌之一,耐碳青霉烯类肺炎克雷伯菌(carbapenem-resistantKlebsiellapneumoniae, CRKP)感染正在逐渐增加[1]。根据全国细菌耐药监测网的耐药报告,2021 年肺炎克雷伯菌的亚胺培南和美罗培南耐药率仍高达20.4%和21.9%[2]。CRKP 感染通常发生在重症监护病房(intensive care unit,ICU),导致严重的院内感染。这些感染常引起多器官功能障碍和感染性休克,导致住院死亡率增加、住院时间延长和住院费用增加[3-4]。感染性休克、急性生理和慢性健康状况Ⅱ评分(acute physiology and chronic health evaluation Ⅱ score, APACHEⅡ score)、Pitt 菌血症评分(Pitt bacteraemia score,PBS)和Charlson 合并症指数增高是CRKP 血流感染(CRKP bloodstream infection, CRKP-BSI)死亡的独立危险因素[5-6]。基于基线临床特征和感染严重程度的综合风险评估对于CRKP-BSI病人的早期个体化治疗至关重要。
CRKP-BSI 病人的死亡率很高,但不同抗菌药物的疗效因所感染病原微生物不同耐药机制而有差异[7],且临床抗菌药物治疗选择有限,最佳治疗方案依然不确定[8]。近年来,根据中国专家共识,以替加环素和多黏菌素B 为基础的抗菌药物疗法已被推荐并广泛用于耐药革兰阴性杆菌[9]。2019年5月,新型β 内酰胺酶抑制剂复合物头孢他啶/阿维巴坦获准在中国使用。尽管如此,在危重病人中,CRKP-BSI治疗方案的确切治疗效果仍不确定。
因此,本研究回顾2016年6月至2020年6月期间在我院ICU 治疗的CRKP-BSI 病人的临床数据。目的是确定与CRKP-BSI 相关的死亡危险因素,并探索不同抗菌药物疗法在危重病人中的治疗效果。
1 资料与方法
1.1 研究对象
2016 年7 月至2020年6月,所有发生在上海交通大学医学院附属瑞金医院内综合、急诊、呼吸和心脏外科ICU 的CRKP-BSI 事件均被纳入研究。如果病人经历了多次BSI,则仅收集第一次信息。排除标准:怀孕、<18 岁或接受BSI 治疗(经验性或确定性)<48 h;信息不完整。
研究方案获得医院医学伦理委员会批准(2019-1-3)
1.2 数据收集
从住院病历中检索数据,并由2 位ICU 医师独立评估。病人的基本资料、Charlson 合并症指数、入院前30 d 医疗机构暴露情况(包括抗菌药物暴露、ICU 收治、手术、3 个月内免疫抑制治疗和12 个月内住院史)。同时评估BSI 发生时可能的来源、疾病严重程度[APACHE Ⅱ评分、PBS 和序贯性器官功能衰竭评分(sequential organ failure assessment, SOFA)]、器官功能障碍[包括生物标志物,如C反应蛋白和降钙素原(procalcitonin, PCT)、急性肾损伤(acute kidney injury, AKI)、肾脏替代治疗(renal replacement therapy, RRT)、感染性休克和机械通气的使用]、抗菌药物方案,以及28 d 死亡率、住院死亡率、住院时间及ICU 住院总时间。
1.3 微生物培养及药敏试验
所有血培养分离物均在医院的临床微生物实验室处理。使用基质辅助激光解吸/电离飞行时间技术进行细菌种类鉴定,VITEK 2 Compact 全自动微生物鉴定及药敏系统进行药物敏感性测试,仪器均来自bioMérieux 公司(Marcy-l'Etoile, France)[10]。最小抑菌浓度(minimum inhibitory concentration,MIC)根据美国临床实验室标准协会 (Clinical and Laboratory Standards Institute, CLSI)建立的折点进行分类。耐碳青霉烯类肠杆菌科细菌(carbapenemresistant enterobacteriaceae, CRE)的定义基于CLSI指南,碳青霉烯耐药性定义为对以下至少1 项的体外耐药:厄他培南(MIC≥2 mg/L)、亚胺培南(MIC≥4 mg/L)或美罗培南(MIC≥4 mg/L,抑菌圈≤19 mm)[11]。
1.4 定义
CRKP-BSI 指至少有1次CRKP 阳性血液培养,且临床征象符合[12]。BSI 发生时间指采集第1 次阳性血液培养的日期。在收到血液培养报告之前,临床医师可选择经验性抗菌药物治疗[13]。使用替加环素和(或)除多黏菌素B 外的任何其他抗菌药物治疗被认为是基于替加环素的治疗;任何涉及多黏菌素B 的治疗均被认为是基于多黏菌素B 的治疗[14-15]。联合治疗是1 种以上体外活性抗菌药物的方案[16-17]。
1.5 研究目标
主要终点是28 d死亡率;对生存和死亡病人进行亚组分析,评估死亡危险因素。分析、比较以替加环素与多黏菌素B 为基础的抗菌药物治疗疗效。还包括基于年龄(≤65 岁比>65 岁)、性别、体质量指数(body mass index, BMI)(≤25 kg/m2比>25 kg/m2)、APACHE Ⅱ评分(≤20 分比>20 分)、有无RRT 以及有无机械通气的亚组分析。
1.6 统计学分析
使用SPSS 23.0 软件进行统计学分析。计数资料以频率和百分比描述,采用卡方检验或Fisher 精确检验进行比较。正态分布的计量资料以±s描述,非正态分布的以M(P25,P75)描述,采用Studentt检验或Mann-WhitneyU检验进行比较。将单变量分析中显著的变量(P<0.1)添加到逐步多元逻辑回归模型中,以确定28 d 死亡率的独立风险因素。使用Kaplan-Meier 法进行生存分析。Cochran-Mantel-Haenszel 检验用于各亚组分析(年龄、性别、BMI、APACHEⅡ评分、RRT 和机械通气)。所有统计检验均报告为双尾检验,P<0.05为差异有统计学意义。
2 结果
2.1 CRKP-BSI病例资料
本研究纳入81例CRKP-BSI病人,其中男63例(77.78%),女18例(22.22%),病人基本临床特征见表1。菌血症常见的来源是腹腔感染(46 例,56.79%)、呼吸道感染(18 例,22.22%)。BSI 发生时,51.85%(42 例)和75.31%(61 例)的病人发生AKI 和感染性休克,29 例(35.80%)病人接受RRT,65 例(80.25%)病人需机械通气支持。CRKP-BSI发生后的平均APACHE Ⅱ评分为24(18, 28)分,SOFA 评分为8(6, 11)分。28 d 死亡率和住院死亡率分别为54.32%(44/81)和65.43%(53/81)。
表1 病人临床特征及CRKP-BSI危重病人28 d全因死亡率相关因素分析[±s/M(P25,P75)/n(%)]Tab 1 Clinical characteristics and analysis of factors associated with 28-day all-cause mortality of critically ill patients with CRKP-BSI [±s/M(P25,P75)/n(%)]
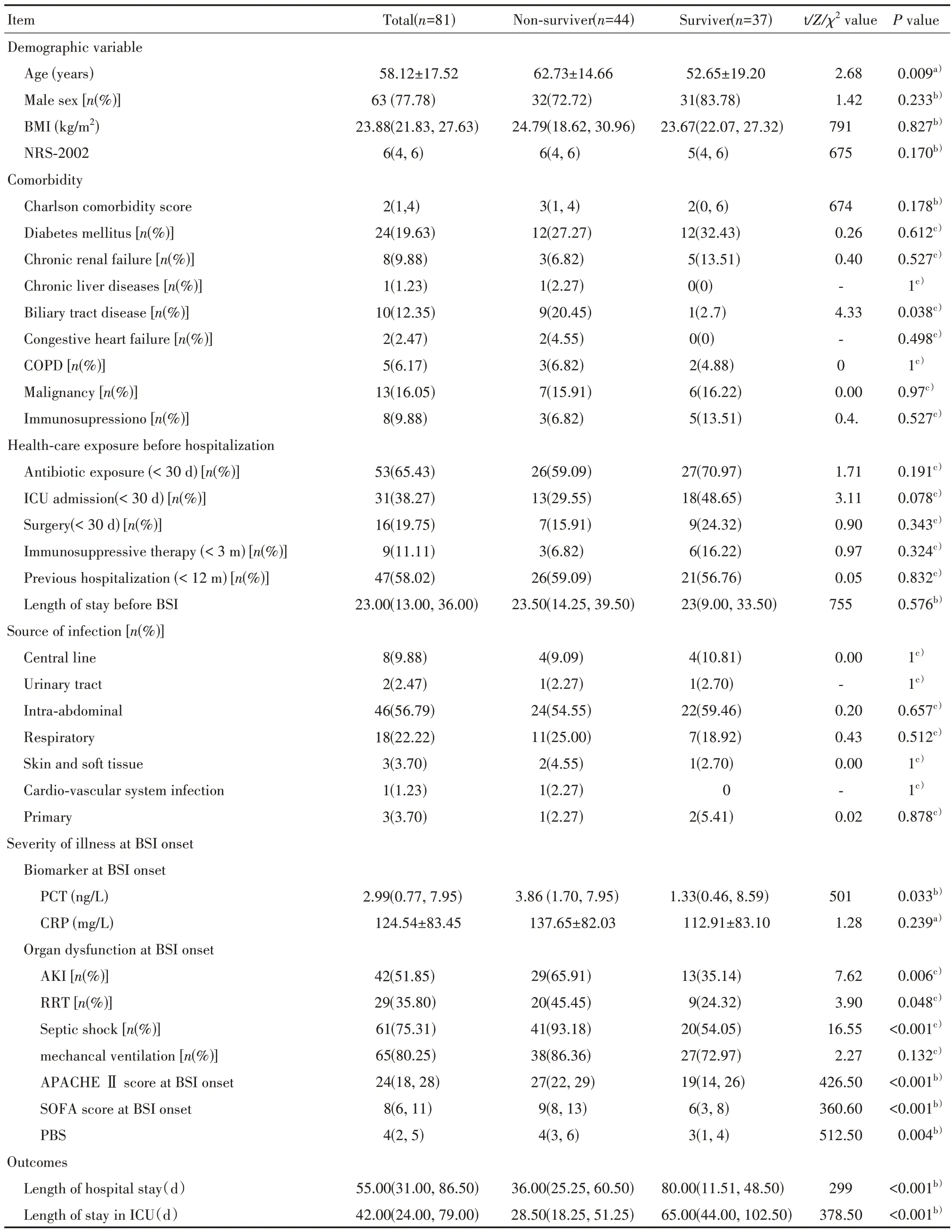
表1 病人临床特征及CRKP-BSI危重病人28 d全因死亡率相关因素分析[±s/M(P25,P75)/n(%)]Tab 1 Clinical characteristics and analysis of factors associated with 28-day all-cause mortality of critically ill patients with CRKP-BSI [±s/M(P25,P75)/n(%)]
BMI: body mass index; COPD: chronic obstructive pulmonary disease; PCT: procalcitonin; CRP: C reaction protein a): t-test; b): Mann-Whitney U test; c): Chi-squared test
Item Demographic variable Age (years)Male sex [n(%)]BMI (kg/m2)NRS-2002 Comorbidity Charlson comorbidity score Diabetes mellitus [n(%)]Chronic renal failure [n(%)]Chronic liver diseases [n(%)]Biliary tract disease [n(%)]Congestive heart failure [n(%)]COPD [n(%)]Malignancy [n(%)]Immunosupressiono [n(%)]Health-care exposure before hospitalization Antibiotic exposure (< 30 d) [n(%)]ICU admission(< 30 d) [n(%)]Surgery(< 30 d) [n(%)]Immunosuppressive therapy (< 3 m) [n(%)]Previous hospitalization (< 12 m) [n(%)]Length of stay before BSI Source of infection [n(%)]Central line Urinary tract Intra-abdominal Respiratory Skin and soft tissue Cardio-vascular system infection Primary Severity of illness at BSI onset Biomarker at BSI onset PCT (ng/L)CRP (mg/L)Organ dysfunction at BSI onset AKI [n(%)]RRT [n(%)]Septic shock [n(%)]mechancal ventilation [n(%)]APACHE Ⅱ score at BSI onset SOFA score at BSI onset PBS Outcomes Length of hospital stay(d)Length of stay in ICU(d)Total(n=81)58.12±17.52 63 (77.78)23.88(21.83, 27.63)6(4, 6)2(1,4)24(19.63)8(9.88)1(1.23)10(12.35)2(2.47)5(6.17)13(16.05)8(9.88)53(65.43)31(38.27)16(19.75)9(11.11)47(58.02)23.00(13.00, 36.00)8(9.88)2(2.47)46(56.79)18(22.22)3(3.70)1(1.23)3(3.70)2.99(0.77, 7.95)124.54±83.45 42(51.85)29(35.80)61(75.31)65(80.25)24(18, 28)8(6, 11)4(2, 5)55.00(31.00, 86.50)42.00(24.00, 79.00)Non-surviver(n=44)62.73±14.66 32(72.72)24.79(18.62, 30.96)6(4, 6)3(1, 4)12(27.27)3(6.82)1(2.27)9(20.45)2(4.55)3(6.82)7(15.91)3(6.82)26(59.09)13(29.55)7(15.91)3(6.82)26(59.09)23.50(14.25, 39.50)4(9.09)1(2.27)24(54.55)11(25.00)2(4.55)1(2.27)1(2.27)3.86 (1.70, 7.95)137.65±82.03 29(65.91)20(45.45)41(93.18)38(86.36)27(22, 29)9(8, 13)4(3, 6)36.00(25.25, 60.50)28.50(18.25, 51.25)Surviver(n=37)52.65±19.20 31(83.78)23.67(22.07, 27.32)5(4, 6)2(0, 6)12(32.43)5(13.51)0(0)1(2.7)0(0)2(4.88)6(16.22)5(13.51)27(70.97)18(48.65)9(24.32)6(16.22)21(56.76)23(9.00, 33.50)4(10.81)1(2.70)22(59.46)7(18.92)1(2.70)0 2(5.41)1.33(0.46, 8.59)112.91±83.10 13(35.14)9(24.32)20(54.05)27(72.97)19(14, 26)6(3, 8)3(1, 4)80.00(11.51, 48.50)65.00(44.00, 102.50)t/Z/χ2 value 2.68 1.42 791 675 674 0.26 0.40-4.33-0 0.00 0.4.1.71 3.11 0.90 0.97 0.05 755 0.00-0.20 0.43 0.00-0.02 501 1.28 7.62 3.90 16.55 2.27 426.50 360.60 512.50 299 378.50 P value 0.009a)0.233b)0.827b)0.170b)0.178b)0.612c)0.527c)1c)0.038c)0.498c)1c)0.97c)0.527c)0.191c)0.078c)0.343c)0.324c)0.832c)0.576b)1c)1c)0.657c)0.512c)1c)1c)0.878c)0.033b)0.239a)0.006c)0.048c)<0.001c)0.132c)<0.001b)<0.001b)0.004b)<0.001b)<0.001b)
2.2 CRKP-BSI病人28 d死亡率的危险因素
单因素分析表明,死亡病人比生存病人年龄更大(P=0.009)。两组间男性比例、BMI 和营养风险筛查2002 评分相似;然而,死亡病人患有胆道疾病可能性更高(P=0.038)。两组病人发生BSI 前的医疗机构暴露时间及住院时间相似。除原发性BSI病人外,其余不同感染源组间死亡率相似。所有原发性BSI 的病人均未死亡。在BSI 发作时,死亡病人的PCT 水平较高(P=0.033);AKI 和感染性休克的频率较高(P=0.006;P<0.001);需RRT 病人更多(P=0.048);两组间机械通气比例差异无统计学意义(P=0.132)。此外,死亡病人的APACHE Ⅱ评分(P<0.001)、SOFA 评分(P<0.001)和PBS(P=0.004)更高。住院时间和ICU 住院时间较短(P均<0.001)(见表1)。
多因素分析发现,入院前患胆道疾病及BSI 发生时SOFA 评分升高是病人28 d 全因死亡的危险因素,而住院时间较长,28 d 死亡率则较低(见表2)。

表2 CRKP-BSI 危重病人28 d 全因死亡率的多因素Logistic回归分析Tab 2 Multivariate Logistic regression analysis of predictors of 28-day all-cause mortality of critically ill patients with CRKP-BSI
2.3 CRKP-BSI危重病人的抗菌药物应用情况
81 例CRKP-BSI 病人的抗菌药物治疗和结果见表3。6 例(7.41%)单药治疗,替加环素4 例、多黏菌素B 1 例及头孢他啶-阿维巴坦1 例;75 例接受联合治疗(92.59%),最常见的联合药物包括碳青霉烯(58 例,71.60%),替加环素(40 例,49.38%)、多黏菌素B(25 例,30.86%)、阿米卡星(9 例,11.11%)、磷霉素(13 例,16.05%)和头孢他啶-阿维巴坦(3 例,3.70%)。根据抗菌药物选择情况,分为3 种治疗方案:以替加环素为基础(44 例,54.32%)、以多黏菌素B 为基础(26 例,32.10%)和其他(11 例,13.58%)。3 组的28 d 死亡率差异无统计学意义(56.82%、57.69% 和36.36%,P=0.715)。

表3 CRKP-BSI病人抗菌药物方案Tab 3 Details of antibiotic regimens of patients with CRKP-BSI
2.4 替加环素与多黏菌素B 为基础抗菌方案的效果比较
替加环素组和多黏菌素B 组的人口统计学和临床特征见表4。多黏菌素B 组的病人年龄(64.15±14.29)岁高于替加环素组(55.73±19.49)岁,P=0.041。多黏菌素B 组的男性比例较低(61.54%比88.64%,P=0.008)。血流感染发生后,两组间临床特征或疾病严重程度差异无统计学意义。
表4 替加环素组与多黏菌素B组的一般资料和临床特征比较[±s/M(P25,P75)/n(%)]Tab 4 Comparation of the demographics and clinical characteristics between tigecycline- and polymyxin B-based regimen group [±s/M(P25,P75)/n(%)]
a): t-test; b): Mann-Whitney U test; c): Chi-squared test
Item Demographic variables Age (years)Male sex [n(%)]Body mass index (kg/m2)NRS-2002 Comorbidities Charlson comorbidity index Diabetes mellitus [n(%)]Chronic renal failure [n(%)]Chronic liver diseases [n(%)]Biliary tract disease [n(%)]Congestive heart failure [n(%)]COPD [n(%)]Malignancy [n(%)]Immunosuppression [n(%)]Health-care exposure before hospitalization [n(%)]Antibiotic exposure (< 30 d)ICU admission (< 30 d)Surgery (< 30 d)Immunosuppressive therapy (< 3 months)Previous hospitalization (< 12 months)Source of infection [n(%)]Central line Urinary tract Intra-abdominal Respiratory Skin and soft tissue Cardio-vascular system infection Primary Severity of illness at BSI onset Biomarker at BSI onset PCT (ng/L)CRP (mg/L)Organ dysfunction at BSI onset AKI [n(%)]RRT [n(%)]Septic shock [n(%)]Mechanical ventilation [n(%)]APACHE Ⅱ score SOFA score Pitt bacteremia score Outcomes 28-day mortality [n(%)]In-hospital mortality [n(%)]Length of stay(d)Length of stay before BSI(d)Length of stay in ICU(d)Tigecycline-based regimens (n=44)55.73±19.49 39(88.64)25.51±4.06 5(4, 6)2(0, 4)12(27.27)4(9.09)0 4(9.09)0 3(6.82)6(13.64)1(2.27)28(63.64)17(38.64)8(18.18)2(4.55)29(65.12)5(11.36)0 28(63.63)7(15.91)2(4.55)1(2.27)1(2.27)2.55(0.89, 7.95)133.39±84.90 24(54.55)17(38.63)36(81.82)39(88.64)24.07±7.41 8.00(6.00, 11.00)4.00(3.00, 5.00)25(56.82)29(65.91)63.00 ± 43.02 23.00(12.00, 34.00)41(26, 79)Polymyxin B-based regimens (n=26)64.15±14.29 16(61.54)23.60±5.85 6(4, 6)3(1.75, 4.25)8(30.77)3(11.54)1(3.85)6(23.08)2(7.69)1(3.85)6(23.08)3(11.54)18(69.23)10(38.46)6(23.08)3(11.54)12(46.15)2(7.69)1(3.85)12(46.15)9(34.62)1(3.85)0 1(3.85)3.96(0.81, 14.59)137.78±81.24 15(57.69)10(38.46)20(76.92)20(76.92)23.15±8.56 8.00(5.75, 11.25)4.00(2.75, 6.00)15(57.69)18(69.23)69.88±45.57 24.50(14.50, 54.50)51(21, 81)t/Z/χ2 value-2.08 7.13 1.61 0.25 0.25 0.1.0.00-1.59-0.00 0.47 1.17 0.23 0.00 0.25 0.38 2.63 0.01-2.04 3.24 0.00--1.64-0.20 0.07 0.00 0.25 0.92 0.44 0.02 0.136 0.01 0.08-0.63 0.46 0.25 P value 0.041a)0.008c)0.112a)0.303b)0.125b)0.754c)1.0c)0.371c)0.207c)0.135c)1.0c)0.494c)0.280c)0.634c)0.988c)0.621c)0.537c)0.105c)0.934c)0.371c)0.153c)0.072c)1c)1c)1c)0.635b)0.842a)0.798c)0.998c)0.621c)0.336c)0.663a)0.864b)0.712b)0.943c)0.775c)0.529a)0.429b)0.822b)
替加环素组与多黏菌素B 组28 d 死亡率差异无统计学意义(56.82%比57.69%,P=0.943)。28 d生存曲线如图1所示(P=0.811)。
此外,为了阐明疾病严重程度的一些变量和指标对以替加环素和多黏菌素B 为基础治疗结果的影响,根据病人的年龄(≤65 岁比>65 岁)、性别、BMI(≤25 kg/m2比>25 kg/m2)、APACHEⅡ评分(≤20比>20)、RRT 使用和机械通气使用情况,将病人分为6 个亚组。在亚组分析中,两组抗菌药物间28 d死亡率差异无统计学意义(见图2)。
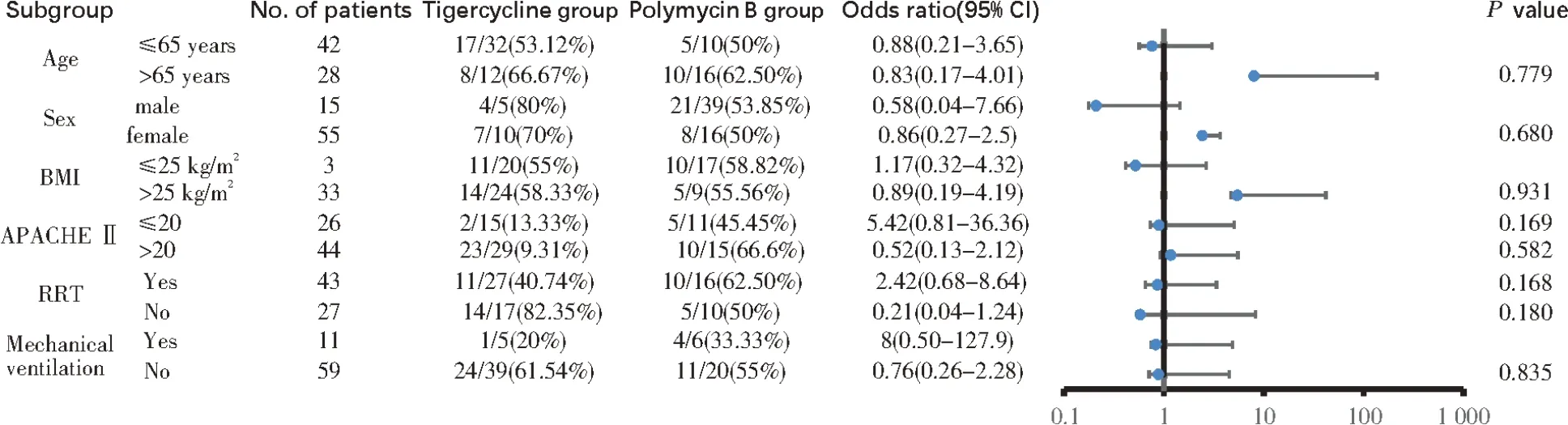
图2 不同亚组分析评估替加环素组与多黏菌素B组的疗效Fig 2 Therapeutic efficacy assessment of tigecycline- and polymyxin B-based antimicrobial regimens by different subgroup analysis
3 讨论
CRKP 感染是世界范围内危及生命的健康问题。与CRKP-BSI 相关的死亡率(33%~70%)是发生在其他身体部位感染的3 倍[18]。与对碳青霉烯类敏感的肺炎克雷伯菌BSI 相比,有留置胃管、碳青霉烯类使用史、低蛋白血症以及APACHE Ⅱ评分高的非移植病人,CRKP-BSI的风险增加[5]。危重病人感染CRKP-BSI的风险更高,因为其病情更重、应用免疫抑制和频繁使用侵入性手术;ICU 获得性感染已被证明是导致CRKP-BSI发展的强大致病因素[3]。值得注意的是,病人群体的异质性,如感染源、潜在疾病严重程度以及发病时严重程度,对于评估CRKP-BSI 预后很重要。这些BSI 难以根除,最终会扩散全身,甚至致死。因此,评估CRKP-BSI的疾病特征、住院死亡风险因素和治疗结果非常重要。
本研究分析81 例危重病人CRKP-BSI 死亡率和治疗结果的危险因素。APACHEⅡ和SOFA的平均评分以及28 d 死亡率均高于先前报道。较高的死亡率可能归因于菌血症来源的差异和病人疾病严重程度的异质性。CRKP-BSI 的感染源对预后影响大,PANORAMA 研究显示,原发性BSI 是最主要来源(48%),其次是胃肠道感染(21%)[19]。EUROBACT 研究显示,原发性血流感染(23.7%)和导管相关感染(21.4%)是常见的来源,以下是呼吸道(21.1%)和腹腔内感染(11.6%)[20]。本研究病人多有复杂腹腔感染和呼吸道感染,分别占总人数的56.79%和22.22%,28 d 死亡率54.55%和25.00%。腹腔感染通常需要多次引流治疗,且效果难以评估[21]。呼吸道感染的引流问题可能与不良预后相关[22]。此外,病人的潜在状况和疾病严重程度直接影响预后。本研究死亡相关危险因素与之前报道一致,包括年龄较大、胆道疾病、高水平PCT;高APACHE Ⅱ评分、SOFA 评分和PBS;以及BSI 发生时出现AKI和感染性休克。此外,多因素分析结果显示,入院前患胆道疾病及BSI 发生时SOFA 评分升高是28 d 死亡的危险因素[6,23]。因此,死亡风险高低基于BSI 发病时的疾病严重程度,应尽早实施充分的源头控制和适当的抗菌治疗[24-25]。另外,报道肺炎克雷伯菌在胃肠道定植率高达77%。胆道疾病反复发作导致抗菌药物应用增加,增加耐药菌定植的风险。在免疫低下、屏障受损等情况下,由定植转为局部甚至全身感染[26]。
针对CRKP 的抗菌药物治疗选择非常有限,替加环素和黏菌素/多黏菌素B 已被中国多药耐药革兰阴性杆菌治疗共识小组推荐,并在国内广泛使用[9],并且成为侵袭性感染的首选药物[27]。一项回顾性队列研究发现,82 例CRKP-BSI 病人中,联合治疗(多黏菌素B 联合阿米卡星)可降低30 d 死亡率(37.5%比64.75%,P=0.01)[28]。然而,多黏菌素B治疗过程中,有剂量不足、治疗失败、不良反应和异质性耐药的报道[29]。替加环素是一种广谱甘氨酰环肽抗菌药物,在体外显示出抗CRE 的活性。由于剂量不足和血清浓度低,替加环素对CRE 感染,尤其是BSI的疗效存在争议[30]。一项多因素分析表明,替加环素的使用是CRKP-BSI 发展的独立危险因素(OR=3.915,P=0.005)[31]。然而,另有研究显示,替加环素组的总体死亡率与对照组相似(OR=0.96,95%CI: 0.72~1.22;P=0.73),且联合治疗和高剂量方案疗效更好,亚组分析无显著的不良反应[32]。这些数据强调了在高危重症病人中联合抗菌治疗CRKP-BSI 的效用[17,33]。本研究联合应用抗菌药物治疗CRKP-BSI,分别有40例和25例接受替加环素或多黏菌素B 联合治疗。尽管联合治疗的使用率很高,但28 d 死亡率仍保持在50%以上,这表明需要重新思考和评估这两种药物的疗效。
抗菌药物治疗与预后相关,很少有研究在真实世界中比较多黏菌素B 与替加环素的治疗效果。一项研究分析中国台湾16 家医院64 例由CRKP 和耐碳青霉烯类大肠埃希菌引起的血液感染病人,结果提示接受黏菌素单药治疗的病人死亡率高于接受替加环素单药疗法的病人(57.1%比19.2%,P=0.035)[34]。然而,Shen 等[14]进行回顾性研究,纳入89 例CRKP-BSI 病人,与替加环素治疗相比,接受多黏菌素B 治疗的病人显示出生存益处(风险比为0.068,95%CI: 0.018~0.260,P<0.001)。然而,由于人群疾病的异质性,这些结论不宜推广到其他情况的病人。本研究包括44 例接受替加环素治疗的病人和26 例接受多黏菌素B 治疗的病人;两者的死亡率均较高,且亚组分析中都没有观察到显著的组间差异。头孢他啶-阿维巴坦和其他酶抑制剂已成为CRKP-BSI 治疗的新选择,需要进一步的临床研究来评估临床疗效[35-36]。
本研究有一些局限性。首先,回顾性研究存在不可避免的偏倚。其次,病原体相关因素,如详细的药物敏感性测试和耐药性基因检测,并未进一步分析。第三,关于抗菌药物的药物剂量和疗程,未记录。第四,未分析病人的免疫状态。第五,是小样本单中心研究。需进一步精心设计多中心前瞻性研究来证明这两种药物的疗效。
CRKP-BSI 的危重病人预后较差和死亡率较高。较高的SOFA 评分、既往胆道疾病病史是28 d死亡率的独立危险因素。在以替加环素和多黏菌素B 为基础的联合治疗下,28 d 的死亡率仍较高,并且两种方案的疗效差异无统计学意义。在目前治疗CRKP 感染的药物有限的时代,应对携带CRKP 的病人进行防控,防止耐药微生物在高危病人中传播。
