神经节苷脂联合亚低温治疗新生儿缺氧缺血性脑病的疗效及对患儿行为智能发育影响
2024-01-05武育菁
杨 夏, 武育菁
(江苏省徐州市儿童医院 新生儿内科, 江苏 徐州 221000)
新生儿缺氧缺血性脑病(hypoxic-ischemic encephalopathy,HIE)是临床上严重威胁新生儿生命安全的一种疾病,其可以对患儿神经功能造成损害,导致患儿残疾甚至死亡[1]。缺氧是HIE发病的主要原因,患儿常表现为肌张力异常、颅内压升高等。为避免病情恶化造成器官进一步受损,需要对患儿进行及时治疗。神经节苷脂对神经细胞的再生和神经细胞膜的恢复有明显促进作用,可以减轻脑部炎性反应,在各种血管性神经损伤疾病中表现良好。亚低温物理疗法治疗HIE,其对于脑损伤有明显抑制作用,能有效保护患儿脑部神经。有研究表明,在药物的基础上联合亚低温治疗HIE,能有效提高疗效,促进患儿神经功能恢复[2]。基于此,本研究将神经节苷脂和亚低温联合应用于HIE的临床治疗中,观察其疗效和对患儿血清相关指标的影响,报告如下。
1 资料与方法
1.1研究对象:选取2018年1月至2022年12月本院收治的148例HIE患者,通过随机数字表采用简单随机分组法分为实验组和对照组,每组各74例。两组患者一般资料比较差异无统计学意义(P>0.05),见表1。纳入标准:符合HIE的临床诊断标准[3],临床表现:明确相关产科病史(导致胎儿宫内窘迫),胎儿出生时有明显重度窒息症状,不久后呈现异常神经系统状态,经MRI确诊;患儿体重>2.5kg;均为足月儿;预计生存期≥15d;HIE病情程度为中、重度患儿;临床资料完整;入院前未进行任何治疗;患儿家属签署知情同意书。其中病情程度判定标准[4]:①中度:患儿肌张力减低,原始反射减弱,常有惊厥发生,嗜睡,瞳孔缩小,伴随轻微呼吸衰竭。②重度:患儿呈昏迷状,肌张力松软,无原始反射,持续性发生惊厥,瞳孔扩大或不对称,伴随明显呼吸衰竭。排除标准:合并先天性脑萎缩等脑部疾病;对本研究药物不耐受者;糖尿病妊娠儿;合并严重感染者;合并免疫功能不全者;颅内出血者。本研究经医学委员会同意。
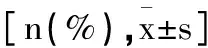
表1 一般资料比较
1.2方法:入院后,两组患儿均给予相应的基础治疗:①结合患儿孕周、肺成熟度,给予吸氧或机械通气,维持患儿正常呼吸水平;②维持患儿正常血糖水平,对其颅内压进行监控;③静脉滴注补充患儿机体所需维生素C,并适当对患儿进行早期听、触和视觉的训练。对照组在此基础上使用神经节苷脂(西南药业股份有限公司,国药准字H20093712,规格:2mL∶20mg)治疗,20mg神经节苷脂混合20mL葡萄糖注射液(浓度为5%),行静脉滴注,1次/d。实验组在对照组基础上进行头部亚低温治疗:使用6~12℃降温帽将患儿头部包裹,在其前额中间放置温度探头,监测并维持患儿体表温度在33℃左右,治疗维持3d。治疗结束后等待6h患儿自然复温,也可使用远红外线辐射加速复温(升温速度0.2~0.5℃/h)。两组均连续治疗14d。
1.3观察指标:①疗效:治疗后,依照相关指南[5]对两组疗效进行评估:患儿体征恢复正常,无临床HIE症状,惊厥消失为显效;症状和体征明显改善为有效;症状和体征均无改善甚至恶化为无效。(显效+有效)/总例数×100%=总有效率。②新生儿行为神经评分[6](neonatal behavioral neurological assessment,NBNA):治疗前及治疗3、7和14d后,对两组行为神经功能进行评分,包括五个方面(行为能力、被动肌张力、主动肌张力、原始反射和一般评估),共20项,每项2分,共计40分,得分与患儿行为神经功能成正比。③临床表现恢复时间:治疗后,比较两组原始反射、肌张力、吸吮和眼部运动功能恢复的时间及呼吸衰竭纠正的时间。④智能发育:治疗前后,采用智能发育商数(development quotient,DQ)对两组智能发育情况进行评估,主要包括大运动、精细运动和适应性行为三个指标,每项指标满分100分,得分与智能发育水平成正比[7]。⑤神经损伤标志物:治疗前后,抽取患儿股静脉血3mL,取上清,采用ELISA法检测两组S100β蛋白、神经元特异性烯醇化酶(neuron-specific enolase,NSE)和髓磷脂碱性蛋白(myelin basic protein,MBP)水平。(6)血清炎性因子:治疗前后,取两组股静脉血5mL,取上清,采用ELISA法对两组白细胞介素-8(interleukin-8,IL-8)、超敏C反应蛋白(hypersensitive C-reactive protein,hs-CRP)和肿瘤坏死因子-α(tumor necrosis factor alpha,TNF-α)水平进行测定。

2 结 果
2.1两组患者疗效比较:治疗后,实验组治疗总有效率高于对照组,差异显著(P<0.05),见表2。
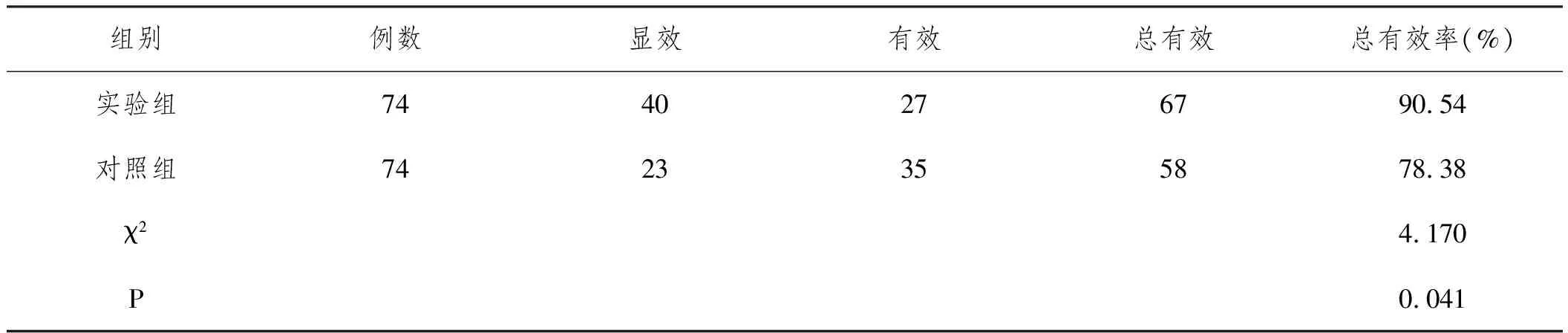
表2 两组患者疗效比较
2.2NABA比较:重复测量方差分析结果显示,治疗前后NABA评分组间效应、时间效应、分组与时间交互作用均有统计学意义,实验组、对照组治疗后NABA评分呈升高趋势,且实验组治疗后各时间点NABA评分均高于对照组(P<0.05),见表3。
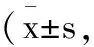
表3 NABA比较分)
2.3临床表现恢复时间比较:治疗后,实验组各临床表现恢复时间明显短于对照组(P<0.05),见表4。
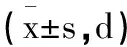
表4 临床表现恢复时间比较
2.4智能发育水平比较:治疗前,两组智能发育各指标得分比较(P>0.05);治疗后,两组智能发育各指标大运动、精细运动、适应性评分均较治疗前升高,且实验组升高值大于对照组(P<0.05),见表5。
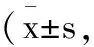
表5 智能发育水平比较分)
2.5神经损伤标志物水平比较:治疗前,两组神经损伤标志物水平比较(P>0.05);治疗后,两组神经损伤标志物S100β蛋白、NSE和MBP水平均较治疗前降低,且实验组降低值大于对照组(P<0.05),见表6。

表6 神经损伤标志物水平比较
2.6炎性因子水平比较:治疗前,两组炎性因子水平比较,差异无统计学意义(P>0.05);治疗后,两组炎性因子IL-8、hs-CRP和TNF-α水平均较治疗前降低,且实验组降低值大于对照组(P<0.05),见表7。

表7 炎性因子水平比较
3 讨 论
临床上HIE发生的主要原因是围产期窒息,其会导致患儿脑部缺氧影响神经功能[8]。HIE的临床症状为癫痫、痉挛等,其死伤率高达30%,给患儿家庭带来严重不良影响[9]。神经节苷脂是一种含唾液酸的鞘糖脂,在神经系统中含量较多,其可以加快神经组织的修复,改善神经传导,具有一定的神经保护作用[10]。相关研究显示,亚低温疗法对炎性因子的释放有明显抑制作用,能改善HIE患儿脑缺血再灌注损伤,对神经功能有一定程度的保护效果[11]。
本研究结果发现,实验组治疗总有效率、各时间点NABA得分和智能发育各指标得分明显高于对照组,且实验组各临床表现恢复时间明显短于对照组,提示神经节苷脂联合亚低温治疗HIE拥有较好疗效,能改善患儿的行为神经功能和智能发育水平,加快临床症状恢复。头部亚低温通过人工诱导使HIE患儿头部温度降低,以此减缓机体的脑细胞代谢速率,对无氧酵解过程也有明显抑制作用,进而延迟患儿发生继发性能量衰竭,使患儿脑部神经损伤得到减轻,改善其神经功能[12]。存活的HIE患儿会出现不同程度的神经系统损伤,相关神经后遗症会很大程度上影响其智能发育,但两岁以内的新生儿脑部细胞发育较快,拥有较高的代偿功能和可塑性,使用头部亚低温对其进行治疗后,可以缓解患儿脑部血管痉挛,改善脑部血流动力学,减少患儿神经相关后遗症的发生率,进一步改善其神经行为功能和智能发育水平。联合神经节苷脂治疗,可以进一步调控神经细胞的生长和分化,增强脑部供血能力,缓解患儿的病情,疗效更佳。S100β蛋白对细胞形态有调节效能,能影响神经的可可塑性,其水平越高,反应机体神经损伤越严重;NSE是一种分布于中枢神经的催化酶,能维持神经细胞正常的生理共功能,神经受损后其会渗入外周血;MBP 在机体神经受损后,会释放入外周血,病情越重,其水平越高。实验组S100β蛋白、NSE和MBP水平明显低于对照组,提示联合治疗可以有效降低机体神经损伤标志物水平。头部亚低温可以对内源性毒性物质起到抑制作用,避免脑细胞结构蛋白受到破环,进而起到保护脑细胞的效果。联合神经节苷脂治疗可以减轻患儿的神经毒性,对神经细胞由明显保护作用,改善其神经功能,进一步降低神经损伤标志物的水平。王葆辉等[13]认为,选择性头部亚低温可有效保护HIE患儿脑功能,改善神经运动发育结局。IL-8可以加重神经细胞炎症反应,加快神经细胞凋亡,对中枢神经造成严重损害;hs-CRP是一种与免疫调节相关的蛋白,机体缺氧感染后,其水平上升;TNF-α多存在于神经元中,其含量会随着机体缺血或缺氧而增加。本研究中实验组IL-8、hs-CRP和TNF-α水平明显低于对照组,提示联合治疗可有效减轻患儿炎性反应,这与上述研究结果一致。患儿脑部缺氧会引起神经细胞受损,局部水肿会引起机体发生炎性反应。头部亚低温治疗通过低温使得脑部耗能降低,抑制兴奋性神经递质的释放,对钙离子的聚集有抑制作用,进而阻止患儿神经细胞的凋亡,减轻脑部水肿,抑制氧自由基的生成,对氧化和氮化应激引起的脂质过氧化有明显抑制作用,减少其造成的神经毒性和损伤,进一步降低患儿体内炎性因子水平[14]。
综上所述,神经节苷脂联合亚低温治疗HIE,其疗效良好,能有效改善患儿的行为神经功能和智能发育水平,缩短原始反射、肌张力、吸吮和眼部运动功能恢复的时间及呼吸衰竭纠正的时间,同时其能降低患儿体内炎性因子和神经损伤标志物的水平。
