冠心病合并射血分数降低患者血运重建策略:经皮冠状动脉介入治疗和冠状动脉旁路移植术的对比研究
2024-01-04王韶屏刘严慈吴铮郑泽彭红玉赵东晖李芳程姝娟柳景华
王韶屏 刘严慈 吴铮 郑泽 彭红玉 赵东晖 李芳 程姝娟 柳景华
心力衰竭(heartfailure,HF)是全球性疾病,冠状动脉粥样硬化性心脏病(简称冠心病,coronary artery disease,CAD)是HF的最常见原因之一[1-4]。对CAD合并左心室射血分数(lef t ventricular ejection fraction,LVEF)减低的患者,在优化药物治疗基础上,积极的血运重建治疗包括经皮冠状动脉介入治疗(percutaneous coronary in terven tion,PCI)[5-7]和冠状动脉旁路移植术(coronary artery bypass grafting,CABG)[8]能够改善心肌缺血,逆转左心室重构[9-12],进而提升患者的远期预后。然而,目前仍缺少随机对照临床试验,比较CAD合并左心室功能不全患者进行PCI或CABG的有效性。
而现有的观察性研究得出的结论并不一致。有些研究发现接受CABG组患者生存率优于PCI组患者[13-16],有些研究发现两组患者生存率比较,差异无统计学意义[5,17-19],而有些发现CABG组患者生存率更低[20]。由于缺少明确的最优化的血运重建策略,2018年欧洲心脏病学会指南[21]建议,对于合并左心室收缩功能不全的CAD患者,血运重建策略由以下因素决定:临床特征(例如冠状动脉解剖特征、是否合并糖尿病、是否合并慢性肾病)、左心室收缩功能不全的程度、患者选择倾向、临床判断以及介入心内科医师和心外科医师之间的会诊意见。
本研究基于真实世界的数据库,比较了CAD且LVEF降低(≤35%)患者接受PCI[应用药物洗脱支架(drug-eluting stent,DES)]或CABG治疗的有效性。
1 对象与方法
1.1 研究对象
本研究回顾性筛查自2005年1月1日至2014年12月31日,于首都医科大学附属北京安贞医院接受PCI(应用DES)或CABG治疗的CAD患者,依据本院术前1个月内的超声心动图检查结果,术前LVEF≤35%的CAD患者纳入本研究。患者纳入以及排除情况见图1。本研究方案通过首都医科大学附属北京安贞医院伦理委员会批准,同时于中国临床试验注册中心登记注册(No.ChiCTR2100044378)。

图1 患者选择和研究流程Figure 1 Patient selection process and study protocol
1.2 数据收集与定义
通过住院病历资料收集了患者的人口学信息、病史资料、实验室检查结果、冠状动脉解剖信息以及手术信息。通过病历和电话联系获得随访数据。基线人口学和临床特征、LVEF值和血管造影参数从本院的病历中获得。基线肌酐水平在术前30 d内测量。估算的肾小球滤过率(estimated glomeru lar filtration rate,eGFR)由肾病研究中的饮食修改简化公式计算。超声心动图检查由本院检查完成。PCI或CABG术前30 d内测量术前LVEF、左心室舒张末期内径(left ventricular end-diastolic diameter,LVEDd)、左心室收缩末期内径(lef t ventricular end-systolic d ia m eter,LVESD)以及是否存在二尖瓣反流(m itral regurgitation,MR)。血运重建后3~12个月的超声心动图检查作为术后超声随访。对于术后有多次超声心动图测量的患者,采用在血运重建3个月后的首次超声心动图检测数据。MR通过半定量数据描述,即:无/未发现(0)、轻度(1)、中度(2)、重度(3)。左主干病变定义为造影直视下,左主干血管内直径狭窄≥50%。多支血管病变定义为3支主要心外膜血管中有1支以上冠状动脉管腔直径狭窄≥70%。完全血运重建定义为3支冠状动脉及其主要分支中,所有造影有意义的病变(直径狭窄≥70%)都达到介入治疗成功的标准(残余狭窄<30%)。上述判断由进行介入手术的心脏科医师目测确定。对于CABG,手术对于每一支直径狭窄≥70%的主要冠状动脉提供了桥血管移植,则认为是完全血运重建。
1.3 研究终点
研究的主要终点指标是短期(术后30 d内)和长期全因死亡率。次要终点指标为因HF再入院发生率、再次血运重建率。此外,还评估了主要不良心脏事件(包括长期全因死亡、因HF再入院和再次血运重建)和心原性死亡率。除非存在明确的非心原性因素,所有死亡均被判定为心原性死亡。当死亡发生在初次血运重建住院期间,亦判定为心原性死亡。因HF再入院,定义为初次手术出院后再次入院,且住院诊断为HF。再次血运重建包括任何非计划的二次PCI或CABG。按计划出院后90 d内进行的二次PCI(21例)不被判定为再次血运重建。
1.4 统计学分析
使用Stata 14.0(Stata Co rp LLC)软件进行统计分析。PCI组和CABG组患者的基线特征差异通过1∶1匹配协议来进行倾向性评分匹配。对匹配前后所有基线协变量(包括年龄、性别、合并症、冠状动脉病变等)的标准化差异进行估算。标准差<10.0%提示在两个队列中给定的协变量是匹配的。累积发病率用K ap lan-M eier法估计,用Log-rank检验进行比较。在匹配的队列中,使用Cox比例风险回归模型分析。所有统计分析均基于双侧检验,以P<0.05为差异有统计学意义。
2 结果
2.1 基线特征
905例术前LVEF≤35%的CAD患者纳入研究。其中418例(46.2%)为PCI组,487例(53.8%)为CABG组。两组患者基线特征见表1。共498例患者完成1∶1倾向性评分匹配,PCI组和CABG组各249例。在匹配的队列中,PCI组完全血运重建的比例(24.9%)显著低于CABG组(77.9%)(OR0.09,95%CI0.06~0.14,P<0.001)。
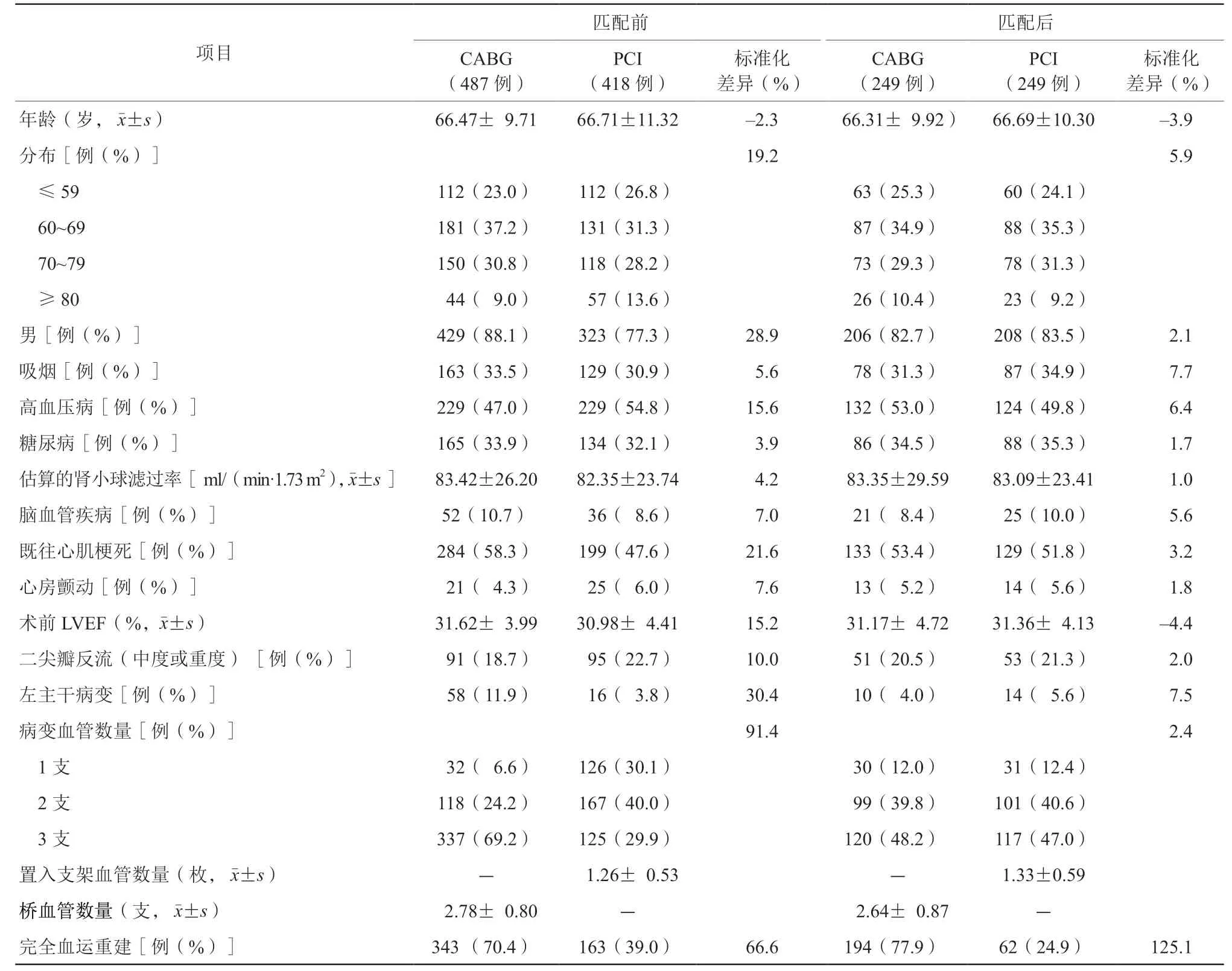
表1 CABG 和PCI 组患者倾向性评分匹配前后基线资料特征比较Table1 Baseline characteristics before and after propensity score matching in patients who underwent PCI or CABG
2.2 短期结果
与CABG组相比,PCI组术后30 d死亡率更低(HR0.29,95%CI0.09~0.88,P=0.029)。两组术后30 d因HF再入院的风险相似(HR0.50,95%CI0.05~5.51,P=0.571)。两组患者在术后30 d内均未发生非计划的再次血运重建。
2.3 长期结果
平均随访时间为4.5年(中位数为3.7年)。最长随访期为11.5年,81.7%的患者完成随访。与CABG组相比,PCI组全因死亡的风险差异无统计学意义(HR1.00,95%CI0.67~1.50,P=0.990;图2)。两组间心原性死亡风险也相似(HR1.00,95%CI0.64~1.56,P>0.999;图3)。与CABG组相比,PC I组因H F再入院的风险差异无统计学意义(HR0.81,95%CI0.40~1.64,P=0.561;图4),但PC I组再次血运重建的风险显著增加(HR14.46,95%CI3.43~60.98,P<0.001;图5),差异有统计学意义。两组间发生主要不良心脏事件的风险相似(HR1.26,95%CI0.90~1.77,P=0.171;图6)。
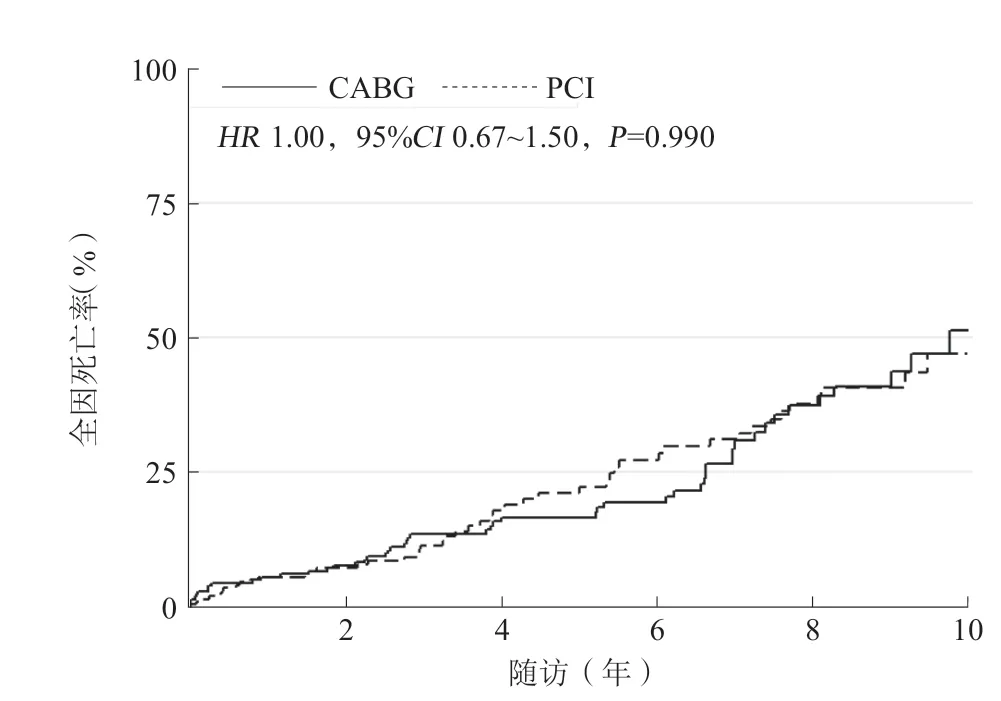
图2 PCI 和CABG 的全因死亡风险比较Figure 2 PCI versus CABG for risk of all-cause death

图3 PCI 和 CABG 的心原性死亡风险比较Figure 3 Comparison of cardiogenic death risk betw een PCI and CABG

图4 PCI 和CABG 的因心力衰竭再入院风险比较Figure 4 PCI versus CABG for risk of heart failure hospitalization

图5 PCI 和CABG 的再次血运重建风险比较Figure 5 PCI versus CABG for risk of repeat revascularization
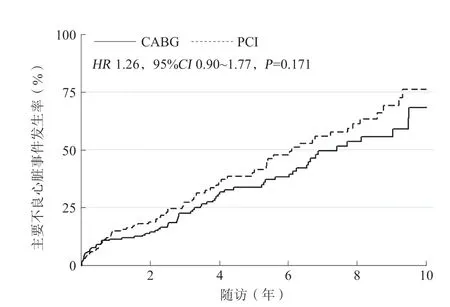
图6 PCI 和 CABG 的主要不良心脏事件比较Figure 6 Comparison of major adverse cardiac events between PCI and CABG
2.4 LVEF改善
为了比较PCI及CABG对LVEF和左心室重构改善作用,对308例术后3~12个月有超声心动图随访的患者进行了倾向性评分匹配。共150例患者完成1∶1倾向性评分匹配,PCI组和CABG组各75例。PCI组超声心动图随访在术后5.5(3.3,7.0)个月完成,CABG组在术后6.9(5.1,9.6)个月进行。PCI组患者比CABG组有更显著的LVEF改善(交互作用P=0.031)(表2,图7)。PCI组术后左心室大小有显著性(LVESD,P<0.001)或接近显著性 (LVEDd,P=0.073)的缩小。然而,两种治疗策略(PCI与CABG)之间差异无统计学意义(LVESD,交互作用P=0.136;LVEDd,交互作用P=0.312)。PCI和CABG对MR的严重程度差异均无统计学意义(交互作用P=0.710)。
表2 CABG 和PCI 组患者倾向性评分匹配后左心室重构比较Table 2 Left ventricular remodeling in propensity score-matched cohort

表2 CABG 和PCI 组患者倾向性评分匹配后左心室重构比较Table 2 Left ventricular remodeling in propensity score-matched cohort
注:CABG,冠状动脉旁路移植术;PCI,经皮冠状动脉介入治疗;LVEF,左心室射血分数;LVEDd,左心室舒张末期内径;LVESD,左心室收缩末期内径;MR,二尖瓣反流。
特征 基线 随访 P 值 交互作用P 值LVEF(%)PCI 31.75±3.85 43.49±11.22 <0.001 0.031 CABG 31.42±3.30 39.53± 9.75 <0.001 LVESD(mm)PCI 48.34±9.13 44.06±10.94 <0.001 0.136 CABG 49.24±7.18 47.36±11.10 0.154 LVEDd(mm)PCI 60.48±7.82 58.53± 9.41 0.073 0.312 CABG 61.07±6.80 60.49± 9.63 0.673 MR 分级PCI 0.99±0.80 0.99± 0.81 >0.999 0.710 CABG 1.20±0.66 1.15± 0.69 0.599
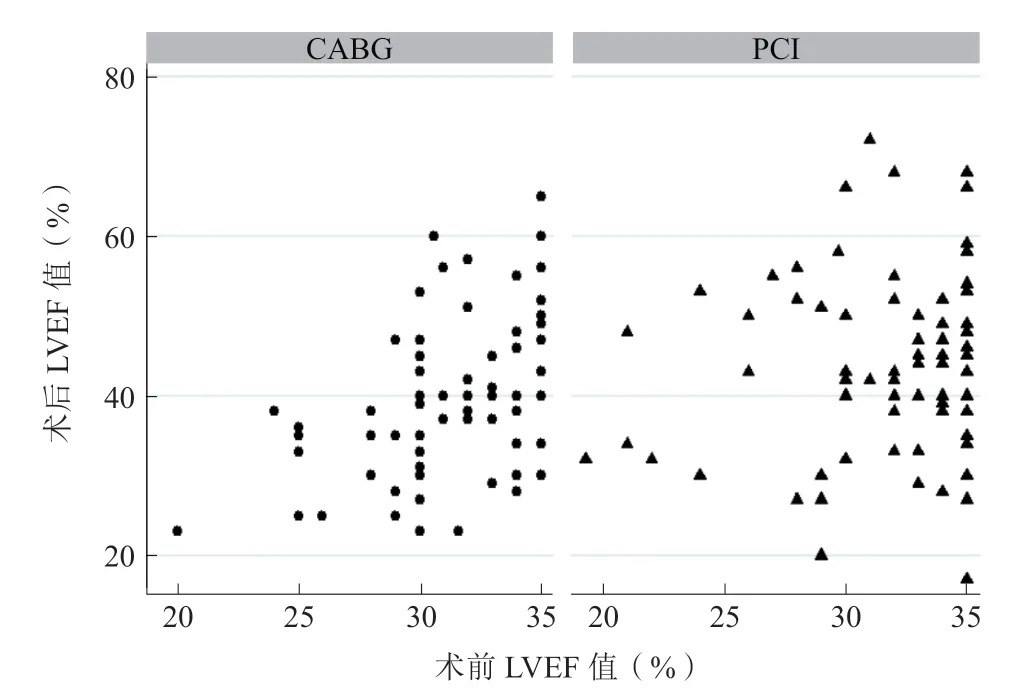
图7 PCI 和CABG 患者血运重建前后的LVEF 值分布Figure 7 Individual preoperative and postoperative LVEF distribution among patients who underwent PCI or CABG
3 讨论
C A D合并LV E F降低(≤35%)患者中,与CABG相比,PCI患者术后30 d死亡率更低,LVEF改善更多,但再次血运重建的风险较大。远期死亡率及因HF再入院风险,PCI组与CABG组相似。
在对比PCI与CABG的临床试验中,合并左心室功能不全的CAD患者在很大程度上被排除在外或被严重低估[22-25]。至今尚未有随机对照的多中心研究,比较PCI与CABG在左心室功能不全患者的临床获益。一些观察性研究发现,与CABG相比,PCI术后患者的远期死亡率更高[13-15]。而另一些研究发现,PCI与CABG术后患者生存率相似[5,17-19]。
在比较不同研究的结果时,需要考虑研究设计以及研究纳入患者的基线差异。例如,患者临床特征和冠状动脉解剖特征在不同的研究中存在差异,这可能会影响左心室功能不全患者接受PC I或CABG的预后。与本研究相比,M a r u i等[14]研究中的患者年龄更大(69.0岁比66.7岁),肾功能更差[eGFR,51.9 m l/(m in·1.73 mm2)比83.09 m l/(m in·1.73 mm2)],三支血管病变的发生率更高(CABG组:100%比48.2%;PCI组:100%比47.0%)。上述这些因素都可能影响PCI与CABG之间的比较。另外,与本研究相比,Yang等[5]研究人群有更高的完全血运重建率,PCI组和CABG组分别为92%和95%。在本研究中,PCI组和CABG组分别为24.9%和77.9%。Marui等[14]和Nagendran等[13]的研究纳入的患者中部分使用裸金属支架或仅完成经皮冠状动脉血管成形术。这些因素可能会在PCI和CABG的对比中,更多地体现出CABG的优势。术前左心室收缩功能(LVEF)损伤程度是否会影响PCI和CABG的获益对比,也值得进一步研究[12]。
目前比较两种血运重建方式对左心室功能不全患者LVEF改善效果的临床数据十分有限。在本研究中,发现PCI能更好地改善LVEF。这与既往研究在LVEF中度降低的患者(36%≤LVEF≤40%)中的结果不同[12]。在这些患者中,PCI与CABG带来的LVEF改善相似。存活心肌数量、糖尿病、术前LVEF值以及LVEDd可能与血运重建后LVEF的改善程度有关[26-28]。虽然在本研究中,陈旧性心肌梗死病史、糖尿病和术前LVEF值都通过倾向性评分予以了匹配,但是否有其他相关因素影响了不同血运重建方式对LVEF的改善程度,可能需要更大样本量的前瞻性研究进一步证实。
这是一项单中心的非随机观察性研究。随访日期来自医疗记录和电话联系,但并未对所有患者进行完全跟踪。因此,与任何其他观察性研究一样,本研究可能会受到选择偏倚的限制。本研究尝试应用倾向性评分匹配用以降低两组患者基线偏倚的发生。但并没有冠状动脉解剖风险评分(SYNTAX评分)和存活心肌的评价等相关数据。因此,这些变量并未出现在倾向评分匹配中。此外,本研究样本量相对有限,资料并未区分第一代和第二代DES,这可能会给PCI组带来一定混淆。无论采取何种血运重建策略,随访期间的优化药物治疗仍然是HF治疗的基础。在缺乏相关数据的前提下,本研究未能纳入这些因素。更大样本量的前瞻性随机对照研究有助于进一步证实,PCI和CABG对CAD合并LVEF降低患者临床获益的影响。
在CAD合并LVEF降低(≤35%)患者的血运重建治疗中,PCI和CABG有相似的长期死亡和HF住院风险。PCI有较低的短期死亡风险和更多的LVEF改善,但再次血运重建风险较高。以增加再次血运重建的风险为代价,PCI有可能成为CABG的替代选择。CAD合并LVEF降低患者最佳的血运重建策略仍然是未来需要探讨的问题。
利益冲突 所有作者均声明不存在利益冲突
