基于罗丹明B酰肼的化合物铜离子络合能力测定的新方法
2023-12-31陈健敏朱丹虹蔡小真刘思弯
陈健敏, 朱丹虹, 蔡小真, 刘思弯
(莆田学院 1. 药学与医学技术学院; 2. 药物分析与检验医学福建省高校重点实验室, 福建 莆田 351100)
铜是人体必需的微量元素之一,它在多种酶和蛋白质的功能中发挥着重要的生理作用[1]。具体而言,铜离子作为酶的辅因子参与神经递质生物合成、细胞呼吸、组织成熟和活性氧(ROS)清除等多种细胞过程[2]。与酶和肽结合的铜离子大多是人体必需的,而过剩的游离铜离子的累积会促进ROS的生成,从而产生毒性[3],让人患上神经退行性疾病,包括Wilson病、Menkes综合征、阿尔茨海默病和帕金森病等[4]。临床上使用铜离子络合剂是治疗机体铜离子过剩或调节其失调的一种很有潜力的方法,但目前铜离子络合剂只局限于Wilson病的治疗[5]。临床用于治疗Wilson病的铜离子络合剂只有D-青霉胺、三丁糖和四硫代钼酸盐3种[6],然而这些药物会引起严重的副作用,如诱发免疫复合物肾炎、神经系统症状、严重结肠炎、贫血和白细胞减少等[7-9]。因此,研究一种能够测定化合物铜离子络合能力的方法,用于筛选更加安全和有效的新型铜离子络合剂具有必要性。
测定化合物铜离子络合能力的方法一般都是基于铜离子的分析技术。近年来出现了许多检测铜离子的分析技术,包括离子选择电极(ISE)、表面等离子体共振光谱(SPRS)、原子吸收光谱(AAS)、电感耦合等离子体原子发射光谱(ICP-AE)和电感耦合等离子体质谱(ICP-MS)[10-11]。但这些技术均需要复杂、精密的仪器来完成分析过程,不适合现场监测和高通量检测[12]。此外,这些技术大多只能测定总铜离子(结合型和游离型的铜离子)含量[13],而不能直接测定游离铜离子的含量,所以这些技术并不适合直接用于测定化合物铜离子络合能力。因此,有待开发一种不需要复杂的精密仪器,就能直接检测游离铜离子的检测方法,以评估化合物铜离子络合能力。
传统的紫外-可见分光光度法用于测定化合物铜离子络合能力简单方便,主要是以邻苯二酚紫(PV)为探针,检测400~900 nm处的吸光度变化来评价化合物的络合能力[14]。虽然目前大多数研究仍采用这种方法,但一些实验因素易对检测结果产生较大影响,如反应时间、反应介质的pH值和试剂的浓度等[15],导致检测结果不准确。因此,本研究拟开发一种基于罗丹明B酰肼的测定化合物络合能力的新方法,并优化反应条件,为神经退行性疾病潜在药物的筛选提供新的手段。
1 材料与方法
1.1 试剂与仪器
罗丹明 B、水合肼、硫酸铜、杨梅素、曲酸、乙二胺四乙酸(EDTA)、甲醇、乙二醇、正丙醇、N,N-二甲基甲酰胺(DMF)、异丙醇、甘油、乙醇、二甲基亚砜(DMSO)、1,2-丙二醇、乙腈、磷酸二氢钠·二水、磷酸氢二钠·十二水、N-(2-羟乙基)哌嗪-N-(2-乙磺酸)钠盐、TRIS 盐酸盐、浓盐酸、氢氧化钠、硫酸铜、硝酸铜、醋酸铜、氯化铜、硫酸铁、硫酸钴·七水、硫酸铝·十八水、硫酸铬·水合、硫酸锌、硫酸铅、氯化钠、硫酸钾、氯化镉·无水、硫酸镍·六水合物、硫酸锰·一水、氯化汞(购于上海晶纯生化科技股份有限公司)均为分析纯或药用级。
分析天平(上海卓精电子科技有限公司,BSM);紫外-可见分光光度计(日本津岛,UV-2500);荧光-可见分光光度计(日本 Hitachi,IF-4600);核磁共振仪(德国布鲁克,Bruker Avance 500);循环水式多用真空泵(郑州特尔仪器设备有限公司,SHZ-D Ⅲ);旋转蒸发仪(上海央申科技仪器公司,RE-52);真空干燥箱(德国VACUUBRAND公司,MD 4C ND);数控超声波清洗器(昆山市超声仪器有限公司,KQ2200DE);超纯水发生器(德国赛多利斯,Milli-Q-Plus)。
1.2 研究方法
1.2.1 罗丹明B酰肼的合成
罗丹明B酰肼的合成参考文献[16]中的方法并做一些调整。将2.22 g罗丹明B溶于30 mL乙醇中,在冰浴中搅拌30 min,加入10 mL水合肼(质量分数为90%),溶液在60 ℃下冷凝回流,直至粉红色消失。将溶液冷却并倒入水中,用乙酸乙酯分别萃取3次,旋蒸除去溶剂,置于真空下干燥,得粉红色固体1.54 g,产率69%。采用核磁共振分析确证,结果如下:1H NMR (DMSO-d6): δ, 1.07 (t, 12H, NCH2CH3), 3.32 (q, 8H, NCH2CH3), 4.27 (s, 2H, NH2), 6.32-6.37 (d, 6H, xanthene-H), 6.98 (m, 1H, ArH), 7.45 (m, 2H, ArH), 7.76 (m, 1H, ArH)。确认所得产物为罗丹明B酰肼,合成路线和产物结构式如图1所示。

图1 罗丹明B酰肼的合成路线Figure 1 Synthetic scheme of rhodamine B hydrazide

图2 分析方法与设计原理Figure 2 Schematic of the analytical method and principle
1.2.2 化合物铜离子络合能力测定步骤与设计原理
采用罗丹明B酰肼作为探针检测铜离子的方法已有报道[16],原理是铜离子能够诱导罗丹明B酰肼水解,生成罗丹明B而使溶液即刻呈现粉红色和荧光特征。因此,本研究假设诱导罗丹明B酰肼的铜离子只能为游离铜离子,那么在反应介质中加入待测化合物,与部分铜离子形成络合物,只有剩余的游离铜离子能与罗丹明B酰肼反应;该化合物的络合能力越强,剩余的游离铜离子越少,生成的罗丹明B就越少,溶液颜色就越浅,仪器检测的信号就越弱。这样就可以通过检测溶液的颜色或吸光度的变化来测定被测化合物的铜离子络合能力。
1.2.3 铜离子分析方法的优化
因化合物铜离子络合能力测定方法是基于铜离子分析方法,所以先对铜离子分析方法进行优化。为获得最佳分析条件,研究了溶剂、罗丹明B酰肼浓度、铜离子浓度及来源、pH值、反应时间和反应温度对分析方法性能的影响。实验条件:取100 μL铜离子溶液(10 mmol/L)置于试管中,并将1 mL罗丹明B酰肼溶液(使用乙腈作为溶剂)和1 mL水加入试管中充分混合;溶液反应一定时间后,在400~800 nm波长范围内记录紫外-可见光谱。特殊实验条件将在结果与讨论中体现。
1.2.4 化合物铜离子络合能力测定方法
得到铜离子分析方法的最佳条件后,便可设计测定化合物的铜离子络合能力的方法与步骤。将100 μL待测化合物(sample)与100 μL铜离子溶液(2 mmol/L)混合并反应10 min。然后向混合物中加入1 mL罗丹明B酰肼溶液(2 mmol/L,乙腈为溶剂)和1 mL水,充分混匀。所得溶液反应一定时间后,记录溶液的紫外-可见吸光度(D557 nm)。以溶解待测化合物的溶剂作为空白对照(control)代替待测化合物溶液,按上述步骤操作。铜离子络合能力(%)可根据以下公式计算:
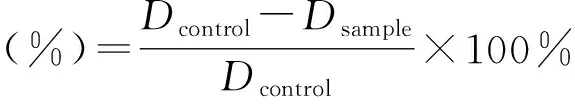
1.3 统计学分析

2 结果与分析
2.1 反应溶剂与缓冲溶液对测定方法的影响
为了选择最佳的反应溶剂,考察不同溶剂(甲醇、乙二醇、正丙醇、DMF、异丙醇、甘油、乙醇、DMSO、1,2-丙二醇和乙腈)对分析方法的影响。在考察不同溶剂的影响时,罗丹明B酰肼溶液的浓度始终保持1 mmol/L不变。首先,溶剂不能影响罗丹明B的紫外-可见吸收,且溶剂自身不能使罗丹明B酰肼水解,因此记录各溶剂溶解罗丹明B酰肼后的紫外-可见光谱,结果如图3A所示。除了乙二醇(ethylene glycol)外,其他溶剂在400~800 nm波长范围内均无明显吸收,不干扰生成的罗丹明B信号的检测。上述结果表明,除乙二醇外,罗丹明B酰肼在所有试验溶剂中均稳定。当在这些溶液中加入铜离子,水解罗丹明B的信号强弱如图3B所示。虽然不同溶剂可引起吸光度的变化,但罗丹明B的峰值波长基本维持在557 nm,因此其可作为紫外-可见信号的检测波长。乙腈(acetonitrile)作为溶剂时,产生的吸光度最大,是甘油(glycerol)的2倍多,说明乙腈最有利于罗丹明B酰肼的水解;反应后产生的吸光度越高,方法的灵敏度越高。因此,确定乙腈作为罗丹明B酰肼的溶剂。
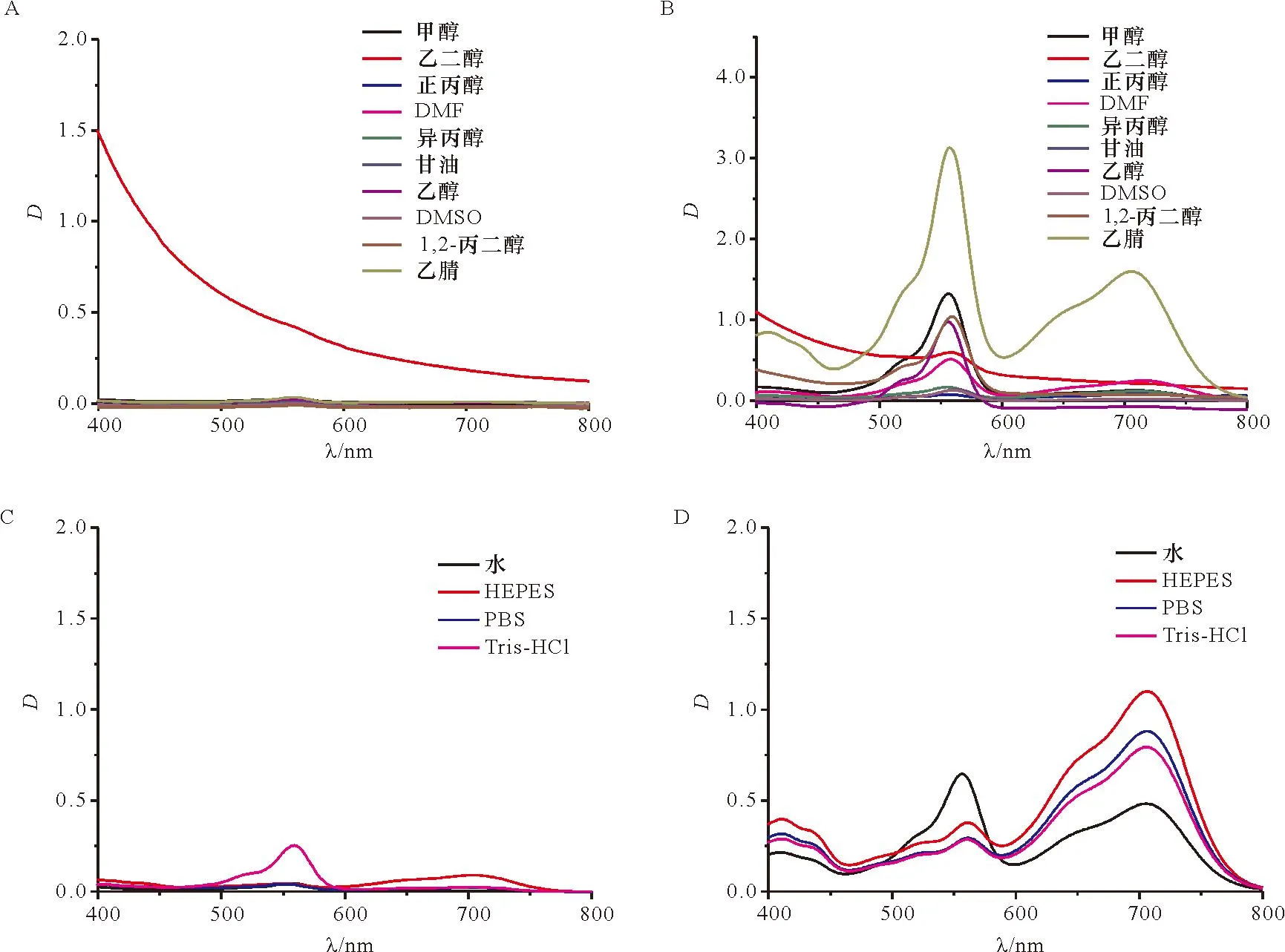
A.不同溶剂中罗丹明B酰肼自身水解;B.不同溶剂中铜离子诱导罗丹明B酰肼水解;C.不同缓冲溶液中罗丹明B酰肼自身水解;D.不同缓冲溶液中铜离子诱导罗丹明B酰肼水解A. Spontaneous hydrolysis of rhodamine B hydrazide in different solvents; B. Copper ion-catalyzed hydrolysis of rhodamine B hydrazide in different solvents; C. Spontaneous hydrolysis of rhodamine B hydrazide in different buffer solutions; D. Copper ion-catalyzed hydrolysis of rhodamine B hydrazide in different buffer solutions.图3 不同溶剂和缓冲溶液中罗丹明B酰肼的自发水解和铜离子诱导水解Figure 3 Spontaneous hydrolysis and copper ion-induced hydrolysis of rhodamine B hydrazide in different solvents and buffer solutions
硫酸铜为离子化合物,所以无法使用纯乙腈作为溶剂。因此,考察水和不同缓冲溶液体系(HEPES、PBS和Tris-HCl)对罗丹明B酰肼水解的影响,结果如图3C(体系不加铜离子)和3D(体系加入铜离子)所示。从图3C可以看出,在Tris-HCl缓冲体系下,罗丹明B酰肼不稳定,自身发生了水解,因此不能选择该缓冲体系;而水、HEPES和PBS体系下罗丹明B较为稳定,几乎没有发生自身水解的现象。图3D结果显示,在罗丹明B的特征峰557 nm处,水比其他3种缓冲溶液体系的信号更强。结合以上实验结果,同时考虑检测方法的成本、简便和环保等因素,最终确定水作为硫酸铜的溶剂。因此,结合前面溶剂试验结果,确定了本研究的检测方法采用水-乙腈混合溶剂体系。
2.2 水相pH值对测定方法的影响
通过加入少量的HCl或NaOH(0.1 mol/L)获得不同pH值的水相,考察了水相pH值对罗丹明B酰肼水解的影响,结果如图4所示。图4A显示了在不同pH值下,罗丹明B酰肼自身水解情况。酸性条件下,罗丹明B酰肼大量水解,pH值越小水解程度越高;碱性条件下,罗丹明B酰肼少量水解,也呈现pH值越大水解程度越高的规律;在pH中性条件下,罗丹明B酰肼最稳定,几乎没有发生自身水解的现象。有研究表明,酰肼的水解随着pH值的降低而逐渐增加,而在中性介质中未观察到可测量水解情况[18],与本实验研究结果相符。不仅如此,本实验研究同时发现pH值高于7也在一定程度促进了酰肼的水解。以上研究结果表明罗丹明B酰肼在酸性或碱性溶液中均不稳定。进一步考察了不同pH值条件下,加入铜离子诱导罗丹明B酰肼水解的情况,结果如图4B所示,表明铜离子在中性和弱酸性介质中比其他pH值下更能明显诱导罗丹明B酰肼的水解,在综合考虑检测方法的简易程度后,确定了实验pH值为7.0。
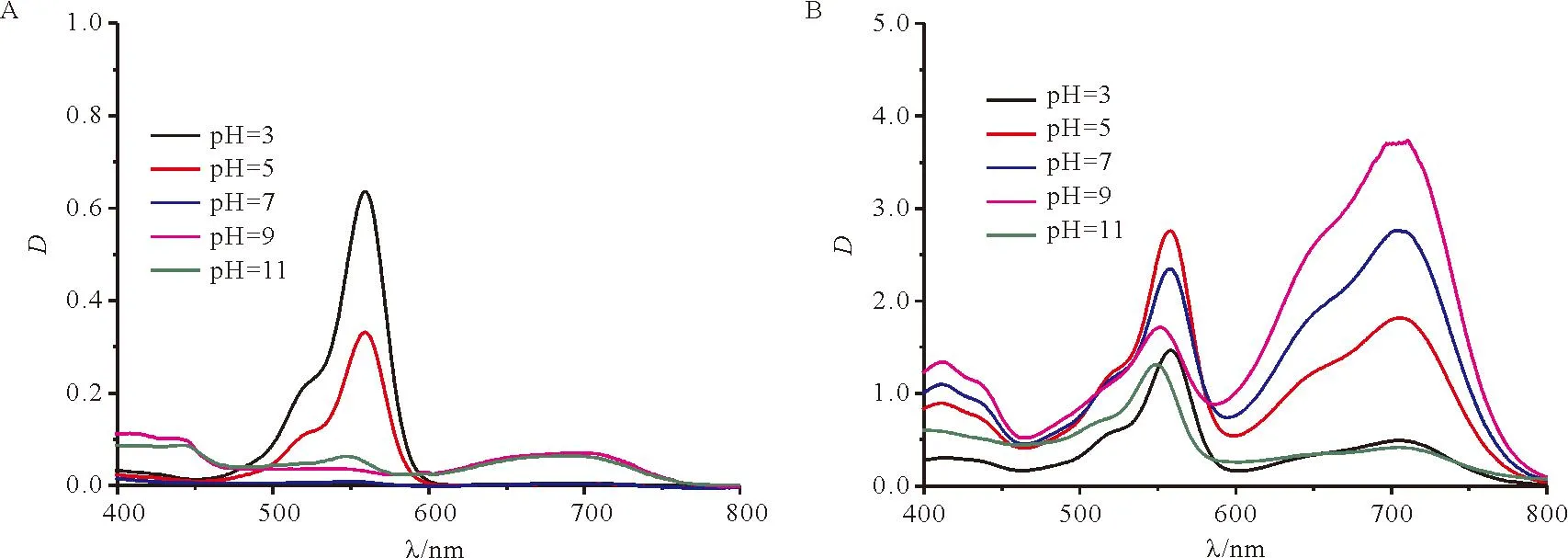
A.不同pH条件下罗丹明B酰肼自发水解反应的变化规律;B.不同pH条件下铜离子诱导罗丹明B酰肼水解反应速率的变化趋势A.Under different pH conditions, the pattern of spontaneous hydrolysis of rhodamine B hydrazide molecules changes; B. Under different pH conditions, the rate of copper ion-catalyzed hydrolysis of rhodamine B hydrazide shows a changing trend.图4 pH值对罗丹明B酰肼自发水解和铜离子诱导水解的影响Figure 4 Effect of pH on spontaneous hydrolysis and copper ion induced hydrolysis of rhodamine B hydrazide
2.3 反应时间与温度对测定方法的影响
考察了不同反应时间(1、3、5、7、10、15、20、25和30 min)对罗丹明B酰肼水解程度的影响。于设定的不同时间,记录反应溶液在557 nm波长处的吸光度,绘制时间-吸光度曲线,如图5A所示。结果发现,铜离子与罗丹明B酰肼反应十分迅速,在1 min时吸光度接近0.8,随后3、5和7 min内吸光度缓慢增加,到10 min后基本达到最大值,再随着时间的延长,吸光度没有明显变化。这一结果与现有的报道一致[17-18],铜离子可高效的促进酰肼进行不可逆的水解反应。因此,综合考虑信号稳定和方法的简易性,本研究方法确定反应时间为10 min。考察了不同反应温度(15、25、37和50 ℃)对罗丹明B酰肼水解程度的影响,结果如图5B所示,发现在15~50 ℃范围内温度对方法的影响不显著,考虑到方法的简易性,将反应温度设为室温(25 ℃)。

A:反应时间对铜离子诱导罗丹明B酰肼水解的影响;B:温度对铜离子诱导罗丹明B酰肼水解的影响A: The effects of reaction time on the copper ion-catalyzed hydrolysis of rhodamine B hydrazide; B: temperature on the copper ion-catalyzed hydrolysis of rhodamine B hydrazide图5 反应条件对铜离子诱导罗丹明B酰肼水解的影响Figure 5 Effect of reaction conditions on the copper ion-induced hydrolysis of rhodamine B hydrazide
2.4 试剂浓度对测定方法的影响
研究了铜离子和罗丹明B酰肼浓度对分析方法的影响,记录反应溶液在400~800 nm的紫外-可见光谱,结果如图6所示。图6A表明,反应溶液的吸光度随着铜离子浓度的增加而增加;当铜离子浓度达到10 mmol/L时,在557 nm处的吸光度为3.025;铜离子浓度为2 mmol/L时,吸光度则为0.92。当吸光度高于1时,浓度与吸光度的关系将偏离Lambert Beer定律[19]。因此,本分析方法确定铜离子浓度为2 mmol/L。罗丹明B酰肼浓度对分析方法的影响如图6B所示。反应溶液的吸光度与罗丹明B酰肼浓度呈正相关,罗丹明B酰肼浓度在4 mmol/L时在557 nm处的吸光度为1.031,而在2 mmol/L时为0.825。因此,出于同样的考虑,确定罗丹明B酰肼的浓度为2 mmol/L。

A.不同浓度铜离子的吸光度变化;B.不同浓度罗丹明B酰肼的吸光度变化A. Absorbance changes of copper ion at different concentrations; B. Absorbance changes of Rhodamine B hydrazide at different concentrations.图6 铜离子和罗丹明B酰肼不同浓度下的吸光度Figure 6 Absorbance of copper ion and rhodamine B hydrazide at varying concentrations
2.5 铜离子源及其他金属离子对测定方法的影响
考察不同铜离子的来源(浓度均为2 mmol/L)对罗丹明B酰肼水解的影响,结果见图7A。发现不同的铜离子来源对诱导罗丹明B酰肼的水解有一定的影响,以罗丹明B特征吸收峰557 nm作为判断依据,诱导能力依次为硫酸铜(cupric sulfate)>硝酸铜(cupric nitrate)>醋酸铜(cupric acetate)>氯化铜(cupric chloride),结果表明硫酸铜更适合于该分析方法。同时还考察了其他12种金属离子(浓度均为2 mmol/L)对罗丹明B酰肼水解的情况(图7B)。结果表明,大部分金属离子不能诱导罗丹明B酰肼的水解。能够诱导的金属离子的水解能力依次为Fe3+>Hg2+>Al3+>Cu2+>Cr2+。这表明本研究建立的方法同样可用于测试化合物与这些金属离子的络合能力。另外,当测试过程中混入这些金属离子,也会对此方法的分析测试结果产生影响。

A.不同铜离子源对罗丹明B酰肼水解的影响;B.不同金属离子对罗丹明B酰肼水解的影响A. Effect of different copper ion sources on the hydrolysis of rhodamine B hydrazide; B. Effect of different metal ions on the hydrolysis of rhodamine B hydrazide图7 不同金属离子诱导罗丹明B酰肼水解的比较Figure 7 Comparation on the hydrolysis of Rhodamine B hydrazide induced by different metal ions
2.6 测定方法的可行性验证
为了验证该分析方法的可行性,选择了常见的铜离子络合剂曲酸(kojic acid)和EDTA作为模型化合物。利用该方法测试不同浓度的曲酸(0~20 mmol/L)和EDTA(0~20 mmol/L)的铜离子络合能力,结果见图8A和8B。从图8A可以看出,557 nm处的吸光度随着曲酸浓度的增加而逐渐降低,表明曲酸对铜离子的络合作用导致促进罗丹明B酰肼水解的游离铜离子数量减少。同样随着EDTA浓度的增大,557 nm处的吸光度也呈现下降趋势,而且下降程度比曲酸更大(图8B)。结果表明,在相同浓度下EDTA对铜离子的络合强度更大,使得游离铜离子数量减少更多,表明EDTA对铜离子的络合能力强于曲酸。根据方法部分提及的公式可计算铜离子络合能力(%),进而绘制得到络合能力-浓度曲线,如图8C和8D所示。对曲线进行拟合后,可计算得到引起50%最大效应的化合物浓度(EC50)。曲酸和EDTA的EC50值分别为11.92和1.11 mmol/L,表明EDTA对铜离子的络合能力是曲酸的10倍多。上述结果表明,该分析方法能够有效定量测定并比较化合物的铜离子络合能力。
2.7 杨梅素的铜离子络合能力测定
杨梅素(myricetin)是一种黄酮醇类化合物,主要存在于杨梅、山茶等植物中,具有抗氧化、抗衰老等生理活性,对预防神经退行性疾病也有一定的作用[20-21]。体内铜离子过剩容易引起神经退行性疾病,因此研究杨梅素是否具有络合铜离子的特性,以探究其是否能够在预防神经退行性疾病方面发挥作用。采用上述分析方法对杨梅素的铜离子络合能力进行测定,结果见图9。首先记录杨梅素与罗丹明B酰肼混合体系的紫外光谱图,考察杨梅素是否使罗丹明B酰肼水解,及杨梅素是否在罗丹明B紫外可见吸收处有吸收(如有,可设计空白实验给予校正);结果如图9A所示,杨梅素本身不会使罗丹明B酰肼水解,而且在相关波长范围内无紫外吸收,因此不干扰测定。杨梅素络合能力的测试结果如图9B所示,在557 nm处的吸光度随着杨梅素浓度的增加而有所降低,但杨梅素浓度大于1.25 mmol/L后,吸光度变化趋于平稳,证明杨梅素络合铜离子已达到饱和,浓度的进一步提高无法再提高络合能力。将络合能力-浓度曲线进行拟合后,可计算得到杨梅素EC50值0.89 mmol/L,表明其络合铜离子的能力比EDTA(1.11 mmol/L)更强。结果表明,杨梅素对预防神经退行性疾病有一定的作用。通过对杨梅素的铜离子络合能力的测定分析,进一步证明了该分析方法能够有效地用于评价化合物的铜离子络合能力。
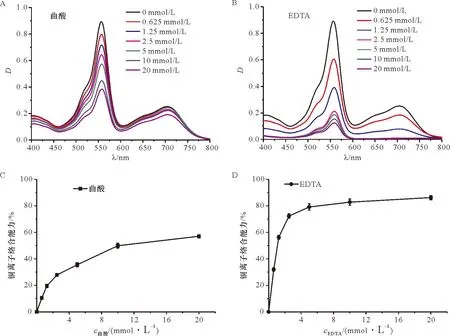
A:不同浓度的曲酸对铜离子的络合作用;B:不同浓度的EDTA对铜离子的络合作用;C:曲酸与铜离子络合能力关系;D:EDTA与铜离子络合能力关系A: The complexing effect of kojic acid at different concentrations on copper ion; B: The complexing effect of EDTA at different concentrations on copper ion; C: Relationship between kojic acid and copper ion complexing ability; D: Relationship between EDTA and copper ion complexing ability图8 曲酸与EDTA络合铜离子能力的比较Figure 8 A comparison of the copper ion complexing abilities of kojic acid and EDTA

A:杨梅素与罗丹明B酰肼混合液的吸收光谱;B:杨梅素对铜离子诱导罗丹明B酰肼水解的影响A: Absorption spectra of myricetin mixed with rhodamine B hydrazide solutions; B: Effect of myricetin on the copper ions induced hydrolysis of rhodamine B hydrazide图9 杨梅素对罗丹明B酰肼及其铜离子诱导水解的影响Figure 9 The effect of myricetin on rhodamine B hydrazide and its copper ion-induced hydrolysis
3 讨论
本研究提出一种以罗丹明B酰肼和铜离子为探针,测定化合物络合铜离子能力的方法,对影响分析方法的各种实验条件进行了优化,最终确定分析的最佳条件如下:反应体系采用乙腈和水体积比1∶1混合溶剂,pH=7,铜离子及罗丹明B酰肼的浓度均为2 mmol/L,反应时间为10 min,反应温度为25℃,体系中应避免混入Fe3+,Hg2+,Al3+和Cr2+。以典型的铜离子络合剂曲酸和EDTA作为模型化合物,证明了该分析方法的可行性。在此基础上,又利用该方法对杨梅素预防神经退行性疾病的机制进行了研究,发现杨梅素的铜离子络合能力高于EDTA,表明其有可能通过清除体内过剩的铜离子而起到预防神经退行性疾病的作用。
理论上,EDTA为六齿配体,与铜离子形成较稳定的六齿锯齿构型的六配位配合物;曲酸为五齿配体,与铜离子形成比较稳定的五齿锯齿构型的五配位配合物;而杨梅素分子中含有邻位羟基,能与铜离子形成较稳定的四配位平面构型配合物。根据配位数与配合物构型的差异,3种配体与铜离子的络合能力顺序应为EDTA>曲酸>杨梅素。
然而,本研究结果却显示杨梅素的铜离子络合能力高于EDTA,这似乎与理论预测相反。可能是因为杨梅素分子结构中除邻位羟基外,还含有5个羟基,这些羟基可以通过氢键等与水分子及其他小分子相互作用,这有利于杨梅素与体内其他配位体的相互作用,增强其与铜离子的络合能力。不过,杨梅素表现出更高铜离子络合能力的真正原因,还需要进一步探究。
综上,本研究所开发的测定化合物铜离子络合能力的方法简单实用,能用于筛选铜离子络合剂并探索治疗神经退行性疾病药物作用机制的研究。
作者贡献声明
陈健敏:负责研究设计、数据分析及论文撰写;朱丹虹:参与实验操作及论文修改;蔡小真、刘思弯:完成实验操作及结果分析。
利益冲突声明
本研究未受到企业、公司等第三方资助,不存在潜在利益冲突。
