丹参与滇丹参正交后代育性鉴定及花部形态与生化活性
2023-12-29田红彦袁翔宇贺陆洋徐绍忠赵昶灵陈天凤殷举娇
邹 转,田红彦,袁翔宇,贺陆洋,徐绍忠,赵昶灵,陈天凤,殷举娇
(云南农业大学农学与生物技术学院,昆明 650201)
【研究意义】滇丹参(SalviayunnanensisC. H.Wright)又名云南鼠尾草,为多年生草本植物[1]。与中药丹参同属且药理活性相似[2],因此往往作为丹参的代替品使用[3]。丹参(SalviamiltiorrhizaBunge)始载于《神农本草经》,因其疗效显著被列为上品[4],也是历版《中国药典》收载中药丹参的唯一基源植物[5]。近年来,虽然丹参种植面积扩大,但是丹参种质混杂、退化问题增多。长期在种植上形成只种不选和栽培管理方式不合理也使人工栽培丹参的产量和质量严重下降。【前人研究进展】舒志明等[6-7]选择3个不育类型的丹参作母本、陕西丹参作父本进行杂交育种。刘竟飞等[8]采用单交育种法对2个不同的丹参品种进行正反杂交,发现植物花粉粒发育过程中往往会积累营养物质,营养物质的积累为植物花粉粒的生长发育提供能量。朱广廉等[9]研究表明花粉败育与花粉和花药中游离脯氨酸含量的变化密切相关。张丽等[10]研究表明淀粉含量、可溶性糖及游离脯氨酸在不育系萝卜花药中显著低于保持系。因此,推测植物雄性不育的主要是由花药发育过程中营养物质缺乏引起的。能量代谢对植物生命个体而言具有十分重要的作用,植物的正常生长与发育以植物能进行正常的能量代谢为前提。【本研究切入点】以丹参和滇丹参及其正交后代为材料,观察花的形态以及测定不同大小花蕾的生理生化指标。【拟解决的关键问题】探索丹参和滇丹参正交后代杂种不育的原因,为丹参新种质的开发利用提供理论支持。
1 材料与方法
1.1 供试材料
选取2019年云南农业大学农学院中药材研究所筛选的滇丹参(云南蒙自)为父本、引自河南的丹参为母本进行杂交获得正交后代F1。以亲本及其正交后代为试验材料,2020年6月至2021年11月种于云南农业大学试验农场。所用亲本丹参和滇丹参经云南农业大学郭凤根教授鉴定。
1.2 试验方法
1.2.1 花粉活力测定 2021年4月、7月、10月采集丹参、滇丹参及其正交后代的花粉粒,用解剖针将花粉挑出,放置于载玻片上的清水中,搅动水滴,使花粉分散,分别利用TTC与I2-KI对花粉进行染色,待染色完成后利用蔡司显微镜观察花粉粒颜色,找到花粉粒相对分散的视野在同一面积视野内对染色花粉粒数进行统计。3种材料每个月各进行1次花粉活力测定,共进行3次花粉活力测定,取平均值。花粉活力(%)=视野内被染色花粉数/视野内所有花粉数×100。
1.2.2 花的形态观察 于花期对2个亲本及其正交后代植株进行定点取样,每株30朵小花,分别来自主花序上、中、下3个部位,每个部位各10朵。花瓣上下唇瓣的长宽及花丝、花药长度利用游标卡尺进行测量,用Excel进行数据统计、SPSS进行数据分析,比较正交后代与2个亲本的差异。
1.2.3 生理生化指标测定 选择不同时期的花蕾(现蕾期到盛花期)用数码游标卡尺准确测量花蕾大小后依据花蕾长度将其分为5个发育阶段(造胞细胞时期:花蕾长度<1.5 mm;花粉母细胞时期:花蕾长度1.5~3.5 mm;四分体时期:花蕾长度3.5~5.5 mm;单核期:花蕾长度5.5~7.5 mm;成熟期:花蕾长度7.5~9.5 mm),将样品放入冰盒内带回试验室后剥去花萼,称取每个发育阶段的样品1.5 g,3次重复。利用液氮速冻后研磨,立即测定SOD、POD、CAT活性;再称取6 g样品液氮速冻,研磨置于-80 ℃冰箱冻存用于可溶性蛋白、可溶性糖、脯氨酸和丙二醛(MDA)含量的测定。测定结果取3次重复的平均值。G-250考马斯亮蓝法测定可溶性蛋白含量;可溶性糖测定采用蒽酮比色法;游离脯氨酸测定采用酸性茚三酮法;MDA含量测定采用TBA法;SOD活性测定采用NBT法;POD活性测定采用愈创木酚法;CAT活性测定采用高锰酸钾滴定法,以上试验均参照李合生[11]的方法进行。采用 Excel 2010记录并整理数据、采用SPSS做显著性分析。
2 结果与分析
2.1 花粉活力测定
如图1所示,对丹参、滇丹参及其正交后代花粉粒分别进行TTC、I2-KI染色,滇丹参和丹参的花粉粒被TTC染液染成红色,被I2-KI染成蓝黑色,说明滇丹参与丹参的花粉粒具有活力;而正交后代的花粉粒经TTC染色,花粉粒未呈现红色;I2-KI染色后正交后代花粉粒也未呈现出蓝黑色,说明正交后代花粉粒无活力。2021年4月、7月、10月对丹参、滇丹参及正交后代花粉进行TTC染色,在3次花粉活力的测定结果中,滇丹参的花粉活力最低为86%,最高达99.47%,3次平均花粉活力为94.63%;丹参花粉活力最低为86.1%,最高达98.93%,3次平均花粉活力为91.61%;而正交后代最高的花粉活力仅2%,3次平均花粉活力为1.76%,即平均花粉败育率为98.24%。在3次花粉活力检测的I2-KI染色中,滇丹参的花粉活力最低为71.43%,最高为100%。3次平均花粉活力为86.7%;丹参的花粉活力最低为91.23%,最高达100%,3次平均花粉活力为95.16%,而正交后代中花粉活力最高仅3.67%,3次平均花粉活力为2.56%,即平均花粉败育率为97.44%。故判断正交后代为雄性不育株系。

A、B、C依次为丹参、滇丹参、正交后代TTC染色结果;D、E、F依次为丹参、滇丹参、正交后代I2-KI染色结果。A, B and C are the TTC staining results of S.miltiorrhiza,S.yunnanensis and their F1 generations; D, E and F are the I2-KI staining results of S.miltiorrhiza, S.yunnanensis and their F1 generations.图1 丹参、滇丹参及其正交后代花粉活力测定Fig.1 Determination of pollen vitality of S.miltiorrhiza, S.yunnanensis and their F1 generations
2.2 花的形态观察
2个亲本的花丝长度存在显著差异,正交后代的花丝长度介于亲本之间,但与2个亲本均无显著差异;3种材料的花药长度间均存在显著差异。正交后代花瓣的上下唇长、宽均介于2个亲本之间;丹参花瓣的上唇长、宽均小于正交后代和滇丹参,但正交后代和滇丹参间无显著差异;丹参花瓣的下唇长、宽均大于正交后代及滇丹参,但正交后代和滇丹参间无显著差异,正交后代花瓣的下唇长、宽均介于2个亲本之间(表1)。
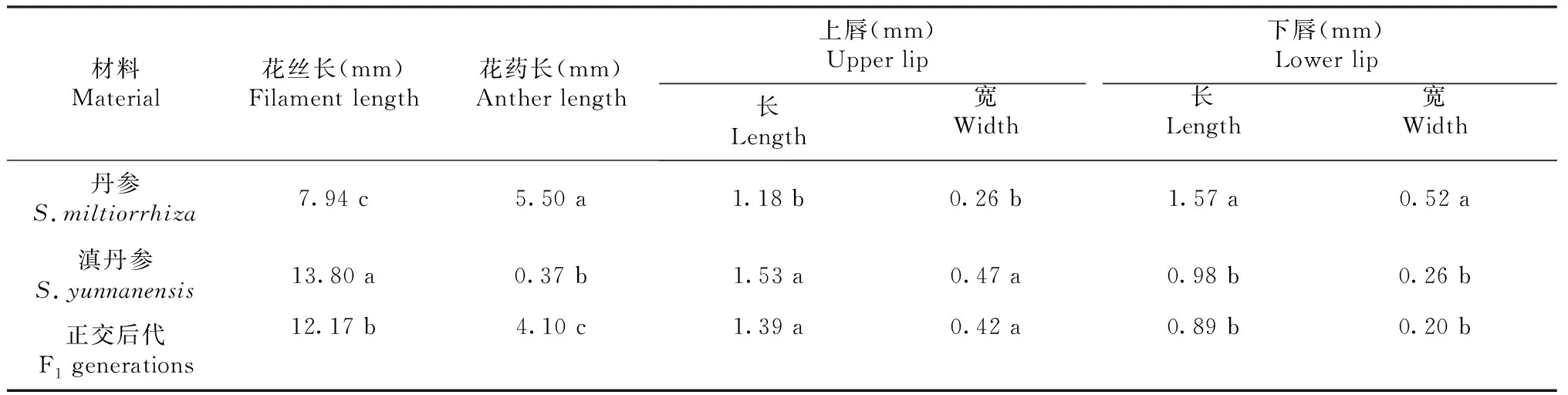
表1 丹参与滇丹参及其正交后代花的形态特征Table 1 Morphological characteristics of the flowers of S.miltiorrhiza, S.yunnanensis and their F1 generations
2.3 生理生化指标比较与分析
图2-A显示,在整个花蕾发育过程中,正交后代与滇丹参、丹参的MDA含量均呈上升趋势,尤其是正交后代MDA含量在四分体到成熟期呈明显上升趋势。在整个发育过程中,正交后代MDA含量均高于2个亲本,到成熟期时,正交后代的MDA含量是亲本的1.6倍以上。
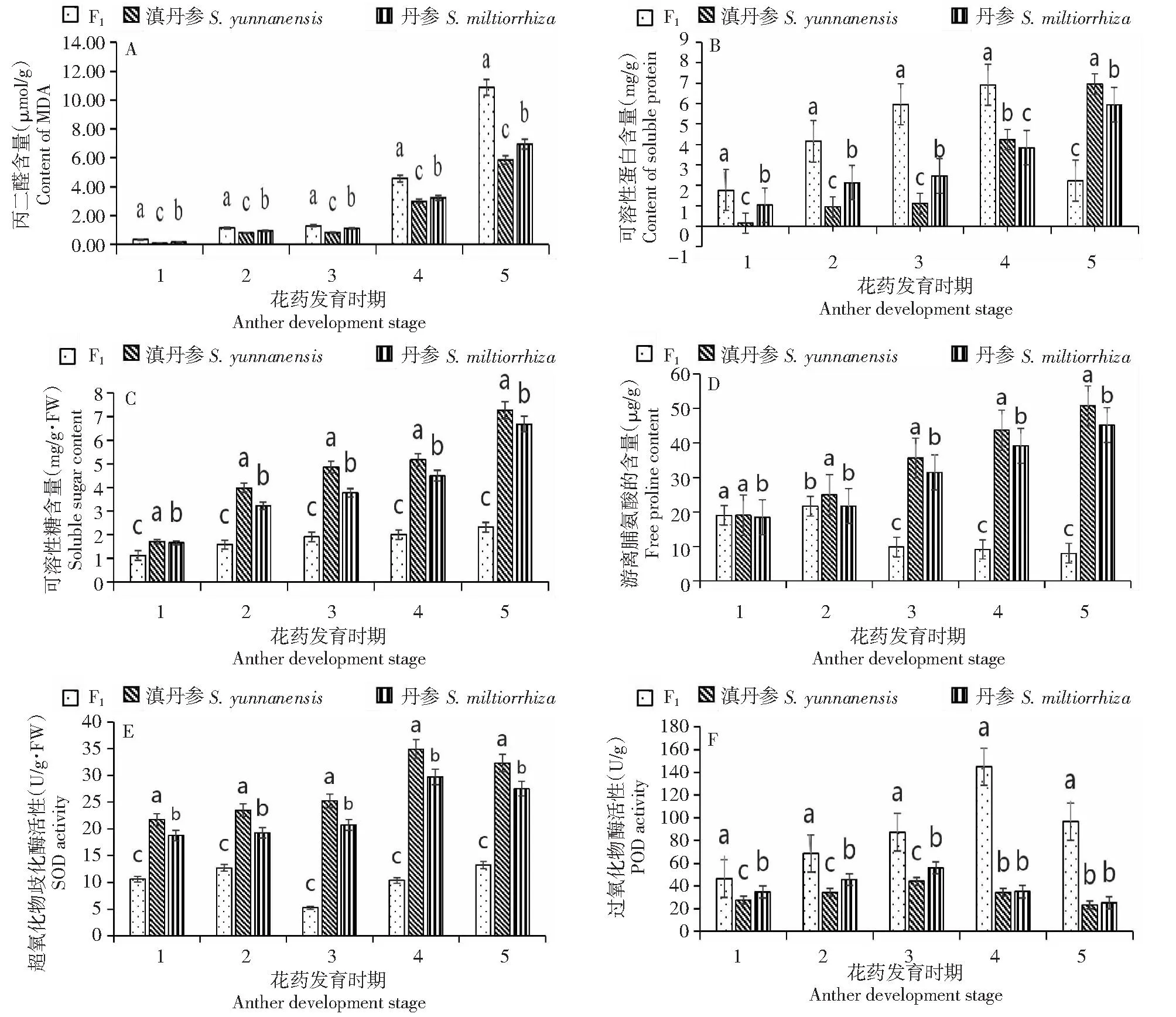
不同小写字母表示不同材料在同一发育阶段差异显著(P < 0.05),1、2、3、4、5表示花蕾发育的5个阶段,分别表示花蕾造胞细胞时期、花粉母细胞时期、四分体时期、单核期、成熟期。Different lowercase letters indicate significant differences in different materials at the same developmental stage(P < 0.05), 1, 2, 3, 4 and 5 represent the five stages of flower bud development, which respectively represent the bud cell forming stage, pollen mother cell stage, tetrad stage, monocyte stage and mature stage.图2 不同发育时期试验材料生理生化指标变化Fig.2 Changes in physiological and biochemical indicators of three materials at different development stages
图2-B显示,在前4个时期,丹参与滇丹参及其正交后代在花蕾发育过程中可溶性蛋白的变化趋势大致相同,均呈上升趋势。但从单核期到成熟期,正交后代中可溶性蛋白含量急剧下降,滇丹参与丹参的可溶性蛋白含量却依然呈上升趋势。正交后代可溶性蛋白含量在前4个时期均高于2个亲本;成熟期时,正交后代的可溶性蛋白含量显著低于亲本,此时2个亲本可溶性蛋白含量是正交后代的1.7倍以上。
图2-C显示,随着花蕾发育,3种材料中可溶性糖含量均呈升高趋势。但在整个发育过程中,正交后代中可溶性糖含量仅略微升高;从花粉母细胞时期到成熟期,滇丹参、丹参可溶性糖含量是正交后代的2倍以上。
图2-D显示,正交后代中游离脯氨酸呈先上升后下降的趋势,在四分体时期显著下降;亲本在整个发育过程中均呈上升趋势。从四分体时期开始,滇丹参和丹参的游离脯氨酸含量分别是正交后代的2倍以上。
图2-E显示,亲本花蕾的SOD活性从造胞细胞到单核期呈升高趋势,在成熟期略微下降;正交后代中的SOD活性呈先升高后下降再升高的趋势,四分体时期下降到最低;在整个花蕾发育过程中,2个亲本的SOD活性均高于其正交后代,尤其是从四分体时期到成熟期,2个亲本的SOD活性均是其正交后代的2倍以上。
图2-F显示,正交后代中POD活性从造胞细胞到单核期呈上升趋势但在成熟期下降;滇丹参和丹参的POD活性从造胞时期到四分体时期呈上升趋势,在四分体时期到成熟期POD活性呈下降趋势。在花蕾的整个发育过程中,正交后代的POD活性都较亲本高,单核期和成熟期的POD活性均是亲本的4倍以上。
图2-G显示,滇丹参与丹参及其正交后代在整个花蕾发育过程中CAT活性均呈先升高后降低的趋势,3种材料在四分体时期CAT活性开始降低。正交后代的CAT活性从四分体时期到单核期急剧下降,此时2个亲本CAT活性是其3.9倍,从单核期到成熟期,正交后代的CAT活性无明显变化,此时滇丹参和丹参CAT活性是其3倍以上。
3 讨 论
3.1 花粉活力及育性
花粉是高等植物的雄性配子体,其活力是影响植物有性杂交成功与否的重要因素[12]。对植物花粉活力测定可为人工杂交育种提供重要的数据支撑。刘文婷等[13]研究结果表明,丹参花期花粉活力平均可达80.0%以上。宋振巧等[14]研究表明,丹参花前 48 h近73.15%花粉具有活力,开花前24 h达到最高活力时期,大多数植株在这个时期花药开裂散粉。潘琼等[15]研究结果表明,紫丹参在开花前花粉活力为55.92%,花刚开放时花粉活力为46.08%,此时为紫丹参整个花期花粉活力最低值时期;花开放后花粉活力逐渐增强,至大部分花药散粉时花粉活力达整个花期最强,为90.86%;之后花粉活力逐渐减弱,但直至花冠脱落时仍有一定活力,花粉活力值为46.19%。贺和初等[16]对水稻花粉败育率为95.1%~100%的植株划分为不育株,孙寰等[17]对大豆不育株的花粉标准与贺和初一致。
本研究中对丹参与滇丹参正交后代花粉活力鉴定时所用的2种染色方法得出花粉败育率均达到95.1%以上,因而认定其为雄性不育类型。
3.2 花的形态特征
花丝是雄蕊的一部分,在花丝长度方面,正交后代花丝长度介于2个亲本之间,没有显著差异;花药是花丝顶端部分也是雄蕊的重要组成部分,舒志明等[18]研究发现的丹参雄性不育均是花药退化严重、花朵小、花丝变短的类型,而本研究中发现的雄性不育株与亲本在花药、花丝、花的大小上均无异常变化。
3.3 杂种不育与生理生化的关系
丙二醛作为交联剂,使膜蛋白、酶及DNA等大分子发生交联反应,MDA含量过多时将导致代谢紊乱[19]。本研究结果表明,从造胞细胞时期到花粉成熟期,正交后代花朵中MDA含量均高于亲本且随着花蕾发育,MDA含量上升趋势明显,尤其是在花蕾成熟期,MDA含量接近亲本的1倍。正交后代中MDA含量的增加可能与花粉粒的败育有关。
蛋白质是植物花蕾正常发育过程中的重要成分[20]。Mascarenhas[21]认为,植物雄性不育系花中可溶性蛋白缺乏是影响其雄性不育的重要原因之一。本研究发现,丹参和滇丹参及其正交后代在花蕾的整个发育过程中,前4个时期,可溶性蛋白含量均增加,但成熟期正交后代中的可溶性蛋白急剧降低,而亲本花朵中可溶性蛋白含量依然增加。从而推测,控制蛋白合成的基因在花药发育过程中可以正常表达,但到花粉成熟期由于某些基因的特异性表达抑制了控制蛋白质合成基因的正常表达,从而导致成熟期可溶性蛋白含量下降,因此可溶性蛋白含量下降也可能是雄性不育的原因之一。
花药的养分输入主要是糖类,其在花药中的含量也是影响小孢子发育的一个关键因素。糖类物质不足可以导致辣椒[22]、棉花[23]和萝卜[24]等植物的花粉败育。本研究结果表明,在花蕾发育的整个时期,丹参与滇丹参可溶性糖含量均呈增加趋势,正交后代的可溶性糖含量在整个发育时期的变化缓慢且均显著低于滇丹参和丹参,从而推测可溶性糖的缺乏可能是导致其不育的原因之一。
脯氨酸在花粉发育的整个时期都具有重要的生理功能。丰富的脯氨酸是花粉正常发育的必要条件[25]。同时,脯氨酸为花粉萌发提供能量和氮源,是合成蛋白质、酶等大分子物质的原料[26]。脯氨酸含量低,花药的抗逆性降低。本研究结果表明,在花粉母细胞以前,丹参与滇丹参及其正交后代的脯氨酸含量基本一致,随着花药发育,丹参与滇丹参脯氨酸含量持续上升,但正交后代在四分体时期脯氨酸含量显著下降,一直保持到花粉成熟期,由此推测游离脯氨酸缺乏也可能是造成花粉败育的原因之一。
SOD能清除植物代谢中产生的活性氧自由基,防止活性氧在体内积累过多导致膜脂受损从而维持膜脂的稳定性[27],膜脂的稳定性是维持细胞正常生命活动的基本条件[28]。在SOD作用下,活性氧歧化为H2O2和O2,植物通过此种反应清除体内的自由基,维持自由基生成和清除系统的平衡。本研究结果显示,在丹参、滇丹参以及正交后代花蕾的整个发育过程中,丹参、滇丹参花蕾中SOD活性均明显高于其正交后代,由此猜测由于SOD活性低,植物代谢中自由基含量增加,在植物体内积累,从而导致脂膜结构受损加剧,影响了正交后代的花粉粒正常发育。
POD在氧化降解内源激素IAA以及体内减少有毒H2O2含量等方面较重要[29]。该酶兼具吲哚乙酸氧化酶—过氧化物酶双重功能特性,在维持体内IAA代谢及库源平衡中起重要作用。袁文静等[30]对亚麻温敏性雄性不育系的POD活性同几种内源激素含量的比较分析得出,IAA含量降低在雄性不育植物中具有普遍性,而POD活性偏高导致代谢旺盛,源库供应出现问题,IAA含量减少导致败育的产生。在玉米、小麦雄性不育研究中都发现不育系花药POD活性高于保持系[31-32],本研究结果表明,在丹参、滇丹参及其正交后代花蕾发育过程中POD变化趋势均一致。但整个发育时期正交后代中POD活性均高于丹参和滇丹参,特别是在单核期和成熟期,POD活性分别是丹参与滇丹参的3倍左右。这说明本研究中由于POD活性过高,正交后代代谢旺盛、库源供应出现问题导致IAA亏损也会引起不育。
CAT被认为是一种保护性酶,可帮助SOD清除生物体内的活性氧[33]。陈贤丰等[34]发现小麦雄性不育花药中的过氧化氢酶活性明显低于可育花药中的CAT活性,因而无法有效消除超氧离子基团,导致H2O2等超氧自由基大量积累进而导致花药壁绒毡层细胞膜脂质过氧化增加而发生败育。本研究结果表明,在花粉母细胞时期以前,丹参与滇丹参及其正交后代CAT活性差异不大;而到四分体时期正交后代的CAT活性开始降低,到单核期时,仅占亲本的1/3,这个结果与陈贤丰等[34]结果一致,因而可以推测,丹参与滇丹参杂种出现不育的原因也可能与H2O2的大量积累有关。
4 结 论
正交后代与亲本材料相比,经TTC、I2-KI分别染色后发现花粉活力差异巨大,可以判断正交后代为雄性不育植株。花的形态变化比较发现,正交后代在花药长、花丝长和上、下唇长、宽等方面与亲本并无显著差别,说明正交后代的花朵形态改变并没有导致其不育。
在正交后代的花蕾发育过程中某些能量物质,如可溶性蛋白、可溶性糖等含量出现大幅度下降导致花粉缺乏能量;其次脯氨酸含量也出现降低进而使花粉抗逆性降低;MDA大量增加对细胞造成伤害以及各种酶活性的变化导致细胞内有害物质增加。正交后代的各种生理生化指标变化都显示其不育不是单一因素的影响而是多种生理指标综合作用的结果。
