外周血Tim3,IL-32,PD-1/PD-L1 用于沙利度胺联合达那唑治疗骨髓增生异常综合征疗效评估价值分析
2023-12-28李国妍
刘 焰,李国妍,陈 超
(山东省菏泽市中医医院药学部,山东 菏泽 274000)
骨髓增生异常综合征(MDS)是一种以髓系细胞发育异常为特点的异质性髓系克隆性疾病,若未及时有效干预,可能会转化为急性髓系白血病,危及生命[1-3]。沙利度胺、达那唑是治疗MDS 的常用药物,前者具有抗细胞因子及免疫调节作用,可抑制肿瘤坏死因子生成及T 淋巴细胞增殖,还可抑制新生血管生成;达那唑为睾酮衍生物,既可直接刺激造血干细胞,又可通过刺激肾脏产生红细胞生成素促进造血,二者联用可发挥协同增效作用。MDS 病因较复杂,相关研究显示,造血干细胞基因突变、细胞免疫缺陷可能与其发病过程密切相关,主要表现为免疫逃逸、造血干细胞恶性克隆等[4-5]。而T 淋巴细胞免疫球蛋白黏液素3(Tim3)可介导肿瘤微环境的免疫抑制,参与多种肿瘤发生、浸润与转移[6]。有研究表明,程序性死亡因子-1/程序性死亡因子- 1 配体(PD - 1/ PD - L1)高表达所致肿瘤免疫逃逸机制是肿瘤发生、发展的重要原因[7-8]。白细胞介素32(IL-32)可介导一系列免疫反应[9]。目前,临床针对MDS 主要采用免疫抑制剂联合雄激素药物治疗,但既往研究多集中于探讨二者联合治疗的效果,鲜有研究联合用药前后MDS患者外周血Tim3,IL-32,PD-1/PD - L1 的表达水平。鉴于此,本研究中分析了上述外周血指标在沙利度胺联合达那唑治疗MDS 前后的表达变化趋势,并结合血常规及骨髓细胞学检查指标判断评估疗效的价值。现报道如下。
1 资料与方法
1.1 一般资料
纳入标准:符合MDS 诊断标准[10],并经骨髓细胞学、免疫分型及病理活检确诊;初次发病;预计生存期> 6 个月。本研究经医院医学伦理委员会批准[批件号:(2017)伦审第(1753)号],患者签署知情同意书。
排除标准:合并肝肾等重要脏器器质性病变;对本研究拟用药物过敏;妊娠期、产褥期或哺乳期;存在自身免疫功能缺陷性疾病或全身感染性疾病;合并其他部位恶性肿瘤;接受细胞毒性药物或接触有血液毒性的化学制品或生物制剂等;重金属中毒或过度饮酒;再生障碍性贫血、原发性骨髓纤维化、大颗粒淋巴细胞白血病或其他累及造血干细胞疾病;严重意识障碍或精神行为异常。
病例选择:选取医院2018 年1 月至2020 年5 月收治的MDS 患者112 例,其中男70 例,女42 例;年龄32~58 岁,平均(46.89 ± 5.10)岁;体质量指数(BMI)20~28 kg/m2,平均(24.09±1.83)kg/m2;病程1~15个月,平均(9.82±2.15)个月。
1.2 方法
1.2.1 资料收集
参考相关文献、咨询专家意见、临床实践,自拟《MDS 患者一般资料调查问卷》,调查患者的年龄、性别、BMI、病程、世界卫生组织(WHO)分型[11]、MDS的国际预后积分系统修订版(IPSS-R)危险度分层[12],其中WHO 分型包括难治性贫血伴原始细胞增多Ⅰ型(RAEB-Ⅰ)、RAEB-Ⅱ、难治性贫血伴环状铁粒幼细胞(RARS)、难治性血细胞减少伴多系发育异常(RCMD);IPSS-R危险度分层,≥2.5分、1.5~2.0分、0.5~1.0分、0分分别为高危、中危Ⅱ、中危Ⅰ、低危。
1.2.2 治疗方法与分组
患者均接受营养支持、心理疏导等对症治疗,口服沙利度胺片(常州制药厂有限公司,国药准字H32026130,规格为每片50 mg),每次50 mg,每日1 次,持续1 周后,剂量增至每日100 mg,再持续1 周后,剂量增至每日200 mg,用药第4 周根据患者病情在每日100~200 mg 范围内调整剂量。服用达那唑胶囊(江苏联环药业股份有限公司,国药准字H32022729,规格为每粒0.1 g),每日0.3 g,每日3 次,连续治疗3 个月。按治疗是否有效分为有效组和无效组。
1.3 观察指标与疗效判定标准
观察指标:1)血常规。治疗前后取患者空腹外周静脉血3 mL,采用全自动血细胞分析仪检测白细胞计数(WBC)、血红蛋白(Hb)、血小板计数(PLT)水平,严格按仪器说明书操作。2)骨髓原始细胞。患者髂后上棘行骨髓穿刺,抽取骨髓液0.2 mL涂片,采用瑞氏-吉姆萨染色,计数200个有核细胞,计算骨髓原始细胞百分比。3)外周血Tim3,IL - 32,PD - 1/ PD - L1 水平。取患者外周血4 mL,分装2管,以乙二胺四乙酸抗凝,每管均添加2 mL 红细胞裂解液,避光反应5 min,磷酸盐缓冲液(PBS)洗涤1 次,离心,弃上清液,PBS 重悬;取100µL,加入Tim3,PD-1,PD-L1抗体,室温避光孵育15 min,PBS 洗涤1 次,离心,弃上清液;加入200 µL PBS 重悬,采用流式细胞仪测定Tim3,PD-1,PD-L1 表达水平;取患者空腹外周静脉血3 mL,2 500 r/ min 离心8 min(离心半径6 cm),分离,取血清,以酶联免疫吸附试验法检测IL-32水平,严格按试剂盒说明书操作。
疗效判定[13]:完全缓解,出血、贫血等症状消失,Hb ≥100 g/ L,WBC ≥4 × 109/ L,PLT 为(80~100)×109/L,分类未见幼稚细胞,且骨髓中原始粒细胞和早幼粒细胞之和占比< 5%,维持时间≥6 个月;部分缓解,上述症状部分消失,骨髓中原始粒细胞和早幼粒细胞之和占比较治疗前下降50%,维持时间≥3 个月;进步,上述症状有所减轻,骨髓中原始粒细胞和早幼粒细胞之和占比下降30%;无效,未达上述标准。将完全缓解、部分缓解、进步纳入有效组,无效纳入无效组。
1.4 统计学处理
采用SPSS 22.0 统计学软件分析。计量资料行Kolmogorov - Smirnov 检验与Bartlett 检验,均服从正态分布且方差齐性时以表示,行独立样本t检验;计数资料以率(%)表示,行χ2检验。外周血Tim3,IL-32,PD-1/PD - L1 间及其与血常规骨髓细胞学指标的相关性采用Pearson 相关系数模型分析,与疗效间的相关性采用Logistic 多因素回归分析;评估价值分析采用受试者工作特征(ROC)曲线,获取曲线下面积、95%置信区间(CI)、敏感度、特异度及cut - off 值,联合评估实施Logistic 二元回归拟合,返回预测概率logit(p),将其作为独立检验变量。采用双侧检验,α=0.05,P<0.05 为差异有统计学意义。
2 结果
2.1 单因素比较
有效组患者91 例,无效组患者21 例。两组患者基本资料见表1,血常规、骨髓细胞学及外周血指标比较见表2。
表2 两组患者血常规、骨髓细胞学及外周血指标比较()Tab.2 Comparison of blood routine,bone marrow cytology and peripheral blood indicators between the two groups()
注:与本组治疗前比较,aP < 0.05。Note:Compared with those before treatment,aP < 0.05.
组别Tim3(%)治疗前2.76±0.25 3.03±0.36 4.081<0.001 WBC(×109/L)治疗前3.03±0.40 2.61±0.37 4.359<0.001治疗后4.78±1.02a 2.70±0.81 8.721<0.001 Hb(g/L)治疗前54.27±6.36 48.10±5.17 4.137<0.001治疗后80.59±10.93a 50.73±8.72 11.677<0.001 PLT(×109/L)治疗前57.12±6.04 51.93±5.05 3.651<0.001治疗后68.53±11.24a 53.14±9.10 5.842<0.001骨髓原始细胞比例(%)治疗前10.25±1.02 11.31±1.13 4.207<0.001治疗后8.16±1.15a 10.94±1.86 8.779<0.001有效组(n=91)无效组(n=21)t值P值治疗后2.02±0.21a 2.95±0.44 14.389<0.001 IL-32(ng/L)治疗前72.18±8.03 80.24±9.11 4.042<0.001治疗后53.67±7.64a 78.15±10.29 12.353<0.001 PD-1/PD-L1治疗前1.79±0.24 2.21±0.36 6.525<0.001治疗后1.65±0.13a 2.17±0.45 9.545<0.001
2.2 相关性分析及价值评估
治疗前后,外周血Tim3 分别与治疗前后IL - 32和PD - 1/ PD - L1(r= 0.662,0.404,0.675,0.666,P<0.05)呈正相关,IL-32 分别与治疗前后的PD-1/PD - L1(r= 0.446,0.672,P< 0.05)呈显著正相关。详见图1。治疗前后外周血Tim3,IL-32,PD-1/PD-L1均与WBC,Hb,PLT 呈显著负相关,与骨髓原始细胞比例呈显著正相关(P<0.05)。详见表3。
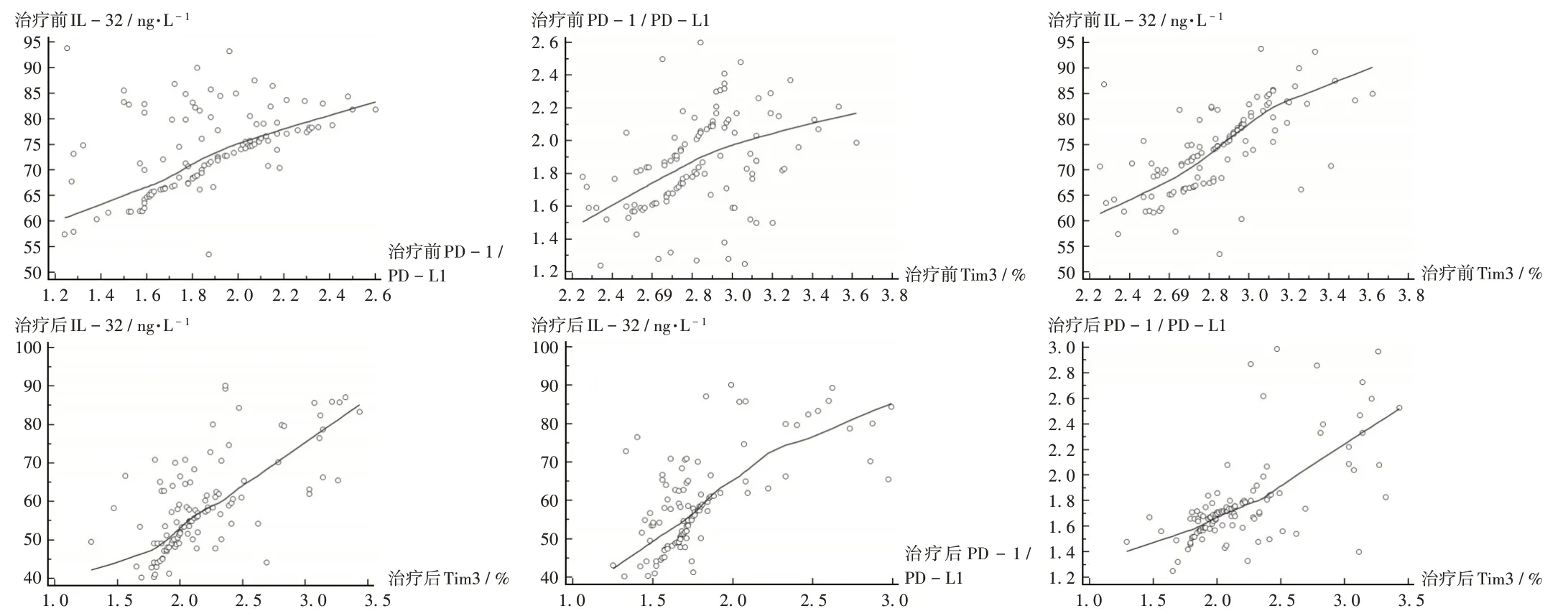
图1 治疗前后外周血Tim3,IL-32,PD-1/PD-L1间的关联性Fig.1 Correlation among peripheral blood Tim3,IL - 32 and PD - 1 / PD - L1 before and after treatment
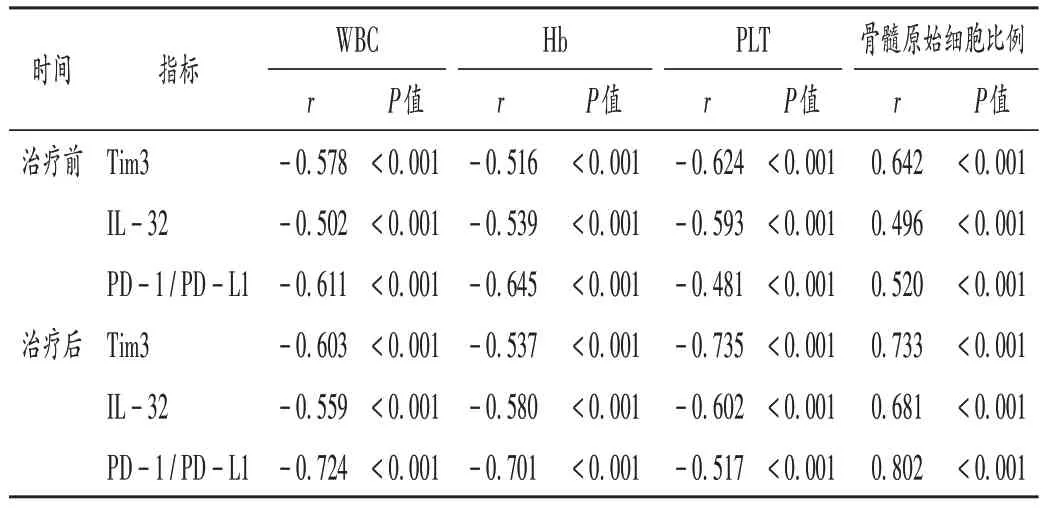
表3 外周血Tim3,IL-32,PD-1/PD-L1与血常规及骨髓细胞学指标的相关性Tab.3 Correlation of peripheral blood Tim 3,IL - 32 and PD - 1 /PD - L1 with blood routine and bone marrow cytology indicators
以疗效为因变量(有效= 0,无效= 1),以病程、WHO 分型、IPSS - R 危险度分层,治疗前及治疗后的WBC,Hb,PLT及骨髓原始细胞比例,外周血Tim3,IL-32,PD-1/PD-L1为自变量,进行Logistic多元回归分析,结果显示,治疗前后外周血Tim3,IL-32,PD-1/PD-L1仍与疗效显著相关(P<0.05)。详见表4。
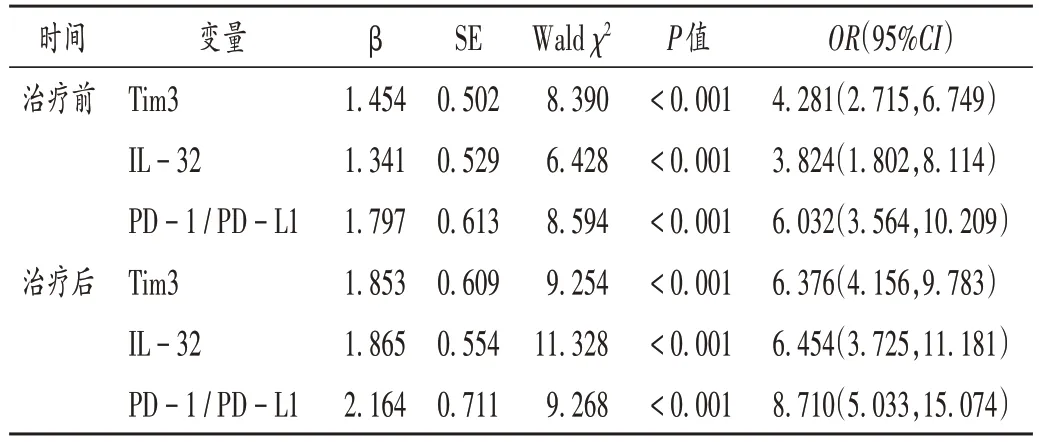
表4 外周血Tim3,IL-32,PD-1/PD-L1与疗效的相关性Tab.4 Correlation of peripheral blood Tim3,IL - 32 and PD - 1 / PD - L1 with the efficacy
ROC曲线显示,外周血Tim3,IL-32,PD-1/PD-L1联合评估沙利度胺联合达那唑治疗MDS 可能无效的AUC最大(0.885),敏感度、特异度分别为76.19%,92.31%。详见表5、图2。
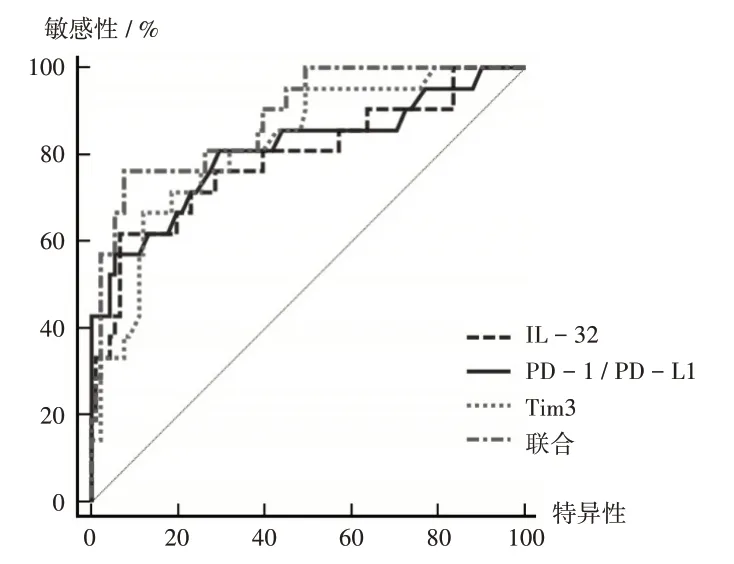
图2 外周血Tim3,IL-32,PD-1/PD-L1对疗效的评估价值Fig.2 Evaluation value of peripheral blood Tim3,IL - 32 and PD - 1 / PD - L1 in the efficacy
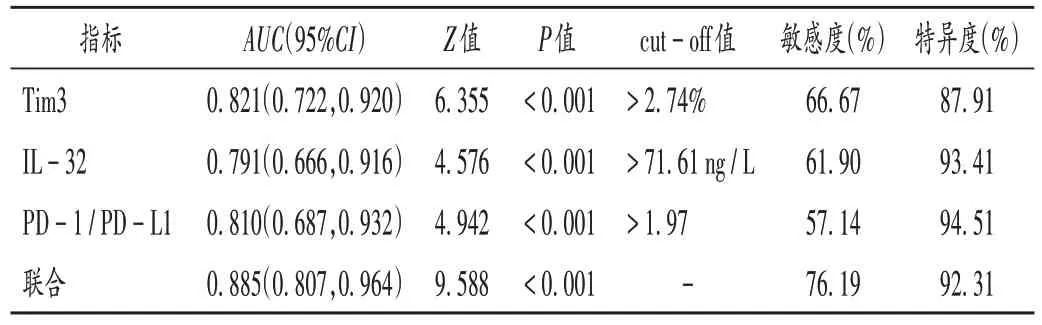
表5 外周血Tim3,IL-32,PD-1/PD-L1对疗效的评估价值Tab.5 Evaluation value of peripheral blood Tim3,IL - 32 and PD - 1 / PD - L1 in the efficacy
3 讨论
近年来,沙利度胺联合达那唑在临床MDS 治疗中受到广泛重视,其中沙利度胺为常见免疫抑制剂,参与免疫调节、抑制细胞增殖、分化及形成造血因子等过程;达那唑是人工合成的甾体类雄激素,有助于抑制骨髓细胞凋亡,但二者联用可能存在耐药及复发现象[14-15]。因此,及时、准确地评价沙利度胺联合达那唑的疗效,有助于客观判断MDS患者的预后。
Tim3 通过结合其配体S 型凝集素半乳糖凝集素9,可产生免疫负调控作用,诱导Th1 细胞凋亡,抑制γ干扰素表达,导致骨髓来源的抑制性细胞异常增殖,从而产生免疫抑制[15-16]。PD-1/PD-L1 是一对负性免疫共刺激分子,其中PD-1主要在T淋巴细胞、胸腺细胞、B 淋巴细胞、自然杀伤(NK)细胞等细胞膜表面表达,PD - L1 是其介导的免疫抑制主要配体[17-18]。ZOU等[19]的研究表明,在肿瘤中,PD - 1 和PD - L1 相互作用能抑制肿瘤微环境中T淋巴细胞活化所致免疫抑制,减弱抗肿瘤效应。IL-32 为细胞炎性因子,其表达在免疫组织中过度上调,杨颖莹等[20]指出,其具有诱导机体免疫细胞凋亡的作用。本研究结果显示,治疗有效的MDS 患者治疗3 个月后外周血3 个指标明显低于治疗前,可能与联合用药纠正了异常免疫有关,推测该联合用药的主要疗效可能与调节3 个指标水平表达存在关联。治疗前有效组与无效组患者外周血3个指标水平存在差异,可能与WHO 分型、IPSS - R 危险度分层等有关。进一步研究可知,治疗前后有效组患者外周血3 个指标水平明显低于无效组患者,结合文献[21 - 23]研究结果,考虑机制可能在于3 个指标表达过度升高,可抑制细胞内磷酸酶增殖,刺激T 细胞受体信号,激发效应T 细胞功能活性,促进大量细胞因子分泌,强化裂解靶细胞效应,降低免疫突触稳定性,从而加快MDS 病情进展,加重患者耐药性,影响疗效。
同时,汪德珍等[24]经Cox 回归分析显示,WBC 和PLT 是地西他滨治疗MDS 预后的独立危险因素。曾俊权[25]指出,MDS患者骨髓中伴有不同程度血管新生,且骨髓原始细胞百分比与血管新生数量呈正相关,有助于指导临床实施对症治疗。对比研究表明,有效组患者治疗前WBC,Hb,PLT 水平在治疗3 个月后有所提高,骨髓原始细胞比例有所下降,这可能归因于联合用药能改善骨髓细胞凋亡程度,增强对髓细胞异常增殖的抑制效果,刺激机体产生正常造血功能,进而促进机体血象、骨髓象改善。Pearson 线性相关性分析结果提示,治疗前、治疗3 个月后外周血3 个指标与WBC,Hb,PLT及骨髓原始细胞比例均存在一定相关性,有望成为评估沙利度胺联合达那唑治疗MDS 效果的有效辅助观察指标。
此外,本研究结果显示,外周血Tim3 与IL - 32 和PD - 1/PD - L1 线性关系良好,表明三者可在MDS 患者机体免疫应答反应中发挥协同作用。为进一步明确3 个指标水平对沙利度胺联合达那唑疗效的评估价值,本研究中绘制了ROC 曲线,结果发现,联合检测3 个指标水平有助于指导临床评估沙利度胺联合达那唑疗效,客观评价MDS 患者预后。另外,在评估联合治疗效果的同时还应将病程、WHO 分型、IPSS-R 危险度分层等因素纳入考虑范围内,以获取更可靠的研究结果。
综上可知,沙利度胺联合达那唑治疗MDS,可有效下调外周血Tim3,IL - 32,PD - 1/ PD - L1 水平,明确上述外周血指标治疗前后的变化情况,可为临床评估MDS疗效提供新思路。
