支气管哮喘患儿感染新型冠状病毒的横断面调查
2023-12-15施婷婷颉雅萍陈容珊印根权何春卉
施婷婷 颉雅萍 陈容珊 印根权 卢 根 何春卉
支气管哮喘(以下简称哮喘)是一种以慢性气道炎症和气道高反应性为特征的异质性疾病,是儿童时期最常见的慢性呼吸道炎症性疾病[1]。哮喘发病机制复杂,病因多样,因反复发作而严重影响儿童学习、生活和身心健康,其中病毒感染是儿童哮喘急性发作的重要诱因之一。在新型冠状病毒(COVID-19)感染大流行期间,中国根据 COVID-19 的传播特性,采取了居家隔离、限制公众聚集活动等措施,控制病原体的传播[2]。在此期间,国内尚未有足够数据特别是儿童数据表明哮喘与 COVID-19感染之间的关系。
自2022年12月初中国调整防疫政策后,逐步有包括儿童在内的大规模人群感染COVID-19,哮喘患儿感染COVID-19后的治疗与管理是值得探讨的问题,包括过敏原特异性免疫治疗(AIT,脱敏治疗)及抗IgE治疗(奥马珠单抗治疗)是否受COVID-19感染影响。
1 方法
1.1 研究设计 横断面调查。 在中国COVID-19防疫政策调整后的1个月(2023年3月10~31日)时间窗内招募广州医科大学附属广州市妇女儿童医疗中心(我院)呼吸、哮喘门诊和脱敏-抗IgE治疗门诊就医的儿童行改良过敏性鼻炎及哮喘患儿COVID-19感染后问卷(简称改良问卷)调查,以招募时间窗近4个月(2022年11月16日至2023年3月16日)发生COVID-19感染并既往诊断哮喘患儿为哮喘组,既往无哮喘病史的儿童为非哮喘组,分析COVID-19感染是否影响哮喘的控制及治疗。
1.2 伦理和知情同意 本研究获得我院伦理委员会审批通过,伦理号:穗妇儿科伦批字[2023]第223A01号。
1.3 诊断标准 ①哮喘诊断:参考儿童支气管哮喘诊断与防治指南(2016年版)[1];②COVID-19感染确诊标准:自测或医疗机构检测COVID-19抗原或核酸抗体阳性。
1.4 哮喘的治疗原则 我院哮喘治疗分为尘螨脱敏、奥马珠单抗、规律吸入糖皮质激素(ICS)和按需用药(未用长期哮喘控制药物治疗的患儿,急性发作时依据病情按需使用缓解药物等治疗),呼吸科医生根据临床判断选择不同方法干预。
1.5 改良问卷 基于广州医科大学附属第一医院呼吸疾病研究所开发设计的《过敏性鼻炎及哮喘患儿COVID-19感染后调查量表》,并得到了用于儿童人群的问卷改良授权。
1.5.1 改良问卷主要内容 包括3部分:①基本人口学特征及临床疾病基本情况(25个条目),②COVID-19疫苗接种情况(6个条目)及感染时症状调查(53个条目),③COVID-19感染前4周(15个条目)和COVID-19感染后哮喘症状变化(15个条目)。问卷共114个问题,均为选择题,部分问题为关联逻辑出现跳题为有效问卷,除此之外出现任意填写缺项均视为无效问卷。
1.5.2 调查时间、现场和填写 在招募时间窗内我院呼吸、哮喘门诊和脱敏-抗IgE治疗门诊中参与改良问卷填写的家长,通过互联网问卷星调查问卷平台,以现场扫码的方式,在改良问卷指导员陪同下现场填写并提交,填写时间约5 min。
1.5.3 改良问卷数据收集与分析 问卷数据审核和分析分别由本研究团队不同人员完成。
1.6 纳入标准 ①填写问卷前晚近4个月内患儿感染了COVID-19,②患儿家长自愿参与问卷调查并完成提交。
1.7 数据剔除标准 鉴于感染COVID-19后2周内的咳嗽症状会影响父母对于哮喘量表的客观评分,故剔除招募期间感染COVID-19后2周内就诊并填写改良问卷的数据。
1.8 分组 根据既往诊断哮喘分为哮喘组和非哮喘组。哮喘组进一步分为尘螨脱敏+奥马珠单抗亚组、尘螨脱敏亚组、规律ICS亚组和按需用药亚组。
1.9 结局指标
1.9.1 主要结局指标 COVID-19感染导致哮喘患儿住院比例。
1.9.2 次要结局指标 (1)哮喘组哮喘缓解期COVID-19感染前4周与感染后症状控制情况,①基于改良问卷第84~93条反映哮喘控制测试量表(ACTTM)情况:得分范围0~25分,<20分为哮喘未控制,20~24分为部分控制,25分为完全控制;②基于改良问卷第92和93条反映哮喘喘息的控制情况的家属视觉模拟评分(VAS)情况:0分为未控制,10分为完全控制。(2)哮喘组哮喘急性期COVID-19感染前4周与感染后症状控制情况,①因哮喘症状,您孩子是否有呼吸困难(改良问卷第86和87条);②因哮喘症状,您孩子是否有夜间醒来或早醒(改良问卷第88和89条);③您孩子是否需要使用急救药物治疗,如硫酸沙丁胺醇吸入气雾剂(改良问卷第90和91条)。
1.10 统计分析 应用EXCEL建立数据库并进行数据录入,采用SPSS 24.0软件进行统计分析。连续变量符合正态分布使用均数±标准差表示,组间比较采用t检验或方差分析;连续变量不符合正态分布使用中位数和四分位间距表示,组间比较采用非参数检验;分类变量采用频数和百分比表示,组间比较采用χ2检验;P<0.05为差异有统计学意义。
2 结果
2.1 病例纳入流程 图1显示,在2023年3月10~31日招募时间窗内我院呼吸、哮喘门诊和脱敏-抗IgE治疗门诊就诊患儿3 390例,向自愿参与调查问卷的865例患儿家长发放了问卷,排除无效问卷32份,有效问卷833份(96.3%)。833例患儿中未感染COVID-19的患儿516例。感染COVID-19并完成问卷调查的患儿317例,其中非哮喘组200例(63.1%),哮喘组117例,尘螨脱敏+奥马珠单抗亚组10例,尘螨脱敏亚组25例,规律ICS亚组29例,按需用药亚组53例。
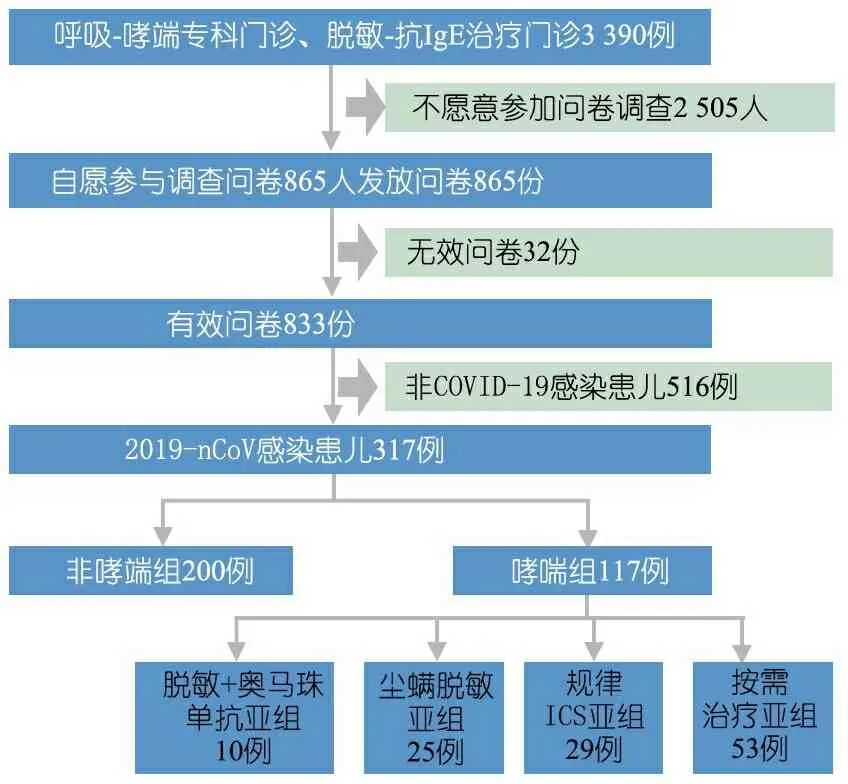
图1 纳入排除流程图
图2显示,317例中268例(84.5%)在2022年12月感染COVID-19,在非哮喘组占88.0%(176/200),在哮喘组占78.6%(92/117),两组差异无统计学意义(P>0.05),2023年1~3月COVID-19感染人数明显下降。

图2 2022年11月至2023年3月感染COVID-19例数分布情况
2.2 一般情况 表1显示,317例患儿中男192例(60.6%),女125例,平均年龄(6.0±3.6)岁,平均身高(115.0±26.0)cm,平均体重(24.2±12.5)kg。哮喘组和非哮喘组,基线数据(性别、年龄、身高、体重)差异无统计学意义(P>0.05),第一诊断及共病差异均有统计学意义(P<0.05),其中呼吸道感染非哮喘组比例高于哮喘组,过敏性鼻炎、食物过敏、过敏性皮炎哮喘组比例高于非哮喘组;过敏原中屋尘螨/粉尘螨、牛奶、鸡蛋、海鲜类食物、猫毛和狗毛、蟑螂和霉菌类差异均有统计学意义(P<0.05),且哮喘组比例高于非哮喘组,而花粉、小麦和花生差异均无统计学意义(P>0.05);已接种和接种2剂COVID-19疫苗比例差异有统计学意义(P<0.05),且哮喘组比例高于非哮喘组,接种1剂和3剂COVID-19疫苗比例差异无统计学意义(P>0.05)。

表1 317例感染COVID-19患儿的一般情况[n(%),xˉ±s]
2.3 临床症状及转归 表2显示,哮喘组与非哮喘组感染COVID-19需要住院治疗比例差异无统计学意义,恢复时间两组差异无统计学意义(P>0.05);无症状感染比例、神经系统症状中头痛比例哮喘组高于非哮喘组,差异有统计学意义(P<0.05),发热、咳嗽有痰和呕吐比例及平均热峰值非哮喘组均高于哮喘组,差异有统计学意义(P<0.05)。
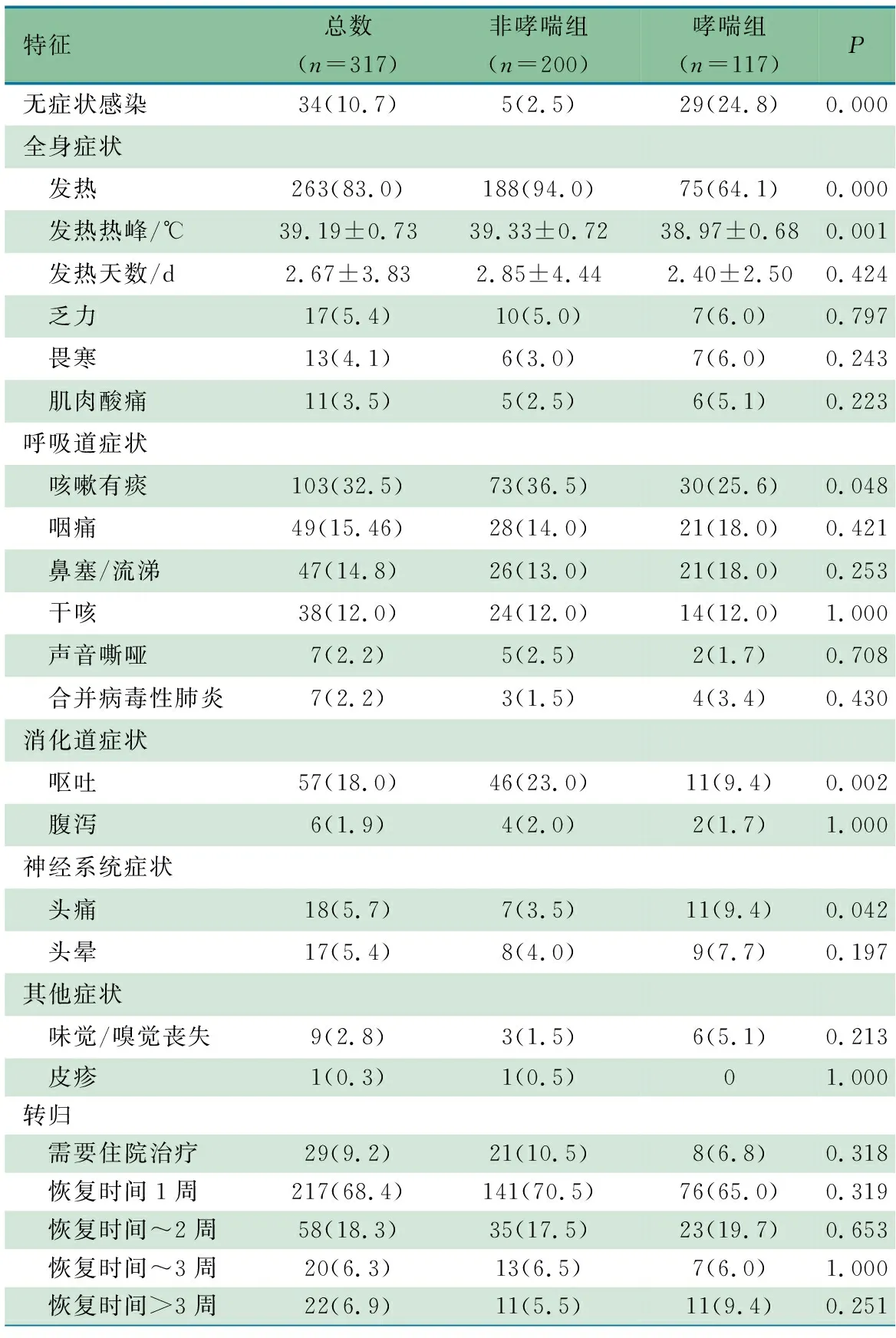
表2 317例感染COVID-19患儿临床症状及转归比较[n(%),xˉ±s]
2.4 哮喘组COVID-19感染前后症状分析
2.4.1 哮喘组不同亚组COVID-19感染前4周与感染后缓解期哮喘症状评估 表3显示,基于ACTTM和VAS评估,哮喘组和4个亚组(尘螨脱敏+奥马珠单抗、尘螨脱敏、规律ICS和按需用药)COVID-19感染前后比较、COVID-19感染前4周哮喘组4个亚组间比较、COVID-19感染后哮喘组和4个亚组间比较,差异均无统计学意义(P>0.05)。

表3 哮喘组不同亚组患儿哮喘缓解期感染COVID-19前后症状分析
2.4.2 哮喘组不同亚组COVID-19感染前4周与感染后急性期哮喘症状评估 表4显示,基于因哮喘症状,是否有呼吸困难、夜间醒来或早醒和需要使用急救药物治疗(如硫酸沙丁胺醇吸入气雾剂)评估,哮喘组和4个亚组COVID-19感染前后比较、COVID-19感染前4周哮喘组和4个亚组间比较、COVID-19感染后哮喘组和4个亚组间比较,差异均无统计学意义(P>0.05)。
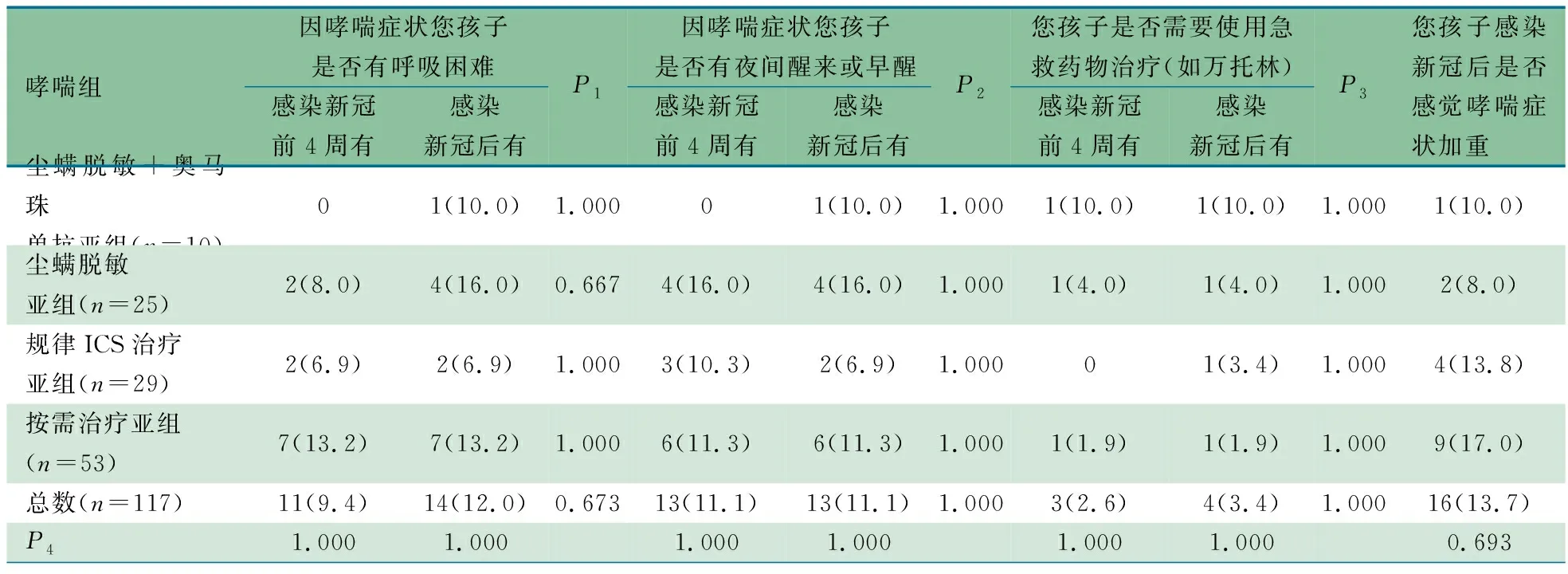
表4 哮端组不同亚组患儿急性期感染COVID-19前后症状分析
3 讨论
许多呼吸道病毒感染已被证实会导致哮喘患者病情加重,因此美国CDC在COVID-19大流行早期将哮喘列为COVID-19感染的风险因素[3]。但在COVID-19感染大流行期间,全球多项研究数据显示,儿童较成人COVID-19感染率低,发病症状轻[4],然而儿童哮喘与COVID-19感染之间的关系尚存争议[5, 6]。目前较多研究数据[6-8]显示,哮喘患儿不会增加感染COVID-19的风险,哮喘与感染COVID-19的严重程度无关。美国CDC发布,有0.1%~1.9%儿童感染COVID-19后需要住院治疗[9];国外回顾性数据表明,感染COVID-19的哮喘患儿比例为10.2%~21%[7, 10]。本研究中,2022年11月16日至2023年3月16日曾感染COVID-19的患儿317例,9.2%患儿需要住院治疗,无重症及死亡病例,哮喘患儿比例36.9%,哮喘组与非哮喘组住院率及感染后恢复时间差异无统计学意义(P>0.05)。本研究中的COVID-19感染患儿重症少及恢复快与国外报道基本一致,但本研究中的住院率及哮喘患儿比例均明显高于国外数据,其原因可能如下:①与中国防疫政策突然调整有关,图2显示84.5%的患儿均在2022年12月呈爆发聚集性感染;②也可能与当时COVID-19病毒株的差异有关;③也可能与本研究为儿童呼吸科就诊患儿的人群选择有关。
国外研究报道COVID-19感染的儿童多为无症状感染或轻症患儿,无症状感染率为12.7%~30.0%[9, 11, 12];欧洲多中心及美国的数据显示[11-13],COVID-19感染患儿发热比例为50.4%~60.5%;哮喘和非哮喘患儿的无症状感染率、发热比例及发热持续时间差异无统计学意义[14, 15]。本研究中,COVID-19感染患儿无症状感染率为10.7%,略低于国外文献报道;发热比例83.0%,高于国外文献报道。值得关注的是,本研究中哮喘组的无症状感染率显著高于非哮喘组(24.8%vs2.5%,P<0.05),哮喘组的发热比例及发热热峰显著低于非哮喘组(P<0.05),与既往国外文献报道不一致。此外,哮喘组的咳嗽有痰、呕吐发生率亦显著低于非哮喘组(P<0.05)。在本研究中哮喘组患儿总体临床症状较非哮喘组轻,其原因可能如下:①哮喘组患儿合并过敏性疾病(如过敏性鼻炎、过敏性皮炎等)及过敏原阳性(如尘螨、牛奶、鸡蛋等)的比例高,两组间差异有统计学意义(P<0.05),说明本研究中的哮喘组患儿是以高2型炎症为主的高过敏性哮喘患儿。血管紧张素转换酶2 (ACE2)是COVID-19感染人体的细胞受体,ACE2基因表达升高会增加机体对COVID-19的易感性[4]。研究证实,呼吸道过敏及过敏原暴露都与ACE2表达降低显著相关,ACE2在高过敏性哮喘患者中表达最低[3, 4]。且在过敏性哮喘患儿中,Th2炎症通路分泌白细胞介素(IL)-4、IL-5和IL-13,这些细胞因子可能会降低呼吸道上皮细胞ACE2的表达从而干扰COVID-19的复制,使感染COVID-19的哮喘患儿获益[16];②在COVID-19感染过程中,干扰素(INF-γ)的分泌可刺激ACE2的表达,但在过敏性哮喘患儿中,通常存在Th1/Th2失衡, INF-γ分泌减少,对COVID-19感染反应不足,降低ACE2基因表达从而减轻疾病的严重程度[17];③可能与过敏性哮喘患儿使用ICS治疗有关,文献报道[4],ICS治疗不会增加COVID-19感染易感性,反而对COVID-19感染具有保护作用。ICS与ACE2表达降低相关[18],布地奈德能抑制IL-6和IL-8的产生,而IL-6水平升高是严重COVID-19感染肺炎病例预后恶化的标记物[19];④文献报道[16, 20],过敏性哮喘患儿的嗜酸性粒细胞(IL-5作用于骨髓的最终产物)增高可能在减轻COVID-19感染症状中发挥重要作用。⑤诊断哮喘患儿的父母更加关注患儿的疫苗接种及日常防护。在本研究中,哮喘组患儿COVID-19疫苗及第2剂疫苗接种率显著高于非哮喘组(68.4%vs43.5%;50.4%vs32.0%;P均<0.05),疫苗接种的保护可能有助于减少病毒感染及病毒复制,从而减轻临床症状,建议提高哮喘患儿COVID-19疫苗接种率。
呼吸道病毒感染是儿童哮喘加重的最重要原因之一,目前仍无大规模数据调查因COVID-19感染导致哮喘加重的比率。国外数项研究显示,哮喘患儿在COVID-19感染期间的加重率为12.4%~24.0%[15, 21, 22]。本研究中,通过患儿家属自行评价的哮喘加重率为13.8%,与文献报道相似,但未收集数据与同期未感染COVID-19哮喘患儿加重率进行比较。AIT其中一个复杂作用机制是诱导Treg和Breg细胞产生IgA、IgG和IgG4阻断抗体从而发生作用[23],而Treg细胞在预防细胞因子风暴和限制组织损伤中发挥重要作用[24],由此可推测AIT诱导的免疫耐受可能对重症COVID-19感染患者中发生的细胞因子风暴具有假定的保护作用。此外,奥马珠单抗治疗即抗IgE治疗可增加INF-γ的产生,进而增强对呼吸道病毒的防御能力,还能降低促炎细胞因子的产生,如IL-33、IL-6、IL-1β和TNF-α,因此对COVID-19感染患者可能亦具有保护作用[25]。因此全球哮喘防治创议(GINA)、英国胸科协会(BTS)等建议[26],对于感染COVID-19或感染后康复的患者,不建议中断AIT治疗及哮喘相关的生物制剂治疗。本研究按不同的治疗方法将哮喘组患儿分为4个不同治疗亚组,发现同一亚组COVID-19感染前后缓解期及急性期症状控制自身对比差异无统计学意义,不同亚组COVID-19感染前后缓解期及急性期症状控制组间对比差异无统计学意义;本研究的数据也表明COVID-19感染大流行期间,哮喘患儿使用脱敏治疗和/或抗IgE治疗不会对其感染COVID-19时的疾病严重程度产生影响,与相关文献报道描述的作用机制表现类似,建议哮喘患儿在COVID-19感染大流行期间不要中断AIT及抗IgE治疗,以便达到良好的控制。
本研究的不足及局限性:①本研究是以父母填写调查问卷为主体的调查研究,数据收集会产生一定的信息偏倚,但因为COVID-19感染的过程对多数家庭而言是印象深刻的,父母均会仔细观察患儿并能够清楚地表达感染时患儿的临床症状,在很大程度上减少了信息偏倚的发生;②本研究人群主要包括轻度至中度哮喘患儿,其中多数属于哮喘控制患儿,缺乏重症哮喘患儿感染COVID-19的临床数据;③本研究为横断面研究,不能确定哮喘与感染COVID-19的因果关系。
