根治切除联合人工材料桥接治疗腹壁型侵袭性纤维瘤病16例报告
2023-12-11刘雅玲周婷周静瑜王沙龙周建平任峰
刘雅玲,周婷,周静瑜,王沙龙,周建平,任峰
(中南大学湘雅二医院 普通外科,湖南 长沙 410011)
侵袭性纤维瘤病(aggressive fibromatosis,AF)是一种临床比较罕见的交界性肿瘤,其发病率占所有肿瘤的0.03%。AF 以局部侵袭为主要特征,一般不具备远处转移能力,手术切除后复发率高,临床治疗较为棘手。随着对AF 研究的不断深入,目前治疗方式有等待观察[1]、局部治疗(手术切除、放疗、冷冻射频)、全身性药物治疗等。AF 分为腹外型、腹壁型和腹内型,其中腹壁型占全部AF 的25%,多起源于腹直肌与既往手术切口,位置浅表,患者常因触及腹壁渐进性增大包块为主诉求诊[2]。腹壁型AF 呈局部侵袭性生长,浸润肌肉筋膜及邻近组织,几乎不发生远处转移,手术是主要根治手段,移除肿瘤后的巨大腹壁缺损常需要疝和腹壁专科团队制定腹壁重建个体化方案。本文回顾性分析中南大学湘雅二医院普外老年外科收治的16 例经病理确诊为腹壁型AF 患者的临床资料,探讨根治切除联合人工材料桥接修复切除后腹壁缺损治疗腹壁型AF 的安全性和疗效。
1 资料与方法
1.1 一般资料
本研究收集了自2013年1月—2021年10月中南大学湘雅二医院普外老年外科收治的16 例腹壁型AF 患者,其中女性15 例,男性1 例;平均年龄35.3 (18~70) 岁;平均体质量指数(BMI)23.6(18.8~30.0)kg/m2。15 例女性中14 例有妊娠史,6 例有剖宫产史。所有患者均为初发,发病部位均为腹壁,14 例来源于腹直肌,2 例来源于腹内斜肌。肿瘤平均长径8.6(4~14)cm。16 例患者均以腹壁包块首诊,2 例有局部触压痛。16 例患者术前均行增强CT 检查,以明确肿瘤范围及毗邻情况。术前常规行肠道准备、呼吸功能锻炼及预防性使用抗生素(表1)。患者均知情同意,本研究经医院伦理委员会批准(批准号:2021047)。
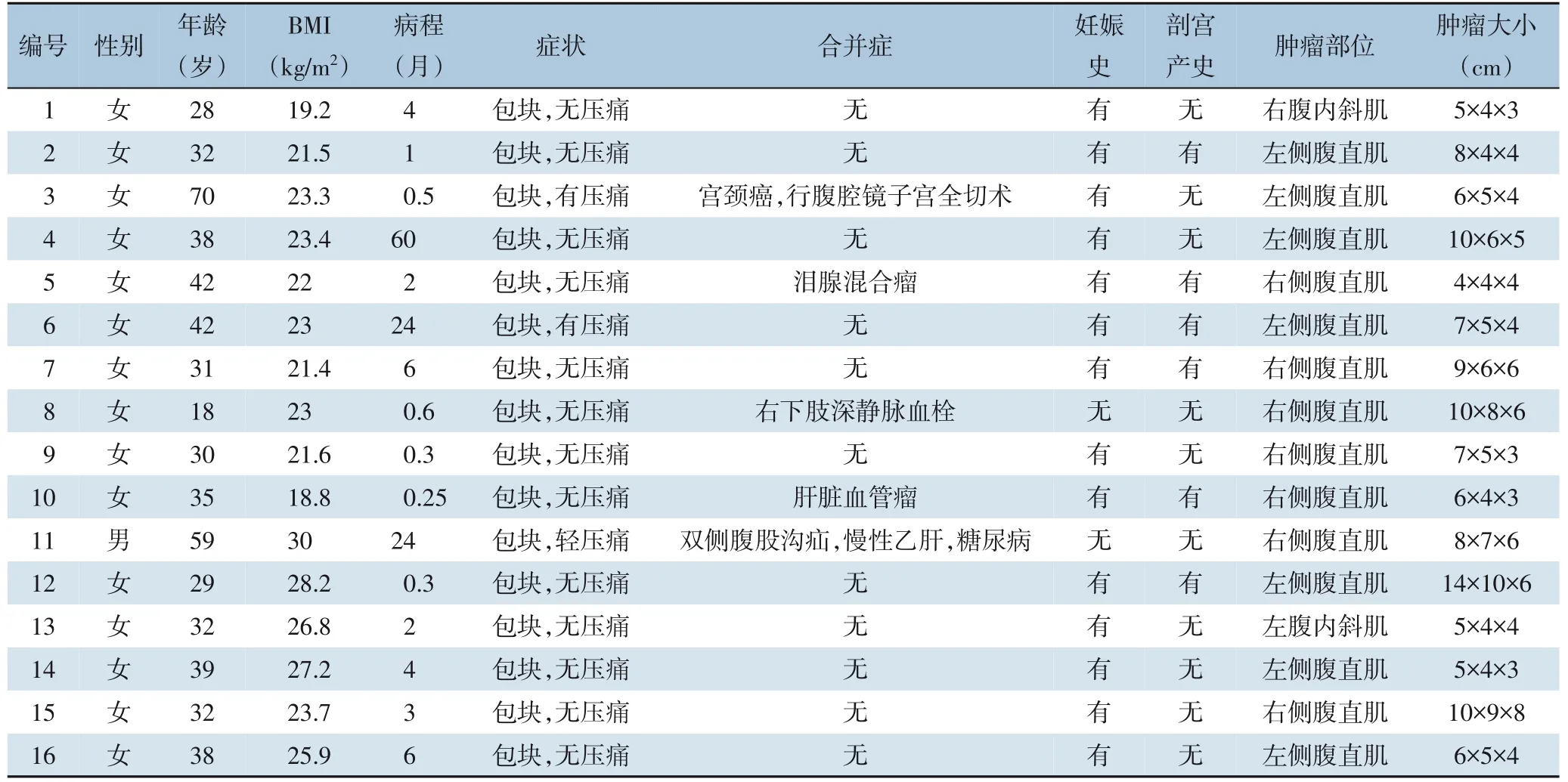
表1 16例腹壁型AF患者临床病理信息Table 1 The clinicopathologic information of the 16 cases of abdominal wall AF
1.2 修复材料
采用的人工材料有轻量型大网孔平片(15 cm×15 cm,15 cm×20 cm;强生公司,天助公司产品),自固定补片(15 cm×9 cm,15 cm×15 cm;Progrip 美敦力公司产品),防粘连复合补片(15 cm×20 cm,20 cm×25 cm;Proceed 强生公司,PCO 美敦力公司,天助公司产品)。固定钉选用5 mm Protack 螺旋钉。
1.3 手术方法
1.3.1 根治切除首先采用平行于肿瘤长轴的纵或横切口,切开皮肤皮下到达肿瘤处腱膜表面,充分游离腱膜前方全层皮瓣,超过肿瘤边缘3~5 cm;然后距离肿瘤边缘3 cm 以上腹白线或肌筋膜层薄弱处快速进腹,探查肿瘤处腹膜面,定位肿瘤边缘,电刀离断腱膜、超声刀离断肌肉,在手指引导下完整切除肿瘤及其周围2 cm 以上正常肌肉肌腱组织。注意肿瘤沿肌纤维走形方向浸润,如有异常,扩大切除范围。靠近肋弓边缘的肿瘤,必要时可以切除剑突、部分肋骨或肋软骨;贴近髂骨或耻骨边缘的肿瘤,紧贴骨质电刀消掉表层骨膜或软骨并烧灼创面,必要时借助骨科骨膜剥离器等器械进行剥离(图1)。包埋重要血管、神经应仔细分离尽量保留相应功能,必要时行人工血管置换或血管移植。

图1 耻骨上AF切除后状态Figure 1 View of the suprapubic AF after resection
1.3.2 腹壁缺损重建肿瘤切除后,根据肌筋膜缺损的部位和大小,选择合适的人工材料。缺损能关闭尽量关闭,不能关闭则使用桥接的方式修复肌筋膜缺损,具体桥接方式有以下3 种。⑴ sublay桥接:主要适用于下腹部腹直肌来源或侧腹部腹内斜肌来源的AF,本组6 例采用此术式。肿瘤切除后,充分显露缺损,游离皮下与前鞘或腹外斜肌腱膜层面以及肌后腹膜前层面,关闭腹膜,如果腹膜缺损过大,难以拉拢,可以将大网膜覆盖固定于腹膜缺损处以隔离腹腔内脏器。置入轻量型大网孔或自固定补片于腹膜前或后鞘前间隙(图2),补片前方放置引流管。由于先前大面积的游离,肌筋膜层缺损的两端常可以间断缝合关闭数针,避免张力过大,无法缝合关闭处缺损则采用双圈固定桥接修复,外圈固定予贯穿肌筋膜层缝合固定展平补片(自固定补片可省略此步骤),内圈固定予2-0 单股聚丙烯缝线(Prolene)连续缝合一圈桥接补片与缺损,放置2 根带负压球的槽型引流管,间断缝合伤口。⑵ 腹膜内补片(intraperitoneal onlay mesh,IPOM)桥接:主要适用于中上腹部腹直肌来源的AF,本组9 例采用此术式。肿瘤切除后,充分显露缺损,游离皮下与前鞘或腹外斜肌腱膜之间层面,根据缺损大小选择合适的防粘连补片置入腹腔,牵引肌筋膜层向中间靠拢,标记穿刺点经皮穿刺或直接贯穿肌筋膜层缝合补片外圈固定10~12 针,相邻两点间缝合补片边缘和腹膜防止形成内疝。两端间断缝合数针缩小缺损,2-0 单股Prolene 连续缝合桥接补片与缺损完成内圈固定。如果缺损周边肌筋膜层薄弱明显,可以用轻量型大网孔平片加做onlay 桥接双层加固(图3),补片前皮下间隙至少放置2 根带负压球的槽型引流管,间断缝合伤口。⑶ 立体桥接:主要适用于下腹部贴近耻骨联合或耻骨的AF,本组1 例采用此术式。肿瘤切除后,充分显露缺损,游离皮下与前鞘或腹外斜肌腱膜层面,沿缺损周边游离肌后腹膜前间隙超过缺损5 cm。向下游离耻骨膀胱间隙,充分显露耻骨联合和双侧耻骨梳韧带。缝合关闭腹膜,如果腹膜缺损过大,难以拉拢,可以利用大网膜或膀胱腹膜瓣覆盖。应用适形裁剪的自固定补片下方插入耻骨膀胱间隙,铺平于腹膜前间隙,予2-0 单股Prolene 缝合或螺旋钉将补片下缘固定于耻骨梳韧带,补片前放置引流管。缝合缩小肌筋膜层缺损,内圈予2-0 Prolene缝线连续缝合桥接补片与缺损,再使用轻量型大网孔平片覆盖于缺损表面,外圈间断缝合边缘数针固定至肌筋膜层,内圈再予2-0 Prolene 缝线连续缝合桥接补片与缺损。如果肿瘤切除破坏了腹股沟韧带,可用裁剪成条带状人工材料进行重建以提供补片支撑固定点(图4)。补片前方放置1~2 根带负压球的槽型引流管,间断缝合伤口。

图2 AF切除后sublay桥接Figure 2 Sublay bridging after AF resection
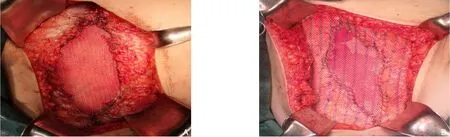
图3 AF切除后IPOM桥接 A:单纯ⅠPOM桥接;B:ⅠPOM+onlay桥接Figure 3 IPOM bridging after AF resection A:ⅠPOM bridging alone;B:ⅠPOM+onlay bridging
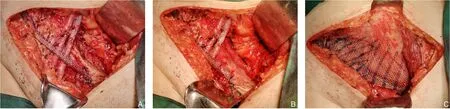
图4 AF切除后立体桥接 A:腹股沟韧带重建;B:下层sublay补片放置;C:上层onlay桥接Figure 4 Three-dimensional bridging after AF resection A:Ⅰnguinal ligament reconstruction;B:Sublay placement in the lower layer;C:Onlay bridging on the upper layer
1.4 术后处理
术后给予敷料填塞创面、腹带加压包扎,常规给予抗感染、营养等对症支持治疗,卧床密切观察5 d,每天检查引流量、性状及是否通畅,调整腹带松紧度,鼓励患者早期床上运动,必要时使用抗凝药物。术后5 d 第一次换药,若无皮下积液,继续观察每天引流量,少于30 mL 即可拔除引流管,术后10~14 d 拆线。常规应用腹带至术后3 个月,3 个月内避免重体力活动。
1.5 随访
所有患者术后3、6、12 个月均在门诊或病房由术者进行随访,包括问诊、视诊、触诊和影像学检查,并于术后1年左右复查腹部CT,结合电话跟踪随访。随访截至日期2022年10月30日。
2 结果
2.1 手术情况
16 例患者腹壁肿瘤均达到根治性切除,术后病理切缘均未见肿瘤残留。手术同期使用人工材料桥接修复肿瘤切除后的腹壁缺损。平均手术时间98(70~235)min,肿瘤切除后腹壁缺损6 cm×8 cm~14 cm×19 cm。人工材料桥接修复腹壁缺损方案中,6 例采用自固定补片sublay 桥接,9 例采用防粘连补片IPOM 桥接,1 例紧贴耻骨病例采用立体桥接(sublay+onlay 桥接)。所有手术均顺利完成。
2.2 并发症
15 例患者术后伤口愈合顺利,所有患者无伤口感染、补片感染、肠梗阻等并发症发生。1 例患者术后第5 天换药时发现皮瓣漂浮,出现术后血清肿,拆除美容缝线开放伤口充分引流后,通过封闭负压辅助闭合技术(VAC)治疗,行二期缝合后治愈。
2.3 手术疗效
中位随访46 (16~110) 个月,随访率100%。所有患者腹壁形态及卷腹运动功能良好,未见肿瘤复发,无慢性疼痛、补片感染、补片膨出及切口疝发生。
3 讨论
AF 组织学形态表现为肌肉成纤维细胞或中间型纤维母细胞肿瘤,病理检查时电镜下表现为正常的有丝分裂,在局部呈侵袭性生长,瘤体无包膜包裹易侵犯周围组织,易复发,不发生远处转移,所以临床上被认为是良性或是交界性病变[3]。文献[4]报道中名称多样,有硬纤维瘤、韧带样瘤、纤维组织瘤增生、腱膜纤维瘤、软组织韧带纤维瘤等。
本病发病较为罕见,每百万人中仅有2~4 例发病,且女性显著多于男性。发病隐匿,局部往往无明显不适症状,就诊时起病已久[5]。AF 分为腹外型、腹内型及腹壁型,腹外型最为多见。腹壁型来源于肌筋膜组织,腹直肌、腹内斜肌及其筋膜最为常见,一般局限于一侧不会跨越中线[6]。现有研究[7]发现AF 发病可能与雌激素水平、Wnt/β-catenin/APC 信号转导通路激活突变及组织创伤修复等相关,在家族性腺瘤性息肉病(FAP)患者群体中发病率显著升高。女性AF 发病往往与雌激素水平及组织创伤修复等相关,本组15 例女性14 例(93.3%) 为有妊娠史的育龄期女性,有6 例(40%) 有剖宫产史。湖南多中心研究结果[8]显示:腹壁型AF 绝大多数发生于有妊娠史的青年女性。从分子水平研究Wnt/β-catenin/APC 信号通路的激活是AF 发病机制之一。Wnt 信号通路激活或APC 基因突变导致细胞内β-catenin 异常积聚,导致肿瘤发生发展。β-catenin 由CMNNB1 基因编码,已有文献[9]报道与AF 相关的T41A、S45F、S45P 三种具体的CMNNB1 突变,其主要影响β-catenin 的稳定性和与α-catenin 的亲和力。本组16 例患者中唯一男性患者检测到CMNNB1 基因外显子3 (T41A) 突变,与文献报道一致。CMNNB1 基因突变位点可能是影响局部肿瘤复发的因素[10],此类患者要密切观察随访。基因检测对于明确病因、评估预后有积极意义,有条件均推荐进行。另外对于多发、多部位、多型结合的AF,要进行结肠镜检查以评估肠道情况是否合并家族性腺瘤性息肉病。
腹壁型AF 呈局部侵袭性生长,绝大多数情况下不发生远处转移,现有治疗方式主要包括手术治疗、保守等待观察[1,11-12]、放疗、化疗、内分泌治疗与非甾体类抗炎药(NSAIDs)、靶向治疗及物理治疗[13]。对于腹壁型AF 来说,等待观察不容易被接受,不仅加重患者心理负担,如若病灶继续增大,会导致手术难度和术后并发症概率增加。在有把握进行根治性切除与腹壁缺损重建的情况下,手术是腹壁型AF 的首选治疗方式。本组患者均实施了根治切除联合同期腹壁缺损修复,取得了满意效果。
对于腹壁型AF 而言,根治切除是第一步,完整的肿瘤切除及保留阴性切缘可以有效避免肿瘤的复发[14-15]。定位肿瘤边缘>2 cm[16],用超声刀结合电刀的方式进行切除,不仅需要彻底地切除病灶,而且需要尽量保留健康的肌筋膜以利重建。超声刀离断肌肉具有不出血、无肌肉收缩反应等优势。另外要注意肌纤维走行方向的病灶浸润,可疑的部位也应一并切除,必要时可送术中快速病检以明确切缘状态。本组1 例紧贴耻骨突入闭孔的AF,使用骨膜剥离器将肿瘤与骨皮质分离,切除腹股沟韧带,将股血管完全裸化后完整切除。
腹壁缺损修复目的在于恢复腹壁肌筋膜层的完整性、恢复肌肉支撑作用提供动态功能保护,防止内脏器官膨出[17],形态和功能都需要考虑。关闭肌筋膜层是腹壁缺损手术追求的目标,可以显著降低复发率和并发症率[18]。通常策略是采用组织结构分离技术(component separation technique,CST)[19]、术前渐进性气腹、肉毒毒素注射[20-21]来增加腹腔容积,主动减容[22]切除大网膜或部分脏器减少腹腔内容物体积,使用人工材料综合应用各种修复技术来完成腹壁重建。CST 针对腹中线区域的缺损修复具有重要意义,可以通过肌筋膜层滑行关闭缺损,位置不同滑行的效果也存在差异。然而临床上还是会碰到肌筋膜层缺损无法关闭的情况,比如腹壁巨大肿瘤根治切除后的缺损、巨大切口疝肌筋膜层缺损、腹壁外伤或严重感染导致的肌筋膜层毁损等,往往需要使用人工材料的桥接来修复[23]。本组腹壁型AF 位于一侧腹直肌或腹内斜肌内,平均长径8.6 cm,在各个方向上均需保留2~3 cm 阴性切缘,另外由于肌肉回缩缺损较切除范围更大,而且常累及多个缺损分区,难以直接关闭,需要使用人工材料结合各种修复技术来完成腹壁重建[19]。此时切口疝修复时常用的基于肌筋膜层滑行关闭缺损的CST,包括腹外斜肌腱膜松解和腹横肌松解术均难以实施,效果也大打折扣,此时使用人工材料桥接修复应为合适选择[17,24]。
腹壁存在如腹白线、脐、半月线等单一承力性腱膜性结构,人工材料桥接类似于构造一个大小不一的单一腱膜性结构,从而达到腹壁结构和功能上的完整。既往文献[25]报道的桥接仅是简单用固定钉将补片和缺损边缘固定,术后易复发和出现局部膨出,完成了双圈固定钉固定后,虽然复发率有所下降,但长期随访的结果显示患者的生活质量显著下降。本组桥接修复以开放手术的方式完成,双圈固定补片,外圈贯穿肌筋膜层缝合固定(自固定补片可免去此步骤),内圈用非吸收缝线连续缝合补片和缺损边缘,使桥接区域的压力均匀地分散在整圈的各个方向上。桥接手术成功的关键在于:⑴ 保持桥接区域人工材料合适张力,防止术后出现膨出;⑵ 人工材料与肌筋膜层有效固定和融合,防止复发。下腹部腹膜延展性大,还可以利用大网膜和膀胱腹膜瓣,大部分腹膜可以关闭,且由于膀胱因素影响IPOM 补片固定,所以选用自固定或轻质大网孔补片做sublay 补片桥接修复较为合适,本组6 例采用sublay 桥接;对于中上腹部缺损,肿瘤切除后腹膜难以关闭,使用防粘连补片做IPOM 桥接是切实可行的[26],本组9 例采用IPOM 桥接;针对下腹紧贴耻骨联合的肿瘤,切除后重建时要先放置1 张补片插入耻骨膀胱间隙,下方牢固固定于双侧耻骨梳韧带,完成桥接修复后,在缺损上方再放置一层补片加固缺损(sublay+onlay),两补片之间会形成小的空腔,从侧面看补片的组合使用形成立体的修复结构,即立体桥接,本组1 例紧贴耻骨病例采用立体桥接修复。补片尽量铺平,避免折叠和卷曲,要足够大超过缺损边缘5 cm 以上并牢固固定[27-28]。补片前方要放置引流管充分引流,推荐使用低负压槽型引流管。
本组全部患者均获得完整随访资料,中位随访46(16~110)个月,无肿瘤复发。其他并发症如血清肿、补片膨出、补片感染、肠梗阻等与其他腹壁缺损并发症类似,规范手术操作、充分引流、减少死腔可以有效预防相关并发症。在本组16 例患者中,仅1 例患者行IPOM 补片桥接修复后出现血清肿,通过开放伤口联合VAC,行Ⅱ期缝合后治愈,随访患者恢复可,无不适。为了便于处理伤口局部并发症,推荐使用间断缝合关闭伤口。余15 例患者均达到伤口甲级愈合。本组观察及随访无慢性疼痛、补片感染、补片膨出及切口疝发生,腹壁形态及功能恢复均令人满意。术后应保证充分的营养与休息、腹带固定3 个月以上、避免重体力劳动,让组织和补片有足够的时间融合。
任何一种技术都有其优缺点,对于复杂的腹壁缺损而言,术前充分地评估和准备、综合运用各种腹壁修复技术、选择合适的修补材料、精准的个体化治疗方案和完善的术后并发症处理是确保手术成功的关键所在。
综上所述,腹壁型AF 的治疗方式主要是手术,根治切除与腹壁重建是影响预后的关键因素,使用人工材料桥接修复AF 切除后的肌筋膜层缺损是安全可靠的。
利益冲突:所有作者均声明不存在利益冲突。
作者贡献声明:刘雅玲负责收集资料,论文撰写;周婷、周静瑜、王沙龙、周建平负责研究实施;任峰负责资料收集,研究实施,论文撰写。
