复方脑肽节苷脂治疗3 884 例颅脑损伤患者安全性再评价
2023-12-06谭安军文君文娟胡浪毕晓梅
谭安军 文君 文娟 胡浪 毕晓梅
颅脑损伤为暴力直接或者间接作用导致头部损伤,作为神经外科急症类型之一,具有进展迅速、病情危急、残疾率高以及预后差等特点,其病死率居于各种创伤性疾病第一位,严重影响患者生命健康[1-2]。复方脑肽节苷脂是临床常见纠正脑代谢异常以及营养脑神经药物,其可以发挥修复损伤神经组织、促进神经元蛋白合成、纠正脑神经代谢异常作用[3]。复方脑肽节苷脂已被应用于多种脑部疾病治疗中,已获得临床医师及患者认可,但是其使用后会出现呕吐、腹泻、腹痛甚至休克等不良反应,因此复方制剂尤其是复方制剂注射制剂不良反应逐渐成为研究者们关注重点,用药安全性已成为其上市后再评价主要内容之一[4]。2009 年科技部设置了科技专项——“药物上市后再评价技术”,其后针对药物上市后安全性再评价研究逐渐增多,并逐渐积累了一些实践经验以及方法[5]。本研究将探究复方脑肽节苷脂注射治疗3 884 例颅脑损伤患者临床安全性,以期为后期临床上应用提供参考依据,现报道如下。
1 资料和方法
1.1 研究对象
研究采用多中心、大样本、前瞻性医院集中监测方法设计,依据医院等级、医院位置及医院类型,纳入全国多家三级、二级中医与西医医院。将2020 年3 月至2022 年2 月在监测机构至少接受1次复方脑肽节苷脂注射液治疗颅脑损伤患者作为研究对象,纳入标准:颅脑损伤依据颅脑CT 以及病史确诊[6];患者入院后采用格拉斯哥昏迷评分[7]显示后9~12 分;有明确的外伤史;患者受伤6 h 内入院接受治疗;患者预计生存时间超过3 个月;患者或者家属同意参与研究,研究进行符合《赫尔辛基宣言》中伦理学标准。排除标准:存在癫痫以及颅内占位性病变等脑部疾病者;伴肾脏、心脏以及肝脏等重要脏器功能异常者;过去即存在颅骨结构缺陷、颅脑损伤或者接受过颅骨去骨瓣术治疗者;伴精神类或者神经疾病者;对复方脑肽节苷脂过敏者;处于妊娠期、哺乳期者。在46 家医院收集数据,其中二级与三级医院分别14 家与32 家,西医与中医分别37 家与9 家,而东部、西部以及中部地区分别17 家、19 家以及10 家。最终纳入研究颅脑损伤患者3 884 例,其中男2 247 例,女1 637例。通过医院信息系统、实验室(检验科)信息系统等收集病人基本信息、用药信息及不良事件发生情况,并详细记录。
1.2 用药方案
作为非干预性研究,患者治疗方案由临床医师制定,主要包含复方脑肽节苷脂注射液(吉林天成制药有限公司;国药准字H22026472/国药准字H22026457,规格:2 mL/5 mL)用药及其他合并用药,10~20 mL 复方脑肽节苷脂注射液溶于250 mL 0.9%氯化钠注射液或者5%葡萄糖注射液中,以2 mL/min 速度缓慢滴注,用药频率1 次/日,用药2 周为一个疗程或者遵医嘱进行用药治疗。
1.3 观察指标
1.3.1 复方脑肽节苷脂注射液用药方案
是否为首次应用、首次用药剂量、溶酶体种类、注射时间、用药频率、合并疗法、用药时间。
1.3.2 临床转归
记录患者临床转归情况,具体包含病愈、好转、无改变、加重,病愈为患者NIHSS 评分减少率超过90%,无任何后遗症,好转为NIHSS 评分减少率范围为45%~90%,存在1~3 及病残,无改变为病情未见改善,存在4~6 级病残,加重为NIHSS 评分减少率≤45%或者评分增加,存在7 级伤残[6]。总有效率=病愈率+好转率。
1.3.3 用药安全性
按照相关标准[8]统计患者用药期间不良事件或者不良反应发生情况,并根据不良事件或者反应严重程度(轻、中、重)进行分类统计,其中轻度为停药后好转,且不需治疗,中度为患者出现短时间损伤,经治疗后恢复,重度为患者出现短暂甚至永久损伤,需要接受治疗甚至延长住院时间。
1.3.4 生命体征监测
统计患者用药前及用药后1 d 体温、脉搏、呼吸频率、收缩压以及舒张压情况。
1.3.5 血常规检查
在用药前及用药后1 d 测定患者血常规情况,主要包括红细胞计数(Red blood cell count,RBC)、血小板计数(platelet count,PLT)、白细胞计数(White blood cell count,WBC),三指标正常分别为(3.5~5.5)×1012/L、(100~300)×109/L、(4~10)×109/L,否则为异常。
1.4 统计学方法
通过SPSS 20.0 软件予以分析处理,呈正态分布计量资料表示为()形式,行t检验,非正态分布计量资料表示为P50(P25,P70),计数资料用频数、频率进行统计描述,差异比较采用χ2检验,以P<0.05 为差异具有统计学意义。
2 结果
2.1 复方脑肽节苷脂注射液用药方案
患者用药剂量为6(4,16)mL,注射时间为90(60,125)min,用药时间为7(4,11)d,其他资料如首次用药、单次使用溶媒剂量、溶酶体种类、用药频率、合并疗法、合并用药等见表1。
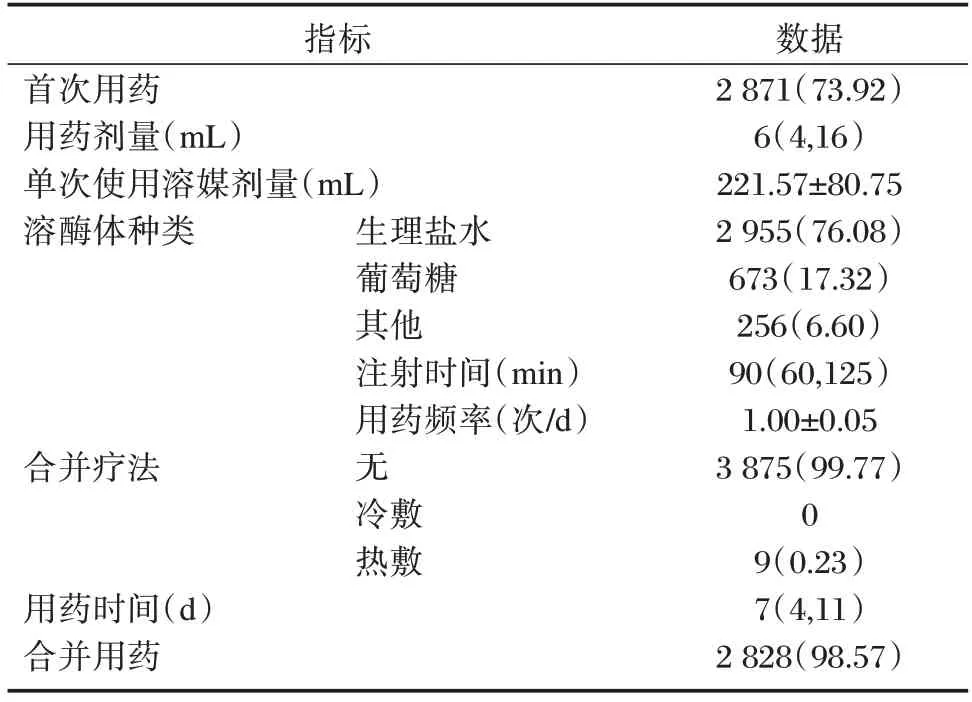
表1 复方脑肽节苷脂注射液用药方案Table 1 Dosage schedule of compound porcine cerebroside and ganglioside injection
2.2 患者临床转归情况分析
患者病愈、好转、无变化、加重、死亡发生率分别为4.04%、83.88%、11.71%、0.28%、0.08%,总有效率为87.92%。
2.3 患者用药后安全性分析
患者不良事件及不良反应发生率分别为7.13%(277/3 884)与0.28%(11/3 884),轻度、中度、重度不良事件发生率分别为4.12%、2.78%、0.41%,轻度、中度不良反应发生率分别为0.18%、0.10%;不良事件主要涉及全身性损伤(1.55%)、呼吸系统(1.29%)、神经系统(1.06%)、胃肠系统(1.83%),不良反应主要涉及皮肤系统(0.05%)、呼吸系统(0.05%)、神经系统(0.03%)、胃肠系统(0.08%)、心血管系统(0.05%);大部分患者不良事件(5.87%)及不良反应(0.28%)均好转。见表2。
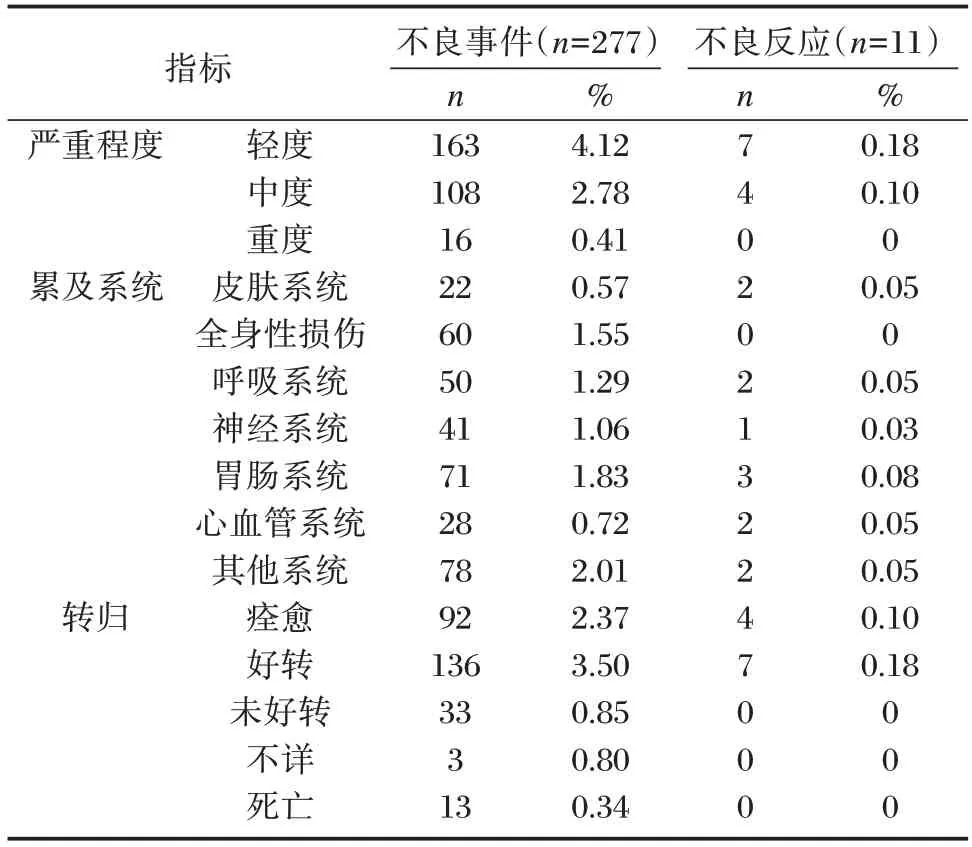
表2 患者用药后安全性分析Table 2 Safety analysis of patients after medication
2.4 患者用药前后生命体征变化
患者用药前后体温、脉搏、呼吸频率、收缩压以及舒张压等比较差异没有统计学意义(P>0.05)。见表3。
表3 患者用药前后生命体征变化()Table 3 Changes in vital signs of patients before and after medication()
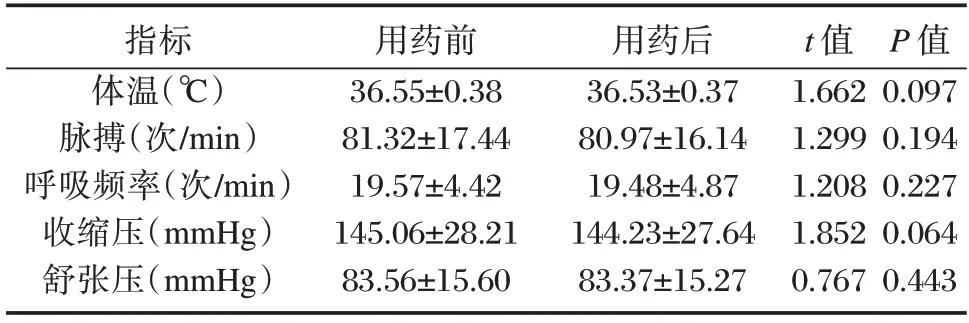
表3 患者用药前后生命体征变化()Table 3 Changes in vital signs of patients before and after medication()
2.5 患者用药前后血常规变化
患者治疗前后RBC、PLT、WBC 异常发生率比较差异没有统计学意义(P>0.05)。见表4。
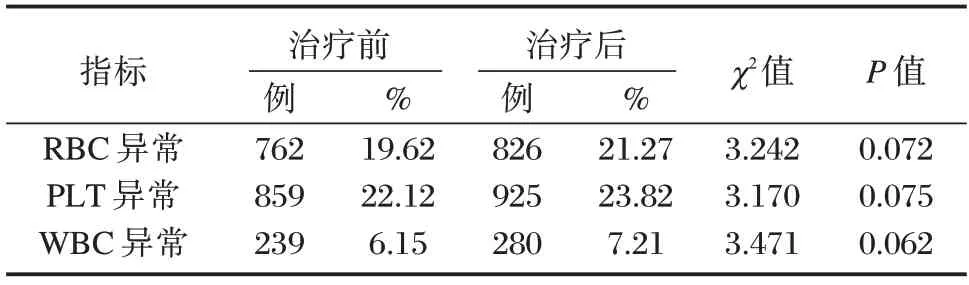
表4 患者用药前后血常规异常情况比较Table 4 Comparison of blood routine abnormalities before and after medication
3 讨论
复方脑肽节苷脂是以次黄嘌呤、多肽以及神经节苷脂为主的神经营养药物,其中次黄嘌呤与多肽可以介导脑组织中物质与能量代谢过程,而神经节苷脂则可以介导神经元分化、生长以及再生过程,均可以促进脑组织损伤修复[9-10]。动物实验结果显示宫内缺氧小鼠脑损伤采用复方脑肽节苷脂处理后有助于减轻小鼠神经功能损伤,其作用机制为复方脑肽节苷脂抑制小鼠星形胶质细胞激活,诱导神经细胞突触以及轴突再生,进而发挥神经保护作用[11]。复方脑肽节苷脂对控制性皮质撞击所致灰质和白质损伤具有明显神经保护作用,激活Nrf2 信号和减轻氧化应激介导的钙蛋白酶激活可能是复方脑肽节苷脂保护脑损伤的机制之一[12-13]。老年脑梗死后认知功能障碍患者接受盐酸多奈哌齐片联合复方脑肽节苷脂治疗,可以改善患者运动功能、神经损伤以及认知功能,同时可以明显改善患者C 反应蛋白、D-二聚体、纤维蛋白原、同型半胱氨酸等指标水平,盐酸多奈哌齐片联合复方脑肽节苷脂治疗用于治疗脑组织损伤疗效显著及安全性高[14]。李兴明等[15]研究显示急性脑梗死采用复方脑肽节苷脂注射液治疗可以明显改善患者神经功能损伤,同时抑制患者体内超敏C 反应蛋白、脂蛋白相关磷脂酶A2以及神经元特异性烯醇化酶水平,且不会增加患者不良反应。国外研究也显示复方脑肽节苷脂注射液可以防止神经元凋亡,通过减少aβ 积累、抑制炎症反应和氧化应激对阿尔兹海默症发挥保护作用[16]。可见脑损伤应用复方脑肽节苷脂注射液治疗有助于减轻脑组织损伤,促进脑神经修复,其治疗疗效显著。本研究中患者治疗总有效率为87.92%,也证实了复方脑肽节苷脂注射液用于颅脑损伤治疗安全性。
本研究患者不良事件及不良反应发生率分别为7.13%与0.28%,不良事件或者不良反应均为轻度或中度,患者大部分通过停药或者对症治疗获得好转,且用药前后患者生命体征及血常规未出现明显变化,显示颅脑损伤患者应用复方脑肽节苷脂注射液治疗安全性高。本研究中患者复方脑肽节苷脂用药剂量为6(4,16)mL,注射时间为90(60,125)min,用药时间为7(4,11)d,所有患者在进行用药时均严格把握用药指征,这在一定程度上有助于防止用药不良反应及事件发生。另一项研究显示重症颅脑损伤接受亚低温治疗患者加用复方脑肽节苷脂治疗后不良反应并未明显增加,也证实复方脑肽节苷脂用药安全性[17]。但是本研究结果也证实,复方脑肽节苷脂注射液应用后不良事件及不良反应涉及多个系统,多见于呼吸系统与胃肠系统,因此在患者用药前需要仔细询问是否存在过敏史及各种伴随疾病,依据患者情况进行用药,合理用药是防止患者用药后不良反应发生重点。
综上所述,颅脑损伤患者接受复方脑肽节苷脂注射液治疗后偶有不良事件发生,但是不良反应发生率较低,疗效显著,且治疗安全性高。尽管如此,后期依然需要参照国内外研究者对于上市后药物安全性评估经验,通过自发上报、主动监测、登记注册、医院集中检测等多种方法,更充分评估复方脑肽节苷脂注射液安全性,为患者安全用药提供更有效参照依据。
