卡瑞利珠单抗+VEGF抑制剂抗血管生成双靶治疗对晚期非小细胞肺癌患者b-FGF、TSGF、VEGF水平的影响
2023-12-05申晓燕马耀先李伟孙桢方晓瑞骆许静
申晓燕,马耀先,李伟,孙桢,方晓瑞,骆许静
许昌市中心医院肿瘤内科,河南 许昌 461000
非小细胞肺癌(non-small cell lung cancer,NSCLC)发病在肺癌中占80%[1-2]。有研究显示[3],靶向药物治疗能极大程度改善并延长表皮生长因子受体等驱动基因以提高NSCLC患者预后。卡瑞丽珠单抗是免疫检查点抑制剂,又称程序性死亡受体1 (programmed death 1,PD-1),为人源化免疫球蛋白G4 型单克隆抗体。该药物为常见抗PD-1 的单抗,目前已有研究证实该药在晚期胆道癌等肿瘤中取得良好效果[4]。研究表明,血管生成能提高癌细胞免疫逃逸[5],抗血管生成药物能通过靶向肿瘤血管使血管逐渐正常化,血管内皮生长因子(vascular endothelial growth factor,VEGF)抑制剂联合PD-1 可产生更持久作用[6-7]。为此,本研究将观察卡瑞利珠单抗与VEGF 抑制剂抗血管生成双靶治疗晚期NSCLC 的疗效,并探讨其对患者碱性成纤维细胞生长因子(b-FGF)、肿瘤特异性生长因子(TSGF)和VEGF 水平的影响现,现将结果报道如下:
1 资料与方法
1.1 一般资料 经我院医学伦理委员会批准,选取2019 年8 月至2021 年3 月许昌市中心医院肿瘤内科收治的63例晚期NSCLC患者纳入研究。纳入标准:符合《NCCN 非小细胞肺癌临床诊治指南》标准[8]且经病理检查确诊为NSCLC;TNM分期为ⅢB~Ⅳ期;非鳞状NSCLC患者;肺癌驱动基因突变阴性者;预生存期超过3 个月者;患者知情同意。排除标准:鳞癌患者;严重出血或近期发生咯血者;血压、血糖无法控制者;免疫系统障碍者;处于抗凝治疗者;重要血管受到侵犯者;精神疾病及认知异常者;合并其他恶性肿瘤者。按随机数表法将患者分为对照组31 例和研究组32 例,对照组中男性19 例,女性12 例;年龄32~78 岁,平均(65.01±10.38)岁;体质量指数(BMI)为23.1~28.7 kg/m2,平均(25.80±3.14)kg/m2;TNM 分期:ⅢB 期20 例、Ⅳ期11 例。研究组中男性21 例,女性11 例;年龄35~80 岁,平均(64.58±10.43)岁;BMI 为22.4~28.5 kg/m2,平均(25.41±3.26) kg/m2;TNM 分期:ⅢB期22例、Ⅳ期10例。两组患者的一般资料比较差异均无统计学意义(P>0.05),具有可比性。
1.2 治疗方法 对照组患者给予注射用卡瑞利珠单抗(苏州盛迪亚生物医药有限公司,国药准字S20190027,规格200 mg)治疗,每次200 mg,第1 天静注1 h,1 次/3 周。同时给予化疗方案:第1 天以500 mg/m2标准静滴培美曲塞,第1~3天以75 mg/m2标准静滴1 h 顺铂;或第1 天、第8 天以1 000 mg/m2标准静滴1 h吉西他滨,第1~3 天静滴顺铂。以3 周为一个化疗周期,根据耐受情况进行化疗4~6 个周期;后每隔3 周静注1 次卡瑞利珠单抗,直至疾病进展或发生不耐受毒性。研究组患者则在对照组治疗的基础上联合贝伐珠单抗注射液(齐鲁制药有限公司,国药准字S20190040,规格100 mg:4 mL)治疗,第1 天,以7.5 mg/kg 标准静滴1 h,1 次/3 周,治疗4 个疗程,或以患者发生无法耐受的毒副反应时停止。
1.3 观察指标与评价(检测)方法 (1)疗效:治疗4个月后评估疗效,疗效评估参照文献[9]标准:4周及以上两个连续观察点病变均完全消失为完全缓解(complete remission,CR);观察点和基线肿瘤符合下降超过30%为部分缓解(partial relief,PR);基线肿瘤符合增加超过20%为疾病进展(progression disease,PD);与CR、PR 标准不符,且无PD 情况为疾病稳定(Stability disease,SD)。(2)血清指标检测:治疗前与治疗4 个月后抽取患者静脉血,采用酶联免疫吸附法检测血清碱性成纤维细胞生长因子(basic fibroblast growth factor,b-FGF)、肿瘤特异性生长因子(tumor specific growth factor,TSGF)、VEGF。(3)免疫指标检测:流式细胞仪(贝克曼,型号CytoFLEX)检测治疗前后两组患者的T细胞亚群水平,包括CD3+、CD4+、CD8+指标,计算CD4+/CD8+比值。(4)不良反应:参照抗肿瘤药物不良反应[10],将患者发生的不良反应分为0~Ⅳ级,记录两组患者的血液毒性、骨髓抑制、神经毒性、肝肾功能损伤、消化道反应发生例数。
1.4 统计学方法 应用SPSS20.0软件进行数据统计学分析。计量资料符合正态分布的,以均数±标准差(±s)表示,组间比较采用t检验;计数资料比较采用χ2检验,等级资料比较采用Z检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者的治疗效果比较 研究组患者的治疗总有效率和疾病控制率分别为31.25%、81.25%,明显高于对照组的9.68%、54.84%,差异均有统计学意义(P<0.05),见表1。
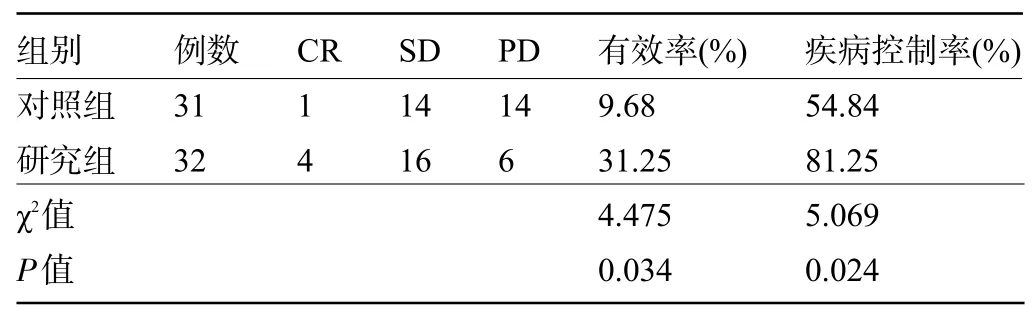
表1 两组患者的治疗效果比较(例)Table 1 Comparison of therapeutic effects between the two groups of patients(n)
2.2 两组患者治疗前后的血清b-FGF、TSGF、VEGF水平比较 治疗前,两组患者的血清b-FGF、TSGF、VEGF水平比较差异均无统计学意义(P>0.05);治疗后,两组患者的血清b-FGF、TSGF水平下降,VEGF水平上升,且研究组患者的血清b-FGF、TSGF、VEGF 水平明显低于对照组,差异均有统计学意义(P<0.05),见表2。
表2 两组患者治疗前后的血清b-FGF、TSGF、VEGF水平比较(±s)Table 2 Comparison of serum b-FGF,TSGF,and VEGF levels between the two groups of patients before and after treatment(±s)
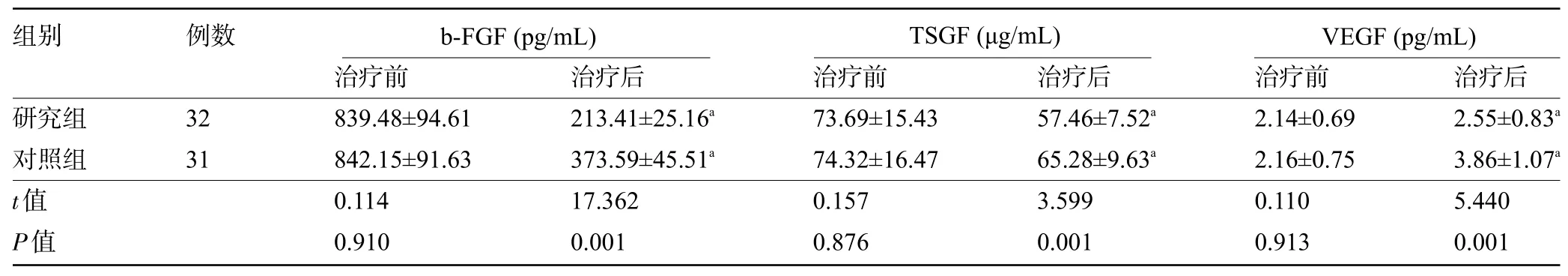
表2 两组患者治疗前后的血清b-FGF、TSGF、VEGF水平比较(±s)Table 2 Comparison of serum b-FGF,TSGF,and VEGF levels between the two groups of patients before and after treatment(±s)
注:与本组治疗前比较,aP<0.05。Note:Compared with that before treatment,aP<0.05.
?
2.3 两组患者治疗前后的免疫功能比较 治疗前,两组患者的免疫功能指标比较差异均无统计学意义(P>0.05);治疗后,研究组患者的CD3+、CD4+及CD4+/CD8+明显高于对照组,差异均有统计学意义(P<0.05),但两组患者的CD8+水平比较差异无统计学意义(P>0.05),见表3。
表3 两组患者治疗前后的免疫功能指标比较(±s)Table 3 Comparison of immune function indicators between the two groups of patients before and after treatment(±s)

表3 两组患者治疗前后的免疫功能指标比较(±s)Table 3 Comparison of immune function indicators between the two groups of patients before and after treatment(±s)
注:与本组治疗前比较,aP<0.05。Note:Compared with that before treatment,aP<0.05.
?
2.4 两组患者的不良反应比较 治疗期间两组患者均未发生Ⅳ级以上不良反应,血液毒性、骨髓抑制、神经毒性、肝肾损害、消化道反应的不良反应等级分布比较差异均无统计学意义(P>0.05),且各反应发生率比较差异也无统计学意义(P>0.05),见表4。

表4 两组患者的不良反应比较(例)Table 4 Comparison of adverse reactions between the two groups of patients(n)
3 讨论
NSCLC早期隐匿性较强,患者确诊时大多处于晚期,治疗难度大且预后差[11-12]。故针对晚期NSCLC的治疗主要以延长患者生存时间并改善其生存质量为原则。PD-1 为肿瘤免疫治疗的代表性药物,极大程度改变了NSCLC 患者的治疗前景,为一线治疗方案[13-14]。本研究使用卡瑞丽珠单抗与VEGF抑制剂联合治疗晚期NSCLC,研究组有效率、疾病控制率高于对照组,提示卡瑞丽珠单抗联合VEGF 抑制剂行抗血管生成双靶治疗相对于单一使用卡瑞丽珠单抗能显著提高近期疗效。原因为卡瑞利珠单抗为人类免疫球蛋白G4单克隆抗体,结合PD-1受体能阻断PD-1信号通路而抑制免疫细胞,提高对癌细胞免疫能力,导致肿瘤坏死、单核细胞浸润在肿瘤内部。贝伐珠单抗能结合血管生长因子能抑制肿瘤血管形成,使异常新生血管逐渐正常化,提高卡瑞丽珠单抗疗效,与其联合能发挥协同作用[15]。邱水晶[16]研究指出,阿特珠单抗和贝伐单抗联合化疗治疗NSCLC 患者,其中位生存时间和无进展生存期明显长于贝伐单抗单独治疗者,与本研究结果一致。
b-FGF为一种多肽,可促进血管生成;研究表明该物质能刺激细胞增殖转移,对肿瘤血管生成有促进作用以参与恶性肿瘤的发生发展[17]。TSGF 为一种非血细胞生长因子,是新型肿瘤标志物,能促进细胞生长、侵袭与转移。正常状态下TSGF产生于T细胞或单核细胞,机体内含量较低;当组织癌变后,TSGF 分泌于癌细胞并入血,使其血清中水平上升,与组织癌变发生恶性循环[18]。VEGF 参与肿瘤血管生成,能诱导肿瘤血管生成,还能诱导调节性T细胞增殖分化等使肿瘤微环境出现免疫抑制[19]。抗血管生成药能使肿瘤血管趋于正常,还能逆转免疫抑制,对淋巴细胞与效应因子运输至肿瘤病灶有促进作用[20]。研究组治疗后血清b-FGF、TSGF、VEGF 水平均低于对照组,提示卡瑞利珠单抗联合VEGF抑制剂能减缓或抑制患者新生血管形成,减慢肿瘤发展速度。
T 细胞亚群水平为机体细胞免疫功能的主要体现,是临床重要的指标[21]。CD3+参与T细胞的信号转导,CD4+能识别抗原信号转导,CD8+是抑制性T细胞,能杀灭细胞,本研究治疗后研究组CD3+、CD4+及CD4+/CD8+比值高于对照组,说明卡瑞丽珠单抗联合VEGF抑制剂进行抗血管生成双靶治疗能有效改善机体免疫功能[22]。该结果原因为血管生长因子上调后可降低肿瘤微环境中T 细胞功能,进而抑制肿瘤免疫反应,给予贝伐单抗对T 细胞转运、浸润具有促进作用,联合卡瑞利珠单抗显著改善患者免疫功能,使NSCLC 患者获得最大收益[23]。两组不良反应情况差异无统计学意义,说明卡瑞利珠单抗联合VEGF 抑制剂不会增加患者不良反应事件,还能有效提高患者生存质量。韩宝惠等[24]研究报道,免疫治疗与抗血管生成双靶治疗对晚期NSCLC 有良好疗效,且安全性较高,为本研究治疗研究提供了更充分的数据支持。肿瘤微环境与免疫反应和血管生成关系较为复杂,如何合理使用免疫治疗、抗血管生成药并确定使用剂量、时长及联合治疗的安全性等,为NSCLC 患者治疗确定最佳用药方案为临床仍需探索解决的难题[25-26]。
综上所述,卡瑞利珠单抗联合VEGF 抑制剂行抗血管生成双靶治疗能有效改善晚期NSCLC 患者症状,提高疗效,改善免疫功能,且无明显不良反应,该治疗方案可供临床治疗参考。
