末端瓣膜式耐高压注射型PICC 优化置管法在肿瘤患者中的应用
2023-11-30夏爱萍朱凤林居燕郭静
夏爱萍 朱凤林 居燕 郭静
经外周静脉置入中心静脉导管(PICC)已经被广泛应用到需长期、间歇输注刺激性、细胞毒性药物的肿瘤患者中,尤其是末端瓣膜式高压注射型PICC(Power PICC SOLO),其强化聚氨酯材质能耐受300 psi(1 psi=6.895 kPa)的高压注射,可以满足肿瘤患者频繁行增强CT/MRI 检查的需求;其最大流速可达5 ml/s,同时可满足更多危急重症肿瘤患者对输液速度的要求。导管末端的瓣膜设计能够有效阻止血液返流和空气进入导管内,可以使用生理盐水预充式注射器或者生理盐水直接冲封管,使日常维护更简单。一体式连接导管使患者带管更安全、舒适;还可以监测中心静脉压,真正实现“一管到底”的目标[1-2]。但是,和其他前端修剪的PICC 导管一样,Power PICC SOLO 也存在着一些导管相关不良事件,例如:导管异位、送管困难、穿刺点渗血渗液、导管堵塞、导管脱出、非计划拔管、导管相关血流感染(CRBSI)等[3-4]。医院肿瘤科自2019 年5 月首次为肿瘤患者置入Power PICC SOLO 导管以来,在遵循PICC 置管规范的前提下,通过在置管实践中探索研究,优化Power PICC SOLO 的置管方法,应用于肿瘤患者的置管中,降低了Power PICC SOLO 导管相关不良事件的发生率。现报告如下。
1 对象与方法
1.1 研究对象
选取2021 年7 月—2022 年7 月在医院肿瘤科需置入Power PICC SOLO 导管的86 例患者为研究对象。纳入条件:患者意识清楚,肢体活动自如,愿意留置PICC 导管,并签署置管知情同意书;患者预期寿命>3 个月,导管可留置时间>3 个月。排除条件:上腔静脉阻塞综合征、穿刺局部皮肤感染、菌血症、穿刺手臂淋巴水肿、静脉回流不畅等PICC 置管禁忌证。患者中男39 例,女47 例。年龄19~87 岁,平均55.68±9.72 岁。乳腺癌18 例,结直肠癌15 例,肺癌12 例,胃癌9 例,胰腺癌8 例,宫颈癌6 例,淋巴瘤6 例,鼻咽癌5 例,其他肿瘤7 例。穿刺静脉:右侧贵要静脉56 例,右侧头静脉6 例,右侧肱静脉4 例,左侧贵要静脉15 例,左侧头静脉3 例,左侧肱静脉2 例。置管前患者均已行胸部X 光摄片检查,常规心电图检查,已排除心电图报告没有P波的窦房结病变患者。按照组间上述基本特征具有可比性的原则分为对照组和观察组,每组43 例。两组一般资料比较差异无统计学意义(P>0.05)。本研究已通过医院伦理委员会审查(编号:202345)。
1.2 置管操作方方法
两组均使用Power PICC SOLO 导管套件,单腔、4Fr 型号;灭菌剖腹手术敷料包;深圳迈瑞PM-9000 心电监护仪,低温灭菌的心电导联线(可替换RA 右锁骨下位置的导联),及灭菌电极片数枚;床边B 超机;红外线热辐射理疗灯;以及其他一次性耗材。两组 Power PICC SOLO 置管操作步骤,都遵循静脉治疗输液规范中PICC 置管规范流程[5-6]。
1.2.1 对照组使用常规的置管操作方法 患者平卧位,连接心电监护仪的心电导联,调节到心电图Ⅱ导联,截取心电图记录(特别观察P波波形)。对照患者近期X 胸片,采取“L”型、“一”字型体表测量方法[7-8],综合确定预置入的PICC 导管的长度。消毒整个穿刺侧手臂,分别在腋下、肩部、手臂下方区域铺灭菌治疗巾,再铺设剖腹单,手臂穿过剖腹单的洞口,建立最大化无菌屏障。最后,用灭菌治疗巾包裹穿刺侧手臂,暴露穿刺部位。B 超探测评估好的静脉血管,选择绿区(上臂的中1/3)为皮肤穿刺部位,采取徒手操作、一针式隧道穿刺法(皮肤穿刺点与静脉穿刺点相距≥2 cm)。根据皮下组织的深浅,以15°~30°的角度穿刺静脉,见回血稍压低穿刺针再进针少许,确认回血通畅;左手松开B 超探头,固定穿刺针,右手缓慢递送导丝通过穿刺针进入血管,顺利送入导丝10~15 cm,B 超探查确认导丝在血管内,退出穿刺针,局部麻醉。根据预测量确定的长度,退出Power PICC SOLO 导管内置导丝,垂直修剪导管(注意不可剪到导丝),再次调整PICC 内置导丝,使导丝头端回缩在PICC 导管内0.5 cm。微创破皮,将穿刺鞘沿导丝送入静脉血管,撤出导丝和扩张器,留导管鞘在血管内,缓慢送入PICC 导管,送入15~20 cm 时,嘱咐患者转头下颌紧贴穿刺侧手臂的肩部,继续缓慢送入PICC 导管至预定长度,退出导管鞘离开穿刺点,撕开导管鞘,撤去。此时,助手协助用灭菌的导联线更换体表右锁骨下(RA)导联,连接灭菌电极片,并将PICC 内置导丝的末端包裹在电极片中[9],引出心电图波形,观察P 波的振幅,当P波振幅达正向最高,开始出现负向波时,停止回送导管,并退出PICC 导管0.5~1.0 cm,此位置确定为导管置入的长度。将PICC 内置导丝平直缓慢地撤出,生理盐水冲封管,固定导管。置管结束,行X 胸片检查再次确认导管头端的位置,根据X 胸片显示的PICC 导管头端的位置,过深时退出导管至理想深度(气管隆嵴下1.2~2.7 胸椎之间)[5]。
1.2.2 观察组 在遵循常规PICC 置管操作流程的基础上,使用优化的置管方法,具体操作如下。
(1)使用物理方法舒张静脉血管:置管前指导患者洗热水澡或热水擦浴;指导患者卧于床上,反复练习手臂的上举、下垂,内收、外展以及肩关节旋转、拉伸的动作;红外线热辐射理疗灯照射穿刺侧手臂、肩关节及锁骨区域半小时,并将红外线理疗灯置于PICC 置管室中备用。送管过程中,如出现送管不畅,除帮助患者放松心情外,可给予红外线理疗灯照射,利用热力作用舒张静脉血管。同时,一边指导患者有规律地缓慢转动、拉伸置管侧手臂,一边尝试轻柔送管,以便找到恰当的间隙,使得SOLO 导管能够顺利通过此处静脉血管内的阻挡,如:静脉瓣膜,静脉弯曲、狭窄处,不顺滑的静脉内壁等。
(2)采取计划性的试送管法,精准修剪SOLO导管:对于心电图检查P波形态不典型的患者,可请心内科医生协助观察置管过程中P波的变化。同时,静脉治疗小组需要安排两位小组核心成员,对照患者近期X 胸片结合体表骨性标志进行体表测量,慎重确定导管预置入的长度[10]。置管过程中,成功穿刺目标静脉后,置入穿刺用导丝,当穿刺导丝顺利置入10~15 cm 时,退出穿刺针,局部麻醉,微创破皮,沿导丝送入穿刺鞘,退出导丝及扩张器留导管鞘在静脉内,直接将未修剪的Power PICC SOLO 导管缓慢送入血管,当送入15~20 cm 时,用灭菌心电导联线更换右锁骨下(RA)导联,并连接灭菌电极片包裹SOLO 导管末端的内置导丝,引出腔内心电图,观察P波振幅,继续缓慢送入SOLO导管,直至引出高尖P波,当P波正向振幅达最高,出现负向波时,开始退出SOLO 导管0.5~1.0 cm,查看SOLO 导管外露长度(Power PICC SOLO 导管全长55 cm),确定导管置入的长度,此时继续缓慢平直地退出SOLO 导管,直至完全退出,将SOLO导管重新放入导管盘中的生理盐水中,并将已使用肝素帽封口的扩张器轻柔送入导管鞘内,妥善固定。根据腔内心电图确定的SOLO 导管置入的长度,准确修剪导管头端。再将已精确修剪的SOLO 导管缓慢轻柔地送入静脉血管内,SOLO 导管末端的倒锥形恰好卡在穿刺点处,导管外露为“0”刻度处。最后,再次确认心电监护仪的心电图P波为正向高尖波形,平直轻柔地撤出支撑导丝,消毒穿刺部位,IV3000透明贴膜固定SOLO 导管。
(3)斜面修剪SOLO 导管的头端,降低导管被递送向前的阻力:改变传统的垂直修剪PICC 导管的方法,优化为45°~ 60°的斜面修剪。传统垂直修剪的导管,在被递送时,其头端是以圆形平面前进,容易被静脉腔不光滑的内壁阻挡。而修剪为斜面的PICC SOLO 导管的头端,则容易穿过静脉腔内的间隙被推送前进。
1.3 观察指标
(1)导管异位:PICC 导管头端位于除上腔静脉下1/3、右心房入口(CAJ)以外的其他任何部位。
(2)PICC 送管困难:静脉穿刺成功回血通畅,能顺利送入导丝10~20 cm,但送PICC SOLO 导管时出现送管不畅。
(3)穿刺点渗血渗液:每次PICC 维护时,穿刺点渗血渗液浸湿敷料直径>0.5 cm。
(4)导管脱出:导管外露长度较置入时,或者较上次维护时增加>1 cm。
(5)导管堵塞(包括完全性堵塞和不完全性堵塞):输液速度减慢、抽不到回血,或推注生理盐水有阻力等表现。
(6)穿刺点局部感染:穿刺点局部红肿热痛,但没有全身感染症状。
1.4 数据分析方法
应用SPSS 20.0 统计软件进行数据分析,计量资料以“均数±标准差”表示,组间均数比较采用t检验;计数资料组间率比较行χ2检验;P<0.05为差异有统计学意义。
2 结果
2.1 两组患者PICC 置管中相关不良事件的发生率比较
观察组在PICC 置管中出现送管困难的比例明显低于对照组,差异有统计学意义(P<0.05);而导管异位的比例两组间的差异无统计学意义(P>0.05)。见表1。
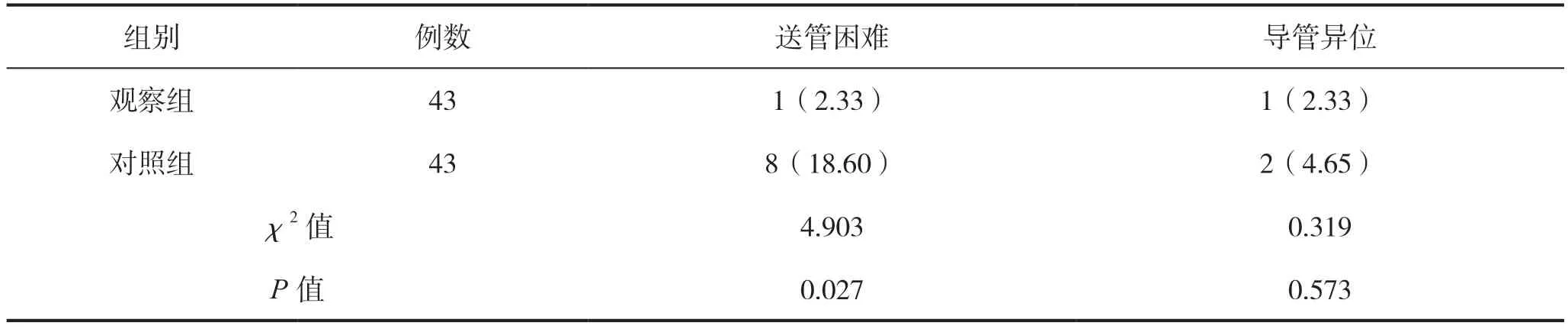
表1 两组PICC 置管中不良事件发生率比较
2.2 两组患者携带SOLO 导管2 个月期间PICC 相关不良事件发生率比较
观察组患者在PICC 带管2 个月期间发生穿刺点渗血渗液、导管脱出的例次均低于对照组,差异有统计学意义(P<0.05);而穿刺点局部感染、导管堵塞的比例两组对比差异无统计学意义(P>0.05)。见表2。
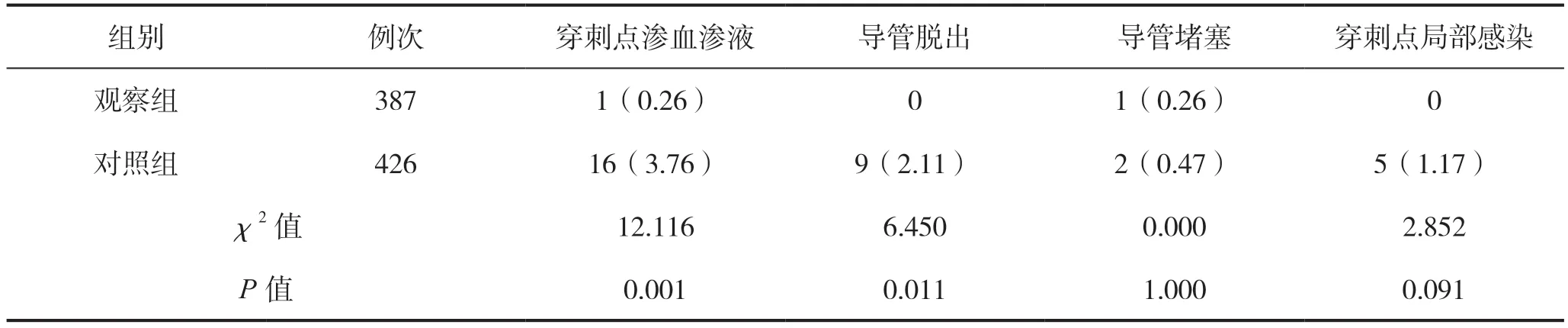
表2 PICC 带管2 个月期间导管相关不良事件发生率比较
3 讨论
3.1 顺应前端修剪PICC 导管的特性,实施防范送管困难的预见性护理措施
相关研究发现PICC 导管送管困难的发生率高达14.22%~40.00%[11],本研究的对照组送管困难的发生率为18.60%,而观察组的发生率则为2.33%。我们根据前端修剪的PICC 导管的特性,探讨了防范导管送管困难的预见性护理措施。首先,分析导管送管困难的原因,主要是患者个体的因素:患者精神紧张导致静脉血管收缩、痉挛;静脉血管本身存在狭窄弯曲、静脉瓣膜的阻挡、静脉窦、静脉的多个属支等都会造成静脉血管内壁不顺滑[12-14],导管难以顺利通过。其次,导管头端结构的因素,Power PICC SOLO 导管其前端开口,需要根据置入的长度进行前端修剪,按照传统的导管修剪方法为垂直90°剪切,在静脉内递送PICC SOLO 导管时,导管头端以直径2 mm 圆形平面前进,静脉血管内稍有阻挡,就会出现送管困难。针对以上原因,采取物理的方法舒张患者的静脉血管,使用临床科室常用的设备:红外线辐射理疗灯照射置管手臂、肩关节及胸部区域,利用其热力的作用舒张患者的静脉,舒缓静脉血管的收缩痉挛[15]。置管前,指导患者练习手臂的伸展、旋转,多角度、多方位地活动肩关节,以改变静脉血管腔内的形态。置管时,一旦出现送管不畅,患者能够熟练配合活动手臂及肩关节,动态地改变静脉血管腔内的形状;同时,置管护士轻柔缓慢地递送SOLO 导管,以便导管头端找到合适的间隙通过此段血管,到达预定位置。张和云[16]在血管造影检查后,明确血管走向的情况下,采取手臂外展旋转式导管送入法,置管成功。肿瘤患者因为反复多次的外周静脉治疗及不同区域的放疗,引起不同程度的组织损伤,导致其血管解剖走向的个体差异较大[17],我们在排除上腔静脉压迫综合征,置管手臂没有血液、淋巴回流障碍的情况下,采取的方法简单易行。即尝试多角度、多方位地活动手臂及肩关节,动态地改变阻碍SOLO 导管前进部位的血管腔的形状,方便SOLO 导管顺应到恰当的间隙通过此段血管腔。为了进一步增加Power PICC SOLO 导管头端的顺应性,依据其强化聚氨酯材质的韧性,以及SOLO 导管进入血管,温度接近体温时,会变得更加柔软的特点,我们改变传统的垂直修剪导管的方法,优化为45°~60°的斜面修剪。如此,PICC SOLO 导管头端的斜面形状,在SOLO导管被递送前进时,就不会轻易地被静脉腔内瓣膜、分叉的属支等不顺滑的血管内壁所阻挡;因为进入体内SOLO 导管的材质变柔软的特性,加上操作者轻柔的动作,能够有效地防止递送导管的过程中损伤血管内膜,从而尽量规避导管相关静脉血栓的风险[18-19]。在分析PICC 送管困难原因的研究里[20],导管头端的结构是导致PICC 送管困难、导管反折、导管异位的原因之一。
3.2 置管过程中实时定位,精准修剪,最终使得导管头端及末端的“O”点均处于理想位置
有研究表明采取微创破皮,或者使用扩张器直接钝性分离穿刺点[21],可以降低穿刺点渗血渗液的发生[22-23]。但是,PICC导管鞘的直径大于PICC 导管,当撤除导管鞘后,穿刺点处受损的小血管、小淋巴管就会出现渗血渗液现象[1]。而Power PICC SOLO导管末端的倒锥形,恰恰是针对PICC 穿刺点渗血渗液而设计的,要让此设计发挥作用,需要Power PICC SOLO 导管的倒锥形正好压迫在穿刺点处,当SOLO 导管的外露部分>1 cm 以上时,其设计的倒锥形就失去止血、止渗液的作用。因此,对于前端修剪的Power PICC SOLO 导管来说,测量导管预置入的长度与导管头端到达理想位置的实际长度之间的误差要<1 cm,才能在置管前做到精确修剪导管。尽管依据体表的骨性标志结合患者近期胸片进行测量的导管长度,准确性已经大大提高,但是与个体实际的静脉解剖结构所要求的导管长度之间,仍然存在着误差[24-25],对于后修剪的PICC 导管,譬如三向瓣膜PICC 导管来说,可以通过实时的腔内心电图准确定位导管头端的位置,到达理想位置以后,准确修剪外露部分的导管。但是,头端修剪的一体式SOLO 导管,需要在置管前,提前测量好导管的长度完成修剪,一旦完成置管,过短的导管其尖端不能到达上腔静脉的下1/3,尤其是右心房入口水平(CAJ)的理想位置;过长的导管势必会增加SOLO 导管的外露长度,不但使SOLO 导管倒锥形设计的作用失效,而且还增加了SOLO 导管末端的重量,过重的导管尾端,势必会增加了SOLO 导管脱出的风险,甚至导致非计划拔管[26]。本研究的对照组,外露部分>1 cm 以上的PICC SOLO 导管中,发生穿刺点渗血渗液、导管脱出的频率较高,也增加了导管维护次数。为了规避以上的风险,我们在遵循最大化无菌屏障,使用灭菌剖腹手术敷料包,严格无菌操作的前提下,计划性地采取试送管法,即先置入未经修剪的PICC SOLO 导管,借助实时的腔内心电图定位技术,得到导管头端到达右心房入口水平(CAJ)的理想位置的导管长度后,轻柔缓慢平直地退出导管,再精确修剪导管,确保最终置入的SOLO 导管头端位于理想位置[27-28],导管末端的“0”刻度位置平穿刺点处。置管结束,再次行X胸片检查,确认导管头端位于上腔静脉下1/3,平右心房入口处。SOLO 导管末端的倒锥形恰好卡在穿刺点,不但发挥止血、止渗液的作用,还起到较好的导管固定作用[29]。
综上所述,通过应用红外线热辐射理疗仪的热力作用,舒张静脉血管;轻柔缓慢地送管与患者多方位、多角度地活动置管侧手臂及肩关节相配合,使得导管顺应血管的走向,顺利到达预定位置;改90°垂直修剪导管头端为45°~ 60°修剪,有利于导管被推送前进;计划性采取试送管法,利用成熟的腔内心电图定位技术,获得准确的导管置入的长度后,再精确修剪导管,最终使SOLO 导管的头端位于右心房入口(CAJ)的理想位置,导管末端的倒锥形(“0”刻度处)恰好卡在穿刺点[30]。降低了Power PICC SOLO 导管相关不良事件的发生率,使得患者带管更安全、舒适、高效。不过,限于本研究的样本量较少,本优化置管的方法能否更规范、经济地解决临床PICC 置管问题,还需要在更多病例实践中不断探索。
