基于“质-量”双标的甘草质量分析方法研究
2023-11-27贾梦楠李天娇包永睿韩晓妮孟宪生
贾梦楠,李天娇, 2, 3,包永睿, 2, 3,王 帅, 2, 3,韩 凌,韩晓妮,孟宪生, 2, 3*
基于“质-量”双标的甘草质量分析方法研究
贾梦楠1,李天娇1, 2, 3,包永睿1, 2, 3,王 帅1, 2, 3,韩 凌4,韩晓妮4,孟宪生1, 2, 3*
1. 辽宁中医药大学药学院,辽宁 大连 116600 2. 辽宁省中药多维分析专业技术创新中心,辽宁 大连 116600 3. 辽宁省现代中药研究工程实验室,辽宁 大连 116600 4. 华润三九医药股份有限公司,广东 深圳 518110
建立以对照药材为基准物质的定性和不依赖多种对照品定量的甘草药材“质-量”双标控制方法。采用HPLC技术,以对照药材为基准物质建立甘草特征图谱,通过Q-TOF-MS技术,鉴定共有峰的化学成分,以对照药材和供试药材特征峰的相似度,明确药材真伪,即“质”;对内标成分“甘草酸”进行准确定量,以内标成分计,计算不同批次供试品中各特征峰的相对含量,取“平均数-标准差”作为特征峰化学成分相对于内标物质化学成分的相对含量下限,依据特征峰相对含量下限明确甘草药材优劣,即“量”。建立的特征图谱及含量测定方法符合方法学考察要求;确定了10个共有色谱峰,鉴定出了5个化学成分,分别为芹糖甘草苷、甘草苷、芹糖异甘草苷、异甘草苷、甘草酸,各甘草供试药材与甘草对照药材的相似度均大于0.90;规定了甘草药材特征峰化学成分相对含量下限。该方法不依赖多种对照品,能清晰、快速地判断药材的真伪优劣,为甘草的质量控制方法提供参考。
甘草;对照药材;质量控制;特征图谱;芹糖甘草苷;甘草苷;芹糖异甘草苷;异甘草苷;甘草酸
甘草为豆科植物甘草Fisch.胀果甘草Bat.或光果甘草L.的干燥根及根茎[1],在我国西北、东北、华北地区均有分布,主产于新疆、甘肃、河北等地[2]。其性平味甘,在临床上常作为清热解毒,祛痰止咳之要药,常用于调和诸药,现代药理学表明其具有广泛的抗肿瘤、抗炎、抗菌、抗病毒、神经保护、肝脏保护等药理作用[3],然而当前不同产地甘草药材质量参差不齐,影响其在临床上的合理应用,因此甘草药材的质量控制十分重要。目前甘草药材质量控制方法主要包括单指标含量测定法[4]、多指标含量测定法[5-7]、一测多评法[8]和指纹图谱与含量测定结合法[9-10],虽能够为甘草药材的控制提供量化数据,但存在着单一指标不能反映药材整体特征、多指标含量测定依赖于多种对照品且某些指标成分不能反映药效、指纹图谱不能清晰直观地判断药材真伪优劣等问题,且中药复杂体系质量评控技术难度和高额成本给中药企业带来了巨大的压力,因而对中药临床合理用药和临床疗效提升的指导和支持作用一直难以体现。
为弥补目前甘草药材质量控制的不足,本研究提出了基于“质-量”双标的甘草质量分析方法研究,紧扣中药多成分、多功效和整合作用的质量内涵和特点,以能够反映其药效的化学成分为指标;采用1种内标物质对特征峰化学成分进行相对定量,尽可能控制供试药材有效化学成分含量同时,不需要大量购买对照品,在满足中药化学成分“整体性”与“清晰性”的同时减轻了中药复杂体系质量评控成本。本方法以对照药材为基准物质构建特征图谱,并以可代表甘草药效的有限个代表性成分作为特征峰,评价对照药材和供试药材特征峰的相似度,可以用于判断甘草的真伪;选用保留时间稳定且价格低廉易获得的内标物质作为定量评价指标,开展基于内标物质的特征峰化学成分相对定量研究,通过内标物质化学成分准确定量,计算供试药材特征峰化学成分的相对含量。基于“质-量”双标的甘草质量分析方法可有效解决甘草有效成分同时快速测定和中药复杂体系质量评控成本高的问题。
1 仪器与材料
1.1 仪器
Agilent-1260II高效液相色谱仪;Agilent 6550 Q-TOF-MS质谱仪(美国安捷伦科技有限公司);KQ5200 V超声仪(昆山市超声仪器有限公司)。
1.2 材料
甘草对照药材(批号120904-201620,中国食品药品检定研究所);甘草药材信息见表1,经辽宁中医药大学中药鉴定教研室张慧教授鉴定为豆科植物甘草Fisch.的根及根茎;甘草苷对照品(批号111610-201908,质量分数95.0%),甘草酸铵对照品(批号110731-202021,质量分数96.2%)均由中国食品药品检定研究院提供;对照品芹糖甘草苷(批号PRF9050224)、芹糖异甘草苷(批号PRF9090722)、异甘草苷(批号PRF9062623)均由成都普瑞法科技开发有限公司提供,质量分数均≥98%,乙腈(质谱级,德国Merck公司);水(纯净水,杭州娃哈哈集团有限公司)。
2 方法与结果
2.1 基于甘草对照药材的特征图谱建立
2.1.1 溶液的制备 取甘草对照药材粉末0.50 g,精密称定,置具塞锥形瓶中,精密加入70%乙醇5 mL,称定质量,超声(功率200 W,频率40 kHz)30 min,放冷,再称定质量,用70%乙醇补足减失质量,摇匀,过0.22 μm微孔滤膜滤过,取续滤液,作为参照物溶液;取供试药材粉末(过40目筛)0.50 g,按上述方法制成供试品溶液。取适量芹糖甘草苷对照品、甘草苷对照品、芹糖异甘草苷对照品、异甘草苷对照品、甘草酸对照品精密称定,置具塞锥形瓶中,精密加入70%乙醇,摇匀,作为混合对照品溶液。
2.1.2 色谱条件 色谱柱:Agilent SB-C18色谱柱(100 mm×4.6 mm,2.7 μm);流动相为0.1%甲酸水(A)-乙腈(B),梯度洗脱:0~3 min,10%~20% B;3~7 min,20% B;7~9 min,20%~26% B;9~13 min,26% B;13~15 min,26%~34% B;15~19 min,34%~36% B;19~22 min,36%~44% B;22~28 min,44%~48% B;28~40 min,48%~70% B。体积流量0.8 mL/min;柱温30 ℃;DAD检测器波长237 nm;进样量3 μL。
2.1.3 特征图谱的建立 将参照物溶液和供试品溶液,每份样品平行2次,按色谱条件依次进样检测,将237 nm波长下的图谱数据由分析检测仪器中导入中国药典委员会“中药指纹图谱相似度评价软件”(2012.130727版本),获得甘草药材的HPLC特征图谱,见图1。以甘草对照药材的图谱为参照谱图,使用中位数进行自动匹配,加以多点校正,共标定10个共有峰,共有峰面积占特征图谱的75%以上,其中9号峰稳定性、重复性、分离度好、位置居中,故以其为参照峰;生成共有模式,与对照药材特征图谱进行比对,见图2。甘草供试品色谱图中应呈现10个特征峰,并应与对照药材色谱图中的10个特征峰保留时间相对应,见表2。
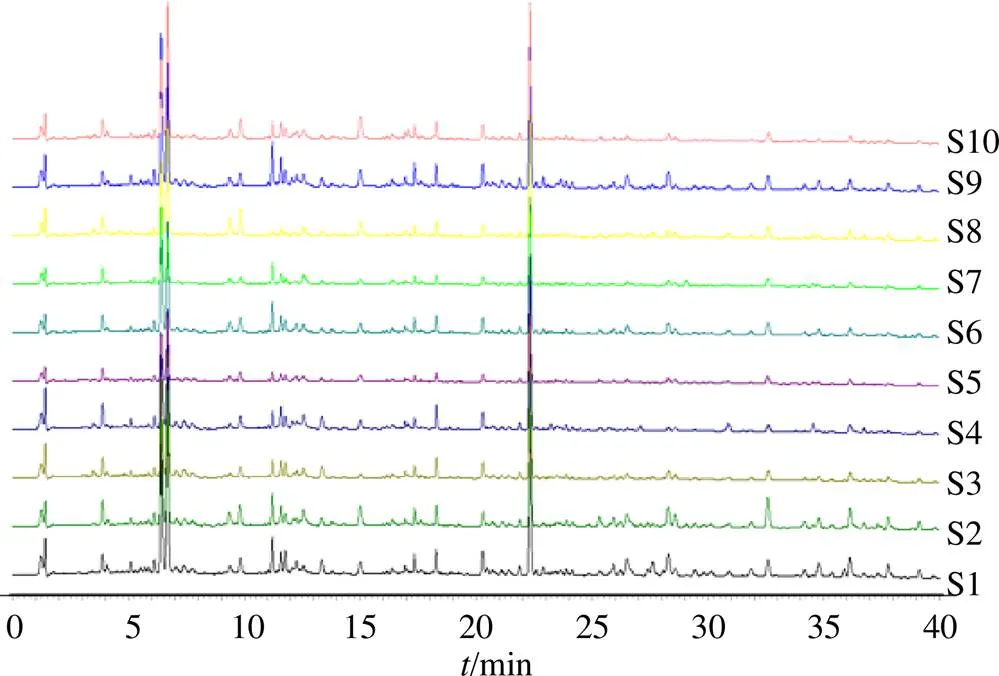
图1 10批供试药材叠加图谱
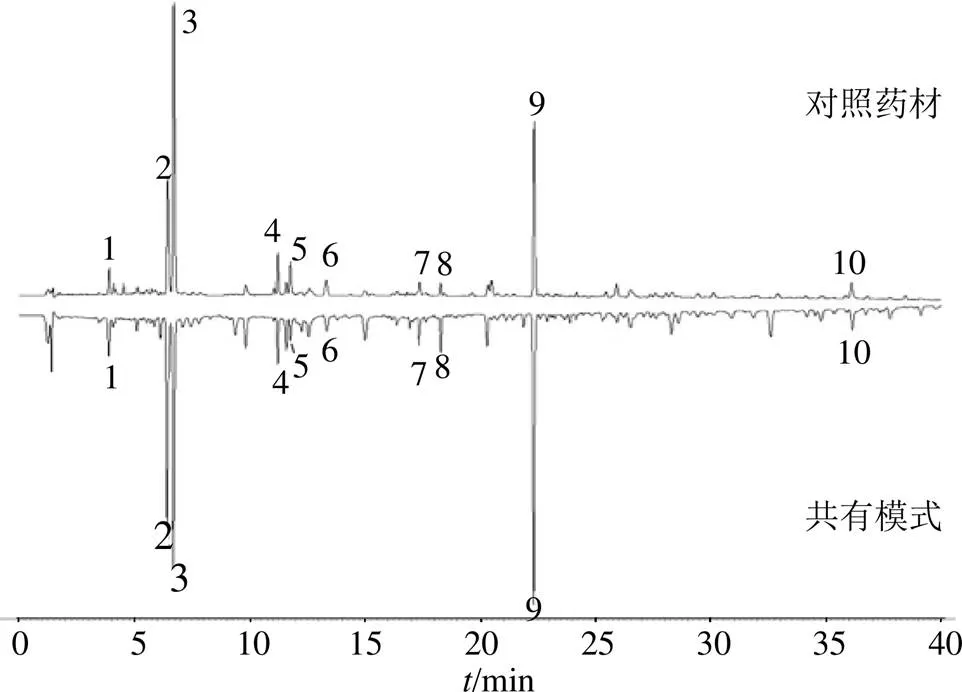
图2 对照药材特征图谱及供试药材共有模式
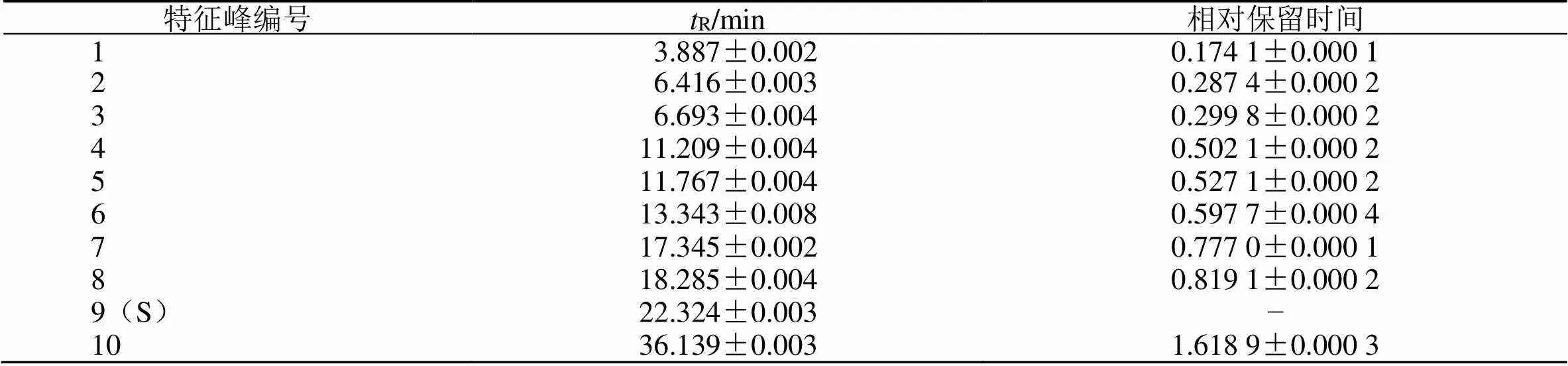
表2 特征峰保留时间及相对保留时间
2.2 方法学考察
2.2.1 专属性试验 分别取混合对照品溶液、供试品溶液进行测定,各主峰与杂质峰分离度良好,专属性强,见图3。
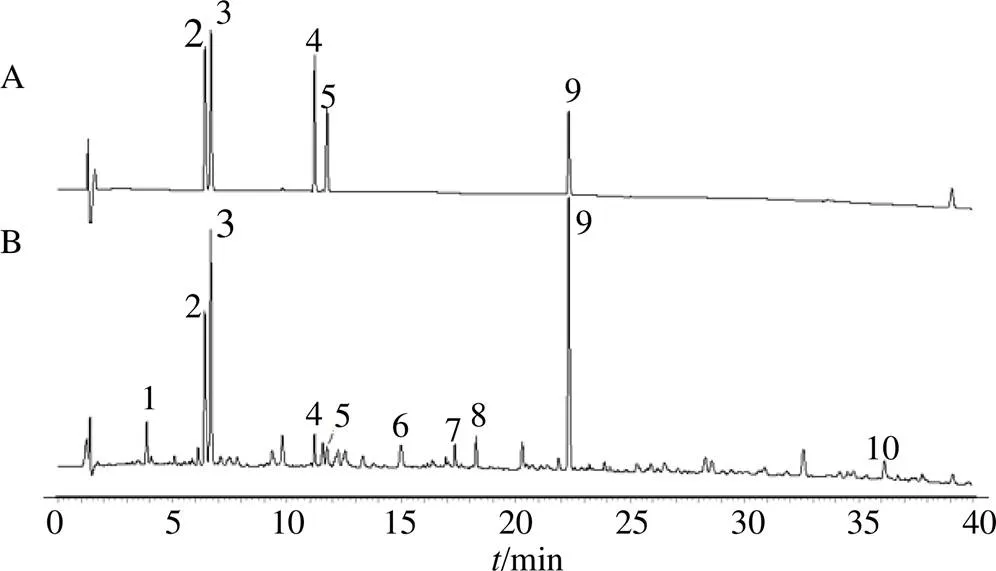
2-芹糖甘草苷 3-甘草苷 4-芹糖异甘草苷 5-异甘草苷 9-甘草酸
2.2.2 精密度试验 精密吸取同一供试品溶液,按“2.1.2”项下色谱条件测定,连续进样6次,测定各色谱峰相对保留时间、相对峰面积,计算RSD。各色谱峰相对保留时间、相对峰面积RSD值在0.8%~0.9%,表明仪器精密度良好。
2.2.3 稳定性试验 精密吸取同一供试品溶液,按“2.1.2”项下色谱条件,分别在0、2、4、8、12、24 h进样6次检测,测定各色谱峰相对保留时间、相对峰面积,计算RSD。各色谱峰相对保留时间、相对峰面积RSD值1.0%~1.2%,表明供试品溶液在24 h内稳定。
2.2.4 重复性试验 按供试品溶液制备方法制备6份供试样品,按“2.1.2”项下色谱条件,分别进样检测,测定各色谱峰相对保留时间、相对峰面积,计算RSD。各色谱峰相对保留时间、相对峰面积RSD值1.9%~2.1%,表明方法重复性良好。
2.3 相似度评价
采用中国药典委员会“中药指纹图谱相似度评价软件”(2012.130727版本)进行数据处理,该软件利用夹角余弦法计算每个色谱图与对照药材图谱相比较的相似度。以甘草对照药材和供试药材特征峰的相似度明确甘草药材真伪,按中药色谱指纹图谱相似度评价系统计算供试品与对照药材特征图谱的相似度应不得低于0.90,甘草供试药材与甘草对照药材的相似度均大于0.96,说明所收集的甘草供试药材的特征峰化学成分基本一致,质量相对稳定。相似度计算结果见表3。
2.4 特征峰化学成分解析
在初步采用Agilent-1260Ⅱ高效液相色谱仪利用相对保留时间与对照品比对的基础上,采用Agilent 6550 Q-TOF-MS质谱仪,进行质谱分析,运用Agilent MassHunter Qualitative Analysis软件,通过对照品比对的方法对负离子模式进行化学成分解析,进一步明确特征峰的准确化学成分。
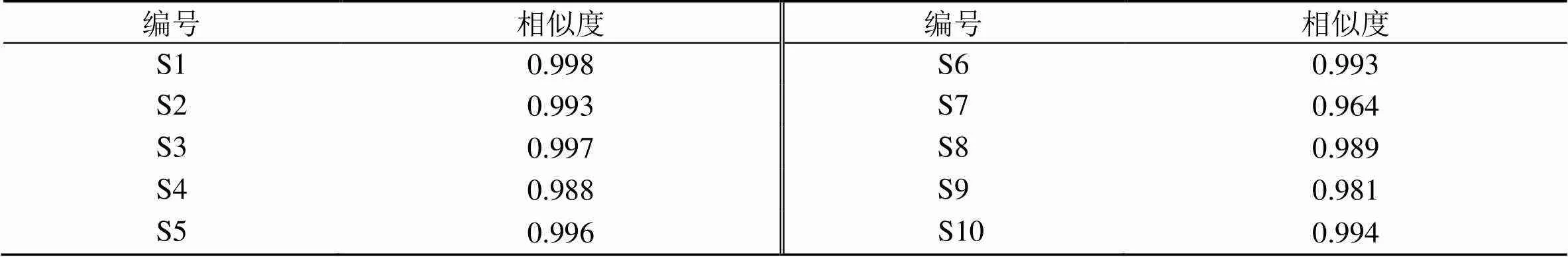
表3 供试药材与对照药材之间的相似度评价结果
2.4.1 色谱分析条件 色谱柱:Agilent poroshell 120 SB-C18色谱柱(100 mm×2.1 mm,2.7 μm);流动相为0.1%甲酸水(A)-乙腈(B),梯度洗脱:0~3 min,10%~20% B;3~7 min,20% B;7~9 min,20%~26% B;9~13 min,26% B;13~15 min,26%~34% B;15~19 min,34%~36% B;19~22 min,36%~44% B;22~28 min,44%~48% B;28~40 min,48%~70% B;体积流量0.6 mL/min;柱温30 ℃;进样量1 μL。
2.4.2 质谱分析条件 电喷雾离子源(Dual AJS ESI),负离子模式,毛细管电压(Vcap)为3500 V,干燥气体体积流量(drying gas flow)为11 L/min,干燥气体温度(drying gas temp)为150 ℃,雾化器压力(neulizer pressure)为172.4 kPa,鞘气温度(sheath gas temp)为350 ℃,鞘气体积流量(sheath gas flow)为10 L/min,质量扫描范围(mass range)为/100~1000。
采用auto MS/MS模式,利用对照品比对及数据库查询等方法对特征峰化学成分进行解析。共鉴定出了10个特征峰中的5个化学成分,其中,2号峰为芹糖甘草苷,3号峰为甘草苷,4号峰为芹糖异甘草苷,5号峰为异甘草苷,9号峰为甘草酸,鉴定结果见表4。
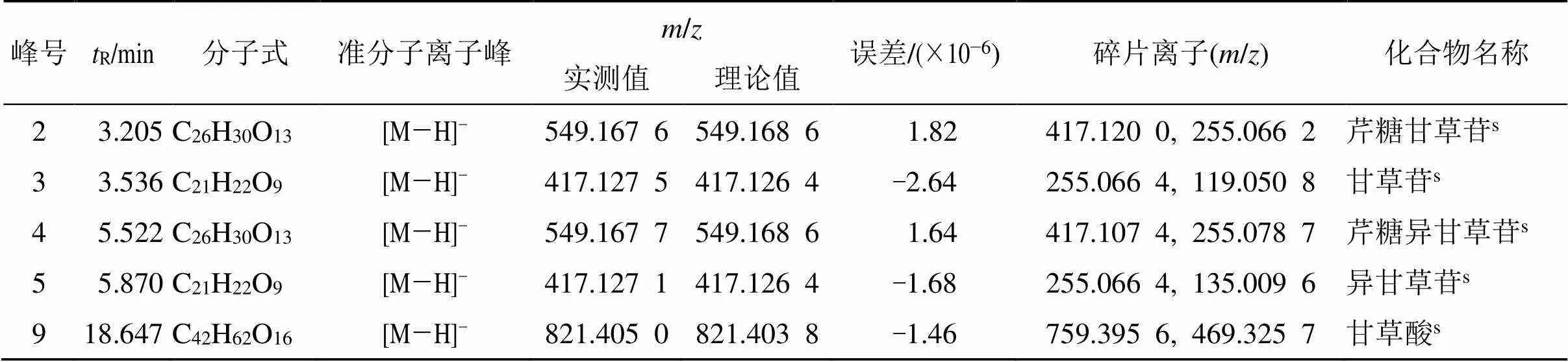
表4 负离子模式特征峰化学成分解析结果
S经对照品比对
SThis compound was identified using reference standards
2.5 基于内标物质的特征峰化学成分相对定量研究
2.5.1 线性关系试验 配制甘草酸的6个质量浓度溶液,按“2.1.2”项下色谱条件,分别进样检测,以质量为横坐标(),峰面积为纵坐标(),绘制标准曲线并进行线性回归,得到线性回归方程=632.3-30.754、=0.999 6。线性范围为2.5~15 μg。结果表明进样量范围内与峰面积呈良好的线性关系。
2.5.2 精密度试验 同“2.2.2”项下方法,计算甘草酸相对峰面积RSD值1.1%~1.2%,表明仪器精密度良好。
2.5.3 稳定性试验 同“2.2.3”项下方法,计算甘草酸相对峰面积RSD值2.3%~2.6%,表明供试品溶液在24 h内稳定。
2.5.4 重复性试验 同“2.2.4”项下方法,计算甘草酸相对峰面积RSD值2.2%~2.5%,表明方法重复性良好。
2.5.5 加样回收率试验 精密称定甘草药材粉末6份,分别精密加入甘草酸对照品适量,按“2.1.1”项下方法制备供试品溶液,按“2.1.2”项下色谱条件,分别进样检测,计算得到甘草酸的平均加样回收率为99.10%,RSD为2.30%。
2.5.6 耐用性试验 精密吸取同一供试品溶液,考察不同规格的色谱柱(Agilent poroshell 120 SB-C18、Agilent poroshell 120 EC-C18)、不同的高效液相色谱仪(Agilent-1260Ⅱ高效液相色谱仪、Agilent-1290型高效液相色谱仪)、不同柱温(25、30、35 ℃)及不同体积流量(0.6、0.8、1.0 mL/min)对检测结果的影响。结果显示,指认出的5个化学成分的相对保留时间的RSD值2.1%~2.3%,相对峰面积的RSD值2.6%~2.7%,表明该方法的耐用性良好。
2.5.7 含量测定 根据《中国药典》2020年版甘草“含量测定”项下方法检测,10批产地供试品均能符合药典规定(含甘草苷不得少于0.50 %,甘草酸不得少于2.0%)。9号峰甘草酸为《中国药典》2020版中甘草“含量测定”项下的指标之一,该峰分离效果好、保留时间稳定、标准品价格低廉,故以其作为内标物质,开展基于内标物质的特征峰相对定量研究。取供试品药材,按“2.1.1”项下方法制备供试品溶液,按“2.1.2”项下色谱条件分析测定甘草酸含量,每个供试品平行2份,结果见表5。计算每个供试品中特征峰化学成分的相对含量[特征峰化学成分相对含量=特征峰峰面积×(甘草酸含量/甘草酸峰面积)],结果见表6。取“平均数-标准差”作为特征峰化学成分相对于内标物质化学成分的相对含量下限,供试药材根据此方法测得的特征峰相对含量不低于该含量下限[11]。
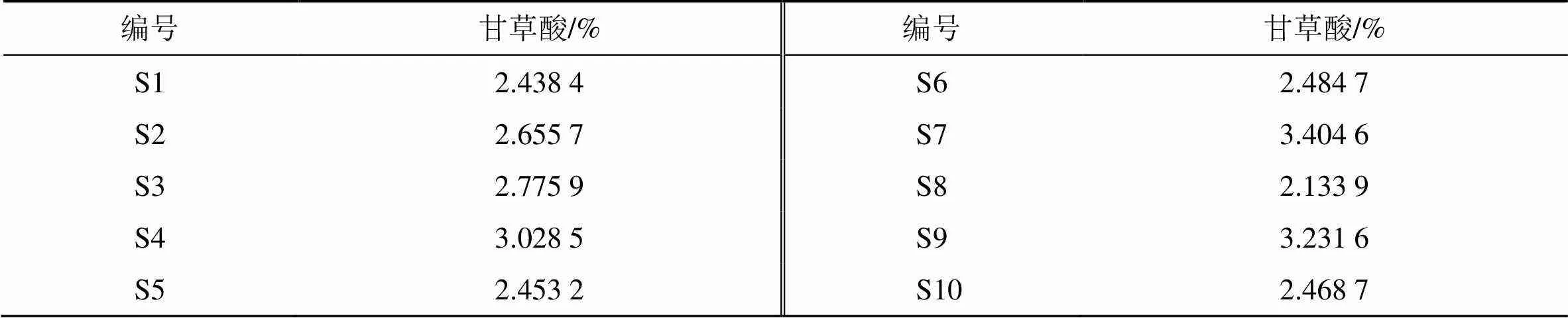
表5 内标物质甘草酸的准确定量结果(n=2)
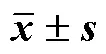
表6 基于内标物质的特征峰相对定量结果(, n = 3)
3 讨论
甘草一药始载于汉《神农本草经》[12],被列为上品,具有调和诸药、解毒等作用,在复方中出现频率很高,被称为“国老”,因此其质量好坏直接影响到诸多方剂的临床疗效。然而甘草的成分复杂多样,其品种来源、生长环境、生长年限、储藏方式均可能导致药效成分含量发生变化,影响甘草药材(饮片)的质量及其在临床合理使用。目前,《中国药典》2020年版中质量控制项仅对甘草药材(饮片)中一种或几种成分进行含量测定,不易判断真伪。而对多种成分进行含量测定,虽可以更全面地对药效成分进行定量,但存在有些对照品价格昂贵、稳定性差且专属性不强等问题,增加了甘草药材(饮片)检测成本,为中药企业带来经济负担。
为解决以上问题,本研究提出了基于“质-量”双标的甘草质量分析方法。通过构建甘草对照药材及10个不同产地甘草供试药材的特征图谱,以价格低廉的对照药材为基准物质,通过评价对照药材和供试药材特征峰的相似度,可以用于判断甘草药材的真伪,即“质”。通过准确定量1种内标物质化学成分,计算甘草药材其余各特征峰的相对含量,确定的各特征峰相对含量的下限能够区分甘草药材优劣,即“量”。本研究所提出的甘草药材的“质-量”控制方法能够有效判断药材的真伪优劣,形成一个科学、可控的中药质量控制体系。
本研究将与对照药材相似度好、信噪比大于10、分离度大于1.5作为特征峰的选取依据,共确定了10个特征峰。本实验采用质谱技术指认出的特征峰化学成分主要为黄酮类和三萜皂苷类[13],其中黄酮类化合物包括芹糖甘草苷、甘草苷、芹糖异甘草苷、异甘草苷,该类化合物具有镇咳祛痰[14-15]、抗炎[16-18]、抗肿瘤[19-20]、抗氧化[21]、抗纤维化[22]等多种药理活性。三萜皂苷类化合物为甘草酸,该化合物具有抗炎、解毒、免疫调节、抗病毒、保肝和稳定细胞膜等作用[23-25]。上述化学成分均为甘草发挥其“清热解毒,祛痰止咳”功效和抗肿瘤、抗炎、抗菌、抗病毒、肝脏保护等药理作用的主要生物活性成分,说明本方法选择的特征峰能够较为科学地反映甘草药材的药效。
本实验所收集的市面所售不同产地供试品,旨在建立基于“质-量”双标的甘草质量分析方法,所收集的甘草供试药材与甘草对照药材的相似度均大于0.90[26],说明所收集的甘草供试药材的特征峰化学成分基本一致,但仅采用10批不同产地的药材规定特征峰相对含量下限,缺乏全面性,因此,需要更进一步大量收集不同产地、不同批次的药材,完善该套方法,以期有效判断药材的真伪优劣,形成一个科学、可控的中药质量控制体系,在满足药材多项质量控制项的同时减轻企业需大量购买对照品的经济压力,推动中医药事业可持续发展。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典[S]. 一部. 2020: 88-89.
[2] 张继, 姚健, 丁兰, 等. 甘草的利用研究进展 [J]. 草原与草坪, 2000, 20(2): 12-17.
[3] 李葆林, 麻景梅, 田宇柔, 等. 甘草中新发现化学成分和药理作用的研究进展 [J]. 中草药, 2021, 52(8): 2438-2448.
[4] 高鸿彬, 刘浩, 夏厚浩, 等. 近红外光谱法快速测定甘草饮片中甘草酸和甘草苷的含量 [J]. 第二军医大学学报, 2020, 41(8): 921-925.
[5] 陈佳, 张权, 杨蕊, 等. 不同生长年限甘草主要成分含量测定及多元统计分析 [J]. 药物分析杂志, 2020, 40(7): 1185-1196.
[6] 陈佳, 张权, 赵莎, 等. 基于HPLC特征图谱、多成分定量结合化学计量学方法评价不同采收期甘草药材的质量 [J]. 中国药学杂志, 2020, 55(18): 1540-1547.
[7] 宁雪, 杨振泳, 王凤文, 等. HPLC同时测定甘草及其炮制品中7种成分的含量 [J]. 中药材, 2020, 43(9): 2146-2150.
[8] 郭立强, 李熙, 刘谦, 等. 一测多评法比较不同产地甘草中6种有效成分含量 [J]. 中国现代应用药学, 2019, 36(24): 3051-3055.
[9] 裴玉琼, 石海培, 严辉, 等. 基于HPLC指纹图谱及多成分一测多评法定量的炙甘草饮片质量评价研究 [J]. 中草药, 2019, 50(18): 4293-4304.
[10] 周越美, 冯超, 史煜华, 等. 甘草浸膏HPLC指纹图谱及多指标成分含量测定研究 [J]. 中国现代应用药学, 2020, 37(9): 1046-1051.
[11] 王梦林, 巴寅颖, 武秋红, 等. 基于有效基准特征图谱质量表征的中药荷叶质量评价研究[J]. 环球中医药, 2022, 15(6): 40-948.
[12] 尚志钧校注. 神农本草经校注 [M]. 北京: 学苑出版社, 2008: 209.
[13] 赵艳敏, 刘素香, 张晨曦, 等. 基于HPLC-Q-TOF-MS技术的甘草化学成分分析 [J]. 中草药, 2016, 47(12): 2061-2068.
[14] Kuang Y, Li B, Fan J R,. Antitussive and expectorant activities of licorice and its major compounds [J]., 2018, 26(1): 278-284.
[15] Wei W, Gao X P, Zhao L,. Liquiritin apioside (LA) attenuates apneic responses to stimulation of laryngeal chemoreceptors but not mechanoreceptors in rat pups [J]., 2019, 33(S1): 733-737.
[16] 王海强, 刘一宁, 陆晓燕, 等. 甘草中抑制脂多糖诱导小鼠RAW264.7产生NO的活性成分研究 [J]. 中草药, 2016, 47(23): 4155-4159.
[17] 杨晓露, 刘朵, 卞卡, 等. 甘草总黄酮及其成分体外抗炎活性及机制研究 [J]. 中国中药杂志, 2013, 38(1): 99-104.
[18] 文丹, 廖媛, 李健春, 等. 异甘草素通过Smad3/Arid2-IR/NF-κB轴改善顺铂诱导的急性肾损伤小鼠炎症反应 [J]. 中国比较医学杂志, 2020, 30(6): 25-30.
[19] Xiang S J, Chen H J, Luo X J,. Isoliquiritigenin suppresses human melanoma growth by targeting miR-301b/LRIG1 signaling [J]., 2018, 37(1): 184.
[20] 于多. 基于NF-κB通路探讨异甘草素抗炎与抗肿瘤双重作用及其机制的研究 [D]. 长春: 吉林大学, 2020.
[21] 降瑞婵, 刘海亮. 甘草中5种活性物质对人脂肪间充质干细胞的抗衰老作用 [J]. 同济大学学报: 医学版, 2021, 42(2): 179-186.
[22] Zhang Y, Zhang L, Zhang Y,. The protective role of liquiritin in high fructose-induced myocardial fibrosis via inhibiting NF-κB and MAPK signaling pathway [J]., 2016, 84: 1337-1349.
[23] 韩瑶聃, 王彬, 王政雨, 等. 甘草酸药理作用的研究进展 [J]. 中国新药杂志, 2012, 21(21): 2499-2505.
[24] Guo X X, Yang W N, Dong B S,. Glycyrrhetinic acid-induced miR-663a alleviates hepatic stellate cell activation by attenuating the TGF-β/smad signaling pathway [J]., 2020, 2020: 3156267.
[25] Tian X, Gan W F, Nie Y S,. Clinical efficacy and security of glycyrrhizic acid preparation in the treatment of anti-SARS-CoV-2 drug-induced liver injury: A protocol of systematic review and meta-analysis [J]., 2021, 11(7): e051484.
[26] 张智, 龙华, 曾罗, 等. 不同产地杜仲雄花指纹图谱的建立及其化学模式识别研究 [J]. 中草药, 2022, 53(22): 7207-7213.
Research on quality analysis method ofbased on “quality- quantity” double standard
JIA Meng-nan1, LI Tian-jiao1, 2, 3, BAO Yong-rui1, 2, 3, WANG Shuai1, 2, 3, HAN Ling4, HAN Xiao-ni4, MENG Xian-sheng1, 2, 3
1. College of Pharmacy, Liaoning University of Traditional Chinese Medicine, Dalian 116600, China 2. Liaoning Multi-dimensional Analysis of Traditional Chinese Medicine Technical Innovation Center, Dalian 116600, China 3. Liaoning Modern Traditional Chinese Medicine Research and Engineering Laboratory, Dalian 116600, China 4. China Resources Sanjiu Medical & Pharmaceutical Co., Ltd., Shenzhen 518110, China
To establish a “quality-quantity” double standard control method of, which is qualitative based on the reference traditional Chinese medicinal materials (TCMM) as standard substances and quantitative without relying on multiple reference substances.HPLC technology was used to establish the characteristic chromatogram ofbased on the reference TCMM as standard substances. The chemical constituents of common peaks were identified by Q-TOF-MS technology, and the authenticity ofwas determined by the similarity of characteristic peaks of the reference TCMM and the tested TCMM. The above statement is “quality”. The relative content of each characteristic peak in different batches of the tested TCMM was calculated by accurate quantition of internal standard component glycyrrhizic acid. The “average value-standard deviation” was taken as the lower limit of the relative content of characteristic peak chemical components relative to chemical composition of internal standard substance, and the quality ofwas determined according to the lower limit of the relative content of characteristic peak. The above statement is “quantity”.The characteristic chromatogram and content determination method met the requirements of methodology investigation. A total of ten common chromatographic peaks were determined, and five chemical components were identified, which were liquiritin apioside, liquiritin, isoliquiritin apioside, isoliquiritin, glycyrrhizic acid. The similarity between the tested TCMM and reference TCMM was greater than 0.90. The lower limit of relative content of chemical components ofcharacteristic peak was defined.The method can judge the authenticity of medicinal materials clearly and quickly without many reference substances, and provide reference for quality control of.
Fisch.; reference traditional Chinese medicinal materials; quality control; characteristic chromatogram; liquiritin apioside; liquiritin; isoliquiritin apioside; isoliquiritin; glycyrrhizic acid
R286.2
A
0253 - 2670(2023)22 - 7306 - 07
10.7501/j.issn.0253-2670.2023.22.005
2023-05-06
辽宁省科技创新领军人才(XLYC1902116)
贾梦楠,女,硕士研究生,主要从事药物分析研究。Tel: 13898369060 E-mail: 657314839@qq.com
通信作者:孟宪生,男,博士生导师,主要从事药效物质组学和作用机制整合研究。E-mail: mxsvvv@126.com
[责任编辑 时圣明]
