次氯酸钠对磺胺二甲氧嗪的降解与风险评价
2023-11-24丁朋飞陆金鑫汤慧俐郑璐杜尔登彭明国
丁朋飞 陆金鑫 汤慧俐 郑璐 杜尔登 彭明国






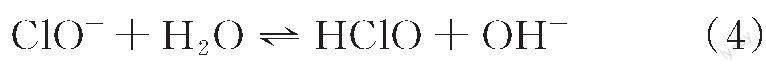











摘要:自來水原水中新兴污染物的存在对饮用水水质安全提出新的挑战。采用氯消毒对典型磺胺类抗生素磺胺二甲氧嗪(Sulfadimethoxine,SDM)进行降解研究,考察余氯初始浓度、pH值、氨氮(NH4-N)等因素对降解的影响,探究SDM氯氧化降解机理,评估其生态风险。结果表明:在SDM初始浓度为15 μmol/L、余氯初始浓度为60 μmol/L的条件下,120 s内SDM去除率达到95.9%,降解过程符合准二级反应动力学。反应速率常数随着余氯初始浓度增大而增大,随着NH4+-N浓度增大而减小,背景阴离子Cl-、NO3-、SO42-对反应影响甚微,HCO3-、CO32-对反应有抑制作用,中性条件下有利于SDM氯氧化反应。基于高分辨质谱HRMS Orbitrap解析出9种降解中间产物,降解过程中发生氯代反应、脱甲基反应和羟基加成反应等。在消毒过程中,SDM的完全去除并不意味着生态风险的有效削减,对饮用水水质安全构成潜在风险。
关键词:磺胺二甲氧嗪(SDM);氯消毒;反应动力学;降解机理;风险评价
中图分类号:TU991.25;X522 文献标志码:A 文章编号:2096-6717(2023)06-0206-09
Degradation and risk assessment of sulfadimethoxine during sodium hypochlorite disinfection process
DING Pengfei, LU Jinxin, TANG Huili, ZHENG Lu, DU Erdeng, PENG Mingguo
(School of Environmental & Safety Engineering, Changzhou University, Changzhou 213164, Jiangsu, P. R. China)
Abstract: The presence of emerging contaminants in the raw water puts forward new challenges to drinking water treatment process. The chlorination of typical sulfonamides antibiotic sulfadimethoxine (SDM) in the sodium hypochlorite disinfection process was studied. The chlorination effects, including the initial concentration of residual chlorine, the pH value of the solution, ammonia concentration, and the inorganic anions, were also investigated. The mechanism of SDM chlorination was explored and the ecological risk was further assessed. The results showed that, under the conditions of the initial SDM concentration 15 μmol/L, the initial concentration of residual chlorine 60 μmol/L, the SDM removal reached high up to 95.9% in 120 s. The degradation process conformed to the pseudo-second reaction kinetics. The constants of degradation rate decreased with the increasing ammonia concentration, and increased with the initial concentration of residual chlorine. Background anions Cl-, NO3-, SO42- had marginal effects on the reaction while HCO3- and CO32- had inhibition effects on the reaction. SDM chlorination can be improved under neutral conditions. Nine degradation intermediates are identified by using high-resolution mass spectrometry HRMS Orbitrap. The degradation process covers chlorination, demethylation and hydroxyl addition reactions. The complete removal of SDM does not imply an effective reduction of ecological risk during disinfection process which poses a potential risk to the safety of drinking water quality.
Keywords: sulfadimethoxine (SDM); chlorine disinfection; reaction kinetics; degradation mechanism; risk assessment
磺胺二甲氧嗪(Sulfadimethoxine,SDM)是一种典型磺胺类人工合成抗生素,抗菌范围广,性质稳定,广泛用于水产养殖和畜牧业[1]。使用SDM可能导致致病菌对药物和消毒产品产生抗药性,SDM的大规模使用导致其通过污水排放等多种途径进入环境水体,中国多个城市的污水、河水等环境介质中都已检出了SDM,浓度高达166 ng/L[2]。SDM进入水环境后会诱导病原菌产生抗药性,或通过食物链进入生物体,进而危害水生生态系统安全[3-5]。
氯消毒是传统水处理工艺中的最后一道防线,然而,在消毒的同时,余氯也与水中的有机物发生反应,生成消毒副产物,影响水质安全[6]。目前广为人知的消毒副产物有卤乙酸类、三卤甲烷、溴酸盐、亚硝胺类等,前体来源为水中的腐殖质、蛋白质等。近年来,随着抗生素、药物和个人护理用品等新兴污染物在环境水体中的不断检出,新兴污染物是否可能是消毒副产物的前体,成为一个急需解答的问题。研究发现,在消毒工艺中,多种新兴污染物生成了消毒副产物,并且毒性明显增强。比如抗菌剂三氯生在氯氧化过程中产生多氯代产物,使抗雌激素活性提高30倍[7],除草剂赛克嗪的氯氧化过程中鉴定出17种中间产物,部分产物对动物和人类具有潜在的致突变性和发育毒性,对水环境产生更大的危害[8]。自来水原水中磺胺类抗生素的存在对饮用水处理工艺提出新的挑战,传统水处理工艺单元(混凝、沉淀、砂滤)无法有效去除水中的磺胺类抗生素[9]。磺胺类抗生素结构中含氨基,可能发生次氯酸与氯胺消毒相似的反应,因此,在氯消毒过程中磺胺类抗生素的行为特征和潜在风险亟待深入研究和评价。
笔者以典型磺胺类抗生素SDM为目标污染物,考察余氯初始浓度、溶液pH值和NH4+-N浓度、无机阴离子等对降解SDM的影响,利用高分辨率质谱HRMS Orbitrap(Q-E Plus)对SDM降解中间产物进行鉴定,探讨SDM降解机制,提出降解路径,评估降解过程中的毒性变化。进一步明晰磺胺类抗生素在消毒工艺中的转化和风险,有助于提出针对性策略和替代消毒工艺,在满足消毒效能的基础上,降低此类消毒副产物所带来的健康风险。
1 材料与方法
1.1 实验试剂
SDM(纯度98%)、NaClO(含14%活性氯)购自阿拉丁公司(上海),甲醇(HPLC级)购自Sigma公司(美国)。二氯甲烷(CH2Cl2)购自永华化学(江苏),分析纯试剂盐酸、亚硫酸钠、硫酸铵、氢氧化钠、二水合磷酸二氢钠、十二水磷酸氢二钠购自上海国药,实验用水均为超纯水(电导率18.3 MΩ·cm)。
1.2 动力学实验
取20 mL SDM溶液置于玻璃器皿中,利用磁力搅拌器搅拌,确保反应均匀。使用稀盐酸和氢氧化钠溶液(1 mol/L)、磷酸盐缓冲液(10 mmol/L)调节溶液pH值,将一定体积NaClO溶液加入到20 mL SDM溶液中,不同反应时间取样,并迅速与过量Na2SO3溶液(12.5 g/L)淬灭反应,确保反应终止。用HPLC-MS/MS测定剩余SDM浓度,探究不同因素(余氯初始浓度、溶液pH值、氨氮浓度、无机阴离子浓度)对降解的影响。所有反应均重复3次,取平均值。
1.3 SDM及其中间产物分析
使用HPLC-MS/MS(Thermo TSQ quantum Access Max)测定SDM浓度。色谱条件:Thermo Access C18色谱柱(3 mm×50 mm,2.6 μm);采用梯度洗脱,流动相为0.1%甲酸水和甲醇,流速1.0 mL/min;柱温25 ℃。质谱条件:负离子模式,扫描模式为SRM,SDM子母离子对m/z为155.8/310.7,轰击电压44 V。
SDM降解中间产物的反应液制备方法:按照1.2节的方法进行SDM降解反应,分别在45、90、240、480 s取样,对应降解初期、中期和末期等反应阶段,降解液混合后进行浓缩和脱盐处理,同时取0 s样品作为空白对照。SDM降解反应溶液均使用超纯水配置。
使用高分辨率质谱HRMS Orbitrap鉴定降解中间产物,进样前需对反应液进行预处理。参照美国EPA 1694方法对降解液进行固相萃取和脱盐[10]。高分辨率质谱测定条件为:Waters HSS T3色谱柱(2.1 mm×50 mm,1.7 μm);流动相为甲醇和水;正负离子同时扫描;离子源鞘气流速12 mL/min;喷雾电压4 kV;分辨率14万。数据分析采用Xcalibur 4.1软件。
1.4 生态风险评价
使用海洋菌费氏弧菌(Vibrio fischeri)作为指示细菌,进行急性毒性试验,考察氯氧化过程中SDM反应溶液的毒性变化。采用生物毒性分析仪(ATD-P1,北京金达清创)测定发光细菌与SDM氯氧化样品接触前后的发光强度,计算水样对发光细菌发光强度的相对抑制率,以表示急性毒性的大小。每个样品测定3组数据,以NaCl(2%)溶液为空白对照,前后各设置两组。相对抑制率I由式(1)计算。
式中:I为相对抑制率,%;Lt为样品发光强度;L0为阴性对照发光强度。
使用生态结构效应关系软件ECOSAR(V2.0,美国环保局EPA),根据SDM及降解产物的分子结构来预测对水生生物(鱼、水蚤、藻类)的生态环境毒性风险。
1.5 指标分析方法
TOC值采用总有机碳分析仪(N/C2100s,德国耶拿)进行测定,基于相关国家标准方法对氨氮、总磷、总氮等进行分析,使用离子色谱(Dionex Aquion,美国赛默飞)测定水中无机离子浓度。
2 结果与讨论
2.1 氯化SDM反應动力学
在SDM初始浓度为15 μmol/L、余氯初始浓度为60 μmol/L、pH值为7的条件下进行SDM氯氧化试验,结果见图1。
图1 表明,在氯氧化过程中SDM 与NaClO 快速反应,反应120 s 时SDM 去除率可达95. 9%。用准二级动力学方程式(式(2)、式(3))拟合实验数据,此方程也成功用于拟合高铁酸盐降解多氯联苯硫醚反应过程[11]。结果表明,拟合相关系数R2 为0. 998 7,二级反应速率常数ka'pp为0. 008 3 μmol/(L·s),SDM 氯氧化反应符合准二级反应动力学。
式中:[SDM]t和[SDM]0 分别为t 时刻、0 s 时SDM 浓度,μmol/L;[HClO] 为溶液中HClO 浓度,μmol/L;ka'pp为准二级表观动力学速率常数,μmol/(L·s)。
2.2 余氯初始浓度对反应的影响
在SDM初始浓度为15 μmol/L,溶液pH值为7时,考察余氯初始浓度对SDM降解的影响,结果见图2和表1。
图2和表1表明,当余氯初始浓度从30 μmol/L增加为90 μmol/L,反应速率常数由0.005 7 μmol/(L·s)升高为0.013 1 μmol/(L·s)时,半衰期从34.4 s减小为3.4 s。随着余氯初始浓度的增加,反应速率常数逐渐增大。这主要是因为次氯酸根离子在水中发生水解反应产生次氯酸,见式(4)。随着NaClO浓度的增加,水中HClO浓度也随之增加,溶液中更多的HClO与SDM反应,导致反应速率加快,降解率增加。
2.3 溶液pH值对反应的影响
考察SDM初始浓度为15 μmol/L、余氯浓度为60 μmol/L条件下不同溶液pH值对SDM降解的影响,见图3和表2。
由图3和表2可以看出,当溶液pH值为7时,反应速率常数最大为0.009 2 μmol/(L·s),半衰期为7.0 s,表明中性条件下更有利于降解过程。溶液pH值对SDM氯氧化有明显影响,碱性条件下(pH值11)反应速率常数最小,仅为0.000 1 μmol/(L·s),次氯酸浓度是氯氧化的主要活性物质,碱性条件极大抑制了次氯酸根离子(ClO-)的水解反应,当pH值大于7.54时,溶液中主要以ClO-为存在形式,次氯酸浓度降低,从而减小了反应速率常数[12]。而酸性条件也不利于SDM氯氧化过程,pH值为3时,反应速率常数为0.000 9 μmol/(L·s),仅为中性条件下的10%。针对解离有机物,次氯酸与分子态有机物的反应速率往往比和离子态高1~4个数量级[13],SDM的pKa为5.92,意味着在酸性条件下SDM主要以离子态为主。因此,酸性条件下次氯酸与离子态SDM的降解速率降低,从而表现出对SDM氯氧化反应的抑制效应。Acero等[14]对敌草隆与异丙隆氯氧化的研究也有类似发现。
2.4 氨氮浓度对反应的影响
氨氮可导致水体产生富营养化,在水环境中广泛存在。考察SDM初始浓度为15 μmol/L、余氯初始浓度为60 μmol/L、溶液pH值为7时氨氮浓度对SDM降解的影响,结果见图4和表3。
图4和表3表明,随着水中氨氮浓度升高,SDM的去除率与反应速率常数逐渐减小。当溶液中氨氮浓度从10 μmol/L增加至30 μmol/L时,反应速率常数由0.007 8 μmol/(L·s)降低为0.002 4 μmol/(L·s)。当氨氮浓度增加到40 μmol/L时,反应速率常数降至最小,为0.001 4 μmol/(L·s),120 s内SDM去除率只有33.8%,说明氨氮对SDM氯氧化反应起显著抑制作用。氨氮和次氯酸发生系列反应,生成氯胺、二氯胺等,导致溶液中次氯酸浓度降低,从而抑制了SDM氯氧化反应[15]。
2.5 背景无机阴离子对反应的影响
水环境中存在的无机阴离子可能会影响消毒效果。在SDM初始浓度为15 μmol/L、余氯初始浓度为60 μmol/L、溶液pH值为7条件下,考察浓度为10 mmol/L的HCO3-、Cl-、NO3-、SO42-、CO32-等5种阴离子对SDM降解的影响,结果见图5和表4。
从图5和表4可以看出,与空白对照的反应速率常数(0.008 3 μmol/(L·s))相比,阴离子Cl-、NO3-、SO42-条件下的SDM氯氧化反应速率常数分别为0.008 1、0.008 2、0.008 3 μmol/(L·s),表明Cl-、NO3-、SO42-对氯氧化过程基本没有影响,这与2,4-二溴苯酚氯氧化研究中的结论一致[16]。此外,阴离子HCO3-和CO32-条件下的反应速率常数明显降低,分别为0.005 8、0.000 2 μmol/(L·s),表明HCO3-和CO32-对SDM氯氧化有抑制作用,并且CO32-抑制作用显著,主要原因是作为常见的活性自由基捕获剂,HCO3-和CO32-会与反应体系中的活性成分反应;此外,CO32-对水中H+的结合力大于ClO-,会与HClO发生反应,降低水中HClO的含量,从而抑制反应过程[17]。
2.6 实际环境水体中的SDM氯氧化反应
采集常州市某实际河水水样,以考察实际环境水体中的SDM氯氧化效果,河水水样的水质指标为:总磷0.04 mg/L、氨氮0.23 mg/L、總氮1.65 mg/L、TOC值7.72 mg/L、pH值7.84、氯离子45.7 mg/L、硝酸根离子0.91 mg/L、硫酸根离子93.2 mg/L、磷酸根离子0.03 mg/L。在初始浓度为15 μmol/L、余氯初始浓度为60 μmol/L,溶液pH值为7的条件下,比较SDM在河水和纯水中的氯氧化反应,结果见图6和表5。
从图6和表5可以看出,在河水中SDM氯氧化反应速率常数为0.005 5 μmol/(L·s),明显低于纯水中的反应速率常数(0.008 3 μmol/(L·s)),反应速率常数降低了33.7%,表明河水中的溶解性有机物对SDM氯氧化过程起到抑制作用。河水中存在大量腐殖酸类有机物,是抑制SDM氯氧化反应的主要因素。腐殖酸结构复杂,富含大量官能团,如-OH、-COOH、-CO、-NH2等,可作为电子供体优先与活性物质发生反应,与SDM形成竞争性反应,从而减慢SDM氯氧化反应过程[18]。在河水背景条件下,TOC值降解前为8.31 mg/L,降解后为8.17 mg/L,TOC值稍有降低,氯氧化过程对水中有机物的降解作用有限,通过氯氧化反应,有机物转换成后续降解中间产物,基本没有矿化。
2.7 氯氧化中间产物与降解机理
对降解液进行固相萃取,使用高分辨率质谱HRMS Orbitrap解析出9种中间产物,基本信息见表6。母物质SDM及氯代SDM(Cl-SDM)的色谱图和二级质谱图见图7。从图7(a)、(b)可以看出,母物质SDM出峰时间为5.43 min,分子离子质荷比m/z为311.080 8,二级质谱中有3个主要碎片离子,分别为311.080 6、156.076 8和108.044 7。
SDM结构中含有氨基,因此氯氧化过程中很容易与次氯酸发生氯代反应,取代氨基上的H,生成一氯代SDM(Cl-SDM,Pr344),见表6、图7(c)、(d)。Cl-SDM在色谱中的保留时间为6.02 min,分子离子质荷比m/z为345.041 5,存在4个主要碎片离子,m/z分别为108.044 7、156.011 4、190.037 8、345.041 7。此外,Cl-SDM中氨基上的H还会进一步被取代,生成二氯代產物(2Cl-SDM,Pr378)和三氯代产物(3Cl-SDM,Pr412)。
脱甲基反应是甲氧基经常发生的氧化反应,Cl-SDM发生脱甲基反应,脱去嘧啶甲氧基上的甲基(-CH3),生成Pr330。此外Cl-SDM还会发生羟基加成反应,在苯环不同位置加入羟基,生成同分异构体Pr360-a和Pr360-b。同样,2Cl-SDM也会发生脱甲基反应和羟基加成反应,分别生成Pr364,Pr394-a和Pr394-b。基于以上分析,提出SDM在氯氧化过程中的可能路径,见图8。
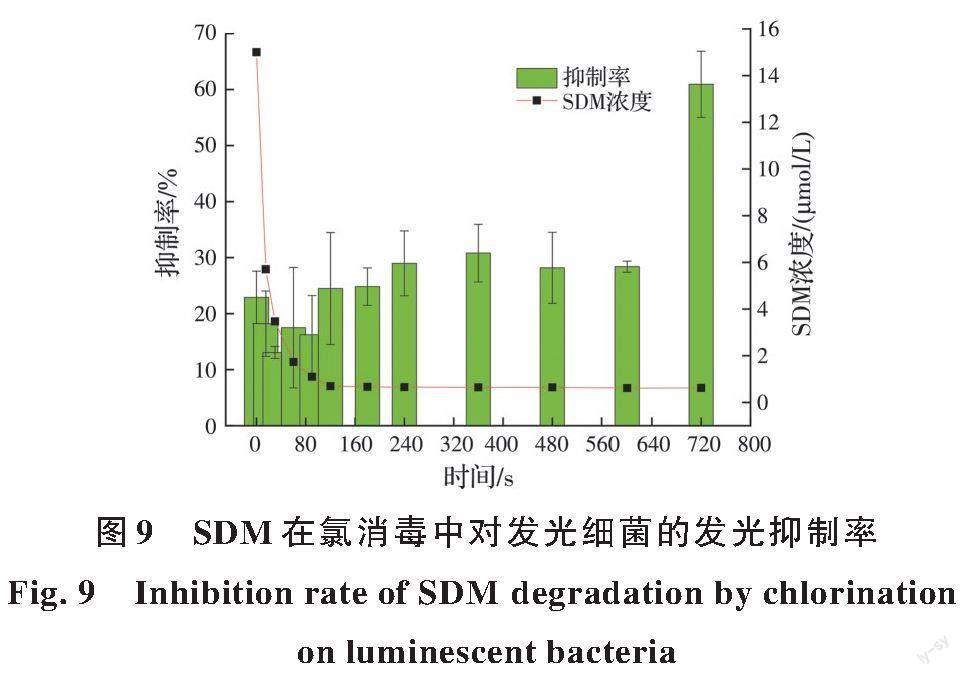
2.8 生态风险预测与评价
在初始浓度为15 μmol/L、余氯浓度为60 μmol/L、溶液pH值为7的反应条件下,SDM进行降解反应。采用费氏弧菌的发光强度抑制率评价氯氧化过程中水样的急性毒性变化(图9)。SDM空白溶液对发光细菌的相对抑制率为22.9%,随着降解反应进行,发光抑制率反而增大。反应时间为120 s时,SDM去除率为95.9%,但发光抑制率反而增加到24.5%,进一步延长反应时间至720 s,反应液对发光细菌相对抑制率增加,发光抑制率增大到60.9%,表明SDM降解过程中生物毒性并没有得到有效去除,发光菌急性毒性反而稍有增大,生态风险依然存在。
使用ECOSAR软件,预测SDM及中间产物对水生生物(如鱼类、水蚤、绿藻)的生态毒性风险,预测结果包括急性毒性LC50(半致死浓度)和EC50(半效应浓度)[19]。从表7可以发现,母物质SDM的鱼类LC50值为116 mg/L,而9个中间产物的鱼类LC50均高于母物质,表明这9个中间产物的鱼类急性毒性低于母物质SDM,针对水蚤和绿藻的毒性预测也有类似特征。发光菌发光毒性抑制率用于评价在氯氧化过程中水样的急性毒性变化,是对水样中母物质和所有中间产物的综合反映。9种中间产物的预测毒性普遍偏低、发光菌毒性抑制率增加、结果趋势不一致的主要原因可能是存在没有被高分辨率质谱鉴定出来、但毒性较大的中间产物。
因此,磺胺类药物在氯消毒过程中生成副产物的生态风险还有待进一步深入分析,以确保饮用水安全。
3 结论
1)SDM氯氧化反应过程符合准二级反应动力学。在SDM初始浓度为15 μmol/L、余氯初始浓度为60 μmol/L、pH值为7的反应条件下,120 s内SDM去除率达到95.9%。
2)二级反应降解速率常数随余氯初始浓度增加而增大,随着NH4+-N浓度增加而减小,中性条件下,SDM氯氧化反应最快,弱酸性和碱性条件下对氯氧化有抑制作用。
3)使用HRMS Orbitrap共鉴别出9种中间产物,SDM氯氧化降解SDM过程主要通过氯代反应、脱甲基反应、羟基加成反应来实现。
4)SDM氯氧化反应过程中急性毒性并没有有效去除,对饮用水水质安全存在潜在威胁。
参考文献
[1] CHOKEJAROENRAT C, SAKULTHAEW C, ANGKAEW A, et al. Remediating sulfadimethoxine-contaminated aquaculture wastewater using ZVI-activated persulfate in a flow-through system [J]. Aquacultural Engineering, 2019, 84: 99-105.
[2] WANG Z, ZHANG X H, HUANG Y, et al. Comprehensive evaluation of pharmaceuticals and personal care products (PPCPs) in typical highly urbanized regions across China [J]. Environmental Pollution, 2015, 204: 223-232.
[3] KÜMMERER K. Antibiotics in the aquatic environment- A review - Part I [J]. Chemosphere, 2009, 75(4): 417-434.
[4] KÜMMERER K. Antibiotics in the aquatic environment- A review-Part II [J]. Chemosphere, 2009, 75(4): 435-441.
[5] XIN X D, SUN S H, ZHOU A R, et al. Sulfadimethoxine photodegradation in UV-C/H2O2 system: Reaction kinetics, degradation pathways, and toxicity [J]. Journal of Water Process Engineering, 2020, 36: 101293.
[6] 王小宁, 杨传玺, 宗万松. 饮用水消毒副产物生物毒性与调控策略的研究[J]. 工业水处理, 2017, 37(1): 12-17.
WANG X N, YANG C X, ZONG W S. Research on biological toxicity of drinking water disinfection by-products and its control strategies [J]. Industrial Water Treatment, 2017, 37(1): 12-17. (in Chinese)
[7] LI L P. Toxicity evaluation and by-products identification of triclosan ozonation and chlorination [J]. Chemosphere, 2021, 263: 128223.
[8] DE BARROS A L C, SILVA RODRIGUES D ADA, CUNHA C C R FDA, et al. Aqueous chlorination of herbicide metribuzin: Identification and elucidation of “new” disinfection by-products, degradation pathway and toxicity evaluation [J]. Water Research, 2021, 189: 116545.
[9] ADAMS C, WANG Y, LOFTIN K, et al. Removal of antibiotics from surface and distilled water in conventional water treatment processes [J]. Journal of Environmental Engineering, 2002, 128(3): 253-260.
[10] SAPOZHNIKOVA Y, HEDGESPETH M, WIRTH E, et al. Analysis of selected natural and synthetic hormones by LC-MS-MS using the US EPA method 1694 [J]. Analytical Methods, 2011, 3(5): 1079.
[11] CHEN J, XU X X, ZENG X L, et al. Ferrate(VI) oxidation of polychlorinated diphenyl sulfides: Kinetics, degradation, and oxidized products [J]. Water Research, 2018, 143: 1-9.
[12] 嚴静娜, 张小寒, 任源. 次氯酸钠氧化消除水中双氯芬酸的动力学及影响因素[J]. 水处理技术, 2017, 43(9): 56-61, 66.
YAN J N, ZHANG X H, REN Y. Kinetic and influencing factors of diclofenac oxidation in water by sodium hypochlorite [J]. Technology of Water Treatment, 2017, 43(9): 56-61, 66. (in Chinese)
[13] ACERO J L, PIRIOU P, VON GUNTEN U. Kinetics and mechanisms of formation of bromophenols during drinking water chlorination: Assessment of taste and odor development [J]. Water Research, 2005, 39(13): 2979-2993.
[14] ACERO J L, REAL F J, BENITEZ F J, et al. Kinetics of reactions between chlorine or bromine and the herbicides diuron and isoproturon [J]. Journal of Chemical Technology & Biotechnology, 2007, 82(2): 214-222.
[15] DING J Q, NIE H, WANG S L, et al. Transformation of acetaminophen in solution containing both peroxymonosulfate and chlorine: Performance, mechanism, and disinfection by-product formation [J]. Water Research, 2021, 189: 116605.
[16] XIANG W R, CHANG J Y, QU R J, et al. Transformation of bromophenols by aqueous chlorination and exploration of main reaction mechanisms [J]. Chemosphere, 2021, 265: 129112.
[17] 李军, 葛林科, 张蓬, 等. 磺胺类抗生素在水环境中的光化学行为[J]. 环境化学, 2016, 35(4): 666-679.
LI J, GE L K, ZHANG P, et al. Progress in studies on photochemical behavior of sulfonamide antibiotics in aquatic environment [J]. Environmental Chemistry, 2016, 35(4): 666-679. (in Chinese)
[18] 闫淑霞, 刘春花, 梁岩. 腐殖酸的结构特性与应用研究进展[J]. 天然产物研究与开发, 2017, 29(3): 511-516.
YAN S X, LIU C H, LIANG Y. Review on structural properties and multiple functionalities of humic acids [J]. Natural Product Research and Development, 2017, 29(3): 511-516. (in Chinese)
[19] 程艳, 陈会明, 于文莲, 等. QSAR技术对高关注化学物质生态环境毒理风险预测[J]. 环境科学研究, 2009, 22(7): 817-822.
CHENG Y, CHEN H M, YU W L, et al. Eco-environmental toxicity risk prediction for substances of very high concern with QSAR approach [J]. Research of Environmental Sciences, 2009, 22(7): 817-822. (in Chinese)
