在气泡中长大的“铜树”
——电解CuCl2溶液的趣味探究实验
2023-11-23吴宁宁
吴宁宁
(南京市第二十九中学 江苏 南京 210036)
一、实验背景
2019 人教版高中化学选择性必修一中电化学部分,电解占据很重要的一部分,在掌握电解原理的基础上从微观角度分析电解过程中电解质溶液内部的变化尤为重要。针对这一节内容,2017年版课程标准中也建议开展电解氯化铜溶液的探究实验。笔者查阅文献发现,关于探究电解氯化铜溶液过程中两极pH 变化的实验很少,但在教学过程中经常会有学生问及电解过程中溶液pH的变化情况。化学是实验的科学,遇到问题时,应积极寻求用实验的方法解决,以实验数据为证据进行合理的解释[1]。
用教材中提供的电解CuCl2溶液的装置开展学生实验,发现实验现象不明显。于是对实验装置进行了改进,并且在实验的过程中,除了获得了两极pH的变化情况,还观察到了异常实验现象——阴极除析出红色物质的同时还有气泡析出。学生基于阴极现象的视觉效果,又对阴极电极加以设计,开展了基于电解CuCl2溶液的趣味实验——在气泡中长大的“铜树”。
二、实验
2019 人教版高中化学选择性必修一教材中本实验是在U形管中进行,但是实际实验中发现电解进行得很慢,实验现象不明显,而且由于U形管管口较细,pH传感器不能伸入管内以实时测定电解过程中两极pH变化。查阅资料发现是因为电极放置在U形管两端,两电极间距离长电解速率慢,作为课堂实验效果不佳[2]。学生讨论后对实验装置进行了改进。将矿泉水瓶从中间切成两部分,上端瓶口部分倒扣在下端瓶身中,做成简易的电解槽,缩短两电极之间的距离,实验一开始就能观察到明显的实验现象,而且也解决了pH传感器的放置问题。
1.电解CuCl2溶液过程中两极pH的变化
1.1 实验用品
(1)实验器材:
自制电解槽一套(配有2B铅笔芯作电极),学生直流电源一个,两支pH传感器,装置示意图如图1所示。
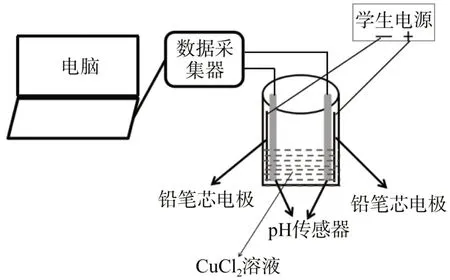
图1 电解CuCl2溶液的实验装置
(2)实验试剂:
pH为4.08、9.16的两份缓冲标准液,0.02 mol/L的CuCl2溶液40 mL,淀粉-KI试纸。
(3)实验条件:
室温,敞开体系,2B铅笔芯作电极,阴阳两极之间距离约为10 cm。
1.2 实验步骤
(1)用缓冲标准液对两支pH传感器进行校正。
(2)将CuCl2溶液加入自制电解槽中,固定好两电极位置。
(3)将两支pH传感器分别放在阴阳两极附近,采集数据,待两支pH传感器示数稳定,接通电源,开始电解。
(4)每隔约1 min时间,交换一次两支pH传感器的位置,且每次都置于相同位置,并尽快固定使溶液稳定。
1.3 实验现象
实验过程中可以观察到,阳极电极上有大量气泡冒出;阴极电极上有红色物质析出,同时也有气泡冒出[3]。实验数据显示,在电解CuCl2溶液时,每次交换pH传感器位置并稳定后,两极附近pH随时间变化情况如图2所示。两极pH相差很大,阴极电极附近溶液呈碱性,阳极电极附近溶液呈酸性。

图2 电解氯化铜溶液过程中两极pH的变化
1.4 实验结论
由实验现象可知,阳极电极上有大量气泡冒出。由电化学原理知道,电解质溶液中的阴离子移向阳极,在阳极上发生氧化反应。CuCl2提供的Cl-、水电离出的OH-移向阳极,Cl-还原性强于OH-,优先在阳极放电,发生氧化反应:2Cl-- 2e-==== Cl2↑。阳极附近溶液呈酸性,说明不能忽视氯气溶于水并和水发生的反应:电解质提供的Cu2+、水电离出的H+移向阴极。阴极有红色物质析出,是Cu2+发生还原反应:Cu2++2e-====Cu;有气泡冒出,且在阴极附近放置一片湿润的淀粉-KI试纸,较长时间内观察不到明显现象,说明不是阳极生成的氯气扩散到阴极并逸出,究其原因应是2H2O+2e-====H2↑+2OH-;同时阴极附近Cu2+被还原成Cu单质,溶液中Cu2+浓度降低,使得其水解平衡逆向移动,二者均使得阴极电极附近H+浓度减小,OH-浓度增大,呈碱性。这也说明电极反应速率很快,超过阳极区H+向阴极流动补充的速率,所以H+的消耗速率大于补充速率,H+浓度减小,阴极实时pH增大。
由实验数据和以上分析可以证明,很多电解题目忽略氯气溶于水,不考虑阴极电极pH 的变化是不合理的[4],纯粹是为了做题而做题,并没有考虑实际情况。
1.5 讨论
此实验中在阴极观察到有气泡冒出,属于超出高中学生认知范围的异常实验现象。这一现象的出现激发了学生的好奇心和探究欲望。学生课后开展了探究实验,反复操作发现当两个电极距离比较近时,阴极有大量气泡产生,两电极距离较远时,阴极气泡较少,现象不明显。学生们群策群力,讨论、分析可能的原因,最终的解释是电极距离近时,阳极产生的Cl2能更快地扩散到阳极,与水反应产生H+,或者Cl2与水反应产生的H+可以更快地迁移到阴极,总之两电极距离近时,有利于增大阴极H+浓度,在电解时与Cu2+产生竞争,共同被还原。
电解实验数据表明,阴极不管用哪支pH传感器,电解稳定后,pH读数都显示溶液呈碱性;阳极无论用哪支pH 传感器,电解稳定后,pH 读数都显示溶液呈酸性,排除了传感器带来的误差。阳极溶液pH 的变化是由于产生的氯气溶于水并和水反应造成的。而阳极产生的H+会移向阴极,使阴极H+浓度增大,和Cu2+产生竞争,在阴极共同被还原。所以观察到阴极有红色物质析出的同时也有气泡产生。
对此推理,学生们提出了探究实验方案——在电解时,使用阴离子交换膜,阻止阳极H+向阴极移动。由于实验条件有限,目前还没能得以执行。
对于电解CuCl2溶液过程中出现的这一异常现象,学生们除了以上的追因探究,还利用这一现象带来的视觉效果设计了一个趣味实验,感受化学之美。
2.在气泡中长大的“铜树”趣味实验
2.1 实验用品
(1)实验器材:
自制电解槽一套(同上),学生直流电源一个,细铜丝。
(2)实验试剂:
0.02 mol/L的CuCl2溶液,NaCl固体,沾有NaOH溶液的棉花团。
2.2 实验步骤
(1)将细铜丝绕在铅笔芯上,像分叉的树枝;组装好装置,如图3所示;

图3 制作“铜树”的电解装置
(2)向CuCl2溶液中加入适量NaCl,搅拌溶解。接通电源,开始电解实验;
(3)观察并记录下阴极的实验现象。
2.3 实验现象
在阴极上,有气泡冒出,同时不断有红色的铜析出,吸附在每一根细铜丝上,像绒毛一样不断长长,稍微晃动溶液,铜绒毛会在溶液中摆动。在电解过程中,阴极电极看起来就像是一棵在气泡中慢慢长大的红色“铜树”,如图4所示。

图4 在气泡中长大的“铜树”实验现象
2.4 讨论
在电解CuCl2溶液时,向其中加入一定量的NaCl,可以增大电解质浓度,增强溶液导电能力,也增大溶液中Cl-浓度,使析出Cl2的速率更快,增大溶液中Cl2的浓度,增强溶液酸性,阴极H+浓度增大,由能斯特方程可知其氧化性增强,与Cu2+的竞争力也增强,在阴极被还原,同时析出红色固体物质Cu,所以学生在电解CuCl2溶液时加入了适量的NaCl固体。
3.实验反思
3.1 实验创新之处在于对教材实验进行了改进,使电解现象出现得更快更明显,而且能够解决氯气污染空气的问题,并且可以进行微型化实验,节约试剂。利用身边触手可及的物质自制实验器具,如矿泉水瓶、铅笔芯、导线内的铜丝等,拉近化学与生活的距离。尤其是实验条件不佳的学校,大大激发了学生大胆尝试创造实验条件的勇气。针对本实验,学生电源没有或者不足的学校,也可以鼓励学生尝试使用充电宝等作为电源。
3.2 学生在实验探究的过程中提升对电解原理的认知程度,拓宽自己的理论知识。理论分析阴极上只有Cu析出,而实验过程中却出现了不一致的现象,除析出红色物质,还有气泡冒出。这一异常现象,激发了学生的探究欲望。查阅资料可知是H+和Cu2+在阴极竞争反应的结果。利用此现象,学生设计了趣味实验——在气泡中长大的“铜树”,实现现象极具观赏性,学生能够主动感受并欣赏化学的神奇和美丽,增加课堂趣味性和学科魅力。
3.3 使用两支pH 传感器,在自制电解槽中实现电解过程中溶液的不同区域pH变化的直观化,有助于学生从微观角度对电解原理进行深入分析。但测两极pH变化的过程中,实验在敞开体系中进行,在此过程中如何避免氯气逸出到空气中,是下一步改进的要点。
3.4 这是一组系列实验,以教材为源,超出教材。真正实现化学学科在复杂、真实的实验情境中发现问题,再用实验来解决问题的学科学习方式。在实验探究过程中,迸发出一些来自实践的思维火花,切实感受到思维的深刻性和独创性得以提升,并感受到实验的魅力,感知学科的价值。纸上得来终觉浅,绝知此事要躬行,凡事一定要多实践、多思考。
三、实验教学总结
首先,本实验教学的价值挖掘。作为一名化学学科老师,笔者深知化学是在原子、分子的水平上研究物质的组成、结构、性质及应用的基础自然科学。因此如何将化学的学科本质落实到自己的课堂上成了笔者经常思考的一个问题,具体表现为教什么、如何教、为什么要教。笔者认为只有在贯穿学科知识的真实情境下,教师加以知识的讲授、方法的引导和情感的培养,学生才能形成一定的价值观念、必备品质和解决问题的关键能力,最终逐渐形成化学学科核心素养。
本节课选自2019 人教版高中化学选择性必修一第四章第二节电解池,教材安排了电解CuCl2溶液的实验,课程标准也建议开展电解CuCl2溶液的探究活动。
笔者认为本节课既是学科知识学习的需要,因为它是电化学知识不可或缺的一部分,同时学生了解电解原理的应用也是社会对工业生产专技人员的要求,本节课对电解原理的教学起到巩固基础知识、提升思维深度的作用。
学生通过查阅资料,从微观角度解释两极pH 的宏观变化。在实验探究过程中,学生的微粒观、变化观、实验观等核心观念逐渐形成。与此同时,宏观辨识与微观探析、证据推理与模型认知、科学探究与创新意识等核心素养得到一定提升。除此之外,实验中的异常现象的充分利用激发了学生在学习中的自主性和创造性,体验到化学之美,同时也为学生的课外自主学习与发展抛砖引玉[5]。
其次,目标建构。通过分析教材和课标,笔者设定了以下三个教学目标,分别是①通过对电解CuCl2溶液现象的观察、实验数据的分析,从微观角度解释宏观现象,完善电化学的知识体系;②引导学生分析实验过程中的异常现象,发展学生宏观辨识与微观探析、证据推理与模型认知、变化观念与平衡思想等核心素养;③通过对异常现象的分析,引导学生设计实验方案验证自己的分析,用理论指导实践,在实践中发现问题、解决问题,培养科学探究与创新意识、科学态度与社会责任等核心素养。
同时,为每一个教学目标确立了相应的评价目标,分别为①通过对电解过程中微观粒子变化本质的讨论和点评,诊断并发展学生对电解原理的认识水平(物质水平、微粒水平);②利用异常现象培养学生的思辨能力、证据推理能力及探究实验设计能力;③通过实验过程,从学科价值视角、社会价值视角等方面诊断并发展学生对化学价值的认识水平,从而实现教学评一致性[6]。
教学重点是认识电解的原理和本质,发展宏观辨识与微观探析、证据推理与模型认知等核心素养;难点是分析电解过程中出现异常现象的原因,并设计实验、动手做实验、观察现象、解释现象、验证猜测。为此笔者采用POE的教学策略[7],在建构主义理论的指导下,利用真实情境促进概念建构,同时融合环环相扣的探究活动发展核心素养,采用讲授、实验、自主合作、探究等多种教学方法,以期达到最好的教学效果。
