高色纯度荧光碳点的制备和应用研究进展
2023-11-22李亚楠刘云刘春艳肖军平
李亚楠,刘云,刘春艳,肖军平
(1 北京科技大学 化学与生物工程学院,北京 100083;2 中国科学院理化技术研究所,北京 100190)
窄带宽的高色纯度荧光材料在超高清显示和照明、超分辨成像和传感、生物成像以及防伪等领域用途广泛。目前发展和研究的高色纯度荧光材料主要是稀土荧光材料[1-2]、有机大分子衍生物[3-4]、Ⅱ-Ⅵ族(CdSe,CdS,ZnS 等)和Ⅲ-Ⅴ族(InP,InAs 等)的半导体量子点[5-6]和卤化物钙钛矿纳米晶CsPbX3(X=Cl,Br 和I)[7-8]等。尽管它们具有色纯度好、量子效率(fluorescent quantum yield,QY)高、窄带宽发射和发光位置可调的优异特性,但稀土材料来源稀少、价格昂贵;Ⅱ-Ⅵ族和Ⅲ-Ⅴ族半导体量子点和卤化物钙钛矿纳米晶通常含有剧毒的过渡金属离子,如镉和铅等,环境危害大。这些不足限制了它们的大规模使用。与之相比,碳点具有合成原料广泛、毒性小、光/热稳定性好、环境友好以及生物相容性好的优点,可以作为上述高色纯度荧光材料的理想替代者,用于超高清显示、超分辨成像等领域。
碳点是由碳核和表面修饰层组成的尺寸小于10 nm 的零维碳材料[9]。依据微结构的不同,碳点可以分为碳量子点(carbon quantum dots,CQDs)(由微小sp2碳共轭结构的核和表面亲水性官能团组成)[10]、石墨烯量子点(graphene quantum dots,GQDs)(边缘存在亲水性官能团的单层或多层石墨烯片)[11]、碳化聚合物点(carbonized polymer dots,CPDs)(sp2碳嵌在sp3碳基底上的聚合或交联产物,通常炭化程度较低)[12]等几种类型[13]。根据自身合成碳点的结构,不同研究者使用碳核发光(π 共轭结构)、表面态发光、发色团的分子态发光以及限域交联提升发光等来解释其发光机理[14]。
色纯度是评估发光材料光学性能的重要因素之一。发光峰半峰宽(full width at half maximum,FWHM)越窄,色纯度越高,因此可用FWHM 作为评价色纯度的指标之一[15]。与发光色纯度较低的传统碳点(FWHM≥60 nm)相比,FWHM<50 nm 的高色纯度荧光碳点种类和数量相对很少;且在发光效率和色纯度上与FWHM≤30 nm 甚至20 nm 的稀土荧光材料、Ⅱ-Ⅵ族半导体量子点和卤化物钙钛矿纳米晶等相比差距显著。因此,迫切需要发展FWHM<50 nm,甚至小于30 nm 的高QY 荧光碳点。基于此,本文主要从高色纯度碳点的合成方法、FWHM 和峰位调制,以及应用等几个方面对高色纯度碳点的国内外研究进展进行了总结与评述。
1 合成方法
依据前驱体种类不同,碳点的合成可分为“自上而下法”和“自下而上法”两种类型[16-17]。“自上而下法”通常以体相碳材料如石墨[18]、碳纳米管[19]、煤[20]等作为前驱体,通过化学氧化、电化学氧化、激光烧蚀等方法将其刻蚀、剥离后得到碳点[21]。为提高其QY,通常需要对其进行表面钝化。然而,即使经过细致的粒子分级,依然很难得到荧光峰FWHM<50 nm 的高色纯度碳点。“自下而上法”以小分子如酸[22]、醇[23]、酚类[24]、胺[25]、染料[26]等,聚合物如聚乙二醇[27]等,生物质如树叶、种子、水果等[28-29]为原料,通过溶剂热、水热、微波法等途径合成碳点。大量文献表明,高色纯度碳点通常由“自下而上法”制备,即使用特定结构的有机小分子和新鲜的植物叶子等作为碳前驱体,通过水热、溶剂热、微波、中温加热和硫酸碳化法等合成(如表1[11-12,30-50]所示)。为获得色纯度好的目标碳点,通常需要使用柱色谱分离技术、萃取、透析等过程对其进行分离纯化,产物收率相对较低。
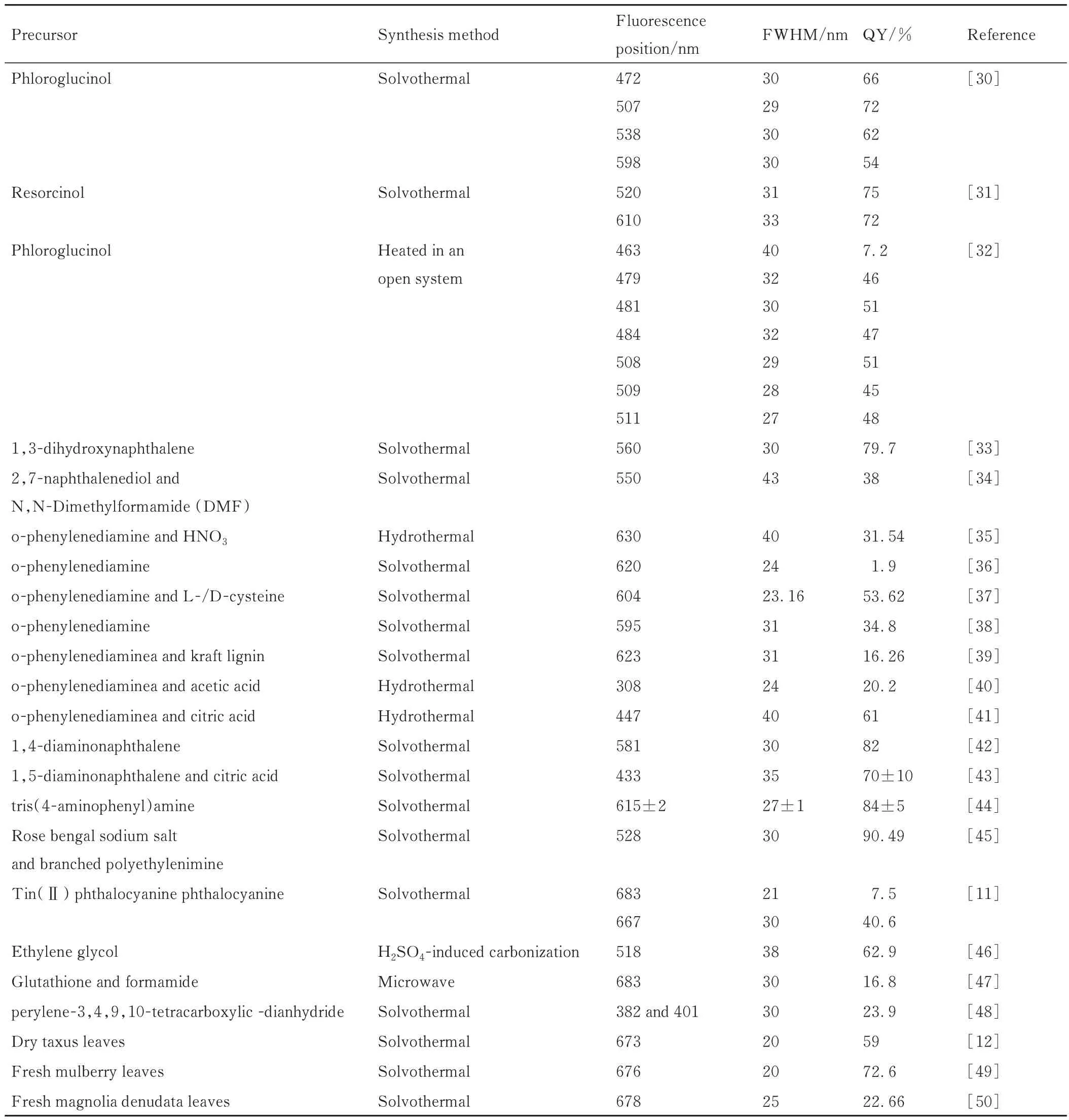
表1 合成高色纯度碳点所用的前驱体、合成方法以及光谱特性Table 1 Precursor,synthesis method and spectral properties of high-color-purity carbon dots
2 影响高色纯度碳点发光性能的因素
广泛的研究表明,前驱体的种类、反应参数(如反应介质、温度以及时间等)、表面官能团结构变化和溶剂化效应等会对高色纯度碳点的结构产生影响,进而改变其发光位置、QY 和FWHM。
2.1 前驱体
高色纯度碳点的合成,通常以芳香化合物如酚、芳胺、有机染料等小分子和生物质如植物叶片等为前驱体,通过溶剂热、水热、微波等过程得到碳点混合物,再结合透析、萃取、柱层析等复杂过程得到目标产物,因此,碳点收率通常较低。
2.1.1 有机小分子
间苯三酚、间苯二酚、萘二酚等酚类小分子是合成高色纯度碳点最常用的前驱体之一。可通过反应参数,如反应温度、时间和介质变化实现发光颜色从蓝色到红色的调制。2018 年,Yuan 等[30]以间苯三酚为前驱体,使用溶剂热法结合柱色谱分离技术得到FWHM 为30 nm左右、发光位置分别在472,507,538 nm和598 nm、QY 超过50%的荧光碳点。此后,该课题组[31]以间苯二酚为前驱体,采用类似的合成方法制备了发光位置在520 nm 和610 nm、FWHM 略大于30 nm、QY 超过70%的绿色和红色荧光碳点。Yoshinaga 等[32]在高沸点溶剂中敞口加热间苯三酚得到了发光峰FWHM 为30 nm 左右的蓝色和绿色荧光碳点,但其QY 明显低于Yuan 等使用溶剂热法合成的碳点。除单环芳烃外,多环芳烃如萘二酚也可用于合成窄带发光的荧光碳点。Kwak 等[33]在硫酸-乙醇介质中热处理1,3-萘二酚2 h,结合柱色谱分离过程得到了QY高达79.7%、FWHM 为30 nm 的黄色荧光碳点。将该碳点固定在SiO2基底上,可以得到发光峰FWHM<40 nm 的碳点固体粉末。He 等[34]将N,N-二甲基甲酰胺(DMF)和2,7-萘二酚溶解在乙醇中,通过高温高压反应得到粗产物。透析粗产物得到了分别在450 nm和550 nm 处有蓝色和黄色发光的双发射碳点,其中黄色碳点的FWHM 为43 nm。上述研究表明,羟基芳香化合物作为前驱体时,可以通过反应参数优化实现碳点发光位置调制。
芳胺也可用于高色纯度碳点的合成,得到的主要是在长波长区域发光的荧光碳点,但QY 较酚基碳点偏低。例如,Liu 等[35]以邻苯二胺(o-PD)作为前驱体、水为介质,在适量硝酸存在下,通过溶剂热过程合成了发光位置在630 nm、FWHM 为40 nm 的红色荧光碳点。Zhang 等[36]在NaSO4存在下,水热处理o-PD 得到黄色荧光碳点。将该碳点质子化后,荧光峰的FWHM从70 nm 降到24 nm,发光位置从550 nm 红移至620 nm。Ru 等[37]在硫酸-乙醇介质中以o-PD 和色胺酸为混合前驱体,通过溶剂热法合成了荧光峰位于602 nm、FWHM 为23 nm 的红色荧光碳点。Zhang等[38]在氯仿介质中溶剂热处理o-PD,得到多色荧光碳点混合物。经柱色谱分离后得到了FWHM 为31 nm、发光位置595 nm 的橙红色荧光碳点。
除o-PD 外,萘二胺、三(4-氨基苯基)胺等也可作为碳源,合成高色纯度的碳点。Han 等[42]柱色谱分离1,4-萘二胺在乙醇介质中的溶剂热产物,得到了FWHM 为30 nm,QY 高达82% 的橙色荧光碳点。Yuan 等[43]以1,5-萘二胺和柠檬酸作为共同前驱体,采用溶剂热法合成了表面有丰富含氧官能团和氨基官能团的碳点。将其在氨水-肼-乙醇溶液中进行表面氨基化后,得到了QY 超过70%,FWHM 为35 nm 深蓝色荧光碳点。Liu 等[44]在叔丁基过氧化氢和HCl 存在下,溶剂热处理乙醇介质中的三(4-氨基苯基)胺,得到了QY 为84%,FWHM 只有27 nm 的红色荧光碳点。研究发现,产物的QY 和FWHM 与前驱体结构密切相关;使用对苯二胺作为前驱体时仅能得到FWHM 为48 nm 的红色荧光碳点。
提高有机分子的共平面性、分子刚性和共轭程度是获得窄带宽发光材料的有效途径之一。基于这一原理,一些含有平面共轭结构的有机分子如有机染料也被用于合成高色纯度碳点。所得碳点的发光位置和FWHM 与原料存在关联。Tong 等[45]使用商品化有机染料孟加拉玫瑰红作为前驱体,合成了FWHM约为30 nm 的绿色荧光碳点。考虑到碳点发光位置和FWHM 与染料本身非常接近,因此认为,碳点的高色纯度发光与前驱体结构密切相关。酞菁是一种分子结构高度共轭的平面分子。Wang 等[11]在DMF 溶剂中溶剂热处理酞菁和锡酞菁染料后,得到了FWHM分别为30 nm 和21 nm、发光峰分别为667 nm 和683 nm、QY 分别为40.7%和7.5%的红色荧光碳点。
除芳香分子外,其他有机小分子,如乙二醇、谷胱甘肽等也可作为前驱体合成高色纯度碳点。本课题组以乙二醇作为前驱体,通过硫酸炭化法合成了FWHM 为38 nm、QY 为63% 的绿色荧光碳点[46]。Pan 等[47]于160 ℃微波热处理谷胱甘肽的甲酰胺溶液,获得了FWHM 为30 nm,QY 为16.8%的近红外荧光碳点。Wang 等[48]以苝-3,4,9,10-四羧酸二酐为前驱体,通过溶剂热法合成了发光峰位于400 nm、QY 为23.9%、FWHM 为30 nm 的高色纯度紫光碳点。
2.1.2 生物质
常规发光碳点合成,可以使用包括动物植物组织[51-53]、果实[54-55]、食物[56-57]、牛奶[58]、果壳[59-60]、指甲[61]等组成和形态各异的生物质前驱体。与之不同,高色纯度碳点的合成,使用的主要是新鲜的植物叶片,得到的是发光处于红外以及近红外区域的荧光碳点。例如,Yang 课题组[12]将干燥的红豆杉叶子研磨成粉后作为碳源,120 ℃溶剂热处理5 h,结合柱色谱分离技术,制备了FWHM 为20 nm 的深红色荧光碳点。Liu等[49]用乙醇萃取新鲜的桑叶,150 ℃热处理萃取液得到的碳点,其FWHM 和发光峰位置与Yuan 等得到的碳点类似。406 nm 激发时,该碳点在乙醇溶液中的QY 高达72.6%。Qu 等[50]将新鲜玉兰叶子清洗干净并在50 ℃干燥12 h,然后将其粉碎后溶解在丙酮溶剂中合成了发光位置在678 nm 的荧光碳点(NMRCDs),它的FWHM 为25 nm。
2.2 合成参数
在碳点的合成过程中,即使使用的前驱体相同,如果反应介质、温度以及时间不同,所得碳点的碳核或表面官能团也可能存在差异。以o-PD 为例,溶剂热或水热过程中使用的溶剂组成和反应时间的变化将带来碳点光谱性能的显著差异。Liu 等[35]的研究发现,使用硝酸水溶液作为溶剂时合成的红色荧光碳点(CPDs-50),其荧光峰位于630 nm,FWHM 仅有40 nm。而在磷酸、硫酸存在下,则难以得到高色纯度碳点。使用HCl,NaNO3代替硝酸时,得到的碳点CPDs-H 和CPDs-N,前者仅能发出微弱的红色荧光;后者的最佳发射则在581 nm。这说明,H+和在CPDs-50 的形成过程中起着关键作用。Xu 等[40]在o-PD 水溶液中加入醋酸作为共同前驱体,通过水热过程合成的碳点粉末(UVB-CDs),它的荧光峰位于深紫外区(308 nm),FWHM 仅有24 nm。与之相比,不加醋酸时得到的产物发光峰位于600 nm。依据结构表征结果,他们将UVB-CDs 的超窄固态发光归因于醋酸引入后sp2共轭单元减小和sp3间隔区域的形成。Zhang等[38]使用三氯甲烷作为溶剂,o-PD 作为前驱体,160 ℃溶剂热处理10 h,结合柱色谱分离技术得到了发光峰位于595 nm、FWHM 为31 nm 的橙红色荧光碳点。结合结构表征,将橙红色超窄发光归因于氯原子和石墨化碳核间的p-π 共轭以及共轭氮原子含量的增加。Ru 等[37]的研究发现,使用o-PD 和色氨酸作为共同碳源,HCl/乙醇、水和硫酸/乙醇作为溶剂,160 ℃溶剂热处理7 h,得到了发光颜色分别为蓝色(B-)、黄色(Y-)和红色(R-)的三种圆偏振发光荧光碳点(R-LCPD)(如图1 所示)。但只有红色荧光碳点(604 nm)的FWHM 为23.16 nm。结构表征表明碳点表面存在丰富的含氧/含氮官能团;随着sp2碳共轭结构和粒径增加,发光位置逐渐红移。
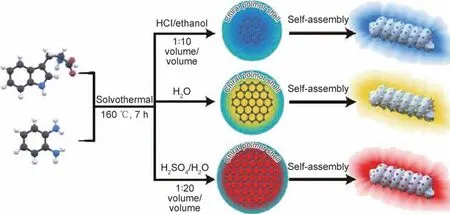
图1 具有全色圆偏振发光的多色发光手性碳化聚合物点的制备过程示意图[37]Fig.1 Schematic of preparation procedure for multicolor-emitting chiral carbonized polymer dots with full-color circularly polarized luminescence[37]
酚也是一种合成高色纯度碳点的重要前驱体。Yuan 等[30]的研究发现,以间苯三酚为碳源,乙醇为溶剂,200 ℃下溶剂热反应9 h 和24 h 获得的粗产物,通过硅胶色谱柱分离纯化后,得到了形貌为三角形,尺寸分别为1.9 nm 和2.4 nm 的高结晶度蓝色(472 nm)和绿色(507 nm)荧光碳点。它们的FWHM 分别为30 nm 和29 nm,QY 分别为66%和72%。向体系中加入硫酸后,同样的温度分别反应2 h 和5 h,得到的则是尺寸分别为3.0 nm 和3.9 nm 的黄色(538 nm)和红色(598 nm)荧光碳点。它们的FWHM 都是30 nm,QY分别为62%和54%。XPS,FT-IR,NMR 以及密度泛函理论(DFT)计算表明,碳点独特的刚性三角结构所带来的电子-声子弱相互作用是该系列碳点获得高色纯度的关键;碳点尺寸增加则是发光位置红移的主要原因。此后,该课题组[31]采用相同的反应温度溶剂热处理间苯二酚4 h 和7 h 后得到了FWHM 分别为31 nm 和33 nm、QY 分别为75%和72%的绿色(520 nm)和红色(610 nm)荧光碳点。反应时间不同导致前驱体脱水炭化程度差异,得到了尺寸分别为2.5 nm 和4.4 nm 的高结晶度三角形碳点。DFT 理论计算表明,与间苯三酚相比,受益于较低的反应势垒,间苯二酚更容易形成尺寸较大的三角形碳点,进而实现长波方向的高色纯度发光。
Liu 等[46]发现,将乙二醇硫酸炭化温度从140 ℃降到80 ℃时,所获碳点荧光峰的FWHM 从59 nm 降到了38 nm,发光位置从蓝光区域红移到了绿光区域。时间分辨荧光衰减过程考察表明,与蓝色荧光碳点(双指数衰减)相比,绿色荧光碳点的衰减曲线符合单指数方程;且在不同荧光位置的荧光寿命几乎没有变化。这说明,在该种碳点上很可能只存在一种微环境相同的发光中心;激子仅能通过一种辐射衰减模式复合,因此,绿色荧光碳点的FWHM 只有38 nm,呈现窄带发光。
2.3 表面官能团结构变化和溶剂化效应
碳点表面官能团结构以及介质的溶剂化效应、pH值变化等也会影响碳点的光物理行为,进而实现窄带宽的高色纯度发光。Zhang 等[36]的研究发现,水热处理o-PD 得到的黄色荧光碳点的发光性能与2,3-二胺基吩嗪的分子态发光类似。使用硫酸对其进行处理后,碳点表面的胺基官能团发生质子化,伴随荧光峰峰位的显著红移(550 nm→620 nm)。更为重要的是,FWHM 从70 nm 降到了24 nm。2,3-二胺基吩嗪发色团的质子化及其与碳点之间的相互作用,是碳点发光峰红移和色纯度显著提升的主要原因。Yuan 等[43]以1,5-萘二胺和柠檬酸作为共同前驱体,通过溶剂热法合成的碳点,其表面存在丰富的含氧官能团和胺基官能团。使用氨水-肼-乙醇溶液对其处理后,碳点表面的含氧官能团消失,发深蓝色光,色纯度得到明显提高,FWHM 从大于80 nm 降到了35 nm。结合理论计算,他们提出消除碳点表面的含氧官能团更有利于获得窄带宽的发光。
溶剂也会对碳点的荧光色纯度和位置产生一定影响。Yoshinaga 等[32]的研究发现,使用间苯三酚作为碳源合成的碳点,其荧光峰的FWHM 随着溶剂极性的增加,从27 nm 增大到了40 nm;发光位置从511 nm 蓝移到了463 nm。这可能与碳点在不同溶剂中的溶剂化效应所带来的碳点表面态和粒子分散性差异等有关。从以上研究可以看出,要获得碳点在特定波长的高色纯度发光,除关注前驱体、反应参数等带来的碳点尺寸、核和官能团结构等的变化外,还需对碳点与溶剂的相互作用,以及随之而来的结构变化予以考量。
3 高色纯度碳点的应用
与目前发展的高色纯度荧光材料,如Ⅱ-Ⅵ族、Ⅲ-Ⅴ族半导体量子点、卤化物钙钛矿纳米晶体CsPbX3(X=Cl,Br 和I)等相比,碳点不含有毒的重金属离子,如镉离子、铅离子等,因此具有环境友好、生物危害小的优点。与稀土发光材料相比,碳点还具有原料来源广泛、成本低的优点,因此在广色域超高清显示器、超分辨成像和传感以及防伪等领域具有广泛用途。
3.1 LED 器件
国际电信联盟(International Telecommunication Union,ITU)发布的“ITU-R 推荐标准BT.2020”(Rec.2020,Recommendation BT 2020)提出,下一代超高清显示器对背光源的色纯度提出了更高要求(FWHM≤20 nm)。常规碳点较低的发光色纯度(FWHM>60 nm)难以满足此要求。从表1 可以看出,高色纯度碳点的FWHM 在20~40 nm。以其作为发光材料更有可能获得色纯度和色彩还原度更好的LED 器件。
以高色纯度碳点作为发光单元,构筑LED 器件主要基于两种原理。一是作为光致发光材料在商品化的蓝色或紫色LED 基底上制备光致发光层,实现高质量的单色和白光发光;二是作为电致发光单元直接构筑单色和白色LED 器件。
北京师范大学的范楼珍教授课题组在这方面做出了引领性的工作。Yuan 等[31]使用透明聚丙烯酸甲酯(PMMA)作为膜材料、高色纯度红色和绿色荧光碳点作为发光单元,在蓝光LED 基底上构筑了红色和绿色碳点薄膜,得到白光LED。器件的显色范围高达110% 的国家电视委员会(National Television Systems Committee,NTSC)色域标准,足以与高色纯度的钙钛矿量子点LED 和半导体LED 器件的性能相媲美。在20 mA 电流驱动下,器件的色坐标为(0.35,0.33),流明效率为86.5 lm·W-1,显色指数(color rendering indexes,CRI)为56.9,且具有很好的器件稳定性。Yoshinaga 等[32]将FWHM 分别为33 nm 和35 nm的碳点作为发光单元,聚乙烯醇(PVA)和聚乙烯吡咯烷酮(PVP)作为膜材料,在紫外LED 基底上构筑了一层碳点基薄膜,得到了高色纯度的单色LED 器件。与碳点在溶液中的荧光相比,器件的发光峰仅略有展宽。
高色纯度碳点也可作为发光单元构筑电致发光层,实现LED 器件的高色纯度单色和白光发光。例如,Yuan 等[30]将制备的高色纯度的蓝色、绿色、黄色和红色碳点分别与聚(N-乙烯基咔唑)(PVK)混合作为电致发光层,构筑的蓝光、绿光、黄光和红光LED,发光峰FWHM 分别为30,32,38 nm 和39 nm,实现了器件的高色纯度和高效单色发光。Yuan 等[43]使用高色纯度深蓝色荧光碳点作为发光单元,PVK 作为主体材料构筑了深蓝色LED 器件。该器件的色坐标为(0.15,0.05),与Rec.2020 标准中的深蓝坐标(0.131,0.046)非常接近;最大亮度高达5240 cd·m-2,最大外量子效率(external quantum efficiency,EQE)为4%,超过之前报道的镉基/铅基深蓝色LED 器件。苏州大学康振辉教授课题组[48]使用高色纯度紫光碳点作为发光单元,PVK 作为主体材料构筑的紫光LED 器件,中心波长位于408 nm,最大亮度为1.63 cd·m-2,EQE 为0.831%,较传统钙钛矿量子点基LED 的EQE 更大(0.31%)。此外,它具有0.62 cd·A-1的高电流效率,稳定的寿命(T50≈50 h)以及3.7 V 的低开启电压,为碳点在紫光LED 领域的应用开辟了新的途径。
3.2 超分辨成像和传感
高色纯度碳点还可以应用到传感方面以实现常规碳点不能实现的应用如超分辨传感以及离子和分子的检测等。Wang 等[11]制备了FWHM 分别为21 nm和30 nm 的两种近红外发射碳点,将其分别命名为GQDs-Sn 和GQDs-OH。它们的发光位置分别为683 nm 和667 nm;在不同激发波长下具有不同荧光寿命。根据不同类型GQDs 获取光谱信息,依据时间“签名”特征进行超分辨率处理。在不使用光谱仪的情况下,成功将其应用于超分辨光谱和空间传感。研究发现,GQDs-Sn的定位误差约为1个像素(10 nm),GQDs-OH的定位误差约为3 个像素(30 nm)。Qu 等[50]将以玉兰叶为前驱体合成的高色纯度近红外碳点(NIR-CDs)与两亲性表面活性剂F-127 自组装制备水溶性胶束纳米探针,可以实现水样和细胞中重金属Pb2+的选择性检测。该探针细胞毒性很小,检测原理基于纳米探针与Pd2+之间形成相当稳定的络合物后导致的碳点荧光猝灭效应。
3.3 生物染色剂
碳点尤其是以新鲜植物叶子作为前驱体合成的红外和近红外高色纯度荧光碳点具有毒性低、生物相容性好、生物组织穿透深度大和可有效避免背底荧光干扰等优点[62-63],因此在生命科学、药学和医疗诊断等领域有着非常广泛的应用前景。吉林大学杨柏教授课题组[35]的工作具有代表性,以o-PD 为前驱体合成高色纯度红色荧光碳点(CPDs-50),并成功应用于生物活体组织的实时成像。研究发现,该碳点可通过血液循环方式进入生物体内;碳点及其代谢产物可通过肾脏系统和肝胆系统排出体外。随后,该课题组[12]还发现,使用红豆杉叶子为前驱体合成的深红色荧光碳点,其FWHM 仅有20 nm,可用于老鼠内深层组织的单光子和双光子荧光成像。复旦大学的熊焕明教授课题组[49]使用桑叶作为前驱体合成的红色荧光碳点喂蚕,得到了可以发出明亮红色荧光的蚕茧。除上述应用外,高色纯度碳点还可用作荧光墨水,用于防伪标签制作[33]。
4 结束语
得益于窄带宽的高色纯度发光特性和优异的光学和化学稳定性,高色纯度碳点在超高清显示和照明、超分辨成像和传感、生物成像以及防伪等众多领域具有广泛用途。尽管目前已经在高色纯度碳点制备和应用方面取得了一定进展,但仍存在一些亟待解决的问题:
(1)在合成方面,与常规碳点相比较,高色纯度碳点制备过程复杂、种类少、产量小。合成时使用的前驱体主要是芳香化合物和植物叶片等,得到的主要是长波方向发光的碳点,短波长方向的紫色、蓝色、绿色高色纯度荧光碳点则相对缺乏。合成方法主要是溶剂热/水热法。为获得高色纯度碳点通常需要使用柱色谱分离技术、透析等方法进行后续的分离和提纯,过程复杂、繁琐,难以实现目标碳点的规模制备,因此,需要发展更为简单的方法,在使用更加绿色、廉价前驱体的基础上,实现不同颜色高色纯度碳点的规模制备。
(2)碳点光谱性能需进一步提升。Rec.2020 标准提出,下一代高清显示器的色纯度要求FWHM≤20 nm,使用红、绿和蓝三原色的色坐标,这对发光材料的性能提出了更高要求。目前报道的高色纯度碳点的性能与此存在着明显差距,因此需要进一步优化碳点的分离与纯化技术,在准确表征碳点结构的基础上,结合理论计算和模拟,揭示高色纯度碳点的发光机制、发光位置和FWHM 与结构的关联关系,实现碳点发光位置的调制和色纯度、QY 的提升。
(3)与常规碳点相比,高色纯度碳点的应用还非常有限。基于其优越的光谱特性,发展高色纯度碳点的新应用领域和提高其应用性能也是该领域的重要发展方向。
