超声移液及微量移液技术进展和展望
2023-11-21张志强张扬邱维宝郑海荣
张志强,张扬,2,邱维宝,郑海荣
(1 中国科学院深圳先进技术研究院,保罗·C·劳特伯生物医学成像研究中心,广东 深圳 518055; 2 南华大学电气工程学院,湖南 衡阳 421001)
微量移液是生物学、化学、医学等领域中科学研究和生产检测的重要环节,是实验过程的基础操作内容[1-2]。微量移液的精准度对科研成果的发现、检测结果的准确性、产品性能稳定性起着至关重要的作用。基于活塞式原理的手持移液器移液精度最高能达到亚微升级,是传统研究工作中常用的精密微量移液工具。但是,移液是重复且烦琐的工作,人工使用移液器进行移液易造成人为因素误差,且易出现漏加液体、遗忘润洗等问题,不仅给工作人员带来很大工作负担,还会导致实验误差和效率低下。
随着现代生物技术的快速发展,特别是近年来蓬勃发展的合成生物学、新药研究以及新冠疫情催化的体外诊断等技术[3-12],经常需要流程化处理大量液体样本,同时单个样本液体含量却逐渐减少,因此对移液技术的通量、精准度和时效性有着越来越高的要求。虽然电动移液器以及基于电磁阀、压电驱动的移液技术在一定程度上解决了人工操作的高负荷以及实验误差问题,并提高了移液精度[13-23],但是这些技术的移液通量没有大幅度提高,仍然难以满足大量样本的流程化处理。基于电场、磁场、光的新型移液技术可以大幅度提高移液精度,但是应用场景局限性大,通用性差,通量也不高[24-28]。发展一种机械化、全自动化、高通量移液方式的迫切需求使得自动化移液工作站应运而生。基于多通道移液模块的自动化移液工作站由于具有定量精准、自动化程度高、摆脱人工操作、可实现高通量等优势,成为了当前主流的移液操作范式[2,13,29-30]。但是,不管是基于活塞式原理的移液器,还是基于电磁阀、压电驱动、电场、磁场和光的各种移液技术,都需要利用吸头、毛细管、喷嘴等移液头进行移液,移液头需要与液体直接接触,存在样品残留和交叉污染的风险,样品损耗量也大,并且在高精度移液中,吸头、毛细管、喷嘴等移液头孔径很小,存在容易堵塞的问题。另外,移液头大都是一次性耗材,大量使用成本高且污染环境。
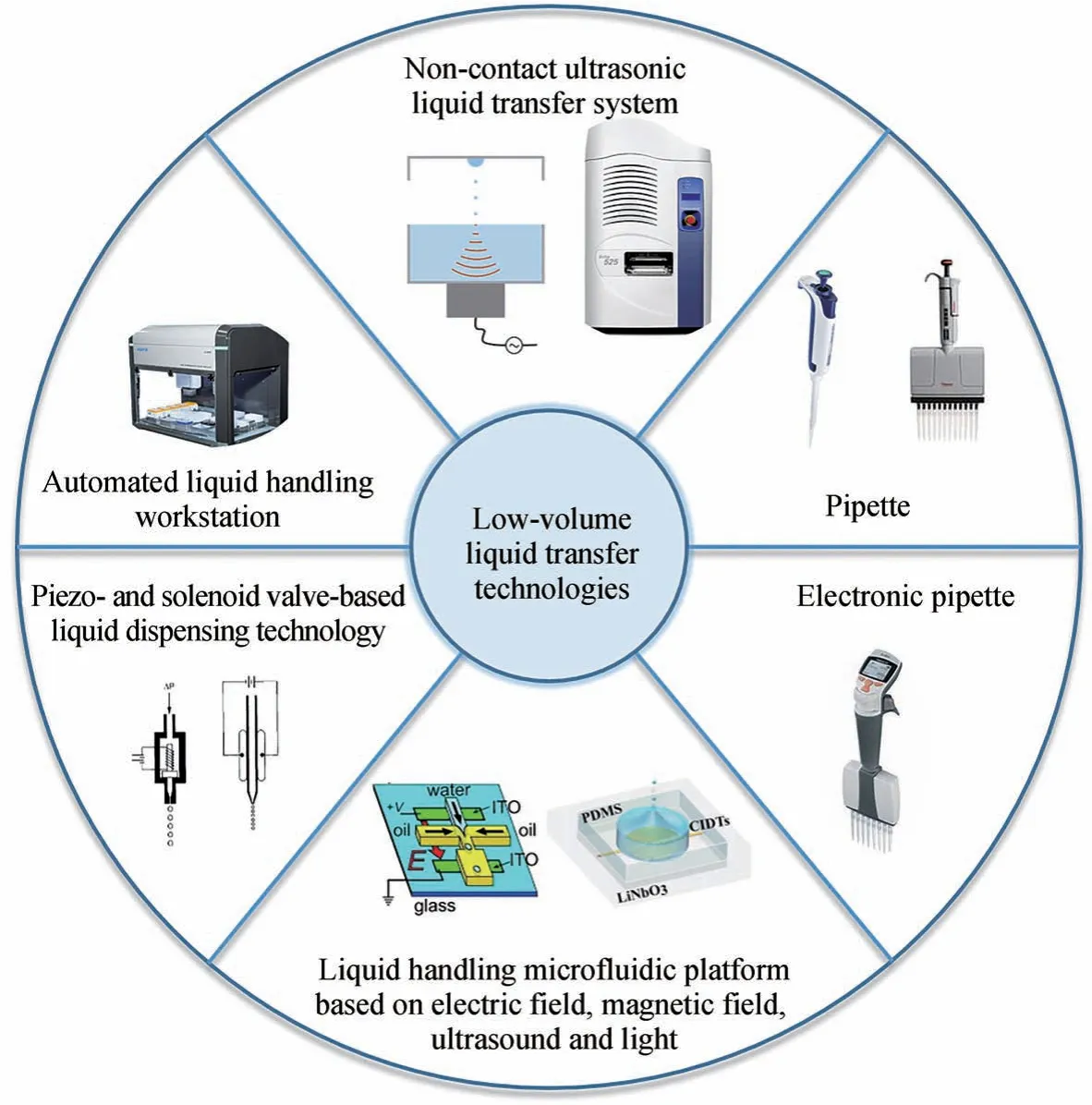
近年来利用聚焦超声波的非接触式移液技术引起了人们的极大关注[31]。非接触式超声移液技术利用超声波直接将液滴从母液容器中喷射到目标容器,无需移液头辅助,液滴在转移过程中不会与任何其他媒介接触,具有无液体黏附及残留、无交叉污染、降低耗材费用、移液速度快的特点,同时具有纳升级以上超高移液精度、节约试剂成本、可保持生物大分子的生物活性等优势,应用前景十分广阔。当前非接触式超声移液技术已经受到诸如合成生物学、药物发现、化合物管理、基因组学、蛋白质组学等应用领域的青睐,得到了业界认可[32-40]。移液过程包括吸液和放液两个过程。传统定义中使用外力将液滴喷射到目标容器,移液头不与目标容器接触的移液技术称为非接触式移液。这种定义主要基于放液过程,没有考虑吸液过程。相比于非接触式超声移液技术(液滴在整个移液过程中不与容器之外的任何媒介接触),基于活塞式原理、压电驱动原理等需要吸头、毛细管、喷嘴等移液头的移液技术仍然属于接触式移液,在移液过程中液体会与移液头直接接触,存在样品残留、交叉污染、堵塞的风险。本文将系统介绍微量移液技术的发展(图1)及现状,重点介绍非接触式超声移液技术的发展及现状,并对微量移液技术未来发展及趋势进行展望。

图1 微量移液技术发展进程Fig. 1 Development process of low-volume liquid transfer technology
1 接触式微量移液技术
1.1 移液器
移液器是实验室定量移取微量液体的常用仪器,可实现精准的微量液体转移。但是在最初的生物化学实验中,实验人员需要用嘴将液体吸入细玻璃管中进行移液,这种方法不仅会危及实验人员人身安全,而且由于精度不高、重复再现性能差,在处理量小的液体样本时异常困难。后来使用的无需口腔辅助的滴管和移液管也主要用于精度要求不高的移液。为了解决这个问题,1957年德国马尔堡大学生理化学研究所Schnitger设计了世界上第一支微量移液器,使可重复再现、精确可靠的微升级移液成为可能[41]。它是基于气体活塞原理,在活塞的推动下,移液器排出部分空气,利用大气压吸入液体,再由活塞推动空气排出液体,从而实现吸液和放液的动作。基于Schnitger的发明,德国Eppendorf公司于1961年推出了世界上第一个商用手动微量移液器。自此之后,移液器彻底改变了科学研究中的液体处理操作方式。
基于气体活塞原理的移液器适用于大多数场景下的移液操作,但是在移液过程中有一段空气存留在系统之中,不适宜吸取黏稠度大的液体和一些挥发性液体,而且移液精度会受到温度和大气压力以及溶液的黏度、挥发性和表面张力的影响[42-43]。因此,人们设计了外置活塞式移液器[44],该移液器中没有空气缓冲,活塞直接与液体接触,消除了温度和大气压力的影响,同时确保了液体特性不会影响准确度,但是活塞与液体直接接触,存在一定量的液体会黏附到移液器内部,而且活塞不能重复使用。随后,基于气体活塞式和外置活塞式技术原理,人们相继发明了多道移液器、可调量程移液器、电动移液器等新型技术,使得移液器在移液精度、移液效率和使用灵活性等方面得到了很大的提升,进一步提高了移液操作的效率和可靠性,同时减轻了实验人员操作负担和伤害风险[18,45-53]。
过去半个世纪,移液器的不断发展给生物、医学、化学等领域和行业给予了极大的支持,能够解决大部分研究中的问题。但是利用移液器的人工移液过程由于受环境条件和人为操作影响,其移液精度和准确度局限于亚微升级,无法在纳升级范围内继续传承下去。另外,利用移液器的手动或半自动移液操作依赖于人工的反复劳动,当样本量大幅度增长时,不仅耗费大量的人力,也会耗费很长的时间。
1.2 自动化移液工作站
随着现代生物化学技术的快速发展和临床诊断需求的提高,高通量分析是现代科学的趋势[54-58]。对于在化合物检测和药物筛选等领域进行大规模实验,以及类似新冠疫情等大规模传染病临床诊断和人群筛查,每天在实验室中分析数千甚至上万个样本都是可能的。而在新兴的合成生物学研究中,海量的工程化试错实验所需的样本数量也是远远超出依赖人工的研究范式能力范畴[59]。传统利用移液器进行手动或者半自动的人工移液操作成为了快速高精度样品处理的瓶颈,难以满足科学研究以及市场的需求。因此,液体处理的全自动化操作代替烦琐的人工劳动,已成为生物、医疗、制药等领域高通量样本处理的趋势[1-2,60]。而且通过自动化移液减小环境影响和人为操作误差是进一步提高移液精度、准确度和重复性的一种有效解决方案[29]。
自动化移液工作站是精密微量移液技术与工业自动化控制技术相结合的产物,是现代生物技术中完成高通量实验过程的必备工具之一。它是将移液器、机械臂、容器、耗材等组件集成在一个自动化的工作平台上,通过软件控制实现全自动化批量移液处理,以实现高通量移液处理的各种应用需求。自动化移液工作站的发展要追溯到20世纪80年代,电机和微处理器技术的发展实现了对马达和阀门功能序列进行编程,从而促进了全自动化移液工作站的发展。后来随着自动化移液工作站技术不断突破,其功能越来越完善和多样化,在生命科学、药物筛选、分子诊断以及临床检测等领域已经得到了广泛的应用[61-63]。由于传统活塞式移液器结构相对简单,到目前为止市场上自动化移液工作站产品大部分是基于活塞式移液技术(图2)。比如,德国Eppendorf公司自动化移液工作站EpMotion系列和瑞士Hamilton公司自动移液工作站Microlab STAR是基于气体活塞移液技术,可以实现200 nL至1 mL的移液量范围,有效简化实验室工作流程,在许多临床研究中心和药物研究中心有着广泛应用。美国Beckman Culter公司自动化移液工作站Biomek i7则是基于活塞原理的液体置换式移液技术,提供移液范围覆盖500 nL~5 mL,可配备96/384多通道移液器和灵活8通道移液器的多个单臂和双臂装置。瑞士Tecan公司生产的Freedom EVO和Fluent系列自动移液工作站允许在同一个工作站上同时使用基于活塞原理的空气置换和液体置换式移液技术,移液范围从500 nL至5 mL,并配备单通道、双通道、四通道和八通道液体处理臂,和高密度的96/384多通道移液臂。每个液体通道都可单独针对液体的类型与体积的变化设置优化的移液参数。

图2 商业自动化移液工作站Fig. 2 Commercial automated liquid handling workstations
相比于手动或半自动移液器,自动化移液工作站大大提高了移液操作的效率和重复性。当前自动化移液工作站以速度快、精准度高、智能化程度高、容量大、持续工作时间长等特性,得到了全世界相关领域公司、医院和实验室的青睐,成为了高通量移液的主流操作范式[64-69]。但是自动化移液工作站所采用的微量移液技术仍然是基于移液头的接触式移液技术,存在样品残留、交叉污染、堵塞等问题。另外,基于活塞式移液技术的自动化移液工作站移液精度仍然受到限制,局限于亚微升级别,难以突破到纳升级。
1.3 高精度移液技术
由于基于活塞原理的移液技术精度局限于亚微升级,人们一直在寻求更高精度的移液原理和技术。而且随着现代生物技术处理的单个样本中样品含量逐渐减少,人们对纳升级或皮升级等更高精度的新型移液技术有着迫切需求。
20世纪80年代左右,人们开始将喷墨点胶技术引入到移液技术中[14-17]。在喷墨点胶技术中,常利用电磁阀和压电驱动挤压通过毛细管的液体产生并喷射出纳升级甚至皮升级的液滴[图3(a)]。由于高的液滴精度、易于自动化、可以保持良好的生物样品活性等特点,基于电磁阀和压电驱动的自动化移液技术很快得到了人们的青睐,并在药物发现、基因组学、组合化学等领域被广泛应用和研究[14-15,30,62,70-72]。1999年,Ted A. Bateman等[30]对比分析了美国Cartesian technologies公司基于电磁阀的PixSys系统和美国Packard BioScience公司基于压电驱动的BioChip系统在高通量筛选领域的应用。基于电磁阀的PixSys系统移液精度范围可达100 nL~10 μL,基于压电驱动的BioChip系统移液精度范围能达到10~100 nL,但是BioChip系统所用毛细管内径69 μm,容易堵塞。在100 nL移液精度时,两种技术的变异系数(coefficient of variation,CV)都在20%以上。另外,相比于传统活塞式移液技术,两种技术在正式移液之前都需要预实验校准,严重影响移液速度,而且两种移液技术中移液头都需要清洗,浪费的液体量较多,样品交叉污染的风险大。后来,随着微机电系统(MEMS)的发展,基于精密电磁阀及压电驱动的移液技术在移液精度和精准性方面有了很大提升。比如,目前BioChip系统可以实现350 pL的移液精度,且CV小于5%。另外,德国BioFluidix公司研发了基于压电驱动的PipeJet TM技术,当前有纳升级分液器和皮升级分液器产品,分别可以实现纳升级(2~70 nL)和皮升级(50~250 pL)的单液滴分配,实现CV在3%以内的高精度微量液体移液。美国BioDot公司基于压电驱动的BioJet Ultra TM技术可产生100 pL~1.0 nL的单个动态液滴体积范围,CV通常小于5%。另外,基于压电驱动的移液技术将毛细管等分配单元与压电驱动的执行器分开,毛细管等分配单元作为一次性使用耗材,可以大幅度提高移液速度,并减小样品交叉污染的风险。
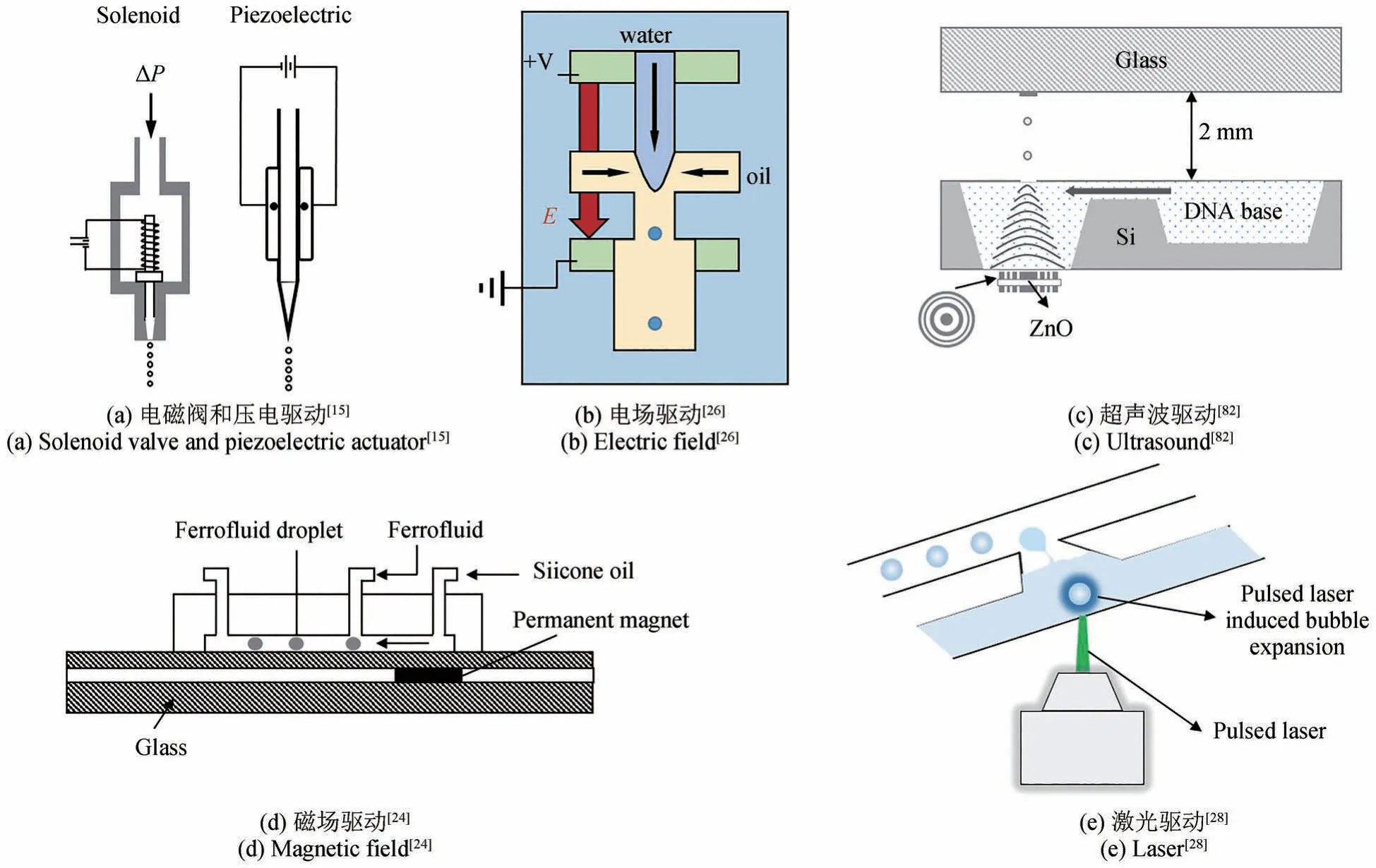
图3 基于不同驱动力的液滴生成技术示意图Fig. 3 Schematic diagrams of droplet ejection based on different driving force
除了比较成熟的基于电磁阀和压电驱动的喷墨点胶技术之外,早期人们研究的基于电场的静电喷射技术和基于超声波的液滴喷射技术也可以用于高精度移液。比如,1952年,Vonnegut等[73-74]基于静电喷射技术实现了皮升级液滴的喷射,并在19世纪60年代用于喷墨点胶技术。1981年,Lovelady等[75]提出了利用聚焦超声波将液滴从液面喷出用于喷墨打印。但是两种技术在当时还不够成熟,没有用于高精度移液。随着微机械加工技术的发展和微流控技术的广泛应用[76-79],基于电场和超声的高精度液滴生成技术在微流控领域得到了广泛应用和研究。例如,2006年哈佛大学Link等[26]提出了一种基于液滴静电荷和外部电场控制皮升级液滴生成的微流控平台技术 [图3(b)]。直流电场和交变电场都可以应用在微流控装置上生成液滴[80-81]。2006年,Kwon等[82]将聚焦超声波喷射液滴的方法应用于皮升级DNA液滴的移取[图3(c)]。除了电场和超声之外,磁场和光也可应用于微流控平台的高精度液滴生成。2010年,Tan等[24]利用圆形永磁体在T型结微流控装置中操纵纳升级磁流体液滴的形成,并报道了附加磁力会引起液滴尺寸的变化 [图3(d)]。2004年,Deshpande等[27]利用光驱动微机械加工的硅薄膜振动实现皮升级液滴的喷出。2011年,Park等[28]在微流控平台上利用脉冲激光产生液滴,液滴体积在1~150 pL范围内连续可调 [图3(e)]。基于电、磁、声、光的液滴生成技术由于具有高的移液精度,实现对液滴的精细操控被广泛研究[24-28,83-87]。这些技术的实现主要基于微机械加工平台,适用于微流控领域应用,可以大幅度降低成本,提高样品处理通量,但是通用性不佳,而且液体与平台直接接触,存在平台清洗、样品交叉污染等问题。另外,除了超声移液技术之外,其他移液技术都需要毛细管、喷嘴等进行辅助,进一步增加了堵塞、交叉污染等风险。
2 非接触式超声移液技术
基于吸头、毛细管、喷嘴等移液头的移液技术,在移液过程中液体会与移液头直接接触,是接触式的移液方式,存在样品残留、交叉污染以及堵塞的风险。近年来,非接触式超声移液技术由于无需一次性移液头辅助,具有无液体黏附及残留、无交叉污染、无堵塞风险以及可以降低耗材费用等优势,展现了重要的应用前景和商业价值。如图4所示,非接触式超声移液技术是一种声镊技术,利用位于液体容器下方的超声换能器发射聚焦超声波,并利用聚焦超声波的声辐射力将微小尺寸的液滴直接从母板容器液体表面向上喷出,进入到液体上方的目标板容器中,实现高精度微量液体的无接触式操控和转移。该方法中移液液滴尺寸可以通过调节聚焦超声波焦点尺寸和超声能量进行精准控制,无需吸头、毛细管、喷嘴等移液头辅助,液滴在转移过程中不与容器外的其他任何媒介接触,从而实现完全非接触式移液。另外,该方法中超声波可以连续激励,实现液滴的快速连续喷出,从而实现高通量、自动化、精准定量移液。

图4 非接触式超声移液技术[88]Fig. 4 Non-contact ultrasonic liquid transfer technology[88]
早在1902年,Lord Rayleigh[89]就提出了声辐射力的概念和理论计算方法。一般来讲,声辐射力是指传播的声波入射到一个障碍物或界面上时所产生的与声传播方向相同的平均压力。超声移液技术的发展最早要追溯到20世纪80年代研究的基于声辐射力的超声喷射液滴用于喷墨打印的技术。前面提到,1981年美国Lovelady等[75]就提出利用弧面超声换能器发射聚焦超声波,将换能器声场聚焦于液面的微小区域,将液滴从液面喷出,用于喷墨打印。该方法无需喷嘴,可以避免堵塞等问题,但是液滴的大小和喷射方向还不能精准控制。随后施乐帕罗奥多研究中心的Quate等[90]于1987年提出了利用平面超声换能器阵列发射聚焦超声波将液滴从液面喷出,并且可以通过调节发射超声波波束改变液滴喷出的位置和方向。1989年Quate等[91]基于实验和理论仿真研究了利用弧面声透镜聚焦的单阵元换能器发射聚焦超声波从液面喷出液滴的方法,通过控制超声波频率和脉冲长度可以调节喷出液滴的尺寸,实现纳升级和皮升级液滴的喷出,同时基于声辐射力理论分析了聚焦超声波与液面的动量耦合以及随后液滴的形成动力学。当聚焦换能器产生的超声波聚焦于液体表面时,液面处的声辐射力是由声束在液体表面的平均能量密度决定,是声压在脉冲时间上的积分所得,与声场压力成正比。当聚焦超声波的声辐射力能够克服液体表面张力的约束时,流体表面会形成凸起;当声辐射力超过阈值时,液面凸起会变高,且由于瑞利-泰勒不稳定性,液滴会从凸起的顶部喷射出来。但是Quate等的理论分析是基于聚焦超声波与液面相互作用区域是声束的半高宽区域以及作用区域中声辐射力是均匀分布的简单假设。因此,该理论分析只能定性地解释液滴喷出的动力学过程,得出超声波频率和脉冲持续时间等声波参数与喷出液滴尺寸的相关关系,并不能准确定量分析液滴尺寸与声波参数的关系。
关于聚焦超声波的声辐射力与液-气液面的耦合机制及对液滴形成过程和尺寸影响的机理少有研究。但是利用超声波喷射液滴进行移液的技术和潜在应用引起了人们的广泛关注。2002年,美国南加州大学Kim团队提出了环状扇形电极自聚焦换能器[图5(a)],在ZnO薄膜上镀有扇形图案化电极,实现平面探头的聚焦以及声束的定向偏转,从而实现了直径小于10 μm 液滴按照设计角度从液面喷出,并在2006年将该技术应用于皮升级DNA液滴的移取[79,82,92-93]。该自聚焦超声换能器能实现几百兆赫超高频超声波的聚焦,能实现小于10 μm的焦点大小,从而实现直径小于10 μm液滴的喷出,液滴体积不到1 pL。但是这种自聚焦换能器能量小,只适用于低黏度液体,且液滴喷射出液面的距离短。2006年,Kim团队基于菲涅尔原理设计了空气反射式声透镜[图5(b)],实现PZT平面换能器的聚焦,可以实现较大的能量输出,并在之后十几年内相继实现了缓冲液、氨基酸溶液以及含有PSL颗粒溶液等从几十微米到几百微米不同尺寸液滴从液面喷出,但是其能量仍然有限,喷射距离不大[94-100]。除了采用聚焦换能器产生的体波进行移液之外,2009年澳大利亚蒙纳士大学Yeo团队提出利用聚焦的声表面波实现了液滴的喷出,并于2018年通过研究调节脉冲长度和超声频率实现了直径60~500 μm液滴的喷出,同时实现了细胞的移取[86,101]。声表面波通常是用叉指换能器(IDT)在压电材料表面产生,是一种沿压电材料表面传播的弹性波,其波长由IDT指宽和间距决定。声表面波在压电基底与流体界面传播时,会以瑞利角向流体中辐射声能,从而产生液滴喷射。2019年,Yeo团队[102]基于前期研究工作提出了基于声表面波的纳升级移液平台。同年,武汉大学Chen等[103-104]利用声表面聚焦波实现了纳升级液滴的移取[图5(c)],液滴内含有细胞,并实现了细胞的三维组装。2021年,天津大学Ning等[105]基于声表面聚焦波实现了直径22 μm液滴的喷出,液滴体积约为5.6 pL。但是与前面提到的自聚焦换能器、空气反射式声透镜换能器类似,声表面波能量小,喷射距离短,一般适用于微流控平台。另外,这三种技术中换能器与液体容器是一个整体,更换液体时存在清洗和交叉污染的问题,无法充分发挥超声移液技术完全非接触式特色的优势。
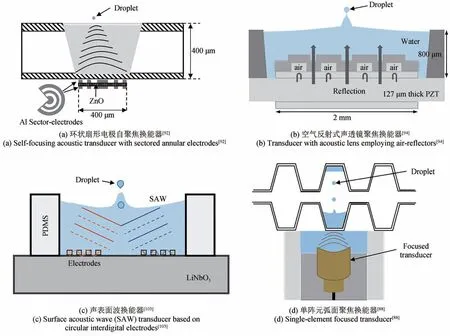
图5 基于不同超声换能器的超声移液技术示意图Fig. 5 Schematic diagrams of ultrasonic liquid transfer technology based on different acoustic transducers
相比前面提到的超声波聚焦方法,利用单阵元弧面聚焦换能器发射的聚焦超声波具有大的输出能量,可以实现大的液滴喷射距离以及可以实现换能器与液体容器分离,从而充分发挥超声移液技术非接触式特色的优势。2012年,美国密歇根大学Fang等[106]基于4 MHz单阵元弧面聚焦换能器实现了含有细胞的纳升级液滴的快速阵列化移取。2017年,日本东京工业大学Tanaka等[107]基于1.5 MHz单阵元弧面探头研究了超声脉冲长度、换能器与液体表面距离及液体表面张力对喷出液滴形态和尺寸的影响,实现了1 μL液滴从微孔板中稳定喷出。2021年,天津大学Guo等[108]基于5 MHz单阵元弧面聚焦超声换能器研究分析液体黏度和表面张力对喷出液滴所需超声激励能量和液滴尺寸的影响,并据此通过控制超声激励能量实现纳升级液滴可控的喷出。单阵元弧面聚焦换能器虽然具有能量大的优势,但是由于制作难度,一般频率都在10 MHz以下,移液液滴精度在纳升级。2021年,中国科学院深圳先进技术研究院郑海荣研究员团队[88]研制了中心频率40 MHz,带宽70%的单阵元高频弧面聚焦超声换能器,并基于同一个换能器通过调节频率(30~50 MHz)、激励电压幅度和脉冲长度,实现了精度可控的皮升级液滴的移取 [图5(d)]。超声移液技术由于具有完全非接触式的特色,并具有精度高、速度快、能保持生物样品活性等特点,除了在药物合成、试剂检测等领域有着重要应用优势之外,在一些新型的生物应用方面也展示了巨大潜力。比如,2006年Aerni等[109]利用非接触式超声移液技术实现阵列式高通量基质溶液的移取,用于基质辅助激光解吸电离质谱的组织切片样品制备。2012年,Harris等[110]将非接触式超声移液技术用于纳升级蛋白质结晶实验。2016年,Kanigowska等[111]将非接触式超声移液技术成功应用于DNA的合成。2021年,Jentsch等[112]将非接触式超声移液技术用于3D生物打印技术。
由于超声移液技术的非接触式特点及优势,人们不仅一直在探索新型的非接触式超声移液方法技术及新型应用,同时还在不断完善非接触式超声移液技术,将该技术推向实际应用。2006年,Labcyte公司推出了基于非接触式超声移液技术的Echo移液系统[图6(a)],移液液滴体积最小可达2.5 nL。随后,Labcyte提出了动态液体分析技术[113-115],并基于Echo移液系统推出了Access实验室工作站,将Echo移液系统与其他设备及附件直接集成于工作台上,允许人们快速地将Echo应用方案编入列表以实现全自动化孔板处理,进一步促进了echo移液系统在领域内的应用。Echo移液系统基于非接触式超声移液技术,以定制微孔板作为液体容器,将超声波能量精准聚焦于液体液面,使母板孔内的纳升级液滴转移至目标板孔内,准确地移取各种液体[116-118],充分发挥了非接触式超声移液技术的优势,其应用跨越许多科学领域,包括合成生物学、药物开发、基因组学、蛋白质组学、诊断学、影像质谱和活细胞转移等[40,110-111,119-121]。时至今日,非接触式超声移液系统作为自动化移液工具已得到了广泛的认可。非接触式超声移液技术的应用不仅仅是移液效率的提升、移液方式的改善,也是实验室自动化和智能化的重要组成部分。目前Echo移液系统在国内外药物研发、基因组学,转换医学、合成生物学等领域都占有很大的应用市场。国内超声移液技术研发起步相对较晚,目前在学术研究和技术产业化方面都已取得了突破性进展。国产研发设备如深圳欢影医疗科技有限公司Arrow系列移液系统[图6(b)]已实现了纳升级超声移液,其移液精度和准确度均已达到行业应用水平。

图6 两种移液系统Fig. 6 Liquid handling system from two companies
3 总结与展望
综上所述,基于活塞式原理的移液器和自动化移液工作站已广泛应用于生物、医学、化学等领域科学研究和工业生产。基于电磁阀和压电驱动的高精度移液技术也已在生物医药、临床检测等领域得到了应用。基于电、磁、光、声的新型高精度移液技术也引起了人们的广泛关注,其中非接触式超声移液技术已得到了行业的认可和应用。总的来说,移液器开创了精密微量移液的时代。在之后的半个世纪里,移液技术不断发展革新,移液操作范式从手动到半自动,再到全自动、高通量不断发展,同时移液的精度也从微升级不断提高到纳升级甚至皮升级。近年来非接触式的自动化超声移液技术由于可以克服接触式移液技术的固有缺陷,有望开启微量移液技术的新纪元。
表1对比了不同微量移液技术的原理、特点和代表性应用。现代生物医学技术的快速发展,使得日常需要使用的液体样本数量越来越多,而单个样本的液体含量却不断减少,从而对移液操作的通量、精度、准确性和可靠性要求越来越高。当前不同的移液技术都有各自的优势和不足。移液液滴的体积越小,移液精度越高,但是同时对移液的准确性和可靠性挑战越大,因而对移液设备的要求越高,从而导致成本大幅度增加。另外,移液速度快和移液操作的并行处理会大幅度提高移液的通量,从而提高实验或工作效率,同时也会增加移液设备的成本。实际应用中移液技术的选择应综合考虑精度、通量和成本,根据应用需求和样品量的具体情况合理选择移液技术和设备。

表1 不同微量移液技术对比Table 1 Comparison of different low-volume liquid transfer technologies
当前基于移液头的接触式移液技术仍然是实验室和工业领域的主流。其中,自动化移液工作站,作为一种可以极大程度提高实验室工作效率、提升准确性的有效解决方案,已成为生物、医疗领域高通量样本处理的趋势。但是基于移液头的接触式移液方法固有的缺陷(如交叉污染、残留堵塞等风险),使得准确性和可靠性在精度要求越来越高的情况下难以保证。由于非接触式移液的独特优势,高通量、高精度、自动化、智能化的非接触式微量移液技术是未来发展的趋势。但是当前非接触式超声移液技术还存在一些不足,限制了其大规模应用:第一,由于超声移液技术结构和所用部件比传统活塞式移液技术复杂且难度大,当前非接触式超声移液系统只有一个移液通道,虽然移液速度快,但是通道数量少限制了其移液通量,与传统自动化移液工作站相比还有一定差距;第二,适用的液体种类和场景仍有诸多限制,溶液容器也局限于特殊的微孔板种类和尺寸,限制了其通用性。因此,研究声辐射力多点并行移液技术,比如通过声人工结构实现声场在液面处的多点聚焦,从而实现多点并行移液,是提高非接触式超声移液技术通量的一种有效方法。另外,简化超声移液模块结构,开发多通道移液技术,也可以大幅度提高超声移液通量。引入机器学习、机器视觉等技术完善基于声波的液体表征、识别技术以及实时检测技术,克服超声移液对溶液容器的局限,提高其通用性,是未来非接触式超声移液技术研究的重点和发展方向。目前商业化的非接触式超声移液系统只有纳升级精度,更高精度的应用需求难以满足,发展皮升级精度的非接触式超声移液系统也是推广完善该技术的一个重要方向。另外,研究发展新型原理的非接触式精密微量移液技术也是需要努力探索的方向。
由于非接触式超声移液技术还未成熟,存在诸多限制,基于接触式微量移液技术的自动化移液工作站仍然会是未来很长一段时间内市场的主流。充分利用活塞式移液技术和基于电磁阀、压电驱动移液技术的各自优势,并改进优化这些技术,进一步提高自动化移液工作站的移液精度、通量、自动化程度和集成化程度是自动化移液工作站发展的下一步目标。另外,发展高效液体表征、识别技术以及移液过程检测技术,提高自动化移液工作站的智能化程度,也是一个重要的发展方向。
除了通用性较高的精密微量移液技术和系统之外,针对特定应用的基于微流控平台的微量液体处理技术和专用芯片以其低成本、便携、可实现高通量和自动化的特点在临床体外诊断领域有着广阔的应用前景。进一步完善基于微流控平台的电、磁、声、光等精密微量移液及液体处理技术,提高其兼容性、可靠性和可扩展性,并推动这些技术走向产业化,实现实际临床应用是一个很有前景的发展方向。同时,探索新型的基于微流控平台的微量移液及液体处理技术也是值得探索的方向。
