经典名方开心散不同粉碎方式下成分含量差异研究*
2023-11-20李胜李超丁辉宋新波
李胜,李超,丁辉,宋新波,2,3
(1.天津中医药大学制药工程学院,天津 301617;2.省部共建组分中药国家重点实验室,天津 301617;3.现代中药海河实验室,天津 301617)
经典名方开心散(KXS)最初记载于唐代孙思邈所著的《备急千金药方·卷十四》,由远志、人参、茯苓、石菖蒲4 味药物组成。经文献考证4 味药物的比例为远志∶人参∶茯苓∶石菖蒲=1∶1∶2∶1[1]。其中远志安神益智,交通心肾,祛痰消肿;人参补气固脱,生津养血,宁心益智;茯苓利水渗湿,健脾宁心;石菖蒲开窍豁痰,醒神益智,化湿开胃[2]。各味药物活性物质之间相互协同,配伍主治好忘。临床常被用来治疗阿尔茨海默病[3-4]、血管性痴呆[5]、认知障碍[6]等以记忆功能障碍为主要表现的疾病,同时对抑郁[7-8]、失眠[9]、疲劳[10]、糖脂代谢紊乱[11]等疾病亦有积极的治疗效果。
散剂作为中药常用剂型之一,是指将药物粉碎后混匀成粉末状,具有制备简单、起效迅速、服用方便、有效成分利于溶出、药材利用度高、节约药物资源等优势,在历代方剂中使用频率颇高,历史悠久[12-13]。《中华人民共和国药典》2015年版记载的粉碎方法有“用时捣碎”“用时打碎”“切碎”“碾碎”“砸碎”“打成碎块”“研粉”“研末”“挫成粉末”“水飞”等方法[14]。目前,KXS 的相关研究主要集中于化学成分[15-16]、药理机制[17-18]及体内代谢[19]方面,而关于KXS 制备工艺方面的研究相对较少,其粉碎方式的研究未见文献报道。因此,本研究以KXS 为研究对象,以传统捣碎、传统碾碎、现代机器粉碎对药材进行处理,采用高效液相-二极管阵列检测器(HPLCPDA)法检测非挥发性成分,顶空固相微萃取-气质联用(HS-SPME-GC/MS)法检测挥发性成分,旨在探究不同粉碎方式对KXS 成分含量的影响,为KXS药材粉碎工艺提供参考依据。
1 仪器与试药
1.1 仪器 手持式红外测温仪,苏州特安斯电子有限公司;DLS 粒径测定仪,美国布鲁克海文仪器公司;LC 高效液相色谱仪,SHIMADZU日本岛津公司;HyPURITY C18色谱柱(250 mm×4.6 mm),塞默飞世尔科技有限公司;7890B-7000D 三重四极杆气质联用仪,美国Agilent 公司;手动固相微萃进样器,德国Gerstel 公司;HP-5MS 毛细管柱(30 m×0.25 mm×0.25 μm),美国Agilent 公司;SPME 萃取纤维(100 μm PDMS,85 μm Polyacrylate,65 μm PDMS/DVB,50/30 μm DVB/CRA/PDMS),美国Supelco 公司;AL204 型电子天平,梅特勒-托利多仪器(上海)有限公司;KQ2200DB型数控超声波清洗器,昆山超声仪器有限公司;CascadaTM超纯水机,美国PALL 公司;中药捣药罐(纯铜),中药碾药槽(纯铜),天津市宏兴铸造厂;中草药粉碎机,天津市泰斯特仪器有限公司。
远志(批号190601)、人参(批号190704)、茯苓(批号190609)及石菖蒲(批号047-2017122902)均由天津中一制药有限公司提供,经天津中医药大学张丽娟教授鉴定,远志为远志科植物远志Polygala tenuifoliaWilld.的干燥根,人参为五加科植物人参Panax ginsengC.A.Mey.的干燥根和根茎,茯苓为多孔菌科真菌茯苓Poria cocos(Schw.)Wolf 的干燥菌核,石菖蒲为天南星科植物石菖蒲Acorus tatarinowiiSchott 的干燥根茎。
2 方法与结果
2.1 KXS 散剂的制备 按比例称取各单味药,混合,以不同粉碎方式(传统捣碎、传统碾碎、现代机器粉碎)处理,将细粉过6 号筛,直至95%质量以上的药材均已过筛,即得KXS 散剂,每种粉碎方法制备3 份。
2.2 KXS 粉碎过程中温度变化及成品粒径考察
2.2.1 温度测定 粉碎前记录各单味药材的初始温度,粉碎过程中30 s 进行1 次测温(共测5 次),结果见表1 及表2。
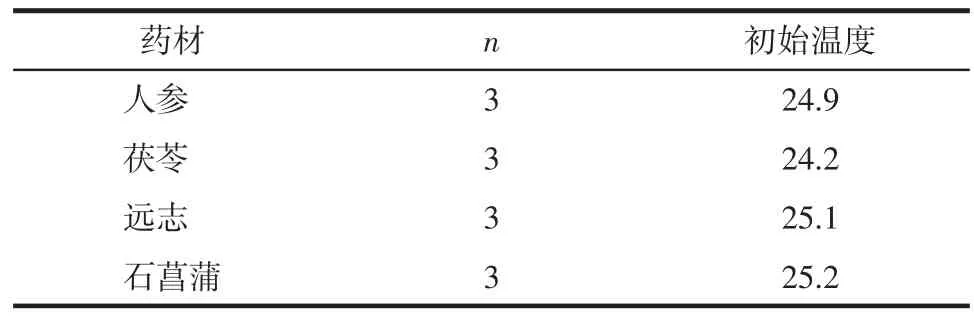
表1 各单味药物的初始温度℃
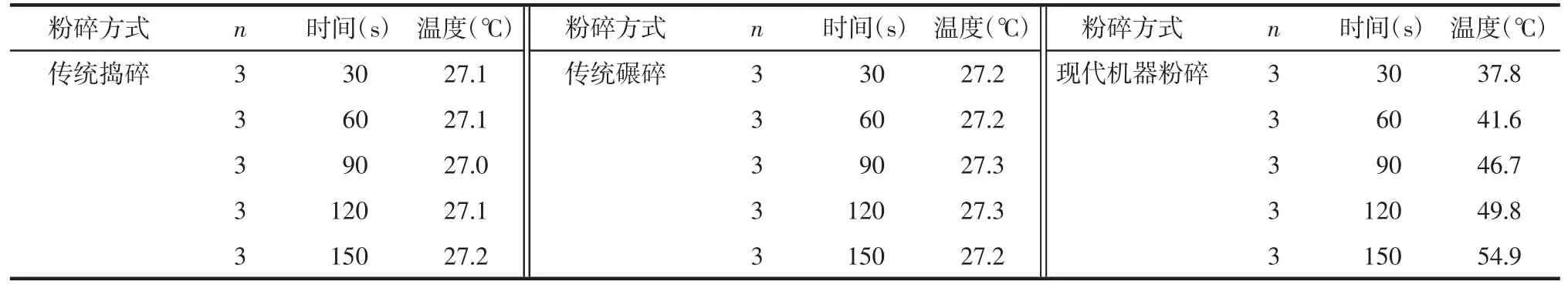
表2 KXS 在不同粉碎过程中的温度变化
2.2.2 粒径测定 精密称取3 种粉碎方式制得的KXS 0.01 g,置于10 mL 容量瓶中,加少量纯水摇匀,再加纯水定容至刻度线,超声混合30 min,拿出冷却至室温,粒径仪测定粒径,结果见表3。
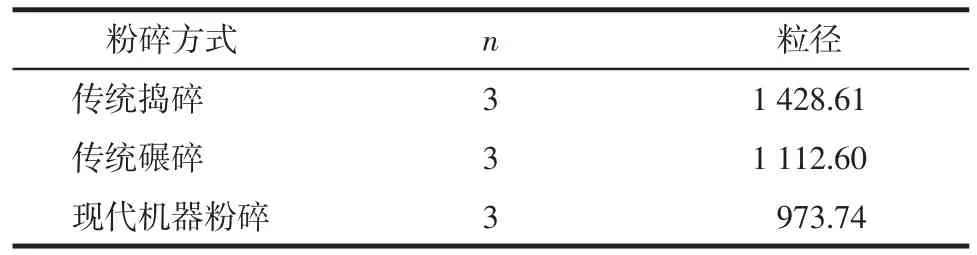
表3 不同粉碎方式制得的KXS 粉末平均粒径nm
2.3 HPLC-PDA 法测定不同粉碎方式下非挥发性成分含量
2.3.2 供试品溶液的制备 精密称取KXS 2.0 g,置于10 mL 容量瓶中,加适量75%甲醇,超声45 min,冷却15 min,再次超声45 min,冷却至室温,加75%甲醇定容至刻度,抽滤,取滤液,用0.22 μm 微孔滤膜过滤,即得。
2.3.3 色谱条件 色谱柱:HyPURITY C18色谱柱(250 mm×4.6 mm);柱温:30 ℃;流动相:0.05%磷酸水溶液-乙腈,梯度洗脱:0~25 min,19%~21%乙腈;25~35 min,21%~21%乙腈;35~40 min,21%~32%乙腈;40 ~55 min,32%~40%乙腈;55 ~60 min,40%~95%乙腈;60~65 min,95%~95%乙腈;65~75 min,95%~19%乙腈;流速1 mL/min;进样体积50 μL;检测波长203 nm。混合对照品溶液、供试品溶液色谱图见图1。
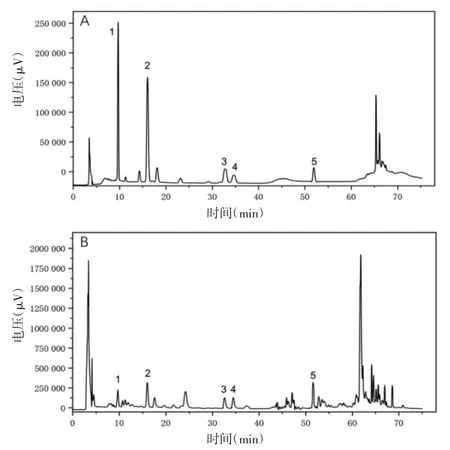
图1 混合对照品和KXS 样品液相色谱图
2.4 方法学考察
2.4.1 线性关系考察 精密量取系列质量浓度的标准品溶液,75%甲醇配制成6 个不同浓度的混标溶液,按照“2.3.3”项中的色谱条件进样,以峰面积为纵坐标,浓度为横坐标,计算回归方程及相关系数,结果见表4,表明其线性关系良好。
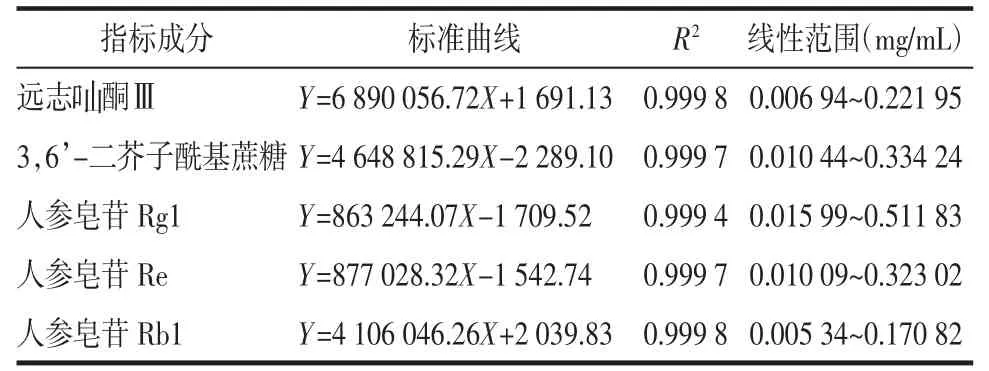
表4 KXS 各指标成分的线性关系考察结果
2.4.2 精密度实验 精密量取“2.3.1”项中5 种标准品溶液各1 mL,置于5 mL 容量瓶中,加75%甲醇定容至刻度线,按照“2.3.3”项中的色谱条件连续进样6 次,记录峰面积,计算远志酮Ⅲ、3,6’-二芥子酰基蔗糖、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1 峰面的RSD 值,结果分别为1.24%、1.48%、1.06%、1.11%、1.35%,RSD 值均小于3.0%,表明仪器精密度良好。
2.4.3 重复性考察 取“2.1”项中制备的KXS,按“2.3.2”项中的方法制备供试品溶液,按“2.3.3”项中的色谱条件进样,记录各组指标成分的峰面积,计算RSD 值,该条件下各指标成分的峰面积RSD 值分别为2.64%、0.54%、2.49%、2.78%、1.47%,RSD 值均小于3.0%,表明该方法重复性良好。
2.4.4 稳定性考察 取“2.1”项中制备的KXS,按“2.3.2”项中的方法制备供试品溶液,按“2.3.3”项中的色谱条件进样,分别在0、2、4、8、12、24 h 分别进样1 次,记录各组指标成分的峰面积,计算RSD 值。远志酮Ⅲ、3,6’-二芥子酰基蔗糖、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1 的峰面积RSD 值分别为1.14%、0.52%、1.47%、1.49%、1.46%,RSD 值均小于3.0%,表明该供试品溶液在24 h 内稳定。
2.4.5 加样回收率考察 精密称取已知指标成分含量的KXS 2.0 g,分别加入约与样品等量的各对照品,按“2.3.2”项中的方法制备供试品溶液,按“2.3.3”项中的色谱条件进样。计算远志酮Ⅲ、3,6’-二芥子酰基蔗糖、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1 的平均加样回收率并计算RSD值,平均加样回收率分别为96.56%、97.88%、99.32%、98.37%、99.20%,RSD 值分别为0.77%、0.83%、1.62%、1.37%、0.96%。
2.4.6 不同粉碎方式对KXS 非挥发性成分的影响 精密称取传统捣碎、传统碾碎、现代机器粉碎条件下制备的KXS 样品每份2.0 g,按“2.3.2”项中的方法制备供试品溶液,每种粉碎方法制备3 份供试品,按“2.3.3”项中的色谱条件进样检测,记录峰面积,代入标准曲线方程,计算出各指标成分的含量,结果见表5。
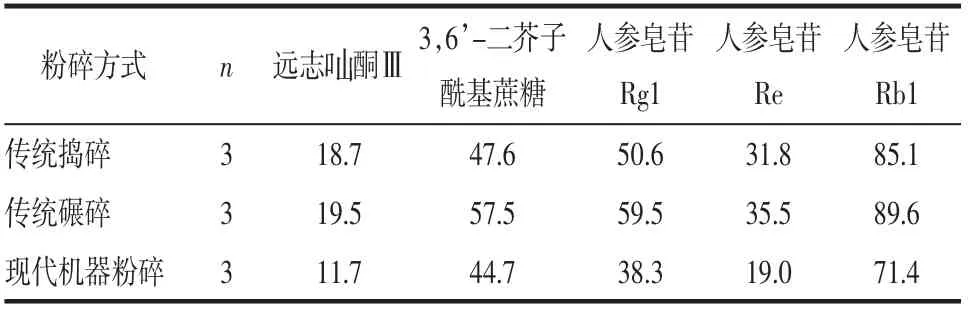
表5 不同粉碎方式下5 种成分的含量测定结果 μg/g
结果显示,传统捣碎及碾碎制得的KXS 中各指标成分含量均高于由现代机器粉碎制得的KXS,而捣碎与碾碎相比,由碾碎制备的KXS 中各指标成分含量较高。
2.5 HS-SPME/GC-MS 法测定不同粉碎方式下挥发性成分含量
2.5.1 顶空固相微萃取条件 分别称取“2.1”项中的KXS 粉末各0.1 g 于20 mL 的顶空瓶中,迅速压紧瓶盖,备用。
2.5.2 色谱质谱条件 色谱柱:Agilent HP-5MS 毛细管柱(30 m×0.25 mm×0.25 μm);进样口温度:250 ℃;载气为氦气(>99.999%);载气流速:1 mL/min;分流比为2∶1;程序升温条件:以初温45 ℃保持2 min,以12 ℃/min 的速率升至117 ℃,以1 ℃/min 的速率升至138 ℃,再以4 ℃/min 的速率升至142 ℃,保持0.5 min,最后以20 ℃/min 的速率升至230 ℃,保持3 min。孵化温度为55 ℃,孵化时间为55 min,吸附时间为40 min,解吸时间为300 s;质谱检测器离子源为EI 离子源,电离电压为70 eV,离子源温度为230 ℃,四极杆温度为150 ℃,质量扫描范围为30~500 amu,全扫描模式采集,质谱标准库为NIST17。
2.5.3 不同粉碎方式对KXS 挥发性成分的影响 KXS总离子图如图2所示,根据匹配度、保留指数及参考文献对各色谱峰进行定性分析,采用峰面积归一法确定各成分的相对百分含量[20],结果见开放科学(资源服务)标识码(OSID)。从不同粉碎方式处理的KXS 中共鉴定出56 种共有化合物,分别占总挥发性成分的93.19%(捣碎)、94.16%(碾碎)、94.04%(现代机器粉碎),可将其分为8 类化合物,包括醚类、萜类、醇/酸/醛类、酯/酮类、碳氢化合物。其中醚类占比最高,达80.38%,种类有7 种;萜类种类最多,有36 种,占比为12%;醇/酸/醛类6 种、酯/酮类4 种、碳氢化合物3 种,分别占比为0.99%、0.24%、0.19%。
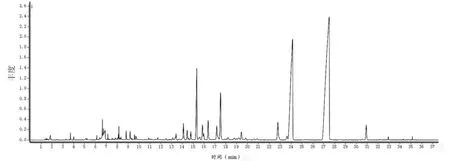
图2 KXS 挥发性成分的总离子流图
选取8 种相对百分含量较高的化合物进行分析,结果显示,(+)-长叶环烯、β-石竹烯、β-细辛醚在传统捣碎条件下占比最大,分别为1.09%、1.15%、43.98%。其中(+)-长叶环烯、β-石竹烯在传统捣碎、碾碎条件下占比差异不大,在现代机器粉碎条件下占比最小,分别为0.93%、1.02%。β-细辛醚在传统碾碎、现代机器粉碎条件下占比差异不大,在传统碾碎条件下占比最小,为43.22%;白菖烯、异丁香酚甲醚、γ-细辛醚在碾碎条件下占比最大,分别为1.45%、4.84%、24.32%。其中白菖烯在传统捣碎、碾碎条件下占比差异不大,在现代机器粉碎条件下占比最小,为1.27%。异丁香酚甲醚、γ-细辛醚在传统碾碎、现代机器粉碎条件下占比差异不大,在传统捣碎条件下占比最小,分别为4.21%、23.62%;甲基丁香酚和α-细辛醚在现代机器粉碎条件下占比最大,分别为6.58%、1.40%。甲基丁香酚在传统碾碎、现代机器粉碎条件下占比差异不大,在传统捣碎条件下占比最小,为5.54%。α-细辛醚在传统捣碎、碾碎条件下占比差异不大,在传统碾碎条件下占比最小,为1.16%。
3 讨论
粉碎方式作为中药材前处理的一种,对其药效的影响不容忽视,在粉碎过程中温度与粉末粒径可能对KXS 的成分含量有所影响,因此本实验对这两个因素进行了考察。结果表明,虽然散剂粉末均通过6 号筛,但由于机器粉碎在粉碎过程中混合更加均匀,粉碎力度更大,同时由于机器刀头剧烈摩擦,因此粒径较其他两种粉碎方式要小且在粉碎过程中升温非常明显,温度最高达55 ℃,传统碾碎比传统捣碎制得的散剂粒径更小,在温度方面差异不大且各批次间基本没有差异。
对于5 种非挥发性成分,现代机器粉碎制得的KXS 均低于其他两种制法,推测由于高温使各种物质之间发生了相互作用,导致其部分成分发生了变化,且粉碎过程中的剧烈搅拌更加加剧了这种情况。而传统捣碎、碾碎均为人工操作,在粉碎过程中温度相差不大,但碾碎制得的KXS 成分含量略高于捣碎,推测是由于碾碎更加能够将各单味药物混合均匀,也更加能够将其充分粉碎,所得粉末粒径更小所造成;HS-SPME/GC-MS 法鉴定出的56 种共有成分均占总挥发性成分的90%以上,其中由传统碾碎制备的KXS 挥发性成分占比最高,为94.16%。除3 种细辛醚外,(+)-长叶环烯、β-石竹烯、白菖烯、异丁香酚甲醚、甲基丁香酚的占比也高于其他成分,推测在KXS 发挥药效时起到潜在作用。此8 种成分中,有6 种在由传统捣碎、碾碎制得KXS 中的相对百分含量较高,虽然某些成分在传统捣碎、现代机器粉碎制得的KXS 中占比较高,但均与传统碾碎相差不大。因此,综合两种检测KXS 成分含量的方法,在其前处理过程中,以传统碾碎制备KXS 能够较大程度保留其成分。对于本方,从目前的结果来看不同的粉碎方式已对其成分含量产生了一定影响,此种差异是否会在药效方面产生影响,还有待进一步研究证实。
