贝伐珠单抗联合XELOX方案对结直肠癌根治术后患者血管内皮生长因子水平的影响
2023-11-18袁明霞胡巍潘连生
袁明霞 胡巍 潘连生
结直肠癌作为临床常见消化道肿瘤,其病因涉及不良饮食习惯、遗传等,具有较高发病率,调查显示,该病病死率位居全部恶性肿瘤第二位[1]。目前,对于中晚期结直肠癌,临床多采用结直肠癌根治术治疗,以有效切除肿瘤组织,同时术后辅以化疗干预,以更好的杀灭肿瘤细胞,延长患者生存时间[2]。XELOX 方案为结直肠癌常用化疗方案,其中奥沙利铂可结合肿瘤细胞DNA,抑制细胞复制,卡培他滨可转化为5-氟尿嘧啶(5-FU),杀伤肿瘤细胞,从而提高患者存活率[3]。但研究发现,XELOX方案单独应用总体有效率仅50%左右,疗效不达预期[4]。近年有研究指出,肿瘤细胞的转移主要依赖血管生成,而血管内皮生长因子(VEGF)为促血管生成重要因子,其可加速肿瘤血管新生,促使肿瘤转移或复发[5]。贝伐珠单抗是一种新型分子靶向药物,其主要作用于VEGF,可阻碍血管新生[6]。鉴于此,本研究旨在观察贝伐珠单抗联合XELOX方案对结直肠癌根治术后患者VEGF 水平的影响。现报道如下。
1 资料与方法
1.1 一般资料
选取新余市中医院内三科2019 年4 月—2022 年2 月收治的89 例结直肠癌患者。纳入标准:结直肠癌符合相关诊断标准[7];有结直肠癌根治术适应证,且行该术治疗;原发性肿瘤;临床分期为Ⅱ、Ⅲ期;重要脏器功能正常;卡氏功能状态评分>70 分,体力状况评分<2 分;精神、认知正常。排除标准:合并肾脏、肝脏等其他部位恶性肿瘤;合并传染性、感染性疾病;交流障碍;入组前接受相关化疗、分子靶向药物等治疗;对研究药物过敏。用随机数字表法将患者分为对照组(n=45)、治疗组(n=44)。研究经本院医学伦理委员会同意。患者均知情同意本研究。
1.2 方法
两组均行结直肠癌根治术治疗。术后4 周,对照组用XELOX 方案治疗,予奥沙利铂(生产厂家:远大医药黄石飞云制药有限公司,批准文号:国药准字H20103129,规格:100 mg)静脉滴注,将130 mg/m2奥沙利铂溶于500 mL 5%葡萄糖注射液(生产厂家:江西长江药业有限公司,批准文号:国药准字H36021429,规格:500 mL∶50 g)滴注,于6 h 内完成,第1 天;予1 000 mg/m2卡培他滨(生产厂家:正大天晴药业集团股份有限公司,批准文号:国药准字H20143044,规格:0.5 g)餐后口服,2 次/d,第1~14 天;1 个化疗周期为3 周,共治疗3 个周期。治疗组用贝伐珠单抗(生产厂家:Roche Diagnostics GmbH,注册证号:国药准字S20170036,规格:0.4 g/瓶)联合XELOX 方案治疗,XELOX 方案同对照组,予7.5 mg/kg 贝伐珠单抗静脉滴注,于30~90 min 完成(根据患者耐受度调整),于化疗周期第1 天滴注,共治疗3 个周期。两组均接受6 个月随访。
1.3 观察指标及判定标准
(1)实验室指标:抽取两组术前、治疗3 个周期后空腹肘静脉血3 mL,以3 000 r/min 离心处理10 min,吸取血清,置于-20 ℃冰箱内贮存、待检;①肿瘤标志物水平:用电化学发光法测定癌胚抗原(CEA)、糖类抗原19-9(CA19-9)、糖类抗原242(CA242)水平;②VEGF 水平:用放射免疫分析法测定VEGF 水平。(2)毒副反应:参照文献[8],记录两组治疗期间毒副反应发生情况。(3)复发率:随访期间间隔3 个月复查1 次CT 或钡餐X 线等检查,评估并记录两组复发情况,复发:检查可见新的肿瘤病灶生成,或残留病灶体积增大。
1.4 统计学处理
2 结果
2.1 两组一般资料对比
两组一般资料对比,差异均无统计学意义(P>0.05),具有可比性,见表1。
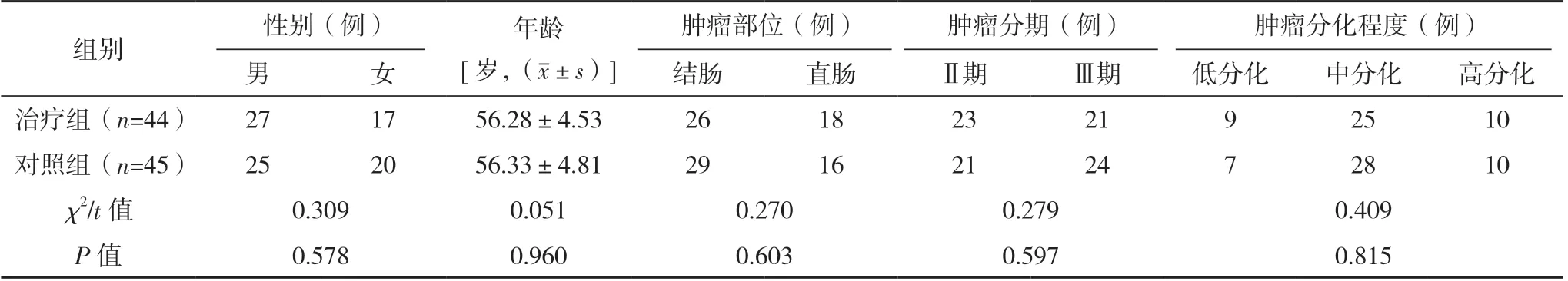
表1 两组一般资料对比
2.2 两组肿瘤标志物水平对比
两组术前CEA、CA19-9、CA242 水平对比,差异均无统计学意义(P>0.05);两组治疗3 个周期后的CEA、CA19-9、CA242 水平均较术前降低,且治疗组各指标水平均更低,差异均有统计学意义(P<0.05)。见表2。
表2 两组肿瘤标志物水平对比(±s)
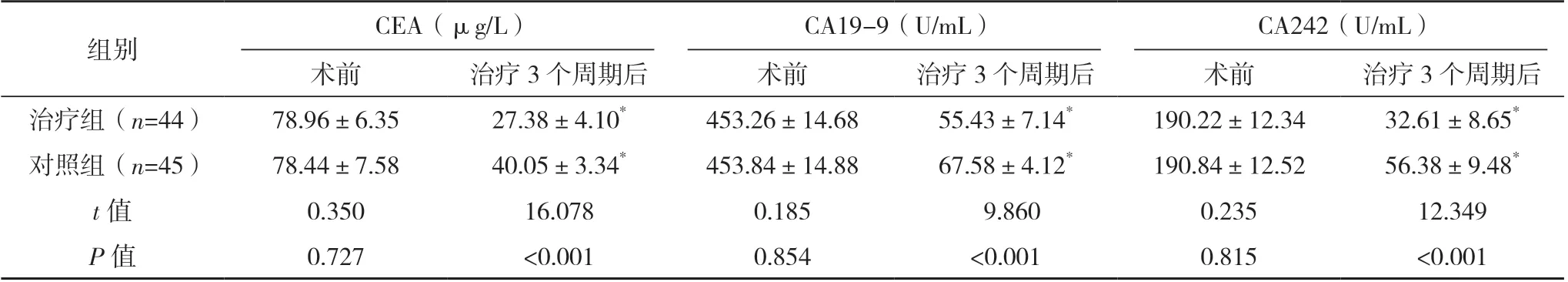
表2 两组肿瘤标志物水平对比(±s)
*与本组术前比较,P<0.05。
组别CEA(μg/L)CA19-9(U/mL)CA242(U/mL)术前治疗3 个周期后术前治疗3 个周期后术前治疗3 个周期后治疗组(n=44)78.96±6.3527.38±4.10*453.26±14.6855.43±7.14*190.22±12.3432.61±8.65*对照组(n=45)78.44±7.5840.05±3.34*453.84±14.8867.58±4.12*190.84±12.5256.38±9.48*t 值0.35016.0780.185 9.8600.23512.349 P 值0.727<0.0010.854<0.0010.815<0.001
2.3 两组VEGF 水平对比
两组术前VEGF 水平对比,差异无统计学意义(P>0.05);两组治疗3 个周期后的VEGF 水平均较术前降低,且治疗组水平更低,差异均有统计学意义(P<0.05)。见表3。
表3 两组VEGF水平对比[ng/L,(±s)]
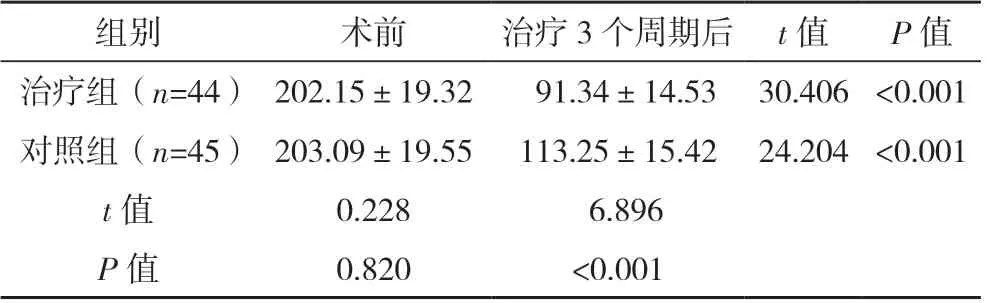
表3 两组VEGF水平对比[ng/L,(±s)]
组别术前治疗3 个周期后 t 值P 值治疗组(n=44) 202.15±19.32 91.34±14.53 30.406 <0.001对照组(n=45) 203.09±19.55 113.25±15.42 24.204 <0.001 t 值0.228 6.896 P 值0.820<0.001
2.4 两组毒副反应对比
两组胃肠道症状、骨髓抑制、脱发、肝功能异常、白细胞降低发生率及毒副反应总发生率比较,差异均无统计学意义(P>0.05),见表4。
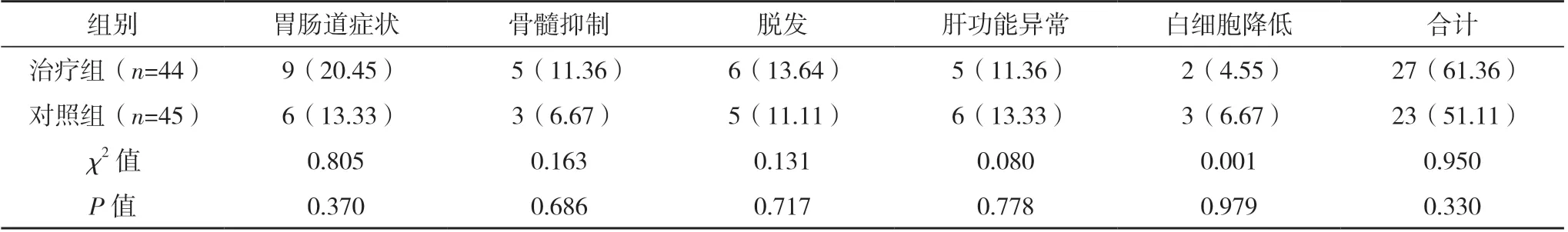
表4 两组毒副反应对比[例(%)]
2.5 两组复发率对比
随访发现,两组患者全部存活,其中治疗组无复发,对照组复发4 例,两组复发率(0 vs 8.89%)比较,差异无统计学意义(χ2=2.286,P=0.131)。
3 讨论
结直肠癌根治术作为结直肠癌主要治疗方案之一,其可有效切除肿瘤组织,遏制疾病进展,但部分患者术后仍需采取辅助化疗、放疗等方案,以提高患者整体获益[9]。同时有研究表明,结直肠癌根治术后早期行化疗干预,利于延长患者寿命,提升其生存质量[10]。
目前,临床多采用XELOX 方案治疗结直肠癌,其中奥沙利铂为广谱抗肿瘤药物,其以肿瘤DNA作为靶向部位,铂原子与DNA 形成交叉联结,可拮抗DNA 复制、转录[11]。卡培他滨为5-FU 前体药物,经三步酶链反应可转化为5-FU 作用于肿瘤细胞S 期,阻滞细胞DNA 合成,从而杀伤肿瘤细胞,抑制转移及复发[12-13]。但临床应用发现,结直肠癌患者单纯采用XELOX 方案化疗的整体效果有限,患者整体预后不佳[14]。贝伐珠单抗是一种单克隆抗体,其抗体可竞争性结合VEGF 受体,阻止内皮细胞分裂,且可降低VEGF 活性,阻碍肿瘤血管新生[15]。同时有研究指出,贝伐珠单抗可降低血管内皮细胞通透性,协同化疗药物干预,利于药物渗入肿瘤血管,从而提高肿瘤细胞杀伤效果[16-17]。CEA、CA19-9、CA242 为临床诊断、评估结直肠癌预后常用标志物,其表达增加提示肿瘤细胞增殖,且复发风险高[18]。本研究结果显示,治疗组治疗3 个周期后的CEA、CA19-9、CA242 水平均较对照组低,且VEGF 水平也较对照组低,说明结直肠癌根治术后患者采用贝伐珠单抗联合XELOX 方案治疗利于降低肿瘤标志物与VEGF 水平。分析原因在于,贝伐珠单抗协同XELOX 方案治疗,可阻止肿瘤原有血管再生及新血管形成,促使肿瘤血管退化,阻断病灶血供,从而遏制残存细胞生长,同时该药物通过增加血管通透性,利于化疗药物递送,增强药物敏感性,从而更好地消灭肿瘤病灶,提高整体治疗效果,降低CEA、CA19-9、CA242 及VEGF 水平[19-20]。本研究还发现,两组间胃肠道症状、骨髓抑制、脱发、肝功能异常、白细胞降低发生率对比无差异,说明贝伐珠单抗安全性较好,不会增加毒副反应发生。有关复发率方面,随访6 个月,治疗组无复发,对照组复发率为8.89%,说明贝伐珠单抗联合XELOX 方案治疗可在一定程度上减少结直肠癌复发率,但两组间复发率对比无差异,这一结果可能与随访时间短有关,未来仍需延长随访时间、增加样本量进行进一步研究观察。
综上所述,结直肠癌根治术后患者采用贝伐珠单抗联合XELOX 方案治疗利于下调肿瘤标志物水平,降低VEGF 水平,且药物安全性好。
