次氧化锌火法脱氯制备高纯氧化锌的工艺研究
2023-11-16张建彬申玉芳覃庶宏王盛强张静冰
王 松,张建彬,申玉芳,覃庶宏,王盛强,张静冰
(1.桂林理工大学材料科学与工程学院,有色金属及材料加工新技术教育部重点实验室,广西桂林 541000;2.武宣县汇丰实业有限责任公司,广西武宣 545900)
锌是全球消费量仅次于铁、铝、铜的十分重要的有色金属原材料。中国作为全球最大的锌消费国,尽管拥有世界第二大的锌矿产资源[1],但是矿山分布散而小,大型矿山少,且富矿少、贫矿多[2],因此中国也是最大的锌进口国;此外,在长期的工业发展中积累了大量的含锌工业废弃物,尚未得到很好的利用。为了缓解中国资源短缺、实现经济可持续发展,加强对中国丰富的低品位氧化锌矿石和各种含锌二次资源的利用已成为中国锌工业持续健康发展的有效选择[3]。
回转窑工艺[4-5]是中国目前处理各类含锌资源[6]的常用工艺,其原理是将各种含锌物料与还原碳配料混合后送入回转窑中,在高温下含锌物料中的锌被还原为锌蒸气并上升到回转窑的上部空间与氧气反应生成氧化锌微粒,氧化锌微粒随尾气一起挥发经回转窑尾部的收尘设备收集得到次氧化锌烟尘产品,该产品是湿法炼锌的重要原料之一[7]。次氧化锌烟尘中含有大量的氟、氯元素[8-9],如果不经处理直接用于湿法炼锌系统[10-11],不仅会腐蚀设备,影响电解锌的质量,而且会生成Cl2、HCl等有毒气体,危害作业人员生命健康,因此有必要对次氧化锌进行脱氯处理。目前,比较成熟的脱氯方法有湿法碱洗脱氯[12]和火法脱氯[13-14]。其中,湿法碱洗脱氯工艺虽然操作简单,但碱洗后需要水洗,不仅耗用大量的水资源,而且碱洗液和水洗液的处理也很复杂[15-16];火法高温脱氯常用的设备为多膛炉和回转窑,工艺成熟且流程简单、脱氯率高、操作稳定。本文对火法焙烧次氧化锌烟尘的脱氯反应进行热力学分析,并结合实验探讨焙烧过程的物相及形貌变化,确定最佳脱氯工艺参数,进而对次氧化锌中氯的脱除提供参考。
1 实验材料和方法
1.1 实验材料
次氧化锌粉尘来自中国广西某工厂。采用X射线荧光光谱仪(XRF)分析粉尘的化学成分,采用化学滴定法分析氯含量,结果见表1。图1为次氧化锌的X 射线衍射(XRD)谱图。由图1 可看出,次氧化锌的主要物相为ZnO、Fe3O4、ZnFe2O4、PbO、KCl、FeOCl 等。其中,FeOCl 是由挥发的FeCl3与收尘设备中的水蒸气反应生成的,加热后会再次分解为FeCl3。
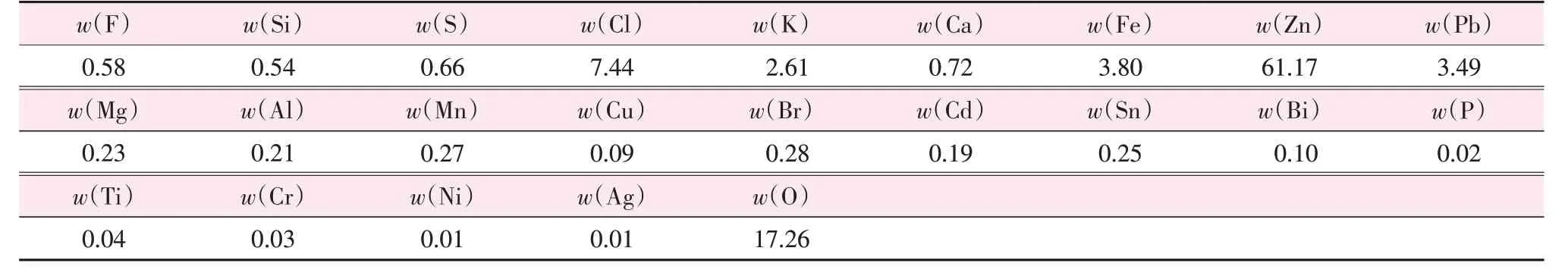
表1 次氧化锌的化学组成Table 1 Chemical compositions of zinc oxide dust %
采用扫描电子显微镜(SEM)对次氧化锌粉的微观形貌进行分析,结果如图2所示。由图2可见,原料中有大量杂质物相存在,其中氧化锌为直径在100~200 nm的超细粉体颗粒,杂质晶体呈针状或树枝状团簇,粒径为200~500 nm,各相相互交织团聚在一起形成无规则团状物。
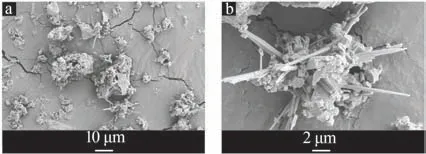
图2 次氧化锌的SEM图Fig.2 SEM images of zinc oxide dust
1.2 实验原理
根据次氧化锌粉尘的XRD分析结果可知,次氧化锌粉尘中的氯化物主要以KCl、FeOCl 的形式存在。此外,次氧化锌中还可能存在的氯化物有ZnCl2、FeCl3、PbCl2等。
在次氧化锌的焙烧过程中,氯化物可能发生如下反应:
图3 为反应式(1)~(5)的标准摩尔吉布斯自由能变(ΔG)随温度的变化曲线。由图3可知,所有反应式的ΔG值均随着温度的升高而降低,表明随着温度的升高,反应更容易发生;在1 000 ℃时,除KCl外所有反应的ΔG值均低于0,表明该氯化物能够在此温度下挥发。KCl 的挥发温度为1 450~1 500 ℃,传统的回转窑工作温度区间为1 100~1 400 ℃,在此温度区间下KCl 熔融为液态,故此时KCl 的挥发遵循液体的挥发规律。
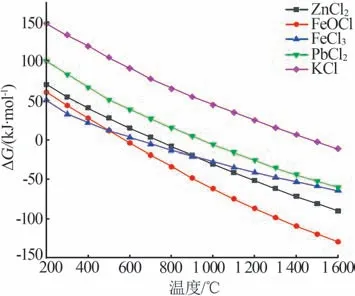
图3 次氧化锌焙烧过程的热力学计算结果Fig.3 Thermodynamic calculation results of zinc oxide dust sintering process
1.3 实验过程
在坩埚中称取一定量的次氧化锌粉末,然后将坩埚置于马弗炉中,设定马弗炉升温速率为5 ℃/min。待炉温升高到指定温度后焙烧,焙烧结束后随炉冷却到100 ℃以下,称其质量并测定氯、锌含量。
采用化学滴定法测定氯含量。称取1 g次氧化锌于50 mL去离子水中搅拌溶解30 min后过滤;取25 mL滤液于锥形瓶中,加入两滴溴酚蓝指示剂,滴加硝酸(质量分数为5%)使溶液变为黄色并过量3~5滴;然后加入1 mL二苯碳酰二肼指示剂,用硝酸汞标准溶液滴定至溶液由黄色变为紫色;记录消耗硝酸汞溶液的体积,进而计算出次氧化锌中氯元素的含量。
采用电感耦合等离子体原子发射光谱仪(ICPAES)测定次氧化锌的锌含量。称取0.1 g 次氧化锌于50 mL聚四氟乙烯烧杯中,加入少量水润湿,随后依次加入15 mL 盐酸溶液、5 mL 硝酸溶液、3 mL 氢氟酸溶液;然后将聚四氟乙烯烧杯置于120 ℃电热板上加热直至样品完全蒸干,取下烧杯待冷却至室温后加入15 mL硝酸(质量分数为5%)溶液,并定容至10 L容量瓶中;采用ICP-AES 测定溶液中的锌离子浓度,进而计算出次氧化锌中的锌含量。
2 实验结果与讨论
2.1 焙烧过程对次氧化锌氯脱除率和氧化锌含量的影响
取一定量的次氧化锌于马弗炉中在不同温度下焙烧2 h后考察次氧化锌氯脱除率、氧化锌含量与焙烧温度的关系,结果如图4所示。由图4可以看出,次氧化锌的氯脱除率随焙烧温度的升高而增加,且氯脱除率与焙烧温度呈线性关系。这主要是因为次氧化锌中的氯化物主要为KCl和FeOCl,其中FeOCl含量较少且在焙烧过程中分解为Fe2O3和FeCl3,FeCl3沸点较低在焙烧过程中最先脱除;而KCl 的熔点较低为770 ℃,沸点较高为1 420 ℃,因此在900~1 100 ℃下KCl熔融为液态,此时氯脱除率与温度呈良好线性正相关。对于液态分子,其运动速率随着温度的升高而加剧,其中一些速率较大的分子脱离平衡态的束缚而逃逸出液面成为气体分子,因此,任何温度下液体都在蒸发。随着液体温度的进一步升高,分子的平均动能增大,速率增大,从液面逃逸出去的分子数量增多,因此,液体的温度越高,蒸发得就越快。在焙烧温度为1 100 ℃、保温时间为120 min时,氯脱除率达到了97.63%。
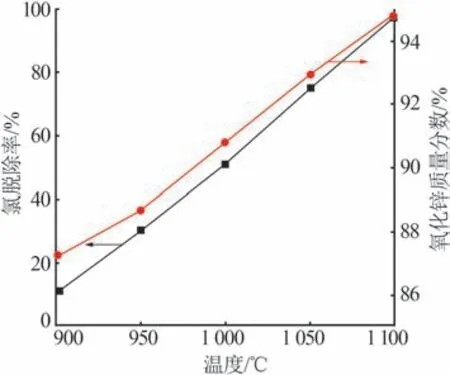
图4 次氧化锌氯脱除率、氧化锌质量分数与焙烧温度的关系Fig.4 Relationship between zinc oxide dust chloride removal rate, zinc oxide mass fraction and sintering temperature
由于次氧化锌中的锌主要以ZnO 的形式存在,ZnO 熔沸点均较高,分别为1 975、2 360 ℃,远高于焙烧温度,因此在次氧化锌的焙烧过程中锌的损失可忽略不计。在1 100 ℃下焙烧2 h后次氧化锌的质量损失率为19.69%,次氧化锌中的氧化锌质量分数为94.81%,可见高温焙烧可以极大地提升次氧化锌的品位。在次氧化锌焙烧温度为1 100 ℃条件下考察次氧化锌氯脱除率、氧化锌含量与保温时间的关系,结果如图5所示。从图5可以看出,氯脱除率随着保温时间的延长而升高,但随着保温时间的延长,挥发速率逐渐减小,由于FeOCl 的含量较少且挥发温度较低,因此该图主要揭示了KCl的挥发规律,即其符合液体的挥发规律。对于液体物质的蒸发,其速率除与温度有关外,还与液体表面积有关,表面积越大,蒸发速率越快,而随着保温时间的延长,液体质量逐渐减少,表面积也随之减小,因此蒸发速率减小。随着次氧化锌中氯化物等低熔沸点物质的挥发,次氧化锌中氧化锌品位也在不断升高,且其变化趋势基本与氯化物的脱除率变化趋势相同。

图5 次氧化锌氯脱除率、氧化锌质量分数与焙烧时间的关系Fig.5 Relationship between zinc oxide dust chloride removal rate, zinc oxide mass fraction and sintering time
2.2 焙烧过程对次氧化锌物相的影响
图6 为不同温度下焙烧2 h 后得到的次氧化锌的XRD 谱图。由图6 可知,随着焙烧温度的升高,归属于KCl 的衍射峰强度逐渐降低,最终消失;而属于FeOCl 的衍射峰在900 ℃的焙烧条件下就已消失,说明在900 ℃之前FeOCl 就已经分解挥发,因此对次氧化锌的焙烧工艺起主要作用的是KCl;经过1 100 ℃焙烧后次氧化锌的物相除ZnO 外,还存在Fe3O4、ZnFe2O4。该结果再次证明了焙烧过程能够有效去除次氧化锌中的氯元素。

图6 焙烧温度对次氧化锌物相的影响Fig.6 Effect of roasting temperature on zinc oxide dust phase
图7为1 100 ℃、不同保温时间条件下焙烧得到的次氧化锌的XRD 谱图。由图7 可以看出,归属于FeOCl 的衍射峰在焙烧0.5 h 后消失,归属于KCl 的衍射峰在焙烧1 h后消失,这主要是因为在1 100 ℃下氯化物挥发的速率很快;焙烧1.5 h后次氧化锌的XRD谱图仅检测到ZnO、Fe3O4、ZnFe2O4相,说明熔点较低的铅化物随着氯化物一同挥发出去。

图7 保温时间对次氧化锌物相的影响Fig.7 Effect of holding time on zinc oxide dust phase
2.3 焙烧过程对次氧化锌微观形貌的影响
图8 为次氧化锌在不同焙烧温度下的微观形貌图。由图8可知,随着焙烧温度的升高,次氧化锌颗粒长大为直径在2~8 μm 的球形颗粒,并在球形颗粒间点缀着一些小颗粒。在950 ℃焙烧时颗粒粒径大都小于3 μm;而在1 000 ℃焙烧时颗粒粒径分布在2~8 μm;之后随着温度的升高颗粒粒径虽然没有明显长大,但能清晰地看到颗粒间的小颗粒数量明显减少,这与晶粒的生长过程有关。晶粒的生长是晶界移动的结果,具体表现为一个颗粒的长大,另一个颗粒的缩小或消失,由于杂质、气孔等的阻碍作用,使得晶界移动能力在靠近杂质时减弱,最终出现一个极限直径晶粒,因此表现为小颗粒的数量不断减少。

图8 次氧化锌在不同焙烧温度下的微观形貌Fig.8 Microscopic morphology of zinc oxide dust at different roasting temperatures
图9为1 100 ℃、不同保温时间下次氧化锌的微观形貌图。由图9可知,随着保温时间的延长,次氧化锌颗粒的大小没有发生明显变化,但能看到小颗粒的数量随着保温时间的延长而减少,且有小颗粒嵌入到大颗粒中,表明小颗粒正在被大颗粒吞噬。该结果进一步证明在焙烧过程中晶形的变化过程就是晶体的生长过程。

图9 次氧化锌在不同保温时间下的微观形貌图Fig.9 Microscopic morphology of zinc oxide dust at different holding times
3 结论
本文模拟研究了回转窑焙烧次氧化锌的脱氯工艺。经回转窑还原—挥发—氧化后所得次氧化锌的主要成分为氧化锌,含氯化合物主要为KCl 和FeOCl。热力学分析结果表明,对次氧化锌焙烧脱氯工艺起决定性作用的是KCl,在回转窑工作温度下,KCl熔融为液态,其脱除过程符合液体的挥发规律。实验结果表明,在1 100 ℃、焙烧2 h的条件下,氯脱除率达到97.63%,氧化锌纯度为94.81%,脱氯工艺几乎不会造成锌的损失,实验结果可为同类型的氧化锌烟尘的脱氯工艺提供参考。尽管次氧化锌中的氯含量已经得到有效降低,但作为湿法炼锌的原料,其成分仍较为复杂。为了加强对次氧化锌的综合利用,有必要进一步探索从次氧化锌中分离提纯锌的方法。
