名中医协定方联合穴位敷贴治疗非酒精性脂肪性肝炎临床观察 *
2023-11-14陈天阳金源源王浩艺陈建杰
刘 旭 陈天阳 张 萍 金源源 王浩艺 陈建杰, 成 扬,※
(1.上海浦东新区传染病医院肝病科,上海 201299;2.上海中医药大学附属曙光医院肝病研究所,上海 201203)
非酒精性脂肪性肝病(Non-alcoholic fatty liver disease,NAFLD)涵盖了从单纯性脂肪肝到非酒精性脂肪性肝炎(Non-alcoholic steatohepatitis,NASH)的一系列病变,可进展至肝硬化或肝细胞癌,目前尚无治疗NASH 效果确切的药物[1,2]。上海市名中医陈建杰教授治疗NASH 有独到之处,其临床协定方具有较好效果[3,4]。临床单一手段治疗NASH 存在局限,如何提高效果亟待解决,采用中药外治是近年努力方向之一[5]。本研究在既往工作基础上,采用协定方联合穴位敷贴,探讨其临床疗效和安全性。
1 资料与方法
1.1 一般资料选取2018 年12 月—2020 年12 月来自上海浦东新区传染病医院和上海中医药大学附属曙光医院的150 例NASH 患者。采用随机数字表法将患者按1∶1∶1 比例分为对照组、协定方组、联合治疗组(协定方联合穴位敷贴),每组50 例。研究结束后,对照组患者共失访脱落7 例(因未按研究方案用药或失访);协定方组失访脱落5 例(因未按研究方案用药或失访);联合治疗组失访脱落3 例(因未按研究方案用药或失访)。3 组患者失访脱落率分别为14%(7/50)、10%(5/50)和6%(3/50)。最终纳入临床评价的患者共135 例,对照组43 例,其中男27 例、女16 例;平均年龄(45.31±12.04)岁;脂肪肝轻度14 例、中度25 例、重度4 例。协定方组45 例,其中男27 例、女18 例;平均年龄(43.97±10.58)岁;脂肪肝轻度15 例、中度25例、重度5 例。联合治疗组47 例,其中男28 例、女19例;平均年龄(44.25±11.76)岁;脂肪肝轻度12 例、中度29 例、重度6 例。3 组患者性别、年龄、病情程度等一般资料比较,差异无统计学意义(P>0.05)。本课题已经上海浦东新区传染病医院伦理委员会的批准(批准号:2018-1),并在中国临床试验中心进行了注册(ChiCTR1800016476)。
1.2 诊断标准参考文献[6]制定:(1)无饮酒史或男性饮酒折合乙醇量<每周140 g,女性<每周70 g。(2)肝脏影像学表现符合弥漫性脂肪肝的诊断标准,且无其他原因可供解释和(或)有代谢综合征相关组分的患者出现不明原因的血清丙氨酸氨基转移酶(ALT)和(或)天冬氨酸氨基转移酶(AST)、血清γ-谷氨酰转肽酶(GGT)持续增高(>1.5×ULN)半年以上。(3)排除酒精性肝病、病毒性肝炎、自身免疫性肝炎、肝豆状核变性等可导致脂肪肝的特定肝病,并排除导致脂肪肝的特殊情况如药物、工业毒物、遗传代谢性疾病等。
1.3 纳入标准(1)年龄18~65 岁,性别不限;(2)经B超以及肝功能检查确诊为NASH;(3)试验前4周内未参加过临床试验;(4)签署知情同意书。
1.4 排除标准(1)合并有心、肺、肾等严重原发病者或精神病者;(2)处于哺乳、妊娠期或拟妊娠的妇女;(3)肝功能数值大于检测上限3 倍和(或)肌酐大于检测上限者;(4)正在使用其他药物或正在参加其他临床试验者;(5)过敏体质及对试验方、药成分过敏者。
1.5 剔除标准和脱落标准剔除标准:(1)入组筛选病例失误者;(2)试验过程中合并服用了本研究外其他中、西药物,导致无法正确判断疗效和安全性。脱落标准:没有完成本研究规定的疗程及观察周期者。
1.6 治疗方法饮食和运动调整方案:指导所有患者通过健康饮食和加强锻炼的生活方式纠正不良行为,控制每日膳食热量摄入;避免久坐少动,选择能够坚持的体育锻炼方式,以增加骨骼肌质量、防治肌少症[6]。药物治疗及疗程:协定方组患者给予中药协定方口服。该方由五味子6 g,白术10 g,荷叶10 g,决明子10 g,菊花10 g,苍术6 g,生蒲黄6 g 组成。该方委托深圳三九药业制备配方颗粒,每天2 次,每天1剂。联合治疗组在口服协定方基础上,予以穴位敷贴治疗。敷贴药物为石菖蒲6 g,茵陈9 g,制大黄9 g(该方系浦东新区传染病医院协定治疗方)。将上3 味药研细成粉末状,过筛,用食醋及蒸馏水1∶1 调成糊膏状,制为敷贴,将其敷贴于患者期门穴、日月穴和中脘穴,每次2 h,每天1 次,14 d 为1 个疗程,间隔2 周再进行下一个疗程,共治疗12 次。对照组予以多烯磷脂酰胆碱胶囊[赛诺菲(北京)制药有限公司,国药准字H20059010],2 粒/次,每天3 次,口服。整个疗程共24 周。
1.7 观察指标治疗前后测量计算患者体质量指数(Body mass index,BMI)和腰臀比(Waist-to-hip ratio,WHR),检测肝功能[ALT、AST、GGT、总胆红素(TBIL)]、血脂[三酰甘油(TG)、胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)]和肝脏瞬时弹性硬度检测受控衰减参数(CAP),进行肝脏B超检查。
疗效判断:参照文献[7]制定。临床治愈:治疗后肝脏酶学ALT 恢复正常,肝脏影像学B 超检查恢复正常;显效:治疗后肝脏酶学ALT 下降≥75%,肝脏影像学B超检查分级下降2个等级;有效:治疗后肝脏酶学ALT下降≥50%但<75%,肝脏影像学B超检查分级下降1个等级;无效:达不到有效标准。总有效率=(临床治愈+显效+有效)例数/总例数×100%。
安全性指标:记录患者治疗前后的血、尿、便三大常规和心电图结果,以及治疗过程中是否出现了药物及穴位敷贴的不良反应。
1.8 统计学方法使用SPSS 17.0 软件进行统计处理。计量资料以(±s)表示,多组间比较选择单因素方差分析,组间比较选择LSD 检验,同组治疗前后比较选择配对t检验。计数资料以率(%)表示,多组率的比较选择x2检验。P<0.05为差异有统计学意义。
2 结果
2.1 3 组患者治疗前后肝功能指标水平比较治疗后组ALT、AST、GGT 指标均出现显著下降,差异有统计学意义(P<0.05 或P<0.01)。与对照组比较,协定方组和联合治疗组ALT、AST、GGT 指标下降幅度显著,差异有统计学意义(P<0.05 或P<0.01);与协定方组比较,联合治疗组ALT 和AST 指标下降幅度显著,差异有统计学意义(P<0.05)。见表1。
表1 3组NASH患者治疗前后肝功能指标水平比较(±s)
注:与本组治疗前比较,1)P<0.05,2)P<0.01;与对照组比较,3)P<0.05,4)P<0.01;与协定方组比较,5)P<0.05。
TBIL/(μmol/L)27.3±3.9 26.2±4.1 28.6±4.2 26.7±3.4 28.3±4.5 25.4±3.7组别对照组例数43协定方组45联合治疗组47时间治疗前治疗后治疗前治疗后治疗前治疗后ALT/(U/L)97.8±24.2 75.3±21.91)95.2±25.5 59.4±16.82)3)98.9±22.7 47.5±14.32)4)5)AST/(U/L)87.6±23.1 68.5±22.51)92.4±27.4 63.6±13.82)3)90.6±26.7 50.2±12.92)4)5)GGT/(U/L)180.3±38.9 138.2±35.11)178.6±40.2 90.7±23.42)3)172.3±41.5 88.4±19.72)4)
2.2 3 组患者治疗前后血脂指标水平比较治疗后3 组TC、TG 和LDL-C 均出现下降,其中协定组和联合治疗组显著低于治疗前,差异有统计学意义(P<0.05 或P<0.01)。联合治疗组TG 和LDL-C 下降幅度与协定方组比较,差异有统计学意义(P<0.05)。见表2。
表2 3组NASH患者治疗前后血脂指标水平比较(±s,mmol/L)
注:与本组治疗前比较,1)P<0.05,2)P<0.01;与协定方组比较,3)P<0.05。
HDL-C 1.7±0.4 1.8±0.3 1.6±0.2 1.8±0.3 1.5±0.5 1.9±0.7组别对照组例数43协定方组45联合治疗组47时间治疗前治疗后治疗前治疗后治疗前治疗后TC 5.1±2.2 4.8±1.9 5.0±2.5 4.5±1.81)5.2±2.0 4.3±1.71)TG 2.6±0.7 2.5±0.5 2.7±0.4 1.9±0.71)2.8±0.6 1.8±0.42)3)LDL-C 3.4±0.9 3.1±0.6 3.6±0.8 2.7±0.41)3.5±0.5 2.4±0.32)3)
2.3 3 组患者临床疗效比较对照组临床总有效率为53.5%(23/43),协定方组为71.1%(32/45),联合治疗组为83.0%(39/47)。3 组临床疗效比较,差异有统计学意义(P<0.05),且联合治疗组疗效优于协定方组,差异有统计学意义(P<0.05)。见表3。

表3 3组NASH患者临床疗效比较
2.4 3 组患者治疗前后BMI 和WHR 比较治疗后3 组BMI和WHR指标都出现下降,但对照组下降幅度与治疗前比较,差异无统计学意义(P>0.05),协定方组和联合治疗组指标下降幅度与治疗前比较,差异有统计学意义(P<0.05)。见表4。
表4 3组NASH患者治疗前后BMI和WHR比较(±s)
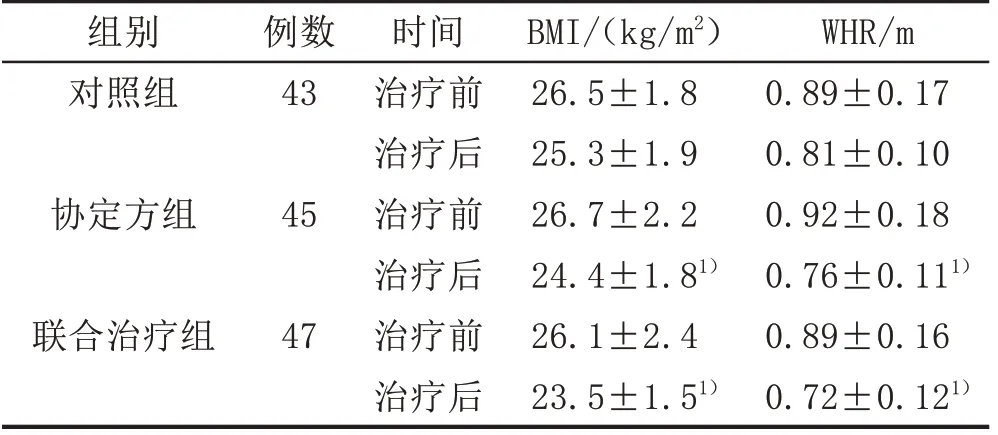
表4 3组NASH患者治疗前后BMI和WHR比较(±s)
注:与本组治疗前比较,1)P<0.05。
WHR/m 0.89±0.17 0.81±0.10 0.92±0.18 0.76±0.111)0.89±0.16 0.72±0.121)组别对照组例数43协定方组45联合治疗组47时间治疗前治疗后治疗前治疗后治疗前治疗后BMI/(kg/m2)26.5±1.8 25.3±1.9 26.7±2.2 24.4±1.81)26.1±2.4 23.5±1.51)
2.5 3 组患者治疗前后CAP 比较治疗后3 组CAP 显著低于治疗前,差异有统计学意义(P<0.05)。协定方组和联合治疗组CAP 下降幅度与对照组比较,差异有统计学意义(P<0.05);联合治疗组下降幅度大于协定方组,差异无统计学意义(P>0.05)。见表5。
表5 3组NASH患者治疗前后CAP比较(±s,dB/m)

表5 3组NASH患者治疗前后CAP比较(±s,dB/m)
注:与本组治疗前比较,1)P<0.05;与对照组比较,2)P<0.05。
组别对照组协定方组联合治疗组治疗后275.51±30.651)251.72±25.491)2)239.03±21.331)2)例数43 45 47治疗前297.88±41.62 289.23±39.18 291.32±38.51
2.6 3组患者不良反应比较 研究期间对照组和协定方组均未出现不良反应。联合治疗组1 例患者穴位敷贴处的皮肤微红,但无肌肤灼痛、瘙痒和皮肤起泡现象;2 例患者于开始敷贴治疗1~2 d 后出现大便溏薄,经评估后予以密切观察,未予特殊处理,随后症状缓解。
3 讨论
由于NASH 发病机制复杂以及缺乏公认的有效治疗方法,已成为临床面临的重大挑战[3,7]。上海市名中医陈建杰教授基于中医理论和长期临床实践,拟定的协定方具有健脾化痰、升清降浊和活血消积之功[4,5],本次研究结果证实了该方良好的效果,且联合穴位敷贴的疗效优于单用协定方组。中药敷贴可以通过腧穴对药物的吸收,使药物直接作用于经络系统,达到内病外治的目的[5,8]。穴位敷贴剂石菖蒲开窍宁神、化湿和胃;茵陈清利湿热、退黄疸;大黄泻下攻积、清热泻火、解毒、活血祛瘀。期门穴有治疗胸胁满痛、胁下积聚的作用,日月穴有缓解胀满、胁肋疼痛的作用,中脘穴有疏肝健脾、消积导滞的作用。药物与诸穴合用具有扶正祛邪、疏通经络气血、调整脏腑功能的功效。
临床常规检查无法准确确定肝脏脂肪变性的程度,需肝穿刺结合病理检查才能判断病情。由于肝活检存在创伤性,不易被患者接受,而肝纤维化脂肪肝一体化诊断检查仪(FibroScan CAP)在量化患者的肝脏脂肪变性和纤维化水平方面具有良好的准确性[9]。本次研究结果显示,CAP 应用于中医药治疗NASH 的临床试验,具有容易被患者接受、能够多次检测等优点。本次研究结果也显示协定方治疗和协定方联合穴位敷贴治疗能够较好地缓解患者症状,进一步验证了该方的临床作用。
综上所述,在协定方口服基础上联合协定制剂穴位敷贴,能够提高临床疗效。穴位敷贴疗法既可以发挥穴位刺激作用,又可以经过皮肤组织吸收药物有效成分,具有效果明确、操作简便的优势,能够发挥中医学“内病外治”的理论特色,适合在基层临床推广应用。
