电解液添加剂对高电压LiCoO2/C电池电化学性能的影响
2023-11-10常海涛
常海涛
(福建南平南孚电池有限公司,福建 南平 353000)
0 引言
电化学储能技术作为一种高效、清洁的能源转换技术,对解决快速增长的能源需求和日益突出的环境问题至关重要。锂离子电池凭借高能量密度、高电势、宽温域工作、无记忆效应和使用寿命长等优势,被广泛应用于各种领域,如通信、运输、储能和航空等[1]。
商业化正极材料的比容量低于负极材料,目前对正极材料的开发仍是锂离子电池的研究重点。已完成商业化进程的主要正极材料有钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、磷酸铁锂(LiFePO4)、三元材料(NCA、NCM)等[2-7]。其中,LiCoO2正极材料由于能量密度高、加工工艺窗口宽、循环稳定性优良等优势在便携式消费电子设备领域中占据了大部分市场。自1991年索尼公司首次实现锂离子电池的商业化应用以来,伴随着技术的不断改革创新,正极LiCoO2搭配负极石墨的电池体系的能量密度由最初的200 Wh/L(80 Wh/kg)跨越式提高至700 Wh/L(280 Wh/kg)。通过如Ti、Mg、Al等各类元素的掺杂,缓解LiCoO2在充电至高电压下的结构变化[8,9]。此外,通过表面包覆手段,高电压下过渡金属元素溶出、电解液分解所带来的表界面副反应等问题得到改善,LiCoO2电池的实际应用电压已由最初的4.2 V提高至4.45 V以上[10,11]。
尽管高电压LiCoO2电池在能量密度方面具有明显的优势,但是其在环境温度适应性上仍存在不少问题。在高温下充放电循环,正负极与电解液之间的副反应增加,引起材料结构变化并导致电池的内阻增加,从而影响锂离子电池的循环性能。因此改善高电压LiCoO2电池的高温循环性能有着重要意义。在电解液中加入功能添加剂被认为是改善锂离子电池在常温和高温下循环稳定性较经济有效的策略。然而,高电压LiCoO2电池(4.2 V以上)相比常规LiCoO2电池(4.2 V)的电化学反应更加复杂,对常规电压体系行之有效的电解液添加剂对高电压钴酸锂/石墨(LiCoO2/C)电池的改善效果可能一般。本文以高电压LiCoO2/C电池作为研究对象,选择不同的添加剂电解液,在常温及45 ℃高温充放电循环下,对比电池各方面电化学性能变化,包括充放电行为、循环性能以及阻抗等,探究电解液添加剂对高电压LiCoO2电池的作用机理。
1 实验部分
1.1 实验材料
电解液A和B在珠海生产,基础锂盐及溶剂由LiPF6/EC+PC+PP组成,A组电解液添加剂含有LiDFOB、FEC、PS、ADN,B组除以上四种添加剂外还添加了HTCN。从A组电解液得到的电池记为方案A,从B组电解液得到的电池记为方案B。
正极LiCoO2材料的适用电压范围为3.0~4.48 V,压实密度为4.1 g/cm3。负极为快充型人造石墨,压实密度为1.7 g/cm3。正负极活性材料参数如表1、表2所示。

表1 正极活性材料参数Table 1 Physical parameters of cathode material

表2 负极活性材料参数Table 2 Physical parameters of anode material
1.2 浆料、正负极片制备及卷芯制备
按照97∶2∶1的质量比分别称取LiCoO2正极材料、导电剂以及PVDF黏结剂,将材料放入搅拌锅中进行干粉混合,混合后加入适量NMP,并持续搅拌,制备得到黏度适宜的正极浆料。负极则按照94∶3∶3的质量比分别称取石墨、导电剂、水性黏合剂制作浆料。按照1.05的N/P设计比,进行正负极涂布,并使用相应的工艺参数对正负极片进行辊压和分切,得到正负极耳。通过焊接机对正负极耳进行焊接,并卷绕得到直径12 mm、高度5.4 mm的1254型卷绕电芯。接下来,将电芯送入烘箱烘烤24 h,以去除水分。烘烤结束后,分别注入A、B两种电解液并封口,然后进行高温老化。完成高温老化后,进行分容测试,最后完成1254型电池的制作,并进行相关测试。
1.3 电化学性能测试
使用深圳新威(Neware)电池测试系统,对电池进行不同倍率的充放电和循环测试,电压测试范围为3.0~4.48 V。充电模式采用恒流恒压的方式:在3.0~4.48 V,采用恒流限压充电;超过4.48 V时,采用恒压限流方式充电,截止电流为1.5 mA(0.02 C,1 C=75 mA)。倍率充电测试范围为0.2 C、0.5 C、1 C、2 C、3 C、4 C、5 C。在不同倍率的性能测试中,放电电流都采用0.2 C。交流阻抗测试采用上海辰华CHI760E电化学工作站进行,测试频率范围为0.01~100 kHz。
材料的形貌表征通过日本日立公司生产的Flex-1000Ⅱ型扫描电子显微镜(SEM)完成;设备配有X射线能量色散谱(EDX),可以对材料进行微区元素分布分析。
2 结果与讨论
2.1 电池首次库仑效率对比
在(25±2) ℃环境温度下,对比了方案A与方案B两组各50只电池化成、分容后的首次库仑效率,如表3所示。方案A中电池的首次库仑效率均值为86.57%,而在电解液中加入1,3,6-己烷三腈(HTCN)添加剂的方案B电池的首次库仑效率均值则达到了88.14%,这主要是由于HTCN添加剂具有高抗氧化性,并且与Co离子有强烈的相互作用。在化成充电过程中,HTCN添加剂在正极表面形成了稳定的CEI膜,从而提升了高电压LiCoO2/C电池的首次库仑效率[12]。
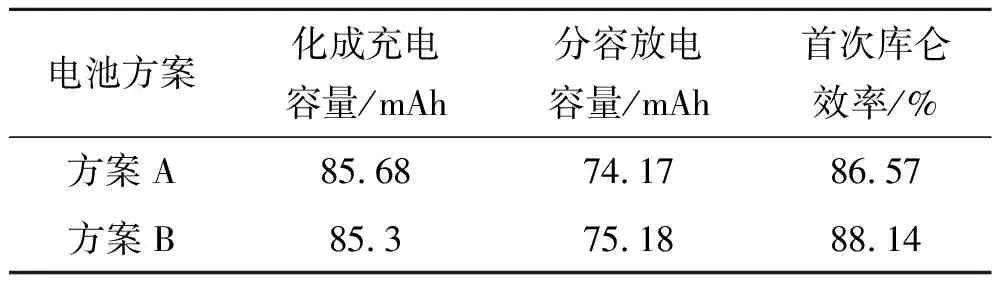
表3 方案A与方案B电池首次库仑效率对比Table 3 Comparison of the first coulombic efficiency for scheme A and B batteries
2.2 电池的倍率充电性能
将方案A与方案B电池以0.2~5 C电流进行恒流充电至4.48 V,之后以恒压充电至电流降低至0.02 C,静置2 h后,以0.2 C电流恒流放电至3.0 V,进行倍率充电性能对比。
如图1及表4所示,随着充电电流密度的增加,含有HTCN添加剂的高电压LiCoO2/C电池在电解液中表现出更高的恒流比和更小的极化现象。在5 C充电倍率下,与未添加HTCN组相比,电池的恒流比提高了12.34%。这表明HTCN添加剂的加入有助于高电压下锂离子的高速运输,并降低电池的极化现象[12]。

图1 方案A与方案B电池4 C、5 C倍率充电曲线对比Fig.1 Comparison of 4 C and 5 C charging curves for scheme A and B batteries

表4 方案A与方案B倍率充电性能恒流比对比Table 4 Comparison of constant current ratio of charging at different rates for scheme A and B
2.3 HTCN添加剂对高电压LiCoO2/C电池循环性能的影响
如图2所示,对比了常温下方案A与方案B电池3 C/0.5 C充放电的循环稳定性,经过300周循环后,方案A电池容量保持率仅为70.99%,而方案B电池容量保持率则高达86.32%。

图2 方案A与方案B常温下充放电循环性能Fig.2 Cycling performance of scheme A and scheme B at room temperature
如图3所示,通过SEM检测循环后的两组电池正极颗粒表面,可以观察到以下现象。方案A中电解液不含HTCN添加剂的电池正极颗粒表面有明显的裂纹[图3(a)],而方案B中添加HTCN添加剂的电池正极颗粒表面更为光滑,并且未发现有明显的裂纹[图3(b)]。这表明HTCN添加剂在高电压LiCoO2/C电池化成过程中所形成的CEI膜更加稳固,减少了高电压下电池内部各类副反应对正极颗粒的侵蚀,抑制了材料内部的损伤和裂纹产生,从而提高了电池的循环稳定性[13]。

图3 循环后LiCoO2颗粒SEM图像(a)方案A;(b)方案B Fig.3 SEM images of cycled LiCoO2 particles (a) scheme A and (b) scheme B
如图4所示,进一步对比在45 ℃高温环境下,方案A与方案B电池3 C/0.5 C充放电的循环稳定性。经过180周循环后,方案A电池容量保持率仅为68.96%,而方案B电池容量保持率则高达91.37%,并且发现,方案A电池的库仑效率已降低至57.15%,而方案B电池的库仑效率仍保持在接近100%的水平。通过对高温循环后脱锂状态下负极颗粒表面EDS扫描检测发现,方案A电池负极颗粒表面检测到Co的质量分数为0.44%,而方案B电池负极颗粒表面检测到Co的质量分数为0.11%,具体数据见表5。Co元素的溶出会导致正极结构的坍塌、电解质盐的不断分解以及正极CEI膜和负极SEI膜的不断破裂和生长。这些因素是导致方案A电池在高温下循环寿命严重衰减的主要原因。这进一步证明了HTCN添加剂能够有效地在正极颗粒表面与电解液之间形成稳固的电极-电解质界面,从而减少高温高压循环下Co离子的溶出[14,15]。

图4 方案A与方案B在45 ℃下充放电循环性能Fig.4 Cycling performance of scheme A and scheme B at 45 ℃

表5 方案A与方案B在45 ℃循环后负极颗粒表面元素含量EDS对比分析Table 5 EDS comparison of surface elements of anode particles for scheme A and B after cycling at 45 ℃
2.4 阻抗分析
进一步对比两组电池在45 ℃高温循环后的阻抗。其中,Rs是由电极材料、集流体以及隔膜等构成的接触电阻,即欧姆电阻;RSEI与C1分别表示Li+穿过SEI膜的阻抗和电容;Rct及C2分别代表电荷转移电阻和双电层电容。由图5及表6数据可看出,两组电池在45 ℃循环前的欧姆电阻Rs没有明显区别。然而,方案A电池在45 ℃循环失效后,接触电阻Rs的增加幅度明显高于方案B电池。这意味着在高温充放电循环过程中,方案A电池的正极材料受到破坏,导致颗粒之间接触不良,从而使接触电阻大幅增加。

图5 45 ℃循环前后方案A和方案B电池阻抗图谱(内嵌图为等效电路图)Fig.5 Impedance spectra of scheme A and scheme B before and after cycling at 45 ℃(the embedded diagram is equivalent circuit diagram)

表6 方案A与方案B 45 ℃循环前后电化学阻抗数据Table 6 Electrochemical impedance data of scheme A and B before and after cycling at 45 ℃
同时,方案A电池在高温循环后RSEI的增加幅度明显大于方案B电池。这说明经过高温循环后,方案A电池的正负极与电解液之间发生的副反应较多,表面形成的CEI膜及SEI膜增厚,导致阻抗大幅增大。另外,在高温循环后,方案B电池的Rct阻抗增加幅度(269 mΩ)也小于方案A电池的Rct阻抗增加幅度(378 mΩ)。这表明HTCN添加剂能优化界面,使其形成的界面膜具有低阻抗和高稳定性的特点,从而减少高温循环过程中对界面和材料结构的破坏[16-18]。
3 结论
通过对两组电池常温循环后的扫描电镜观察、高温循环后负极颗粒表面的EDS测试以及电化学阻抗对比,分析结果表明:在4.48 V高电压LiCoO2/C电池体系中,HTCN添加剂的加入能够有效提升电池在常温及高温下的循环稳定性。HTCN能够在高电压钴酸锂电极表面形成稳定的电极-电解质界面,有效减少常温循环下因LiCoO2材料电极表面的裂纹引起的电解液与界面的副反应,以及高温循环下Co离子溶出。这样可以提高高压LiCoO2电池的电化学性能,对开发具有长循环寿命的高电压和高温LiCoO2/C电池具有重要的研究价值。
