阳离子交换树脂催化合成乳酸甲酯动力学研究
2023-11-10项文雨刘春江张青军
刘 辉,刘 鑫,项文雨,郭 凯,刘春江, ,张青军
阳离子交换树脂催化合成乳酸甲酯动力学研究
刘 辉1, 2,刘 鑫1, 2,项文雨1, 2,郭 凯1, 2,刘春江1, 2, 3,张青军3
(1. 天津大学化工学院,天津 300350;2. 化学工程联合国家重点实验室(天津大学),天津 300350;3. 天津大学浙江绍兴研究院,绍兴 312300)
工业化生产乳酸甲酯需要特定催化剂的动力学数据进行模拟计算.本文研究了在大孔阳离子交换树脂DA330的催化作用下,乳酸和甲醇生成乳酸甲酯的反应动力学.乳酸甲酯是一种重要的化工生产基础原料,多用来作为合成香料和农药的原料.随着化石能源紧缺和环保要求提高,具有可降解和可再生特性的乳酸甲酯及其高聚物的需求也在与日俱增.乳酸甲酯的连续化生产是提高乳酸甲酯产量的关键,具有广阔的研究前景.采用固体大孔阳离子交换树脂代替传统浓硫酸作为催化剂,需要对动力学方程进行重新测定.本文针对乳酸甲酯反应体系外扩散影响、内扩散影响、酯化反应动力学、水解反应动力学分别进行了实验.采用气相色谱对反应体系中的乳酸甲酯含量进行测定.研究发现内、外扩散在实验条件范围内对反应速率无明显影响:以酯化反应为例,搅拌转速达400r/min以上时体系内催化剂颗粒悬浮程度达到峰值,外扩散不影响酯化反应速率;在催化剂颗粒悬浮程度达到峰值之后,催化剂粒径大小不影响酯化反应速率.反应温度在实验范围内对反应速率呈现显著的正相关影响,酯化和水解实验数据拟合均符合Quasi-Homogeneous模型,最终得到DA330催化条件下的反应动力学.
乳酸甲酯;阳离子交换树脂;固体催化剂;动力学研究
乳酸甲酯作为一种羟基酯类化合物,结构中存在羟基和酯基,是一种重要的化工生产基础原料,多用来香料合成及农药生产.作为绿色溶剂,其在制药工业、食品工业以及日化工业等领域具有广阔的应用前景[1-2].工业上合成乳酸甲酯的主要方法是通过浓硫酸催化乳酸和甲醇进行酯化反应,由于乳酸本身的特殊结构及反应温度的影响,乳酸分子易发生分子内脱水碳化反应,最终导致产物收率较低、产品色泽不均,伴随着三废增多的问题[3-4].
近几年用于生产乳酸烷基酯新型催化剂的研究已趋于成熟[5],如固体超强酸[6]、多元催化剂[7-8]、苯乙烯磺酸[9]、复合Louis酸[10]以及生物酶[11]等.但这些催化剂对乳酸甲酯的催化效果并不理想.甲醇分子羟基比例大,相较于其他低级醇,与水和乳酸形成的氢键会更多[12].通过拉曼光谱对甲醇-水体系进行观察:甲醇体积分数超过0.4时,水的四面体结构被甲醇彻底破坏进一步形成大量氢键[13-14].工业用乳酸中含有20%~25%的水,在和甲醇反应生成乳酸甲酯过程中,大量的氢键会影响反应速率及收率.实验表明,在无合适带水剂的情况下,乳酸甲酯的收率只有50%~60%,其他低级醇(C2~5)与乳酸酯化反应较快,且无需带水剂的添加[15].反应精馏可在一定程度上解决此问题,为了正确设计反应精馏塔,需要进行动力学实验.
用甲醇和乳酸作为原料生产乳酸甲酯的化学方程式为

Sanz等[16]以Amberlyst15为催化剂,用Quasi-Homogeneous(Q-H)、Langmuir-Hinshelwood(L-H)和Eley-Rideal(E-R) 3种模型对实验数据拟合并比较.发现Q-H模型拟合出的结果最能反映Amberlyst15对乳酸甲酯酯化和水解反应的催化作用.Jiang等[17]通过D001催化剂研究了乳酸甲酯的反应动力学,分析了搅拌速度、催化剂尺寸、原料初始摩尔比和温度对反应过程的影响,并采用拟均相模型对实验数据进行了关联,得到了对应的动力学方程.孔倩等[18]通过计算机流程模拟,研究乳酸进料过量时反应精馏合成乳酸甲酯的整体流程,得到了最优化的反应条件.
本文考虑工业乳酸中水对反应系统的影响,提出甲醇酯化工业乳酸的表观动力学模型,为后续拟开展的模拟研究提供数据支持.采用DA330大孔强酸性阳离子交换树脂作为催化剂,无需脱水剂,通过工业乳酸(含水量20%)与甲醇进行反应,测定不同温度下的乳酸甲酯生成速率,得到正反应表观动力学模型;关联乳酸甲酯不同温度下的水解速度,得到逆反应动力学模型.此工作对于乳酸甲酯实际工业生产具有一定的指导作用.
1 实 验
1.1 主要仪器和试剂
主要仪器和试剂见表1,DA-330树脂催化剂理化指标见表2.
表1 主要仪器及试剂

Tab.1 Main instruments and reagents
表2 DA-330树脂催化剂理化指标
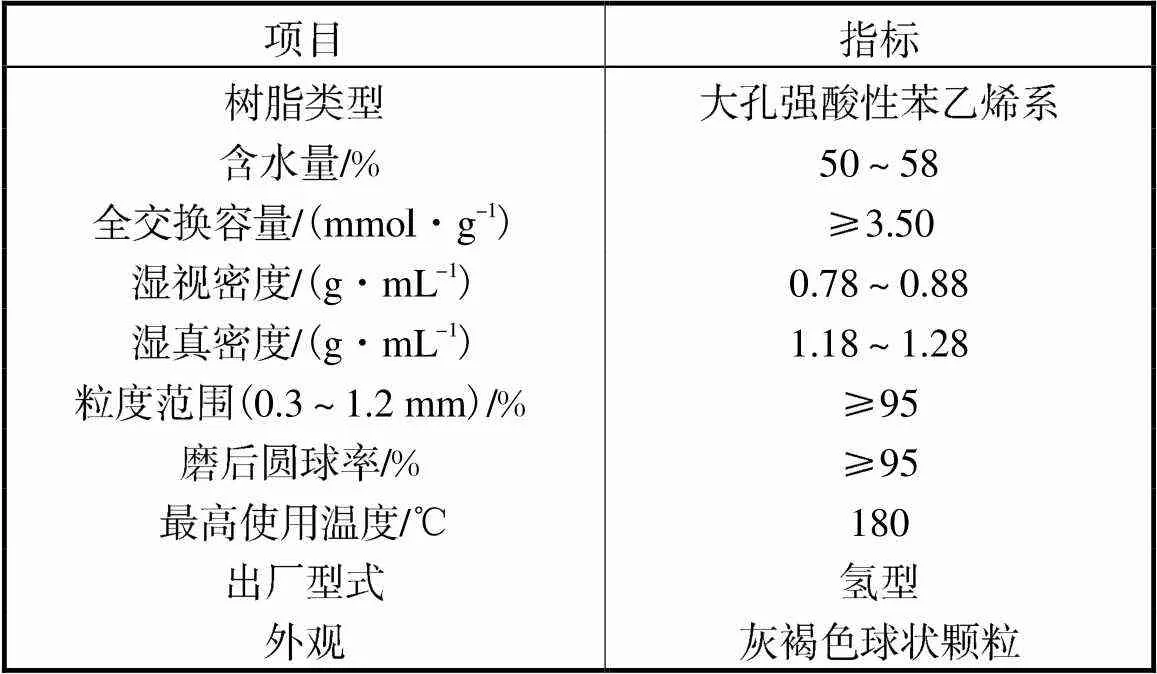
Tab.2 Physical and chemical indexes of DA-330 resin catalyst
1.2 气相色谱条件
参考于文涛等[19]对乳酸甲酯气相色谱分析条件,本实验采用的气相色谱型号为950FID型气相色谱,分离柱为长30m、内径为0.25mm的PEG毛细管色谱柱;氢火焰检测器,氢气发生器输出流量为40mL/min;检测室温度为180℃;气化室温度为180℃;为了保证内标物环己酮和乳酸甲酯无交叉峰,设定为程序升温:进样开始,柱温80℃维持4min,1min内升温至90℃保持不变.经检验,该方法可使环己酮和乳酸甲酯分离干净.
1.3 内标曲线的确定
为了准确测定出样品中乳酸甲酯的含量,采用内标法对样品进行处理.利用环己酮作为内标物,得到与乳酸甲酯相关联的内标曲线[20]:
(1) 称取4.018g(0.04mol)环己酮、4.019g(0.04mol)乳酸甲酯分别放入两个100mL容量瓶,甲醇作为溶剂加至100mL;
(2) 用1mL移液管取1mL环己酮溶液分别移入5个5mL容量瓶内,再分别取0.5mL、1.0mL、1.5mL、2.0mL、2.5mL的乳酸甲酯溶液放入上述5支容量瓶中,加甲醇至5mL,得到标准液;
(3) 将5份标准液用气相色谱分析,得到的曲线如图1所示.

图1 环己酮-乳酸甲酯内标曲线
拟合得到的内标曲线为
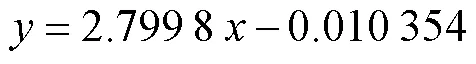


1.4 实验步骤
以酯化反应为例介绍实验步骤如下.
(1) 催化剂与乳酸倒入四口烧瓶内,催化剂添加量占乳酸质量1.5%,插入温度计和冷凝管后密封进料口,甲醇倒入锥形瓶内并密封.
(2) 甲醇和乳酸分别置在水浴锅中预热,冷凝管通水.
(3) 温度稳定后,将锥形瓶中的甲醇倒入四口烧瓶中与乳酸混合,实验装置如图2所示.开启搅拌,并开始计时.以此作为反应的起始时间,每隔一段时间对反应液取样,用气相色谱仪器分析各组分的变化.
检测方法:实验前配置好一定浓度的环己酮标准溶液,用取样器取0.5mL反应器内混合液与0.5mL环己酮标准溶液进行混合,用气相色谱分析混合液的组成,通过内标曲线求解乳酸甲酯的量.

图2 实验装置
2 结果与讨论
阳离子树脂固体作为催化剂的反应可分为拟均相和非均相反应.理想的均相状态要求树脂在液相中完全膨胀,且和聚合物结合的磺酸基团完全解离.非均相的特征是底物和树脂上的磺酸基团直接相互作用[17].本实验不考虑传质阻力,反应速率模型采用拟均相模型进行表示.整个催化过程视为催化剂内部的均相催化,其中反应物、产物和溶剂在液相体系中处于分布平衡.
为了验证无内、外传质阻力的影响,先进行外扩散和内扩散实验.
2.1 外扩散影响
外扩散研究的是搅拌速度对反应转化率的影响,搅拌速度会影响催化剂颗粒在液体中的悬浮程度.以酯化反应为例,实验取工业乳酸56.3g(乳酸0.5mol)和甲醇16g(0.5mol),催化剂0.675g,水浴温度为333K,分别测转速为0r/min、100r/min、200r/min、300r/min、400r/min时反应器内乳酸甲酯的浓度D(mol/L)变化,记录其随时间变化数据,如图3所示.
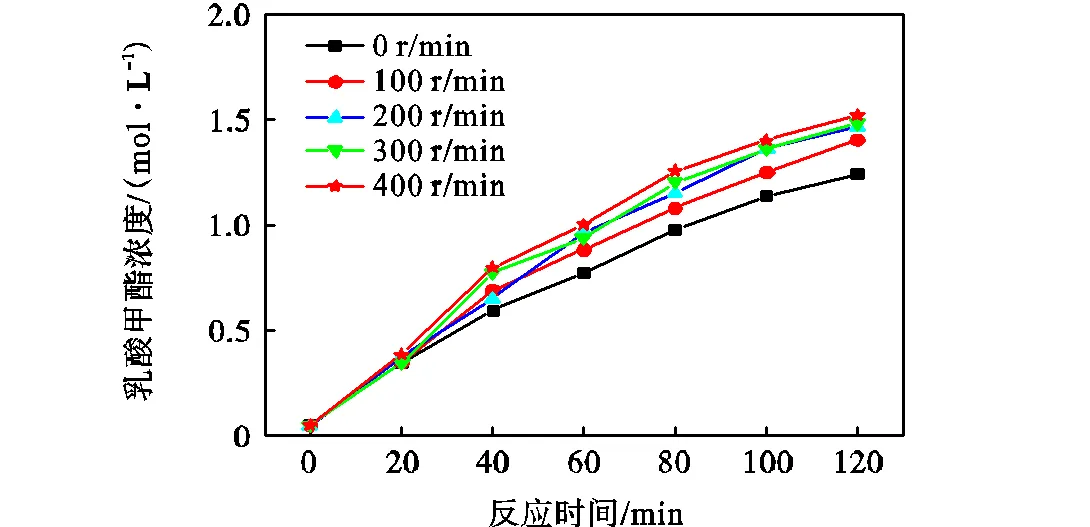
图3 不同转速条件下乳酸甲酯浓度随时间的变化
Chakrabarti等[21]指出对于离子交换树脂参与的催化反应,除非存在体系黏度较高或者搅拌速度很低的情况,否则催化过程中外扩散一般不会影响反应的总速率.对于乳酸甲酯体系,当反应器搅拌速度在400~900r/min范围内,外扩散对反应速率不存在影响[16].由图3可知,在≤400r/min条件下,不同转速下产物浓度随反应时间变化存在差异,验证了低转速搅拌过程中存在传质阻力.随着转速的增加,催化剂颗粒悬浮程度越充分,外部传质阻力减小.搅拌速度400r/min与300r/min对酯化反应速率的影响较为接近,此后所有实验均在400r/min的条件下进行.
2.2 内扩散影响
实验可用催化剂粒径范围为0.3~1.2mm,反应温度333K,反应物添加量与外扩散实验一致,转速固定(400r/min),将催化剂颗粒按粒径分为>0.8mm、0.4~0.8mm、<0.4mm 3组进行反应,测定不同时刻的乳酸甲酯浓度D,如图4所示.
由图4中可以看出,粒径0.8mm以下时,乳酸甲酯浓度与反应时间的关系曲线的斜率基本一致,不同催化剂尺寸下的反应速率在95%置信水平上最大偏差不超过10%,无显著差异.说明在本实验催化剂粒径范围内,内扩散对该反应的反应速率无明显影响,内部传质阻力可以忽略不计.该结论与文献[16]的观点一致.此后所有实验均采用混合粒径的催化剂颗粒.
2.3 酯化反应动力学
实验测定不同温度下的反应速率,取工业乳酸56.3g(乳酸0.5mol)和甲醇16g(0.5mol),混合粒径(0.3~1.2mm)催化剂0.675g,搅拌转速为400r/min,测定333K、343K、353K、363K条件下反应器内不同时刻的乳酸甲酯浓度D,如表3所示.生成的乳酸甲酯浓度与初始乳酸浓度比值即为对应时刻的酯化转化率,处理后得表4.
表3 不同温度下酯化反应D-关系

Tab.3 CD-t at different temperatures
表4 不同温度下乳酸甲酯酯化转化率

Tab.4 Esterification conversion rate of methyl lactate at different temperatures
根据Sanz等[16]的研究,乳酸甲酯的酯化反应适用于Q-H动力学模型,忽略吸附对反应速率的影响,则乳酸甲酯生成动力学模型可表示为


反应初期,乳酸甲酯含量比较小,逆反应可忽略.因此动力学模型可表示为

根据Sanz等[16]以及Jiang等[17]对乳酸甲酯进行的动力学研究,乳酸甲酯的酯化反应为二级可逆反应,且==1,反应过程中乳酸浓度和甲醇浓度相等,故A=B,则式(5)可以简化为

根据化学反应计量式有
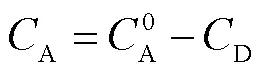
将式(7)代入式(6)后积分可得

将式(7)带入式(8),有
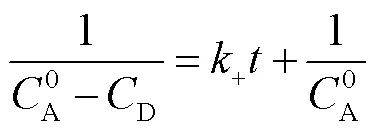

图5 不同温度下-t关系
根据阿伦尼乌斯方程,有
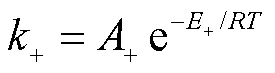
式中:+为酯化反应活化能;+为酯化反应阿伦尼乌斯因子;为摩尔气体常数.
式(10)两边同时取对数,有
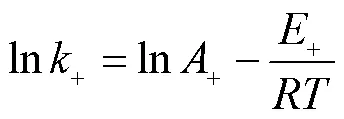
表5 不同温度下的+值

Tab.5 k+ values at different temperatures
图6中通过最小二乘法回归得到的直线斜率为 -5.89×103,截距为12.987,曲线拟合度2为0.9891.故酯化反应活化能为
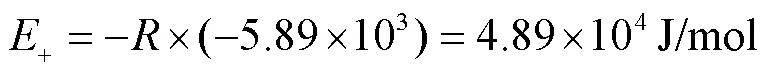
酯化反应的阿伦尼乌斯因子为
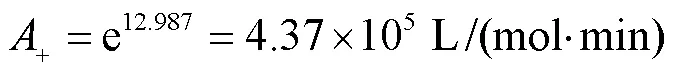
进一步可得酯化反应动力学方程为
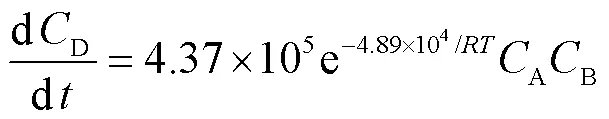

图6 酯化反应的阿伦尼乌斯关系图
2.4 水解反应动力学
在第2.1节外扩散实验中提到酯化反应条件下,400~900r/min范围内转速对反应转化率无影响,证明此时催化剂悬浮程度已到达峰值,故在此范围外扩散对水解反应也应该无影响.第2.2节内扩散实验结论指出不同粒径催化剂对于酯化反应速率不存在影响,酯化反应和水解反应均通过催化剂的酸性位点进行催化,因此水解反应速率同样不受催化剂粒径影响.
取乳酸甲酯52.05g(0.5mol)和蒸馏水9g(0.5mol),混合粒径(0.3~1.2mm)催化剂0.675g,搅拌转速为400r/min,测定333K、343K、353K、363K条件下反应器内不同时刻的乳酸甲酯浓度D,如表6所示.消耗的乳酸甲酯浓度与初始乳酸甲酯浓度比值即为对应时刻的水解转化率,处理后得 表7.
反应初期,乳酸含量比较小,忽略酯化反应.因此动力学模型(4)可简化为
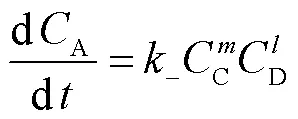
根据Sanz等[16]以及Jiang等[17]对乳酸甲酯进行的动力学研究,乳酸甲酯的水解反应同样为二级可逆反应,且==1,反应过程中乳酸甲酯添加量和蒸馏水相等,则C=D,则

积分可得
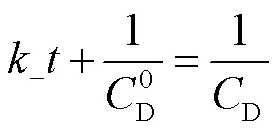
表6 不同温度下水解反应D-关系
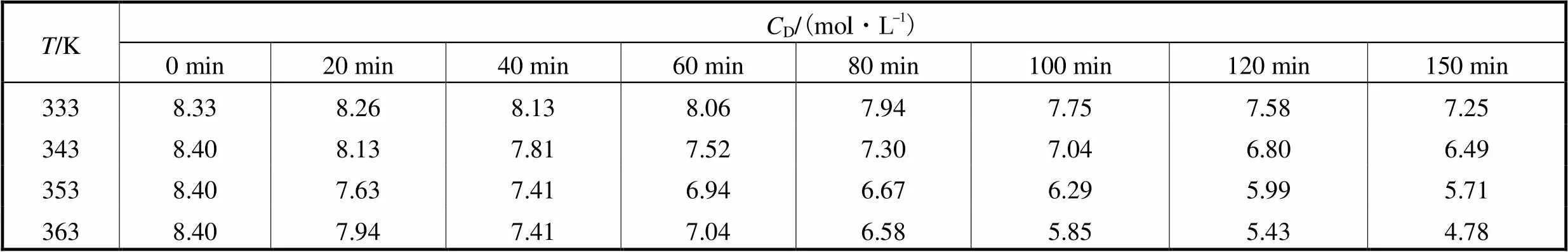
Tab.6 CD-t in the hydrolysis reaction at different temperatures
表7 不同温度下乳酸甲酯水解转化率

Tab.7 Hydrolysis conversion rate of methyl lactate at different temperatures
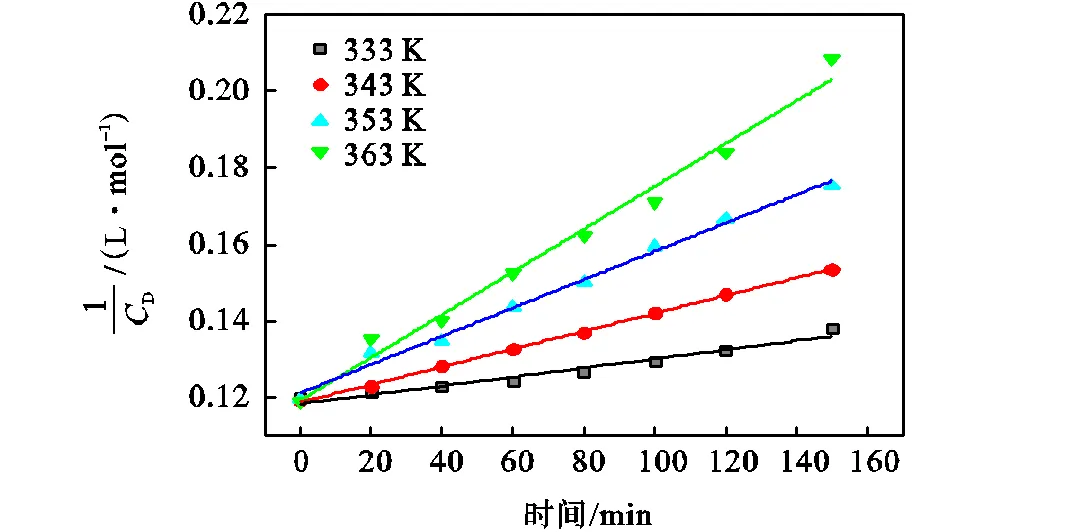
图7 不同温度下-t关系
根据阿伦尼乌斯方程,有
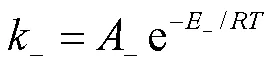
式中:-为水解反应活化能;-为水解反应阿伦尼乌斯因子. 式(18)两边同时取对数,有

表8 各温度下的-值

Tab.8 k-values at different temperatures
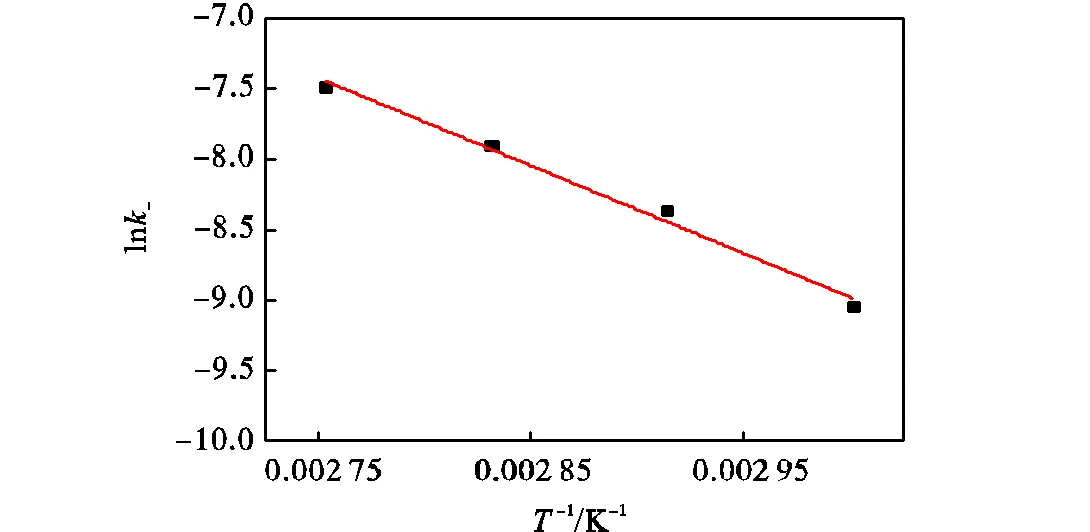
图8 水解反应的阿伦尼乌斯关系图
图8中由最小二乘法回归得到的直线斜率为 -6.23×103,截距为10.908,曲线拟合度2为0.9911.则水解反应的活化能为

水解反应的阿伦尼乌斯因子为
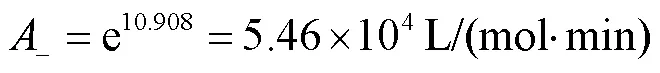
水解反应动力学方程为
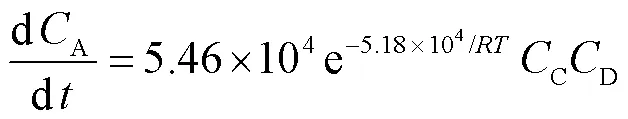
在处理酯化和水解实验数据过程中,有对应的逆反应可忽略的假设,因此应尽量取反应前期的数据点来满足数据处理要求,不需要长时间反应以达到平衡.
对于乳酸甲酯体系,酯化和水解反应同时存在,只是反应程度不同.分开处理的酯化和水解动力学方程在满足假设要求的取点方法下,能够消除对应逆反应的影响,所得到动力学方程具有一定的可行性. 在反应温度、催化剂用量和搅拌转速相同的条件下,可将对应的酯化动力学方程和水解动力学方程合并.结合乳酸甲酯的酯化动力学方程(14)和水解动力学方程(22)可得完整的动力学方程,即为
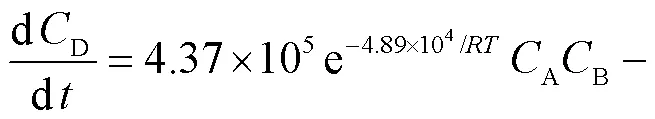

3 结 语
本文研究了含水乳酸与甲醇在阳离子交换树脂DA330催化下的酯化反应表观动力学.研究发现400r/min以上的转速能消除外扩散影响;不同粒径催化剂不存在内扩散影响;反应速率随着温度的增加而增加.在DA330存在条件下,酯化反应动力学活化能为48.9kJ/mol、水解反应活化能为51.8kJ/mol,酯化和水解实验数据根采用Q-H模型进行拟合,得到了拟合程度较好的动力学方程:
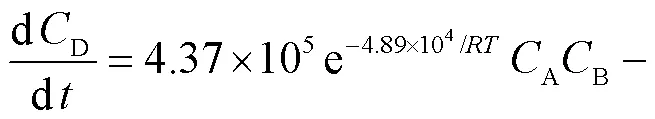
本文的研究结果可为后续乳酸甲酯反应精馏塔或相应反应器的设计等提供依据与参考.
[1]Sanz M T,Murga R,Beltrán S,et al. Autocatalyzed and ion-exchange-resin-catalyzed esterification kinetics of lactic acid with methanol[J]. Industrial & Engineering Chemistry Research,2002,41(3):512-517.
[2]Delgado P,Sanz M T,Beltrán S. Kinetic study for esterification of lactic acid with ethanol and hydrolysis of ethyl lactate using an ion-exchange resin catalyst[J]. Chemical Engineering Journal,2007,126(2/3):111-118.
[3]Liu Xilei,Xu Ling,Wang Juncheng,et al. New insights into the NiO catalytic mechanism on the conversion of fructose to methyl lactate[J]. Catalysis Communications,2019,119:46-50.
[4]Lu X,Wang L,Lu X. Catalytic conversion of sugars to methyl lactate over Mg-MOF-74 in near-critical methanol solutions[J]. Catalysis Communications,2018,110:23-27.
[5]沈介发,张 跃,严生虎,等. 乳酸甲酯的合成研究[J]. 江苏化工,2007,35(5):37-39.
Shen Jiefa,Zhang Yue,Yan Shenghu,et al. Study on the synthesis of lactic acid methanol ester[J]. Jiangsu Chemical Industry,2007,35(5):37-39(in Chinese).
[6]Fan Guodong,Shen Mao,Zhang Zhao,et al. Preparation,characterization and catalytic properties of S2O82-/ ZrO2-CeO2solid superacid catalyst[J]. Journal of Rare Earths,2009,27(3):437-442.
[7]Li K T,Wang C K,Wang I,et al. Esterification of lactic acid over TiO2-ZrO2catalysts[J]. Applied Catalysis A:General,2011,392(1/2):180-183.
[8]Duan Ying,Luo Qianqian,Nie Renfeng,et al. Catalytic conversion of glycerol to methyl lactate over Au-CuO/Sn-beta:The roles of Sn-beta[J]. Catalysts,2022,12(1):104.
[9]Nigiz F U,Hilmioglu N D. Ethyl lactate synthesis by catalytic membranes in a pervaporation assisted membrane reactor[J]. Chemical Engineering & Technology,2018,41(4):836-844.
[10]Tominaga K,Nemoto K,Kamimura Y,et al. Synthesis of methyl lactate from cellulose catalyzed by mixed Lewis acid systems[J]. Fuel Processing Technology,2020,199:106288.
[11]Wang Yilong,Xu Shan,Li Renqiang,et al. Characterization of one novel microbial esterase WDEst9 and its use to make L-methyl lactate[J]. Biocatalysis and Biotransformation,2019,37(3):190-200.
[12]Aparicio S. Computational study on the properties and structure of methyl lactate[J]. The Journal of Physical Chemistry A,2007,111(21):4671-4683.
[13]杨 博. 拉曼光谱法研究典型有机分子-水二元溶液中的氢键作用[D]. 长春:吉林大学物理学院,2020.
Yang Bo. Study of Hydrogen Bonding in Typical Organic-Water Binary Solutions by Raman Spectroscopy[D]. Changchun:School of Physics,Jilin University,2020(in Chinese).
[14]Sidsel D,Jens H,Jay A,et al. Intramolecular hydrogen bonding in methyl lactate[J]. The Journal of Physical Chemistry A,2015,119(37):9692-9702.
[15]苏 涛,庞 起. C1~5醇乳酸酯及丙交酯制备的初步研究[J]. 化工时刊,1999(4):7-12.
Su Tao,Pang Qi. Preparation of lactates of C1—C5alcohols and further preparing lactide from them[J]. Chemical Industry Journal,1999(4):7-12(in Chinese).
[16]Sanz M T,Murga R,Beltràn S,et al. Kinetic study for the reactive system of lactic acid esterification with methanol:Methyl lactate hydrolysis reaction[J]. Industrial & Engineering Chemistry Research,2004,43(9):2049-2053.
[17]Jiang Shaotong,Liu Mo,Pan Lijun. Kinetic study for hydrolysis of methyl lactate catalyzed by cation-exchange resin[J]. Journal of the Taiwan Institute of Chemical Engineers,2010,41(2):190-194.
[18]孔 倩,陆佳伟,王 琼,等. 乳酸过量进料反应精馏合成乳酸甲酯研究[J]. 高校化学工程学报,2021,35(2):280-286.
Kong Qian,Lu Jiawei,Wang Qiong,et al. Study on reactive distillation process for synthesis of methyl lactate with overfeeding[J]. Journal of Chemical Engineering of Chinese Universities,2021,35(2):280-286(in Chinese).
[19]于文涛,施海峰,黄 和,等. 乳酸甲酯脱水体系中丙烯酸甲酯的气相色谱分析[J]. 理化检验-化学分册,2006,42(12):1029-1031.
Yu Wentao,Shi Haifeng,Huang He,et al. Gas chromatographic analysis of the dehydration system of methyl lactate for its methyl acrylate content[J]. Physical Testing and Chemical Analysis(Part B:Chemical Analysis),2006,42(12):1029-1031(in Chinese).
[20]张兰平,王印堂. 乳酸乙酯的气相色谱分析[J]. 河北师范大学学报(自然科学版),1991(1):75-76.
Zhang Lanping,Wang Yintang. Analysis of ethyl lactate by gas chromatography[J]. Journal of Hebei Normal University(Natural Science),1991(1):75-76(in Chinese).
[21]Chakrabarti A,Sharma M M. Cationic ion exchange resins as catalyst[J]. Reactive Polymers,1993,20(1/2):1-45.
Kinetic Study on the Synthesis of Methyl Lactate Catalyzed by Cation Exchange Resin
Liu Hui1, 2,Liu Xin1, 2,Xiang Wenyu1, 2,Guo Kai1, 2,Liu Chunjiang1, 2, 3,Zhang Qingjun3
(1. School of Chemical Engineering and Technology,Tianjin University,Tianjin 300350,China;2. State Key Laboratory of Chemical Engineering,Tianjin University,Tianjin 300350,China;3. Zhejiang Shaoxing Institute of Tianjin University,Shaoxing 312300,China)
The modeling of the commercial synthesis of methyl lactate requires kinetic data for particular catalysts. In this study,the reaction kinetics of the production of methyl lactate from lactic acid and methanol catalyzed by macroporous cation exchange resin DA330 was investigated. Methyl lactate is a key fundamental raw material for synthetic fragrances and pesticides. With the shortage of fossil energy and the increase in environmental protection requirements,the need for methyl lactate and its polymers with degradable and renewable properties is also increasing. The continuous production of methyl lactate is the key to improving the yield of methyl lactate and has broad research prospects. The use of solid macro-porous cation exchange resin as a catalyst rather than traditional concentrated sulfuric acid necessitates a redetermination of the kinetic equations. In this study,the reaction system’s external diffusion effect,internal diffusion effect,esterification reaction kinetics,and hydrolysis reaction kinetics were all tested. The methyl lactate content in the reaction system was determined by gas chromatography. It was found that in the experiment,the effect of internal and external diffusion on the reaction rate can be ignored. For example,in the esterification reaction,when the stirring speed exceeds more than 400r/min,the suspension degree of catalyst particles in the system reaches a peak,and external diffusion has no effect on the esterification reaction rate. After the suspension degree of catalyst particles reaches the peak,the size of the catalyst particle size does not affect the esterification reaction rate. The reaction rate was significantly positively impacted by the reaction temperature. The fitting of esterification and hydrolysis experimental data was consistent with the Quasi-Homogeneous model. Finally,the reaction kinetics under DA330 catalytic conditions were obtained.
methyl lactate;cation exchange resin;solid catalyst;kinetic study
the National Natural Science Foundation of China(No.21706182,No.21706187),the Natural Science Foundation of Tianjin,China(No.21JCQNJC00470).
10.11784/tdxbz202210010
O643.11
A
0493-2137(2023)12-1227-08
2022-10-11;
2022-12-22.
刘 辉(1982— ),男,博士,讲师.Email:m_bigm@tju.edu.cn
刘 辉,hui.liu@tju.edu.cn.
国家自然科学基金资助项目(21706182,21706187);天津市自然科学基金资助项目(21JCQNJC00470).
(责任编辑:田 军)
