食管癌螺旋CT征象与癌组织中EGFR、PCNA表达间的关系
2023-11-10牛莎莎张文涛
牛莎莎 王 力 张文涛
作者单位:466200 河南省项城市中医院
食管癌是常见消化系统恶性肿瘤,具有较高的病死率,但其早期症状并不典型,难以发现,大部分患者就诊时已发展到中晚期[1]。目前临床针对食管癌治疗方式主要为手术切除,并给予放疗、化疗等新辅助疗法,但有研究表明,食管癌患者的预后受肿瘤分化程度的影响,术前准确评估病变部位及长度,明确肿瘤分化程度是提高手术切除率并延长患者生存时间的重要保障[2]。随着影像技术的的发展,螺旋CT成为食管癌术前检查的常用手段,其具备良好的空间重建能力及组织对比度,可从不同方位对病变部位进行快速扫描,为术前病理分期的诊断提供较为全面的信息[3]。表皮生长因子受体(epidermal growth factor receptor,EGFR)是原癌基因的表达产物之一,可促进组织细胞的增殖分化;增殖细胞核抗原(proliferating cell nuclear antigen,PCNA)是细胞增殖合成及表达中的关键因子,二者的过度表达与机体组织细胞的增殖和癌变密切相关[4]。本研究将螺旋CT征象与肿瘤分子生物学指标相结合,从细胞增殖分化的角度,分析食管癌患者的螺旋CT征象与EGFR、PCNA表达间的关系,旨在为临床术前准备诊断食管癌肿瘤分化程度提供参考依据。
1 资料与方法
1.1 一般资料
选取我院2018年10月至2021年10月诊治的110例食管癌患者作为研究对象,其中男性59例,女性51例;年龄35~80岁,平均年龄(56.32±14.17)岁。纳入标准:临床表现符合《食管癌规范化诊治指南》的诊断标准[5];均进行螺旋CT增强扫描;CT检查后2周内行食管癌肿瘤切除手术;术前未进行放疗或化疗;经术后食管病理活检证实为食管癌;患者及其家属知情同意。排除标准:伴甲状腺功能亢进者;合并严重心血管疾病、肝肾功能不全或自身免疫性疾病;碘试剂过敏者。
1.2 方法
螺旋CT检查:运用64排螺旋CT(德国西门子,SOMATOM Definition AS),设置参数:设定螺旋模式,电压120 kv、电流35 mAs,窗位WW/WL:350/50,FOV 330 mm,螺距0.86,图像重建层厚0.6 mm,轴位矩阵设为512×512。患者取仰卧位,检查前指导患者进行屏气及吸气训练,扫描范围自颈部至胃底平面。增强扫描,用高压注射器经肘前静脉注入对比剂碘海醇(北京北陆药业股份有限公司,H19980036),对比剂用量2 ml/kg,流速3 ml/s,扫描延迟时间70~80 s。
EGFR、PCNA检测:手术切除标本经常规脱蜡水化后,采用免疫组化法进行染色及阳性检测,采用DAKO EnVision显色系统进行细胞计数的测定。EGFR阳性标准[6]:镜下随机选择5个高倍视野,阳性信号为细胞质内出现棕黄色颗粒,若阳性细胞比例≥25%则为阳性,反之为阴性。PCNA阳性标准[7]:于高倍镜下计数400个癌细胞,阳性信号为细胞核内出现棕黄色颗粒,若阳性细胞比例≥50%则为阳性,反之为阴性。
1.3 图像分析
所得图像均由2名专业影像学诊断医师采取双盲法阅片并进行图像处理,选择最大扫描层面划取感兴趣区,找出病灶位置,测量病灶长度、管壁增厚情况,记录CT值。食管癌CT诊断标准[8]:病变食管管壁厚度>5 mm;呈环状或局部管壁增厚;增强扫描后呈均匀强化,若肿块坏死则表现为不均匀强化;管壁短径≥10 mm,且局部出现密度不均的软组织结节影即为淋巴结转移。
1.4 统计学方法
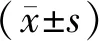
2 结果
2.1 病理检查结果
110例食管癌患者中鳞状细胞癌94例,腺癌16例;斑块型56例,糜烂型35例,隐伏型14例,乳头型5例;低分化36例,中分化49例,高分化25例。
2.2 螺旋CT征象
经轴位扫描后可见110例均存在病变部位管腔增粗,局部管壁不均匀增厚49例,环形增厚32例,管腔内局部肿块29例;病灶位置:食管上段26例,食管中段56例,食管下段18例,食管胃交界处10例;管腔轻度狭窄21例,中度狭窄37例,重度狭窄47,管腔闭塞5例;病变长度10~80 mm;增强扫描后可见不均匀强化86例,均匀强化13例,未见强化9例;冠状及矢状位重建图像可见病变食管出现软组织肿块,层次结构消失,狭窄部位上方或下方食管扩张,32例出现局部浸润。淋巴结远处转移51例,无远处转移59例;侧边冠状位清晰可见食管全长、肿瘤部位及大小、管腔狭窄情况及与周围组织的边界关系。
2.3 食管癌患者螺旋CT征象与EGFR、PCNA表达的关系
食管癌患者EGFR阳性表达率为71.82%(79/110),PCNA阳性表达率为65.45%(72/110)。病变长度>50 mm者EGFR、PCNA表达阳性率均高于病变长度≤50 mm者;管壁增厚>10 mm者EGFR、PCNA表达阳性率均高于管壁增厚≤10 mm者;管腔重度狭窄者EGFR、PCNA表达阳性率均高于轻度狭窄及中度狭窄者;有淋巴结转移者EGFR、PCNA表达阳性率均高于无淋巴结转移者;发生局部浸润者EGFR、PCNA表达阳性率均高于未发生局部浸润者,比较有差异,具备统计学意义(P<0.05),见表1。

表1 食管癌患者螺旋CT征象与EGFR、PCNA表达的关系(例,%)
2.4 不同分化程度的食管癌患者螺旋CT值比较
按照病理结果将食管癌患者分为低分化、中分化及高分化三组。不同分化程度的食管癌患者第一期及第二期螺旋CT值比较有差异,随分化程度的提高呈明显下降趋势(P<0.05)。不同分化程度的食管癌患者平扫CT值比较无差异(P>0.05),但高分化组平扫CT值低于低分化组,差异具备统计学意义(P<0.05),见表2。

表2 不同分化程度的食管癌患者螺旋CT值比较
2.5 不同分化程度的食管癌患者EGFR、PCNA表达比较
不同分化程度的食管癌患者EGFR、PCNA表达有差异,低分化组食管癌患者EGFR、PCNA表达阳性率高于中、高分化组(P<0.05),见表3。

表3 不同分化程度的食管癌患者EGFR、PCNA表达比较(例,%)
2.6 食管癌患者螺旋CT值与EGFR、PCNA阳性表达的相关性
食管癌患者第一期、第二期螺旋CT值与EGFR、PCNA阳性表达呈正相关(P<0.05),见表4。

表4 食管癌患者螺旋CT值与EGFR、PCNA阳性表达的相关性
2.7 典型病例
患者,女性,77岁,上腹部胀满1月余来院。食管活检结果为低分化鳞状细胞癌。螺旋CT征象:食管中段管壁不均匀增厚,病变长度约64 mm,局部可见软组织肿块,密度不均匀,管腔变窄且上方食管扩张,呈不均匀中度强化。第一期CT值约62 HU;第二期CT值约64 HU;平扫CT值约43 HU。见图1。

a为肺窗病变水平位;b、c为平扫水平位、冠状位;d、e、f为胸部增强第一期水平位、矢状位、冠状位;g、h、i为胸部增强第二期水平位、矢状位、冠状位。
3 讨论
食管X射线钡餐造影、胸部CT扫描是目前常用于食管癌的检查手段,X射线钡餐造影能够直观显示食管上皮组织黏膜的变化,但不能清晰反映肿瘤与周围组织的关系,缺乏在局部浸润、淋巴结转移情况及肿瘤分化方面的诊断能力[9]。螺旋CT对判断肿瘤侵袭周围组织有较大优势,同时克服了传统CT平扫中因食管蠕动和呼吸造成的伪影、漏扫和重叠扫描,可提高对食管癌分期及淋巴结转移的诊断准确率,且螺旋CT从水平位、矢状位、冠状位等不同方位进行病变部位的图像重建,具有较高的空间分辨率,可清晰显示肿瘤位置、形态、管腔狭窄情况等[10]。
EGFR是一种广泛存在于机体表皮细胞膜上的跨膜糖蛋白,与其配体结合后可使酪氨酸激酶发挥活性,对组织细胞的增殖分化及凋亡进行调控,参与血管生成及淋巴细胞的侵袭转移[11]。以往研究表明,40%~80%的恶性肿瘤患者的EGFR可呈现异常高表达状态,这种异常状态与肿瘤的新生微血管、局部浸润、淋巴结转移及细胞分化、抗凋亡等密切相关[12]。PCNA是存在于机体组织细胞核内的参与DNA复制的蛋白质成分,也是临床研究中作为反映肿瘤细胞增殖活性的重要指标,已有不少研究报道证实,其在多个部位的实体癌细胞核中呈现异常表达的状态,与肿瘤形成、分化、局部浸润及淋巴结转移等有关[13-15]。本研究检测出的食管癌患者EGFR阳性表达率高达71.82%(79/110),PCNA阳性表达率为65.45%(72/110),且在螺旋CT征象中,病变长度>50 mm者EGFR、PCNA表达阳性率均高于病变长度≤50 mm者;管壁增厚>10 mm者EGFR、PCNA表达阳性率均高于管壁增厚≤10 mm者;管腔重度狭窄者EGFR、PCNA表达阳性率均高于轻度狭窄及中度狭窄者;有淋巴结转移者EGFR、PCNA表达阳性率均高于无淋巴结转移者,这说明不同螺旋CT征象结果患者的EGFR与PCNA的表达存在差异,EGFR与PCNA的阳性表达与肿瘤的形成范围、狭窄程度、淋巴结转移及局部浸润相关,与上述以往研究结果相一致。二者存在相关性的原因可能为螺旋CT可对肿瘤的新生血管及与周围组织结构的关系进行清晰成像,新生血管的形成是造成肿瘤的生长、局部浸润及淋巴结转移的关键,新生血管的形成一般包括血管扩张、内皮细胞增殖迁移、细胞外基质降解等过程[16]。EGFR及PCNA均是引起细胞增殖迁移的关键因子,可通过激活细胞增殖分化的信号通路促进食管病变部位的血管内皮细胞发挥作用,刺激细胞进行有丝分裂,形成新生血管[17]。
螺旋CT增强扫描的原理是碘对比剂在组织微血管及不成熟的管壁结构中渗透,其反映的肿瘤强化程度与肿瘤微血管密度(microvessel density,MVD)及结构相关,螺旋CT的X射线在特定能量水平下穿透机体被检部位时,可在成像上获取对应CT值,注入碘对比剂后,成像出现较为清晰的组织对比度,准确展现不同分化程度的食管癌的图像特点和差异[18]。本研究结果显示:不同分化程度的食管癌患者第一期及第二期螺旋CT值比较有差异,随分化程度的升高呈明显下降趋势;低分化组食管癌患者EGFR、PCNA表达阳性率高于中、高分化组,且食管癌患者第一期、第二期螺旋CT值与EGFR、PCNA阳性表达呈正相关,这提示低分化食管癌患者肿瘤新生微血管更为密集,结构复杂,增强扫描后病灶强化程度更高,CT值更大。分析原因可能为:MVD是肿瘤血管生成的标志,EGFR及PCNA作为肿瘤血管生成的关键调控因子,与MVD有关;而食管癌病变部位的血管形态不规则,分布不均匀,说明肿瘤在生长过程中确有异常新生微血管[19]。肿瘤新生血管生成及通透性可直接影响病变部位碘摄取程度,不同分化程度的食管癌的血液供给和肿瘤血管密度不同,食管癌分化程度越低,病变区域的血供越丰富,血管密度越大,且新生血管结构不完整,基底膜异常,病变组织细胞的通透性增大更易于被碘对比剂渗透,反映的强化程度越高,CT值更大[20]。
综上所述,食管癌患者螺旋CT可清楚反映病变长度、管腔厚度、管腔狭窄程度、淋巴结转移及局部浸润情况,螺旋CT征象与EGFR、PCNA的阳性表达相关,且低分化食管癌患者增强扫描的CT值更大,EGFR及PCNA阳性表达率更高。若将螺旋CT征象与EGFR、PCNA表达结合分析食管癌患者术前肿瘤形成及分化情况,对合理制定肿瘤治疗方案具备一定参考价值。
