小球藻藻渣TEMPO法制备纤维素纳米纤维及阳离子染料吸附研究*
2023-11-09张丽娜刘长斌王连峰
张丽娜,朱 锦,付 月,刘长斌,王连峰
(1.大连交通大学 材料科学与工程学院,辽宁 大连 116028;2.大连工业大学 生物工程学院,辽宁 大连 116021;3.沈阳化工学校,沈阳 110122)
0 引 言
纤维素是一种由β-D-吡喃葡萄糖通过β-1,4糖苷键连接形成的长链线性多糖,分子式为(C6H10O5)n。纤维素是地球上最丰富的生物材料之一,是所有植物纤维的主要成分;由于其生物降解性、可再生性和生物相容性,被认为是最有前途的生物聚合物[1-3]。纳米纤维素是纤维素的纳米级形式,通过纤维素纤维分解(自上而下策略)获得的纳米纤维素可以分为两大类:纤维素纳米晶体(CNC),也称为纤维素晶须和纤维素纳米纤维(CNF),也称为微纤维化纤维素[4]。细菌纤维素(BC)和静电纺丝纤维素纳米纤维(ECNF)也被视为纳米纤维素,他们分别是通过细菌从低分子量糖或通过静电纺丝从纤维素衍生物中积累纳米纤维(自下而上策略)而制成的。然而,CNC和CNF是最常见的纤维素纳米材料[1]。纳米纤维纤维素可以从木材等木质纤维素材料、草本植物中分离,它们是通过纤维素纤维分解(自上而下策略)成纳米级颗粒而分离出来的,而BC和ECNF则分别是通过细菌从低分子量糖或通过静电纺丝从纤维素衍生物中积累纳米纤维(自下而上策略)而制成的。目前,纳米纤维主要从木材和棉花、麦秸、棕榈树等农业副产品中通过酸水解、TEMPO介导氧化、机械分解和酶辅助水解等方法制备[5-8]。
2,2,6,6-四甲基哌啶-1-氧基自由基(TEMPO)介导的天然木材纤维素氧化是在水性条件下,TEMPO将纤维素伯羟基选择性氧化为羧基[9]。TEMPO氧化使纤维素纤维表面引入羧基,由于渗透效应和带负电荷纤维之间的静电排斥,导致纤维素纤维分层和溶胀[10-11]。因此,木材在很低的能耗条件下经轻度粉碎后,就可以获得CNF[10]。
纳米纤维素的应用非常广泛,除了用于制备纳米复合材料[12]、3D打印[13]、包装材料[14]、电子储能材料[15]、生物医疗领域[16]等领域外,在水处理中的应用也越来越受到人们的关注[17]。染料通常用于制药、油漆、纸浆和造纸、纺织和塑料工业。由于染料的顽固性,染料的排放是工业废水的一个重要污染源,会对环境和人类健康构成严重威胁[18-19]。吸附技术是一种经济、有效和可持续的策略[20-21],纳米纤维素已被用作各种污染物吸附剂[22-23],但由于活性官能团的缺乏阻碍了纤维素作为有效吸附剂的应用[24]。
微藻作为单细胞藻类,细胞壁含有丰富的纤维素,因其细胞结构简单,基本不含木质素,可以不经过机械破碎、脱胶等预处理,仅通过简单的纯化工艺就可以分离出大量的纳米纤维[25-27]。此外,相较于陆生植物,微藻生长需求简单,不占用耕地资源,生长快、周期短,可全年大规模养殖,单位面积生产力高[28],是制备纳米纤维素非常好的原料。
本文以小球藻藻渣废弃物为原料,通过TEMPO介导氧化法制备了具有表面富含羧基的TCNF,并以亚甲基蓝(MB)为模型染料测试了TCNF的吸附性能,考察了pH、吸附时间和染料浓度等因素对TCNF吸附性能的影响。
1 实 验
1.1 主要试剂
制备TCNF所用原料为实验室小球藻经油脂提取后的残留物,实验用TEMPO、MB等药品购自于阿拉丁。
1.2 TCNF的制备
TCNF的制备参考Lee[26]和Chen等[8]方法,称取5 g藻渣废弃物加入200 ml 5%(质量浓度)NaOH溶液,150 r/min搅拌条件下80 ℃水浴2 h;水浴结束后离心收集沉淀,并用ddH2O洗涤至中性;沉淀中加入100 mL醋酸钠缓冲液和100 mL亚氯酸钠(1.7% ,pH4.5)溶液,150 r/min搅拌,70 ℃水浴4 h,结束后用蒸馏水洗涤3次,离心收集原纤维。室温下向原纤维中(1 g原纤维含量)加入0.1 mmol的TEMPO,1 mmol溴化钠和5 mmol的次氯酸钠溶液,持续搅拌并用0.5 mol/L NaOH溶液将pH维持在10,直到pH不再变化,离心回收沉淀得TCNF,将TCNF用蒸馏水洗涤3次后,取10 mL冷冻干燥后称重计算TCNF浆液浓度,其余以浆液形式保存在3~5 ℃用于MB吸附研究。
1.3 羧基含量的测定
参考吴慧等[29]方法,准确称取0.05 g TCNF样品,用100 mL 0.01 mol/L的 HCl进行酸化,回收后置于容积为20 mL的顶空测试瓶中。加入4.0 mL浓度为0.08 mol/L NaHCO3溶液。摇晃测试瓶,使样品充分分散,利用顶空气相色谱测试并记录CO2色谱峰面积(S)。
校正系数的确定:在加有4.0 mL浓度为0.08 mol/L NaHCO3溶液的密封顶空样品瓶中分别加入0、100、200、300、400、500 μL浓度为0.01 mol/L的盐酸溶液(重复3次),利用顶空气相色谱检测并记录CO2色谱图信号的峰面积。以加入盐酸的量(mol)为横坐标,CO2峰面积为纵坐标,绘制标准曲线,计算校正系数k。通过式(1)计算羧基含量(高羧基含量TEMPO氧化纤维素的制备与表征)
(1)
式中:CCOOH为TCNF中羧酸基团的含量(mmol/g);S为添加TCNF后CO2的信号峰面积;S0为未添加TCNF检测到的CO2信号峰面积;k为校正常数(mmol-1);m为TCNF样品的质量(g)。
1.4 TCNF的表征
分别利用扫描电子显微镜(SEM,日本电子JSM-7800F)和原子力显微镜(Bruker Dimension Icon AFM)对TCNF进行形貌观测;利用珀金埃尔默Spectrum Two傅里叶红外光谱仪和X射线衍仪(岛津XRD-7000S)进行红外光谱以及X射线衍射分析。X射线扫描在2θ在10°到40°范围内,速度4°/min,步长为0.01°,结晶度指数(Crl)采用Segal方法计算:
CrI(%) =(I002-I0)/I002×100%
(2)
1.5 不同浓度MB紫外吸收校准曲线的建立
称取一定量的MB,配置成不同浓度的MB溶液,利用紫外可见分光光度计测量不同浓度MB在665 nm处的吸光度,调整浓度使其吸光值为0.1至1之间,根据Beer-Lambert定律分别拟合MB标准曲线。
1.6 TCNF吸附动力学分析
在室温条件下,取0.1 g TCNF加入到含有100 mL染料溶液 (10 mg/L) 的烧瓶中,250 r/min搅拌,并分别在0,20,40,60,80,100,120,140,160 min取2 mL溶液离心,用紫外可见分光光度计测量上清液的吸光值并计算剩余溶液中MB的浓度,利用公式⑴计算不同时间下单位质量纳米纤维吸附量(Qt):
(3)
式中:C0为染料初始浓度,Ct是吸附后染料的浓度,单位mg/L;m为吸附剂的质量,单位g;V是吸附染料溶液的体积,单位L。
实验值采用伪一阶(4)和伪二阶动力学方程(5)进行拟合[19]。
(4)
(5)
式中:Qe是平衡时吸附在吸附剂上的染料量,K1、K2是速率常数。
1.7 pH对MB吸附的影响
取0.1 g TCNF悬液加入50 mL 6 mg/L的MB溶液中,用HCL 和NaOH调节染料溶液的初始pH分别为3,4,5,6,7,8,9,10,室温下250 r/min 搅拌吸附80 min后离心,分光光度计测定上清液中染料的浓度,计算不同pH下MB的吸附量,分析染料初始pH对TCNF吸附的影响。
1.8 染料初始浓度对TCNF吸附的影响
取0.1 g TCNF悬液加入50 mL不同初始浓度的MB溶液中,室温250 r/min 搅拌吸附80 min后离心,利用分光光度计测定上清液中染料的浓度,计算吸附量,分析MB初始浓度对TCNF吸附的影响。利用Langmuir和Freundlich等温模型方程进行吸附数据的拟合[19],等温线方程见(5)、(6)。
(5)
式中:Qe(mg/g)为每单位质量吸附剂吸附的染料量,单位:mg/g;Ce为平衡浓度,单位mg/L;KL是Langmuir等温常数,单位:L/mg;Qm最大吸附容量,单位:mg/g。
(6)
式中:Kf为Freundlich常数,n为吸附强度。
2 实验结果与讨论
2.1 TCNF羧基含量的测定
通过用向0.08 mol/L NaHCO3溶液中添加0.01 mol/L的盐酸溶液建立的盐酸用量与峰面积标准曲线如图1所示。盐酸用量与峰面积成线性回归,拟合回归方程为Y=250.8X+13.38(R2=0.98826;X:加入盐酸的量,单位mmol;Y:顶空气相色谱测定的CO2峰面积),得校正系数为k=250.8。测得S0=14.663,S=33.9515,由公式(1)计算得TCNF羧基含量为1.54 mmol/g。
2.2 TCNF的表征
将制备的TCNF悬液冷冻干燥后称重,计算得到TCNF的浓度为1.55%(质量浓度)。利用SEM对样品进行观测,结果如图2。在10 μm尺度视野下,观察到片层结构的TCNF交织在一起呈蜂窝状,100 nm尺度视野下,我们可以看到纤丝紧密的交织在了一起,为了进一步表征纳米纤维的形貌,将TCNF悬液稀释后利用原子力显微镜进行进一步表征,结果如图3。图像中观察到了分散的纳米纤维,利用NanoScope Analysis分析软件的section模式分析TCNF平均直径为2 nm左右,平均长度为300 nm左右,证明我们从小球藻藻渣废弃物中成功制备了纳米纤维。

图2 TCNF的扫描电镜形貌Fig.2 SEM images ofTCNF

图3 CNF的原子力显微镜形貌Fig.3 AFM images ofTCNF
TCNF样品的红外光谱分析结果见图4。在3 332 cm-1处的吸收峰为纤维素分子间-OH基团的伸缩震动[30-31],2 922 cm-1为C-H键伸缩振动出现的特征峰[32],1 603 cm-1为-COONa 特征峰[8],1 409 cm-1的峰证明了—COOH的存在[33],1 032 cm-1为 C—O—C吡喃糖环振动出现的特征峰[34]。
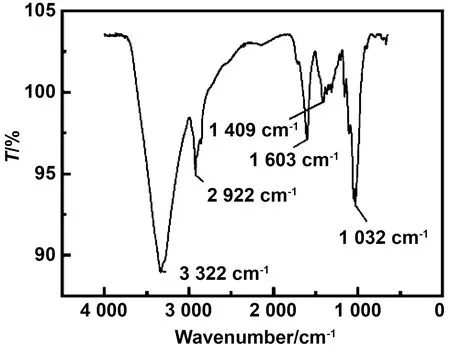
图4 TCNF 的FTIR图谱Fig.4 FTIR spectrum of TCNF
XRD分析如图5所示,主峰在2θ约15°,16.4°,22.5°处分别对应(110)、(11-0)和(002)平面,表明样品以纤维素I为主[35]。根据西格尔方程,TCNF的CrI为59.5%。
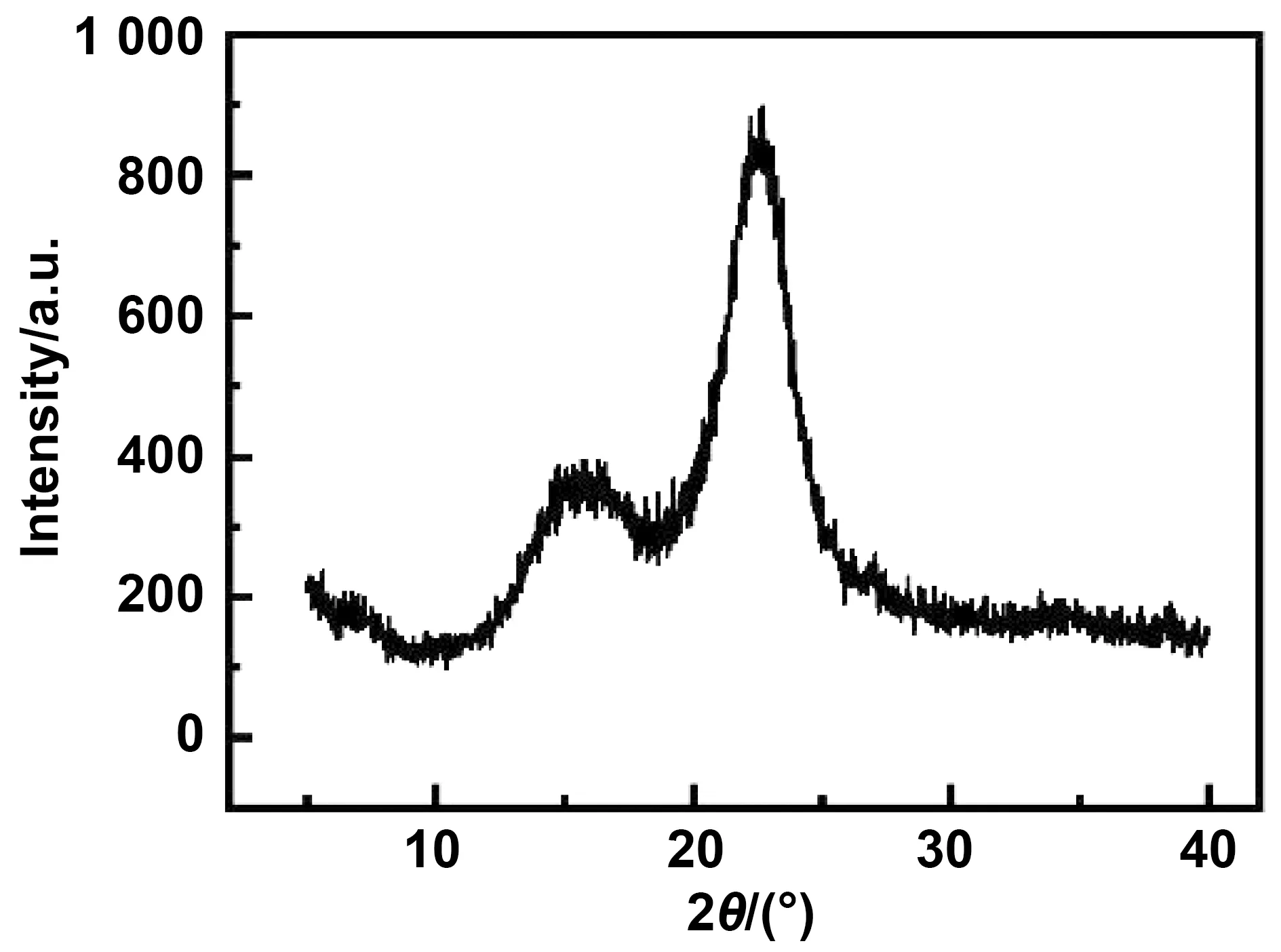
图5 TCNF的 XRD 图谱Fig.5 XRD of TCNF
2.3 不同浓度MB紫外吸收校准曲线的建立
根据不同浓度MB在665 nm处的吸光度进行绘图(图6),从图中可以看出吸光度在0~1范围内,MB的浓度与吸光度呈线性关系,得回归方程分别为:MB:Y=0.1715X-0.0072(Y为MB吸光度,X为MB溶液浓度)。

图6 MB吸光度校正曲线Fig.6 The calibration curves of MB
2.4 TCNF吸附动力学研究
为分析接触时间对不同染料去除的影响,在室温下进行TCNF对MB的吸附动力学实验。结果如图7,MB的吸附量Qt随着吸附时间的增加而增加,在80 min后逐渐趋于稳定,平衡时吸附量为325.67 mg/g。对实验数据利用伪一级、二级动力学方程进行拟合,结果见图8,动力学参数见表1。伪二级动力学模型拟合曲线的相关系数R12远高于一级动力学模型拟合曲线系数R22,采用伪二级动力学模型计算的Qe值(346.02 mg/g)与实验值(325.67 mg/g)(25 ℃,初始染料浓度10 mg/L)接近,这表明TCNF对MB的吸附过程是通过伪二级动力学进行的。

表1 TCNF吸附MB动力学参数Table 1 Kinetic parameters of MB adsorption on TCNF determined using different models

图7 吸附时间对TCNF吸附MB的影响Fig.7 Effect of time on dye adsorption of TCNF
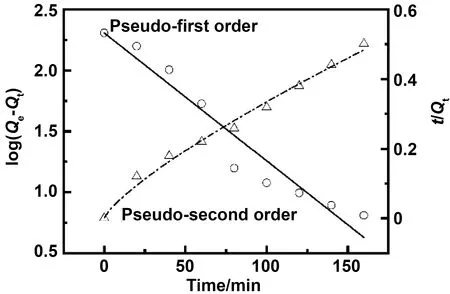
图8 TCNT吸附动力学曲线Fig.8 Adsorption kinetics model of TCNF
2.5 pH对TCNF吸附的影响
利用盐酸和NaOH调整MB溶液的初始pH为分别3、4、5、6、7、8、9、10,加入0.1 g TCNF悬液,在室温条件250 r/min搅拌条件下吸附80 min,吸附结束后离心取上层溶液测吸光度,结果如图9。随着MB溶液pH值的升高,TCNT吸附量逐渐增加,当pH=8时最高为129 mg/g(MB初始浓度为6 mg/L),此后逐渐降低。
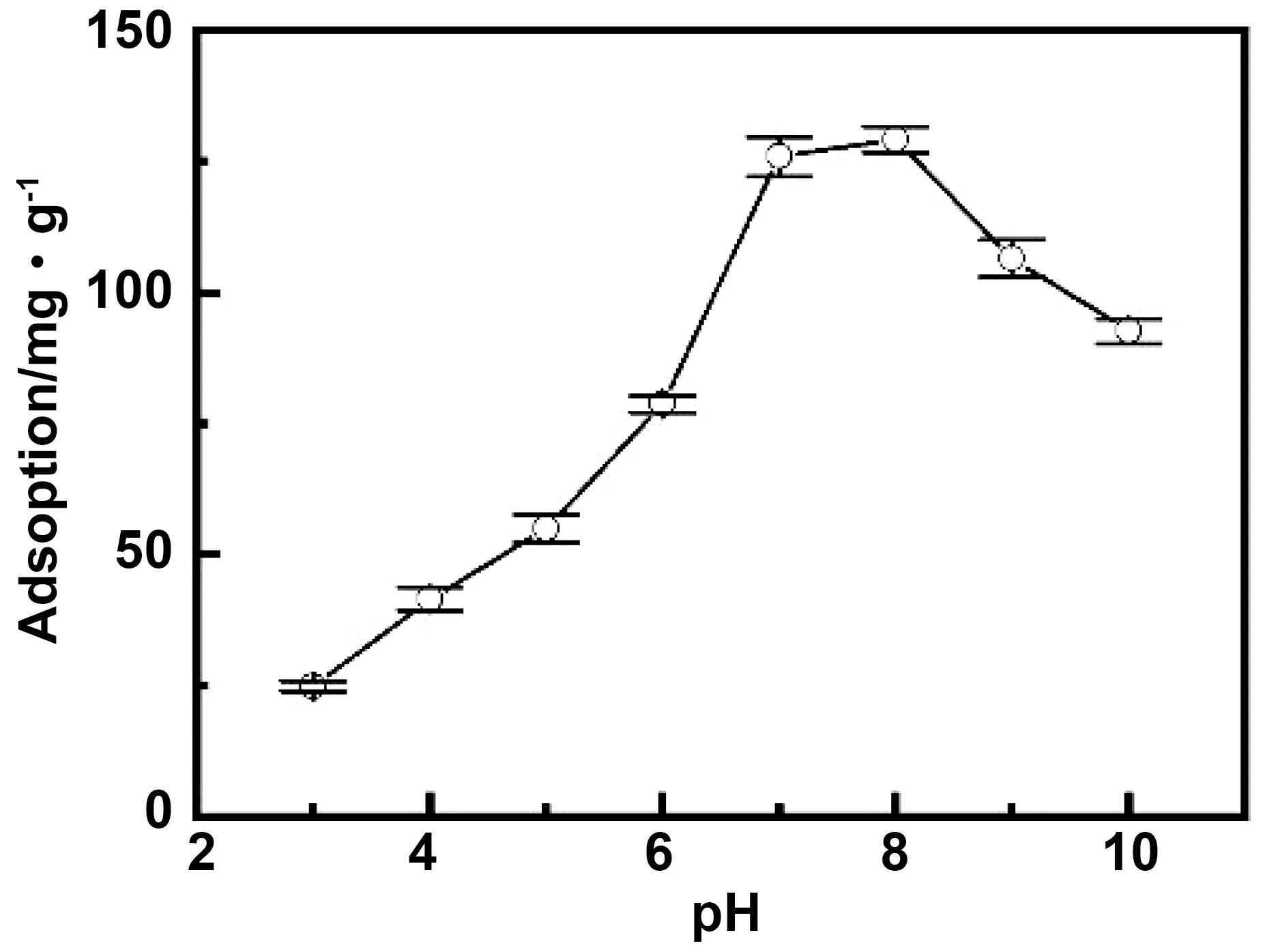
图9 pH对TCNF吸附的影响Fig.9 Effect of pH value of MB solutions on the adsorption capacity of TCNF
2.6 MB初始浓度对TCNF吸附的影响
TCNF对不同浓度初始浓度MB的吸附结果如图10,MB的浓度在0.5~10 mg/L范围内,TCNF对MB的吸附呈线性增加,MB通过浓度差促进传质进而提高TCNF的吸附能力[36],当MB浓度超过10 mg/L之后,随着MB初始浓度的增加TCNF的吸附量增加缓慢,表明染料分子的蓄积抑制了TCNF的吸附。
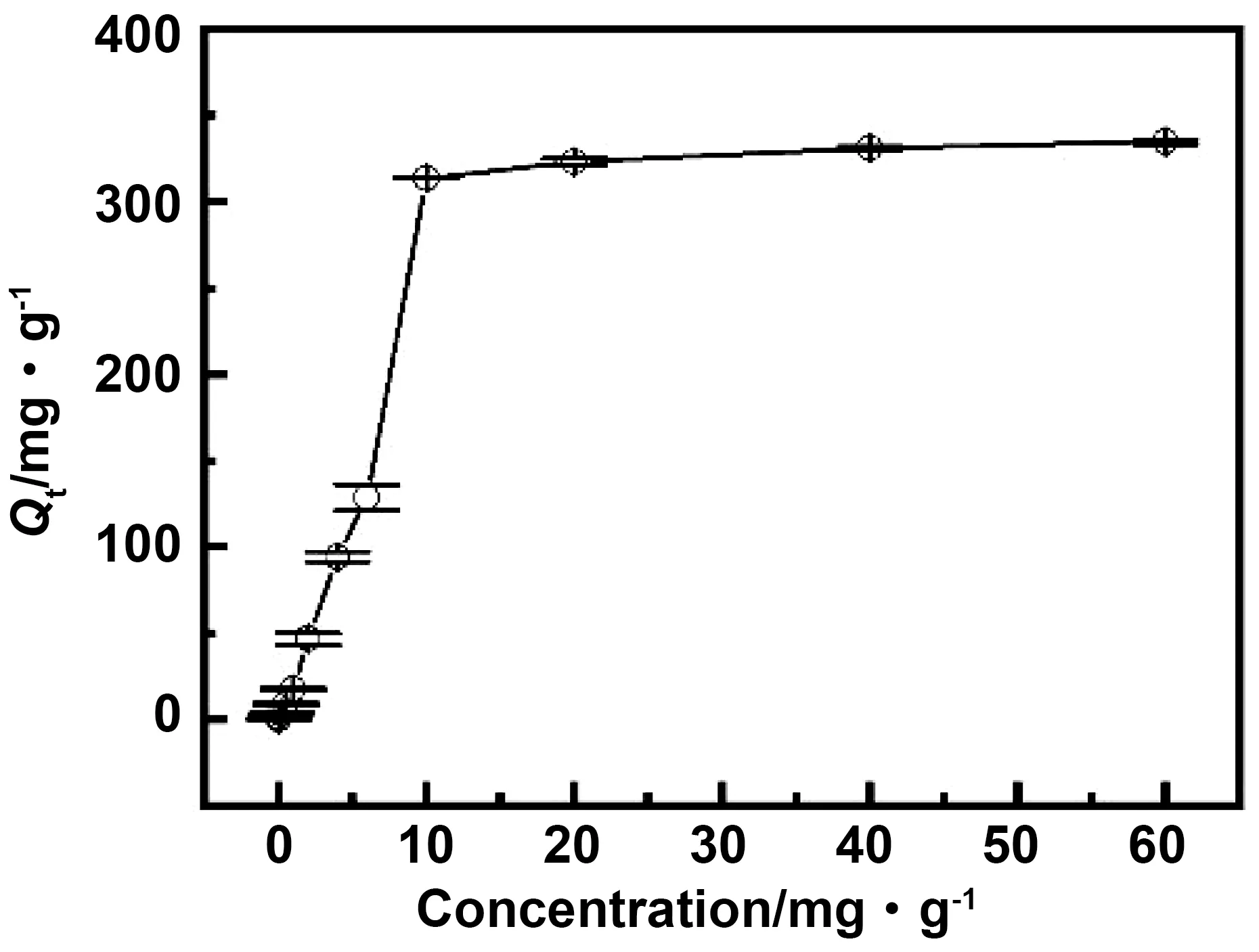
图10 MB初始浓度对TCNF吸附影响Fig.10 Effect of initial concentration of MB on the adsorption capacity of TCNF
2.7 吸附等温线
为确定吸附剂和染料分子之间的相互作用,进一步描述染料的吸附过程,利用Langmuir和Freundlich等温线方程对MB不同初始浓度的吸附数据进行拟合,结果见图11,相关系数见表2。与Freundlich模型相比,Langmuir模型计算出的TCNF最大吸附为333.92 mg/g(初始染料浓度600 mg/L,吸附80 min)接近实验值334.5 mg/g,并且其拟合曲线相关系数R2为0.99754,远高于Freundlich模型拟合曲线相关系数0.74927。因此,实验数据与Langmuir模型拟合最好,说明TCNF表面均匀,表面不同位置的吸附能变化不大,为单层吸附[19]。

表2 TCNF吸附MB不同等温模型参数Table 2 Parameters of the different isotherm models applied to MB adsorption on TCNF
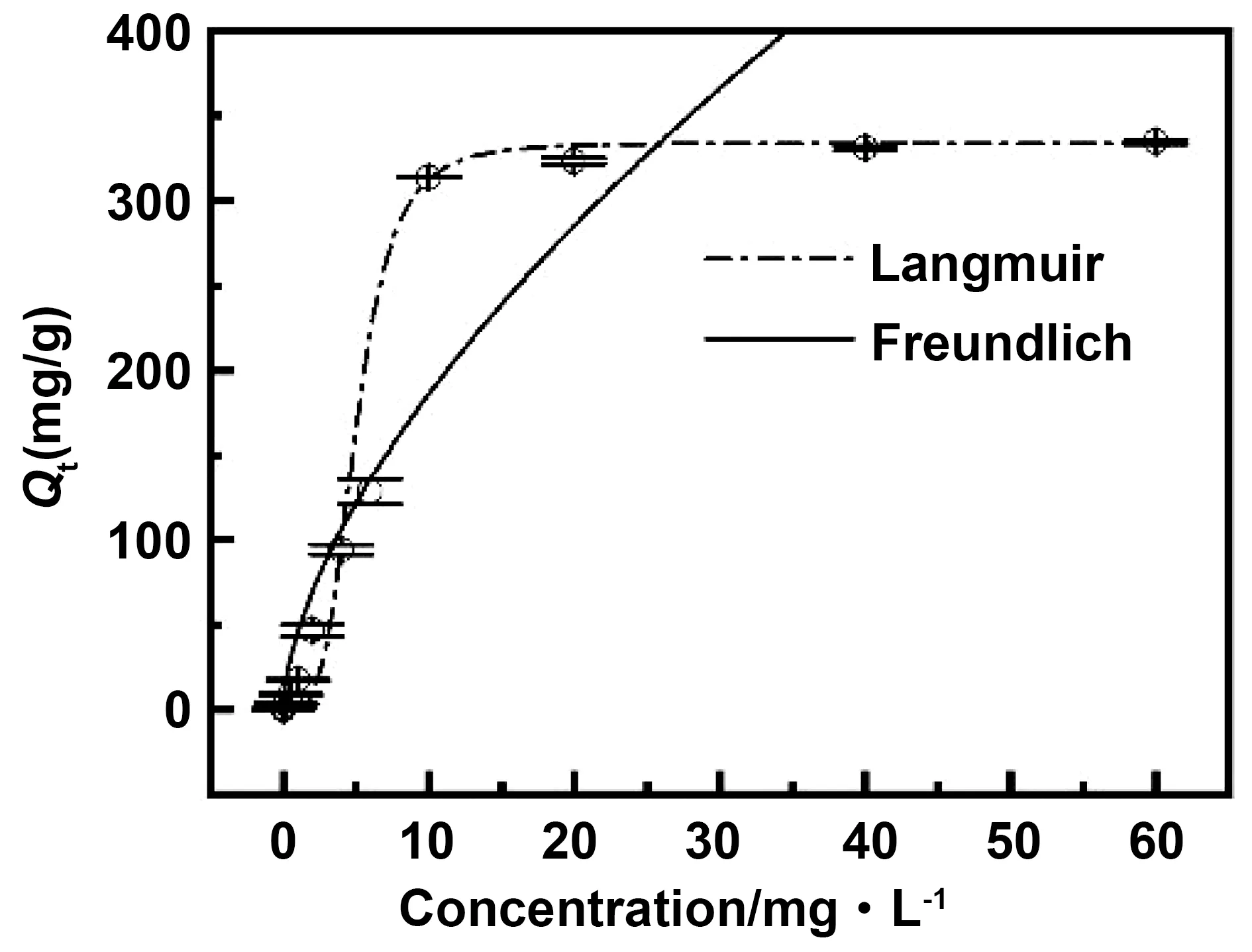
图11 TCNF吸附等温线Fig.11 Adsorption isotherms of TCNF
3 结 论
本研究通过TEMPO介导氧化法从小球藻藻渣中成功制备了TCNF,利用顶空气象色谱法测得其羧基含量为1.54 mmol/g。通过原子力显微镜观测制备的TCNF平均直径为2 nm左右,平均长度为300 nm左右。TCNF对MB吸附研究表明,TCNF在与MB接触80 min后吸附基本达到平衡,吸附过程符合伪二级吸附动力学模型。TCNF对MB的吸附受pH影响比较大,pH=8时具有最大吸附量;此外,在MB初始浓度低于10 mg/L,吸附量随MB浓度升高呈线性增加,MB初始浓度高于10 mg/L以后,吸附量的增加非常微弱,CNNF趋于饱和,在60 mg/L时测得最大吸附量为334.5 mg/g;吸附等温线分析表明,TCNF对MB吸附符合Langmuir模型,说明TCNF表面均匀,表面不同位置的吸附能变化不大,为单层吸附。综上所述,以小球藻藻渣为原料制备纳米纤维过程简单,可有效提高小球藻的经济价值,同时也降低了纳米纤维素制备的原料投入成本,制备的TCNF对MB具有良好的吸附效果,具有广阔应用前景。
