基于LDHs-DGT的环境中活性态Cr原位提取检测方法研究
2023-11-09田佩宁王震张润祺张闯闯周其文赵玉杰
田佩宁,王震,张润祺,张闯闯,周其文,赵玉杰
(农业农村部环境保护科研监测所,农业农村部农产品质量安全环境因子控制重点实验室,天津 300191)
铬(Cr)广泛存在于地壳中,是地幔中第十大丰富元素[1],因其独特的金属特性,广泛应用于医药、电镀、印染、皮革制造等行业,同时Cr 的开采会产生大量的铬渣,管理不当或污染事故,会导致Cr 释放到土壤和水体中,造成土壤、水体、农产品污染[2-4]。世界卫生组织(WHO)、美国环境保护署(USEPA)规定饮用水中Cr 的污染物限值分别为50、100 µg·L-1[5-6],我国《地表水环境质量标准》(GB 3838—2002)仅规定饮用水中Cr(Ⅵ)的限值为50 µg·L-1,原因在于Cr(Ⅵ)的毒性远高于Cr(Ⅲ)[7]。进入土壤中的Cr 会被土壤矿物、氧化物及胶体等吸附固定[8],因此,土壤中的Cr活性远低于水体。《土壤环境质量农用地土壤污染风险管控标准(试行)》(GB 15618—2018)规定的土壤Cr 的风险筛选值为150~350 mg·kg-1,之所以有如此大的差异性,是因为土壤管理模式与pH 值对土壤Cr的活性影响显著,淹水使土壤中活性态或称易动态Cr(Ⅵ)还原,Cr的毒性降低,pH值升高,土壤对Cr,尤其是活性态Cr(Ⅲ)的固持能力增加,使其危害风险减小[9-10]。因此Cr的污染风险是Cr(Ⅲ)和Cr(Ⅵ)协同作用的体现,正确提取和检测活性态Cr(Ⅲ)和Cr(Ⅵ)对于科学评估Cr污染风险至关重要。
梯度扩散薄膜(DGT)技术是以Fick 第一扩散定律为理论基础的原位被动采样技术,是通过对在特定时间内穿过特定厚度的扩散膜的某一离子或易解离配体进行定量化测量、计算,从而获得某一元素活性态浓度的方法[11]。由于DGT是一种原位采样技术,对被测量介质扰动小,不改变测量介质的氧化还原状况,且其孔径与植物根表孔径大小相似[11],部署在环境介质如土壤中,在结合膜与土壤溶液之间会形成浓度梯度,因此,可以模拟植物对重金属的吸收过程,测定的活性态与植物吸收量相关性好[12],是迄今为止较为先进的土壤、水体及水体沉积物活性态重金属提取技术[13-15]。
将DGT 技术用于土壤、水体活性态Cr 的提取检测,已有相关研究,如Ernstberger 等[16]用Chelex-100树脂作为DGT的结合相,测量了水体中活性态Cr(Ⅲ)的浓度;Chen 等[17]用聚季铵盐,Pan 等[18]用N-甲基葡糖胺(N-Methyl-D-Glucamine,简称NMDG)作为DGT装置的结合相测量了水体中活性态Cr(Ⅵ)的浓度;采用一种结合相同时提取土壤或水体等环境介质中Cr(Ⅲ)和Cr(Ⅵ)活性态也有相关报道,如Devillers等[19]开发的锆膜具备此功能,但提取后需要采用两步法进行洗脱。
LDHs是由带正电的金属氢氧化物和可维持电荷平衡的层间阴离子组成的混合金属氢氧化物[20],化学通式为[M2+1-xM3+(OH)2]x+·[Am-x/mnH2O]x-,其中,M2+表示二价阳离子,M3+表示三价阳离子[21]。LDHs 是一种高效的阴离子交换剂,其层间阴离子如Cl-、NO-3等易与CrO2-4、SO2-4交换[22],且LDHs 表面含有大量羟基,使其具有金属阳离子结合的能力,同时自身表现为一定的碱性。采用冷冻干燥方法制备的纳米级LDHs 具有比表面积大、颗粒细致均匀、离子吸附能力强、加酸易崩解等优势[23-24],常常用于土壤或水体环境中活性态金属的提取检测中,如Cd(Ⅱ)、As(Ⅲ)[25-26],但用LDHs 材料作为DGT 装置的结合膜,同时提取测定土壤或水体中的活性态Cr(Ⅲ)和Cr(Ⅵ)的相关研究未见报道。因此,本研究率先采用纳米LDHs 作为结合膜材料,制备了LDHs-DGT,并结合Cr(Ⅲ)和Cr(Ⅵ)的检测方法,对其提取活性态Cr(Ⅲ)和Cr(Ⅵ)的各项性能进行了评估,同时开展了不同水分管理模式下LDHs-DGT 装置动态测定土壤Cr 形态变化的实例研究,以期为Cr 在土壤、水体及沉积物等介质中的形态转化、运移及危害风险评估提供技术支撑。
1 材料与方法
1.1 试剂与材料
实验和试剂溶液用水均为超纯水。Cr(Ⅲ)储备液(1 000 mg·L-1)用Cr(NO3)3·9H2O制备,Cr(Ⅵ)储备液(1 000 mg·L-1)用K2CrO4制备,MgCl2、AlCl3·6H2O、NH3·H2O、丙烯酰胺、四甲基乙二胺等均购于上海麦克林生化科技有限公司,HA、琼脂糖购自Sigma-Aldrich,硝酸纤维素膜购自农环科技(上海)有限公司,Cr(Ⅲ)和Cr(Ⅵ)单元素标准溶液来自国家有色金属及电子材料分析测试中心,所有试剂均为优级纯。塑料容器和DGT 装置使用前均在10%HNO3中酸洗3~24 h,并用超纯水冲洗干净。
1.2 LDHs-DGT制备
LDHs-DGT 装置由保护膜、扩散膜、结合膜和外部支撑框架组成[27-28]。保护膜采用孔径0.45 µm,厚度0.15 mm 的硝酸纤维素膜,扩散膜的制备方法参见Zhang 等[29]的文献。结合膜材料用纳米LDHs 制备[30],具体方法参见张润祺等[24]的文献。
1.3 LDHs性能测试
1.3.1 吸附效率和洗脱效率
吸附效率:将LDHs 结合膜(18 cm2)浸入含有5.0 mg·L-1Cr(Ⅲ)和Cr(Ⅵ)的50 mL 0.01 mol·L-1NaNO3溶液中,用摇床水平振荡(180 r·min-1)0~240 min,测定吸附前后溶液中Cr(Ⅲ)和Cr(Ⅵ)的浓度,计算吸附量,吸附容量实验Cr(Ⅲ)和Cr(Ⅵ)的浓度范围为5~200 mg·L-1,具体方法参见张润祺等[24]的文献。
洗脱效率:将结合膜浸入50 mL 含有50 µg·L-1Cr(Ⅲ)和Cr(Ⅵ)的0.01 mol·L-1NaNO3溶液中,摇床水平振荡(180 r·min-1)24 h后,取出结合膜,测定吸附前后溶液中的Cr(Ⅲ)和Cr(Ⅵ)浓度,用10 mL 0.05、0.1、0.5、1、2 mol·L-1HNO3溶液对结合膜进行洗脱,洗脱时间为12 h,测定洗脱液中Cr(Ⅲ)和Cr(Ⅵ)的浓度。用公式(1)计算洗脱效率。
式中:fe为洗脱效率,%;ce为洗脱液中元素的浓度,µg·L-1;ve为洗脱液体积,mL;vg为吸附膜体积,mL;M为结合膜中元素累积量,ng。
1.3.2 DGT空白和方法检出限
DGT 空白和方法检出限的测定参见张润祺等[24]的文献。
1.3.3 扩散系数的测定
本实验采用磁力搅拌器搅拌式方法测定扩散系数[24],将DGT 装置均匀布置在有机玻璃架上,并将其将浸入3.5 L、pH=6.0、含有50µg·L-1Cr(Ⅲ)和Cr(Ⅵ)的0.01 mol·L-1NaNO3溶液中,用磁力搅拌器搅拌(800 r·min-1),在0~14 h内每隔2 h取出DGT 装置,取出结合膜洗脱,并测定Cr(Ⅲ)和Cr(Ⅵ)浓度,每个处理设置3个平行。用公式(2)计算扩散系数。
式中,slope为结合膜中元素累积量M(ng)随时间t(min)的线性回归方程的斜率;Δg为扩散膜和保护膜的厚度之和,cm;A为LDHs-DGT 装置的窗口面积,cm2;Csoln为溶液中元素的浓度,µg·L-1。
1.4 pH、离子强度、硫酸盐、有机质的影响
探索LDHs-DGT 装置在不同使用环境条件下性能的变化,首先,分别配制pH=3~9 的含有50 µg·L-1Cr(Ⅲ)和Cr(Ⅵ)的溶液各3 L 储存备用,参照张润祺等[24]的文献进行pH 对LDHs-DGT 装置的适用条件影响实验。
类似地,离子强度及干扰离子对DGT 提取测定Cr(Ⅲ)和Cr(Ⅵ)影响实验过程与pH 实验过程类似,离子强度设置为c(NaNO3)=1、5、10、50、100 mmol·L-1,干扰离子以SO2-4为例,设置浓度为c(SO2-4)=0.01、0.1、0.5、1、5、10 mmol·L-1。有机质对DGT 性能的影响实验以腐植酸(HA)为例,设置溶液中m(Cr)/m(HA)=1/0、5/1、1/1、1/5,每个梯度下3个平行。
1.5 Cr(Ⅲ)和Cr(Ⅵ)的竞争吸附
参照张润祺等[24]的文献,设置Cr(Ⅲ)和Cr(Ⅵ)比例分别为3/1、2/1、1/2、1/3 的混合溶液(1 代表Cr的浓度为10 µg·L-1),将DGT 装置在实验溶液中部署6 h后,取出结合膜进行洗脱分析。
1.6 LDHs-DGT的稳定性
为分析LDHs-DGT 使用后DGT 装置吸附的Cr价态的稳定性,以确定DGT 的保质时间,将LDHs-DGT装置部署于300 mL 的含有50 µg·L-1Cr(Ⅲ)和Cr(Ⅵ)的0.01 mol·L-1NaNO3溶液中,部署6 h 后取出装置放入自封袋,并置于5 ℃冰箱中,在第0、1、3、5、7天取出装置并洗脱结合膜,测定洗脱液溶液中的Cr(Ⅲ)和Cr(Ⅵ)浓度,记第n天的测得的Cr(Ⅲ)和Cr(Ⅵ)的浓度为CDGTn(n=1、3、5、7),用第n天与第0天测得的Cr(Ⅲ)和Cr(Ⅵ)的浓度比值(CDGTn/CDGT0)作为稳定性依据。
1.7 LDHs-DGT 应用实例:水分管理对Cr价态变化的影响
土壤Cr的生态风险与Cr的活性和价态有重要关系,而活性态含量、价态变化与土壤水分管理密切相关,为探究LDHs-DGT 应用于土壤Cr 活性与价态变化的可行性,本研究开展了不同水分管理模式下,添加不同价态的Cr 活性及价态变化研究。水分管理设置2 种模式:淹水(3 cm 淹水)、湿润(80%持水量),添加两种价态的Cr:Cr(Ⅲ)[Cr(NO3)3·6H2O]、Cr(Ⅵ)(K2CrO4),分别使土壤中Cr的含量达到土壤筛选值的1.5倍(375 mg·kg-1)。
供试土壤采集于天津市西青区设施农田的耕层(0~20 cm),自然风干混匀后,过2 mm 筛,土壤基本理化性质:pH 为8.01、有机质含量为34.70 g·kg-1、总Cr含量为62.02 mg·kg-1、阳离子交换量为13.46 cmol·kg-1。分别称取6 kg 土壤放入直径20 cm,桶高20 cm的塑料桶内,进行为期60 d 的土壤培养实验,具体处理为:淹水空白对照(Y-CK)、湿润空白对照(S-CK)、淹水外加Cr(Ⅲ)[Y-Cr(Ⅲ)]、湿润外加Cr(Ⅲ)[S-Cr(Ⅲ)]、淹水外加Cr(Ⅵ)[Y-Cr(Ⅵ)]、湿润外加Cr(Ⅵ)[S-Cr(Ⅵ)]。每日对塑料桶称质量,并添加去离子水以保持质量恒定。
分别在第2、4、6、11、16、21、31、41、60天部署长条LDHs-DGT,原位测定土壤活性态Cr(Ⅲ)和Cr(Ⅵ),LDHs-DGT 的长度为15 cm,使用时将LDHs-DGT 垂直插入土壤中,其中0~3 cm 插入淹水层(湿润土壤保持3 cm 空白),3 cm 以下插入土层,每个处理3 个平行。部署48 h后取出LDHs-DGT装置,用超纯水反复冲洗LDHs-DGT 窗口至无土壤颗粒附着,拆开装置,取出结合膜并分段切割(0~3、3~7、7~11、11~15 cm),用6 mL 0.5 mol·L-1HNO3洗脱结合膜2 h,取出洗脱液后平均分为两份,用ICP-MS(美国安捷伦有限公司,7700X)测定总Cr,用超痕量六价铬分析仪(广州谱临晟科技有限公司,ELSpe-2)测定Cr(Ⅵ),用差减法计算Cr(Ⅲ)的含量,得到淹水层(0~3 cm)、浅层土壤(3~7 cm)、中层土壤(7~11 cm)、深层土壤(11~15 cm)的Cr(Ⅲ)和Cr(Ⅵ)含量。
1.8 数据处理与分析
为确保实验结果的准确性,用Cr(Ⅲ)和Cr(Ⅵ)单元素标准溶液配制不同浓度的Cr 标准溶液,并用ICP-MS 和超痕量六价铬分析仪分别测定总Cr 和Cr(Ⅵ),定量误差≤5%。
使用Excel 2021 及SPSS 19.0 统计分析软件对实验数据进行统计、相关性分析及显著性检验,Origin 2021 进行绘图。实验数据均以3 次重复的平均数的形式呈现,2.5~2.6 实验数据用DGT 测量浓度与溶液浓度的比值(CDGT/Csoln)评估DGT 设备对Cr(Ⅲ)和Cr(Ⅵ)的提取效果,即CDGT/Csoln在0.9~1.1 之间认为设备的提取效果好。
2 结果与讨论
2.1 LDHs-DGT空白和方法检出限
DGT用于测定土壤、水体及沉积物中重金属的活性态含量,而重金属的活性态含量通常很低,因此,DGT装置中结合膜的背景值对准确测定重金属的活性态含量有较大的影响[31]。已有研究结果表明,可用于测定活性态Cr 的结合膜中,ZrO2、NMDG 的Cr 背景值分别为0.25、1.86 ng[18,31]。本研究制作的LDHs-DGT结合膜的Cr(Ⅵ)空白值为4.9 ng,未检测出Cr(Ⅲ),略高于Pan等[18]和Gao等[32]的研究。我国《地表水环境质量标准》(GB 3838—2002)规定的I级水中Cr(Ⅵ)的限值为10µg·L-1,假定水体中Cr(Ⅵ)的浓度为限值的1/10,已知改性琼脂糖交联的丙烯酰胺扩散膜中Cr 的扩散系数为5.05×10-6cm2·s-1(25 ℃)[29],将DGT 装置部署于该水体中24 h,结合膜吸附的Cr 量为22.8 ng,是本研究中Cr 背景值的4.6 倍,因此,Cr 的背景值不会影响DGT装置的检测精度。
超痕量六价铬分析仪的Cr(Ⅵ)的检出限为0.08 ng·mL-1,定量限为0.24 ng·mL-1,LDHs 结合膜的空白值为4.9 ng,设待测液体积为3 mL,则LDHs 空白结合膜溶解于待测液,待测液中Cr(Ⅵ)约为1.5 ng·mL-1。如对待测液进行检测,待测液浓度应不低于5 ng·mL-1,结合Cr 的扩散系数可以计算得出,水体中Cr 的检出限应为0.22µg·L-1。
2.2 吸附动力学和洗脱效率
对于DGT 装置而言,通过扩散膜的目标元素,需要被结合膜快速吸附,从而确保吸附界面的目标元素浓度接近于0,形成稳定的梯度扩散[24]。图1 为LDHs结合膜Cr(Ⅲ)和Cr(Ⅵ)的吸附动力学曲线,LDHs-DGT 装置中结合膜对Cr(Ⅲ)和Cr(Ⅵ)的吸附符合一级动力学模型,其中对Cr(Ⅲ)的吸附R2=0.994 2,对Cr(Ⅵ)的吸附R2=0.991 3。本实验中,在240 min 以前,LDHs-DGT装置中结合膜对Cr(Ⅲ)和Cr(Ⅵ)的吸附状况均表现为线性增加,240 min后快速达到平稳,此时Cr(Ⅲ)的吸附量为(213.6±1.0)µg,达到了Cr 总含量的93%,Cr(Ⅵ)的吸附量为(228.4±0.5)µg,达到了Cr 总含量的98%。这说明LDHs 结合膜对Cr(Ⅲ)和Cr(Ⅵ)均有较快的吸附速率,可以作为LDHs-DGT装置的结合膜使用。

图1 LDHs结合膜Cr(Ⅲ)和Cr(Ⅵ)的吸附动力学Figure 1 Adsorption kinetics of Cr(Ⅲ)and Cr(Ⅵ)on LDHs binding gels
对于DGT 装置来说,目标元素被吸附在结合膜上,需要有合适的洗脱剂进行洗脱,以方便测定。LDHs属于碱性材料,遇酸会崩解,在其他学者的研究中发现,pH 低于3 时,LDHs 材料会发生轻微溶解,结构的稳定性会受到影响[30],因此选用HNO3作为洗脱剂,不仅适合该实验,也方便了后续ICP-MS 的测定。实验设置不同浓度的HNO3作为LDHs 结合膜的洗脱液,实验结果见表1,0.05 mol·L-1HNO3对Cr(Ⅲ)和Cr(Ⅵ)的洗脱效率分别为42.50% 和85.24%;0.1 mol·L-1HNO3对Cr(Ⅲ)和Cr(Ⅵ)的洗脱效率为59.34%和77.98%,洗脱效率均低于90%。0.5 mol·L-1HNO3对Cr(Ⅲ)和Cr(Ⅵ)的洗脱效率分别为104.69%和98.91%;当洗脱液浓度超过0.5 mol·L-1时,虽然会使LDHs结合膜快速崩解,但实验结果表明,Cr(Ⅲ)会被氧化为Cr(Ⅵ),使实验结果失真。综上表明:0.5 mol·L-1HNO3是LDHs-DGT装置中结合膜最适宜的洗脱液。
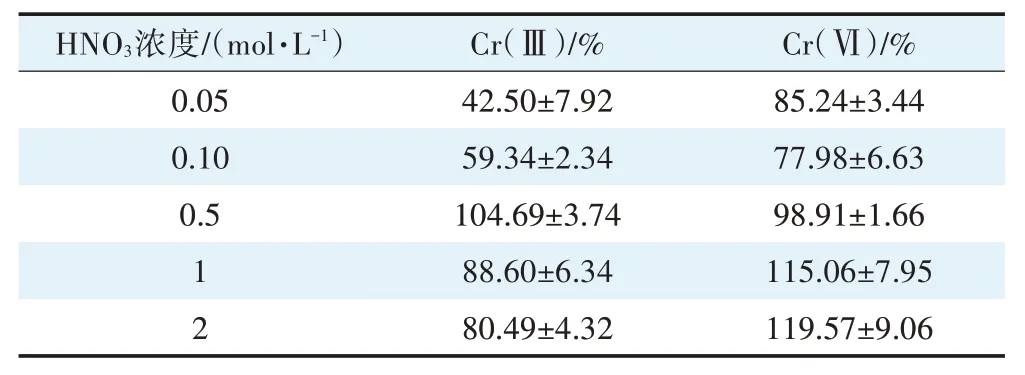
表1 不同浓度HNO3对Cr(Ⅲ)和Cr(Ⅵ)的洗脱效率Table 1 Elution efficiency of Cr(Ⅲ)and Cr(Ⅵ)from LDHs binding gels using HNO3 of different concentrations
2.3 扩散凝胶中的扩散系数
依据梯度扩散薄膜(DGT)基础理论,DGT装置中由于扩散膜的存在,会使得目标元素与结合膜之间有一个浓度梯度,目标物质需要通过保护膜和扩散膜,才能与结合膜相结合,因此若想得到准确的CDGT,必须明确待测离子在扩散凝胶中的扩散速率。
图2为Cr(Ⅲ)和Cr(Ⅵ)的扩散系数曲线,将通过LDHs-DGT装置扩散膜,被结合膜吸附固定的Cr(Ⅲ)和Cr(Ⅵ)的量(ng)对时间(min)作图,可以得到两条线性曲线(R2=0.999),通过公式(2)计算,可以得出:在实验温度为20 ℃的条件下,Cr(Ⅲ)的扩散系数为(3.58±0.02)×10-6cm2·s-1,Cr(Ⅵ)的扩散系数为(7.03±0.09)×10-6cm2·s-1。可以发现,Cr(Ⅵ)比Cr(Ⅲ)的扩散系数大,这表示在相同布置时间且Cr(Ⅲ)和Cr(Ⅵ)浓度相同的条件下,LDHs-DGT 装置中Cr(Ⅵ)的扩散量更大。
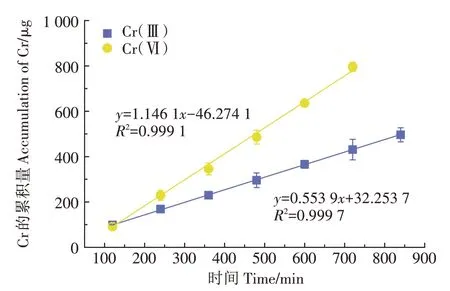
图2 Cr(Ⅲ)和Cr(Ⅵ)的扩散系数曲线Figure 2 Masses of Cr(Ⅲ)and Cr(Ⅵ)diffused through the diffusive gel versus time in a diffusion cell
关于LDHs对Cr的吸附,大多集中于对Cr(Ⅵ)的吸附研究,鲜有对C(rⅢ)的吸附研究[21,33-34],原因可能是Cr(Ⅵ)常以含氧阴离子的形式存在,毒性强,且易与LDHs 结构中的插层阴离子交换,被吸附固定。而Cr(Ⅲ)在常规水体中,常以0 价存在,其运移性差,毒性低,但Visual MINTEQ 3.1 模拟结果表明:水体中仍会存在少量离子态的Cr3(+pH<6),其主要形态为、Cr(OH)2+、Cr(OH)(3aq),见表2。LDHs表面含有大量羟基,同时纳米LDHs 又表现出一定的纳米吸附特性,羟基对Cr3+、、Cr(OH)2+吸附的同时,又会促进Cr(OH)3的解离,从而使LDHs也表现出对Cr(Ⅲ)的吸附[35],将LDHs 制作成DGT 结合膜,放置于扩散膜后,在含有羟基的Cr(Ⅲ)通过扩散膜时,又会促进其解离[36],进而表现出对Cr(Ⅲ)良好的吸附性能。
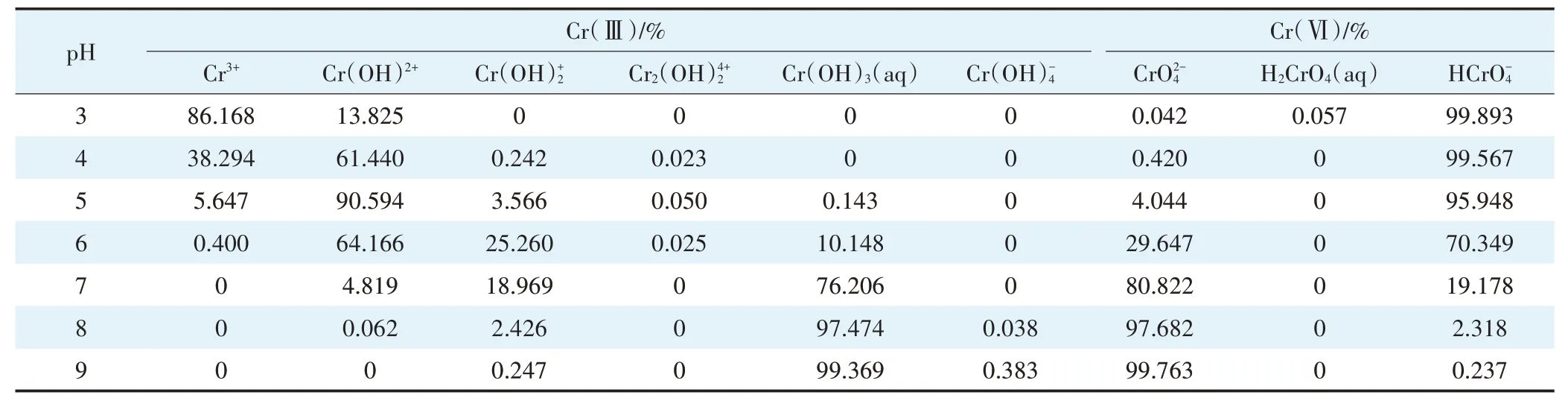
表2 不同pH条件下Cr(Ⅲ)和Cr(Ⅵ)溶液中各组分组成及其所占比例Table 2 Composition and proportion of components in Cr(Ⅲ)and Cr(Ⅵ)solutions under different pH conditions
2.4 LDHs结合膜的吸附容量
在环境中,为了能够实现目标元素的准确测定,LDHs-DGT 装置的吸附容量越高,测定阈值就越高,可适用范围越广。图3 为Cr(Ⅲ)和Cr(Ⅵ)的吸附容量曲线,随着Cr溶液浓度的升高,结合膜中Cr(Ⅲ)和Cr(Ⅵ)的累积量呈现先急速上升,后趋于平缓的趋势,对其进行Langmuir 和Freundlich 吸附等温线模型拟合,结果表明Langmuir 模型拟合结果的R2=0.955 6[对Cr(Ⅲ)的吸附]和R2=0.959 3[对Cr(Ⅵ)的吸附],Freundlich 模型拟合结果的R2=0.868 9[对Cr(Ⅲ)的吸附]和R2=0.866 1[对Cr(Ⅵ)的吸附]。经过计算可得,LDHs 结合膜对Cr(Ⅲ)和Cr(Ⅵ)的最大吸附量分别为181.27 µg·cm-2和176.29 µg·cm-2。与Pan 等[18]开发的NMDG 结合膜相比,吸附Cr(Ⅵ)的容量稍小,但NMDG 结合膜不能用于Cr(Ⅲ)和Cr(Ⅵ)的同时检测中;与Devillers 等[19]使用的ZrO2结合凝胶相比,对Cr(Ⅲ)和Cr(Ⅵ)的吸附容量均高于ZrO2结合凝胶。
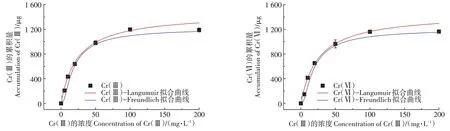
图3 Cr(Ⅲ)和Cr(Ⅵ)的吸附容量曲线Figure 3 Adsorption capacity curves of Cr(Ⅲ)and Cr(Ⅵ)
2.5 pH、离子强度、硫酸盐、有机质的影响
DGT装置使用的环境介质包括土壤、水体及沉积物[37],环境条件的改变,必然会对DGT 测定重金属活性态的准确性产生一定影响,主要表现在:一是温度的改变,影响扩散膜的扩散系数,二是pH 值、离子强度、干扰离子影响了结合膜对目标离子的吸附性能,温度影响扩散膜的扩散系数可以采用温度模型矫正[38],而不同环境条件对结合膜吸附性能的影响需要通过实验来确定。以水体实验为例,当环境因子导致测量获得的CDGT与水体中对应离子的浓度Csoln的比值(CDGT/Csoln)超过0.9~1.1 的范围时,则认为环境因子影响了DGT 的准确性。不同环境因子对LDHs-DGT 装置测定Cr(Ⅲ)和Cr(Ⅵ)的影响如图4所示。

图4 环境因子对LDHs-DGT测定Cr(Ⅲ)和Cr(Ⅵ)的影响Figure 4 Effects of environmental factors on the measurements of Cr(Ⅲ)and Cr(Ⅵ)by LDHs-DGT
对于pH,在pH=5~8 时,0.9≤CDGT/Csoln≤1.1,可见在此范围内,LDHs-DGT 可实现对活性态Cr(Ⅲ)和Cr(Ⅵ)的准确测定,当pH≤4 时,由于LDHs 是一种碱性材料,遇酸会崩解,当pH 太低时,结合膜结构遭到破坏,影响Cr(Ⅲ)和Cr(Ⅵ)的吸附效果[30],当pH 过高(pH=9)时,Cr(Ⅲ)主要以0 价的Cr(OH)3形式存在(表2),运移性减弱,且在高pH 情况下结合膜表面的氢氧化物沉淀也会影响目标离子在结合膜上的吸附[39],过量的H+和OH-会与其他离子竞争,进而导致目标离子的吸附减少[24,40]。可见,LDHs-DGT 装置对pH 的适用范围为5~8,而我国土壤的pH 大多数在4.5~8.5 内,因此本装置适用于我国大多数土壤环境。
由于NO-3广泛存在于水体和土壤中,实验中我们用NaNO3浓度来表征离子强度的大小。当离子强度≤50 mmol·L-1时,0.9≤CDGT/Csoln≤1.1,认为可以实现Cr(Ⅲ)和Cr(Ⅵ)的准确测定;当离子强度升高到100 mmol·L-1时,Cr(Ⅲ)和Cr(Ⅵ)的CDGT/Csoln<0.9,无法实现Cr(Ⅲ)和Cr(Ⅵ)的准确测定,该结果与其他学者的研究类似[18-19,32],造成这一现象的原因可能是会和、发生竞争吸附造成的。并且溶液的离子强度会影响离子的活度系数,在离子强度较高(100 mmol·L-1)时,离子的活度下降,目标元素的扩散速率下降,影响最终吸附效果[39];离子强度可以由于静电相互作用,减少LDHs结合膜结合位点的有效数量,影响对Cr(Ⅲ)和Cr(Ⅵ)的吸附效果[40]。海水和土壤中的离子强度较高,其中海水的离子强度约为60 mmol·L-1[41],土壤中离子强度约为10 mmol·L-1[42],LDHs-DGT装置的最适宜离子强度条件为1~50 mmol·L-1,因此,该装置适合于大多数土壤和水体环境。
由于硫酸盐广泛存在于天然水域和土壤中,并且类似于铬酸盐离子,可能会干扰Cr(Ⅵ)的测定[19],因此,我们研究不同浓度的SO2-4对LDHs-DGT 测定Cr(Ⅵ)的干扰。在c(SO2-4)≤5 mmol·L-1时,CDGT/Csoln的值在0.9~1.1 范围内,认为可以实现对Cr(Ⅵ)的准确测定。当SO2-4浓度达到10 mmol·L-1时,CDGT/Csoln的值降低至0.71,该结果与Gao 等[32]、Devillers 等[19]的研究一致,这种现象出现的原因可能是CrO2-4和SO2-4均为含氧阴离子,结构类似,在结合膜吸附Cr(Ⅵ)时,SO2-4会与CrO2-4产生竞争吸附,打破LDHs结合膜对Cr(Ⅵ)的吸附平衡。因此,LDHs-DGT 装置的最适宜硫酸盐浓度条件为0.01~5 mmol·L-1,只有当硫酸盐与Cr(Ⅵ)的摩尔比超过1 000时,才会出现硫酸盐干扰。
在环境中,由于金属自身的结构特性,可以与有机物质反应,生成金属络合物。腐植酸(HA)有如芳香环、杂环、多环化合物的结构,有如羧基、酚羟基、甲氧基、酰胺基等的官能团[43],会与金属离子通过静电、离子交换、络合的方式相结合[44]。因此,我们设置不同Cr/HA 质量的比例,探究HA 对LDHs-DGT 测定Cr(Ⅲ)和Cr(Ⅵ)的干扰程度,如图4所示,可见在HA存在的情况下,均会使结果变小。经Visual MINTEQ 3.1 模拟不同m(Cr)/m(HA)下Cr(Ⅲ)和Cr(Ⅵ)的存在形态,结果如表3 所示,可以发现,在添加HA 后,Cr(Ⅲ)和Cr(Ⅵ)的形态变化较小,即HA 在Cr形态改变方面作用较小,而HA 的分子大小为0.01~1µm[24,45],本研究DGT 装置保护膜孔径为0.45 µm,凝胶扩散膜的平均孔径大小为30 nm[24,46],在磁力搅拌的作用下,HA 可以透过保护膜,堵塞扩散膜孔径,阻碍Cr(Ⅲ)和Cr(Ⅵ)通过扩散膜,减少扩散量[24],使得CDGT/Csoln下降,因此在实际应用中,若环境中的有机质含量过高,会对检测结果造成不利影响。
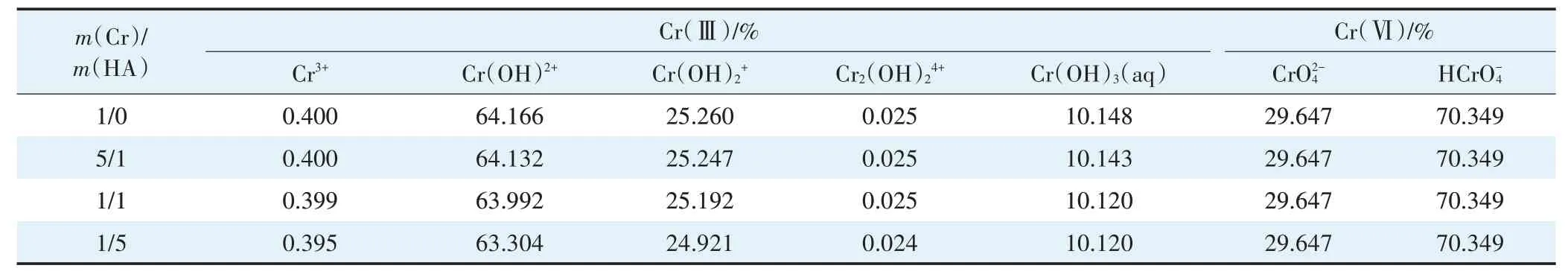
表3 不同m(Cr)/m(HA)比例下Cr(Ⅲ)和Cr(Ⅵ)溶液中各组分组成及其所占比例Table 3 Composition and proportion of components in Cr(Ⅲ)and Cr(Ⅵ)solutions under different m(Cr)/m(HA)
2.6 Cr(Ⅲ)和Cr(Ⅵ)的竞争吸附
将LDHs-DGT 装置放于不同Cr(Ⅲ)和Cr(Ⅵ)浓度比例下的溶液中,实验结果如图5 所示,当CCr(Ⅲ)/CCr(Ⅵ)=3/1、2/1、1/2、1/3 时,CDGT/Csoln值均在0.9~1.1 的范围内,即Cr(Ⅲ)和Cr(Ⅵ)在环境中的浓度不同时,也不会对LDHs-DGT装置测定的准确性产生影响,原因在于LDHs 对Cr(Ⅲ)和Cr(Ⅵ)的吸附机制存在明显不同,对Cr(Ⅲ)的吸附以与LDHs 表面的羟基络合沉淀为主,对Cr(Ⅵ)的吸附以与LDHs 的插层阴离子交换为主[33]。
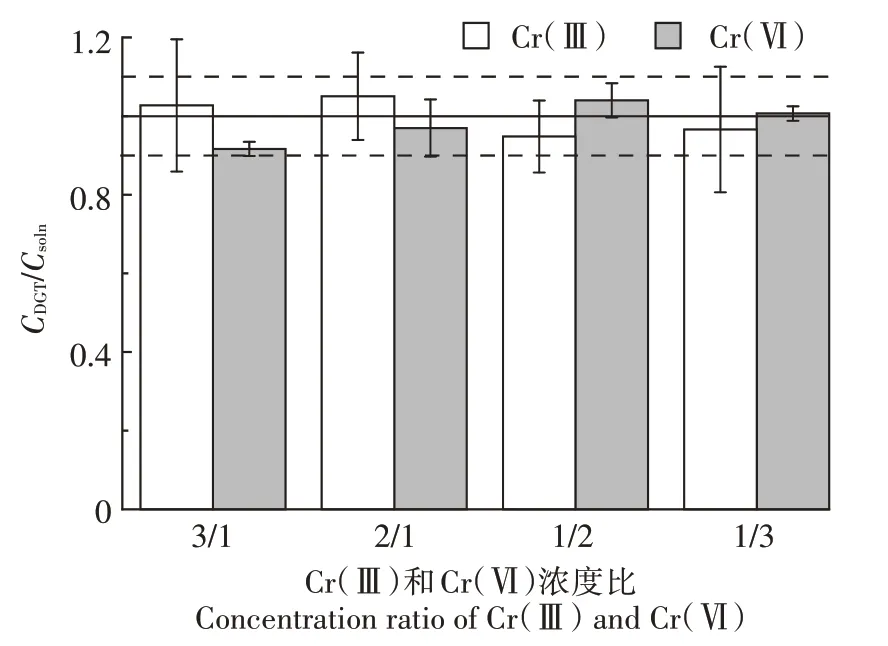
图5 不同比例Cr(Ⅲ)和Cr(Ⅵ)情况下对LDHs-DGT测定的影响Figure 5 Effects of different ratios of Cr(Ⅲ)and Cr(Ⅵ)on LDHs-DGT determination
2.7 LDHs-DGT的稳定性
当LDHs-DGT提取Cr(Ⅲ)和Cr(Ⅵ)后,若Cr(Ⅲ)和Cr(Ⅵ)的价态发生转化,将会直接影响检测结果,导致数据失真,因此,研究LDHs-DGT 吸附后Cr(Ⅲ)和Cr(Ⅵ)的价态稳定性至关重要。LDHs-DGT 中吸附Cr(Ⅲ)和Cr(Ⅵ)的稳定性实验结果如图6所示,在提取后1~7 d,LDHs-DGT 装置中的Cr(Ⅲ)和Cr(Ⅵ)的检测值稍有下降,Cr(Ⅲ)的平均下降速率为0.24µg·L-1·d-1,Cr(Ⅵ)的平均下降程度为1.26 µg·L-1·d-1,Cr(Ⅵ)下降程度大于Cr(Ⅲ),可能是长时间放置Cr(Ⅵ)存在一定的还原,Cr(Ⅲ)存在一定的氧化情况。但方差分析结果表明,在实验时间内,测定结果均无显著差异,但仍存在一定的价态变化。因此,建议提取目标元素后的LDHs-DGT应尽快检测。

图6 LDHs-DGT中吸附的Cr(Ⅲ)和Cr(Ⅵ)的稳定性Figure 6 Stability of Cr(Ⅲ)and Cr(Ⅵ)adsorbed in LDHs-DGT
2.8 LDHs-DGT 应用实例:水分管理对Cr价态变化的影响
为验证LDHs-DGT装置的实际应用效果,开展了水分管理对Cr 价态变化的影响实验,实验结果如图7、图8 所示。图7 为空白对照组和添加外源Cr 后,淹水和湿润土壤中活性态Cr[Cr(Ⅲ)和Cr(Ⅵ)的总和]的含量变化情况,可以发现在空白对照组中,活性态Cr 的含量均呈现先下降后保持稳定的趋势,在淹水6 d内为快速下降期,与初期相比,第6 d的活性态Cr降幅达80%以上,可见淹水会使土壤中Cr 的活性明显降低,与同为含氧阴离子的As 相比,二者性质不同,淹水均会使Cr、As 向还原态转化,但Cr 的转化使Cr的活性降低,而As 的转化使As 的活性增加[47]。实验结果进一步表明:淹水层的活性态Cr 含量大于土壤溶液,这可能是Cr易于向地下水淋溶的原因[48-49]。添加外源Cr 后,随着时间的延长,淹水土壤和湿润土壤中活性态Cr 的含量均表现为下降趋势,这是Cr 在土壤中老化的必然结果。外加Cr(Ⅲ)后土壤活性态Cr的变化幅度明显小于外加Cr(Ⅵ),即Cr(Ⅵ)的活性明显大于Cr(Ⅲ)。
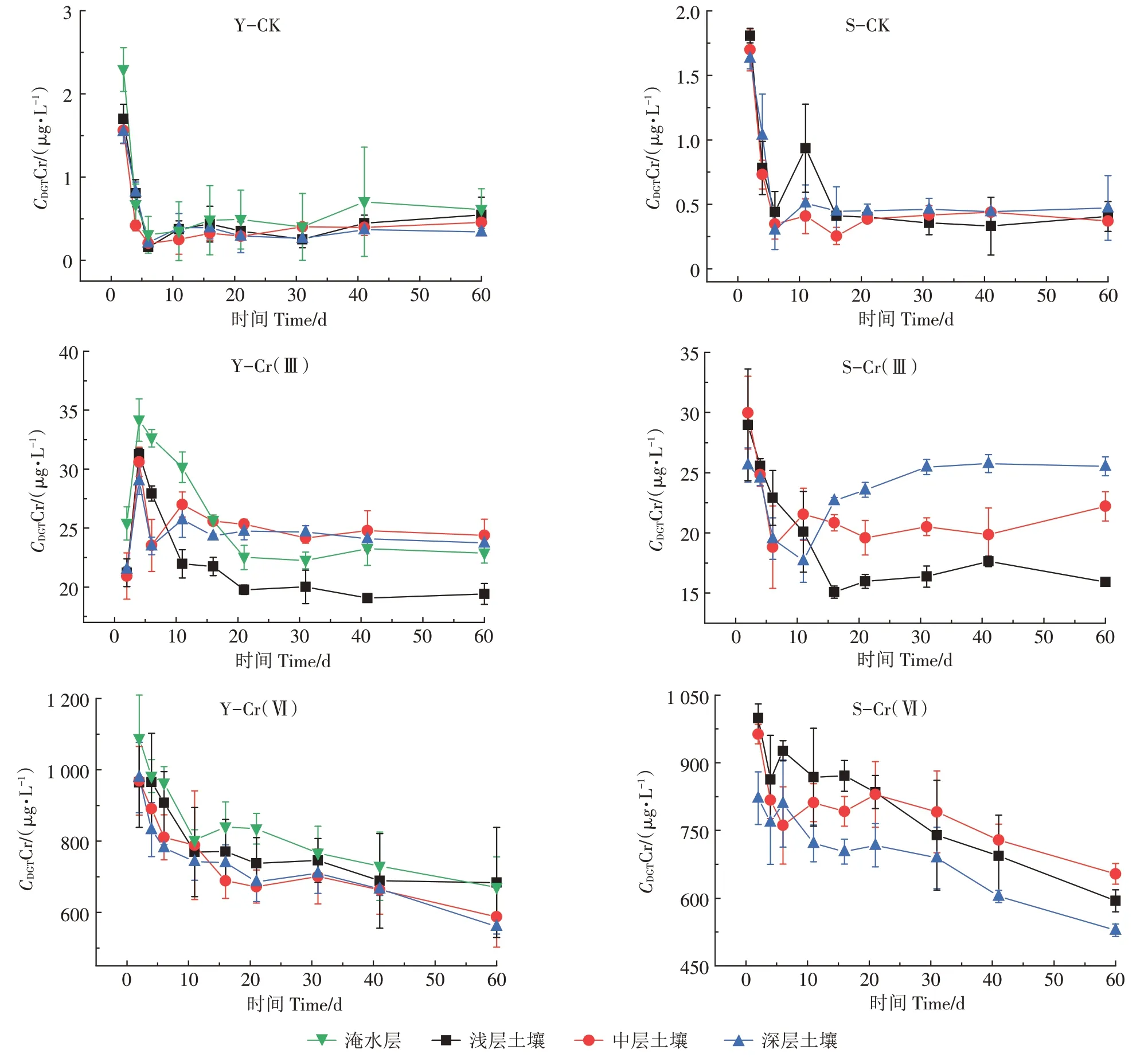
图7 LDHs-DGT测定的空白对照组和外加Cr土壤中总Cr的浓度Figure 7 Concentrations of total Cr in the blank control group and the Cr-added soil determined by LDHs-DGT
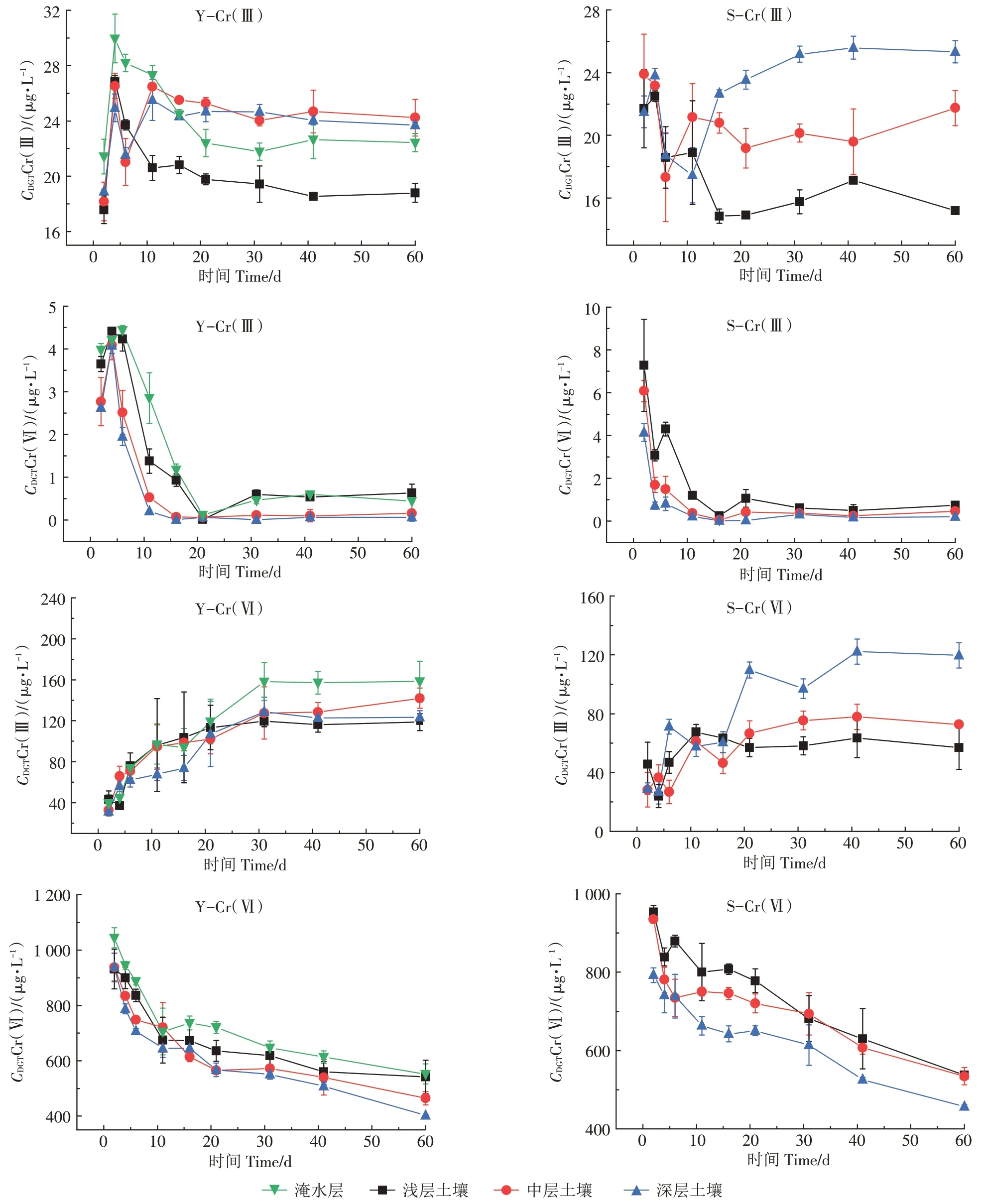
图8 LDHs-DGT测定的外加Cr土壤中Cr(Ⅲ)和Cr(Ⅵ)的浓度Figure 8 Concentrations of Cr(Ⅲ)and Cr(Ⅵ)in soils added with Cr determined by LDHs-DGT
图8 为添加外源Cr 后,土壤中活性态Cr(Ⅲ)和Cr(Ⅵ)的浓度变化情况,在淹水土壤中,外加Cr(Ⅲ)后,Cr(Ⅲ)的变化趋势为:先增加后减少,然后趋于稳定,Cr(Ⅵ)的变化趋势为:先增加,后快速下降,在20 d 左右趋于平稳;外加Cr(Ⅵ)后,Cr(Ⅲ)的变化趋势为:先增加后趋于稳定,Cr(Ⅵ)的变化趋势为:逐渐下降。在湿润土壤中,Cr(Ⅲ)和Cr(Ⅵ)的变化趋势与淹水土壤类似,但也存在一定差异,主要表现在外加Cr(Ⅲ)后,Cr(Ⅲ)在浅层土壤中表现为逐渐下降,深层土壤表现为先下降后升高。
之所以出现以上变化趋势,对于Cr(Ⅵ)而言,土壤无论是在淹水或湿润状态下,土壤Eh 均会低于500 mV[50],从而使Cr(Ⅵ)还原,导致检测的活性态Cr(Ⅵ)含量降低,土层越深,Eh 值越低,Cr(Ⅵ)的降低幅度越大。对于Cr(Ⅲ)而言,淹水和湿润管理对Cr 的活性影响差异较大,主要表现在深层土壤上,淹水使中层和深层土壤的Eh 值差异不显著,而湿润管理会导致表层土壤与中层土壤、深层土壤的Eh 值差异显著,尤其是管理后期这种差异更明显,Eh 值越低,Cr(Ⅲ)的含量越高。同时在浅层土壤中,Fe容易形成次生矿物,将Cr(Ⅲ)固定[8],导致Cr(Ⅲ)含量下降,而在深层土壤中,土壤培养前期(0~11 d),Fe形成次生矿物,先将Cr(Ⅲ)固定[8],在土壤培养中后期(11~60 d),深层土壤环境还原性强,Fe发生还原,固定Cr(Ⅲ)能力减弱[51],致使Cr(Ⅲ)含量逐渐上升,可见Eh 值和Fe对Cr的形态和活性的变化起至关重要的作用。
3 结论
本研究以纳米Mg/Al双层氢氧化物(Mg/Al-LDHs)作为梯度扩散薄膜(DGT)的结合膜材料,开发了一种新型的提取测定环境中活性态Cr 的装置。研究结果表明:LDHs-DGT 装置中LDHs 结合膜对Cr(Ⅲ)和Cr(Ⅵ)均有较快的吸附速率,其最大吸附量分别是181.27 µg·cm-2和176.29 µg·cm-2,该装置可在pH 为5~8、离子强度小于50 mmol·L-1的环境中对Cr(Ⅲ)和C(rⅥ)实现准确提取,能够有效避免干扰离子对装置的影响,空白背景值为4.9 ng,方法检出限为0.22 ng·mL-1,Cr(Ⅲ)和Cr(Ⅵ)在扩散膜中的扩散系数分别为(3.58±0.02)×10-6cm2·s-1和(7.03±0.09)×10-6cm2·s-1。将该装置应用于不同水分管理模式下Cr 形态迁移转化规律实验中,结果表明LDHs-DGT可以高效侦测土壤活性态Cr的时空变化态势,并能对Cr(Ⅲ)和Cr(Ⅵ)的价态变化进行动态监测。综上所述,LDHs-DGT 装置应用前景广泛,可以为环境中Cr 的监测和评估提供技术支撑。
