丝状真菌降解拟除虫菊酯类农药和3-苯氧基苯甲酸研究进展
2023-11-07张梦梅李建龙胡凯弟刘书亮
周 巧,张梦梅,李建龙,胡凯弟,李 琴,刘书亮
(四川农业大学食品学院,四川 雅安 625014)
拟除虫菊酯(pyrethroids,PYRs)类农药由于其杀虫谱广、药效高、对非靶标生物毒性低,被广泛应用于农业、林业和公共领域的蚊虫和害虫防治,是除有机磷农药之外的第二大类杀虫剂,约占全球农药市场的30%以上[1]。PYRs具有光、热稳定性,在自然条件下很难快速降解,其残留引起的环境污染和食品安全问题较为严重[2]。研究表明,PYRs可经消化道、呼吸道和皮肤黏膜进入机体,对微生物、水生动物和无脊椎动物产生高度急性毒性,包括神经毒性、免疫毒性和生殖毒性[3],此外,PYRs的降解中间产物3-苯氧基苯甲酸(3-phenoxybenzoic acid,3-PBA)比母体农药更难降解,毒性更强,不仅是一种潜在的环境污染物,也是一种具有免疫毒性的内分泌干扰物,可导致人体内分泌代谢紊乱,同时3-PBA还能阻止微生物降解母体农药PYRs,其残留进一步加重了对环境及农产品的污染[4]。因此,如何消减环境及农产品中PYRs和3-PBA残留引起了广泛关注。
物理、化学等农残降解方法因设施复杂昂贵和对环境安全性要求高而被限制,而微生物降解是一种安全、高效、廉价和没有二次污染的修复方法,被认为是治理农药环境污染和消减农产品中农药残留的有效途经[5]。目前,微生物降解PYRs和3-PBA已被广泛报道,现已筛选分离到较多PYRs和3-PBA降解细菌,如肺炎克雷伯杆菌、鞘氨醇单胞菌、鞘脂菌、假单胞菌、地衣芽孢杆菌等[6],其研究也已深入到降解基因及降解酶的层面,如来源于不同细菌的estP、pytH、pytZ、pytY、est3385基因编码的羧酸酯酶,estA基因编码的脂肪酶,aps基因编码的氨肽酶,chbE、rhe8、est2基因编码的酯酶,以及pbaA1A2BC、dpeAlA2基因编码的双加氧酶已经被分离鉴定并证明是PYRs及3-PBA降解的关键基因及关键酶[4,7],关于细菌降解3-PBA的调控机制也有研究,来源于文新鞘脂菌(Sphingobium wenxiniae)JZ-1中的pbaA1A2B基因簇对3-PBA降解过程存在转录调控,pbaA1A2B的特异性转录激活因子PbaR响应3-PBA对pbaA1A2B基因簇进行转录激活[8]。
丝状真菌因其具有丰富的氧化酶系,对多种芳香族类化合物、杀虫剂、染料等异生化合物具有较强的降解能力[9],在生物修复中具有独特的优势,相比于其他微生物,丝状真菌是降解顽固异生化合物的优势物种,虽然现已有关于高效降解PYRs和3-PBA丝状真菌的报道,如枝孢菌(Cladosporiumsp.)HU在5 d内可完全降解100 mg/L的氰戊菊酯,米曲霉(Aspergillus oryzae)M4在72 h内对100 mg/L的3-PBA降解率为80.1%,黑曲霉(Aspergillus niger)YAT1在22 h内可完全降解100 mg/L的3-PBA[10],但研究仅停留在对降解菌的降解性质和降解途径方面,对降解酶的研究不深入,降解酶编码的基因少见报道,降解机制的研究仍属空白。
随着分子生物学技术的发展,基因组学、转录组学及蛋白质组学等技术的应用越来越广泛,可通过这些方法对丝状真菌降解过程中的酶进行挖掘,并阐明其降解机制,同时可以通过异源表达、基因敲除等方法对其降解酶的编码基因进行功能验证。因此本文总结了降解PYRs和3-PBA的丝状真菌、降解途径及降解酶,详述了降解酶基因的筛选与验证方法,这不仅可为丝状真菌降解PYRs和3-PBA的降解途径和降解机制的研究提供理论依据,也可为环境及农产品的生物修复提供应用参考。
1 拟除虫菊酯类农药和3-苯氧基苯甲酸概述
1.1 拟除虫菊酯类农药和3-苯氧基苯甲酸基本性质
表1列出了PYRs和3-PBA结构、种类和特点。PYRs是一种人工合成的化合物,其化学结构和生物活性与天然的除虫菊酯类似,难溶于水,自然条件下不易分解。根据其化学结构和毒性,可将PYRs分I型和II型,I型缺乏氰基,主要包括丙烯菊酯和联苯菊酯等;II型具有α-氰基,主要包括氯氰菊酯和溴氰菊酯等,比I型更具有神经毒性[11]。

表1 PYRs和3-PBA结构、种类及特点[11-12]Table 1 Structures,types and characteristics of PYRs and 3-PBA[11-12]
3-PBA是PYRs的主要代谢产物之一,纯品为白色或淡黄色结晶状粉末,熔点147~149 ℃,难溶于水,易溶于有机溶剂,CAS登录号为3739-38-6,分子式为C13H10O3,相对分子质量为214.22。与PYRs相比,3-PBA结构更稳定,在自然条件下更难降解,极性更强,在土壤中的迁移速率也比PYRs快。根据土壤类型、气候和其他条件,3-PBA在土壤中的半衰期一般为180 d,远超过PYRs[12]。
1.2 拟除虫菊酯类农药和3-苯氧基苯甲酸残留现状及危害
PYRs由于低毒、高效被广泛使用,其残留问题也较严重,在土壤、空气、水体及农产品[13]中都有残留的PYRs检出,其中在蔬菜、水果、茶叶等农产品中残留检出量为0.95~4 100.00 ng/g,且氯氰菊酯的检出率最高[14]。随着PYRs的广泛使用,其主要代谢产物3-PBA在土壤、农产品、人类尿液[1]及母乳[15]的检出率也越来越高,是人类尿液中检出率最高的异生物质[16]。
PYRs残留期虽短,但长期低剂量接触PYRs可导致慢性疾病。研究表明,PYRs具有影响离子通道、改变兴奋性神经递质水平、诱导神经细胞凋亡和扰动氧化应激水平等毒性作用,对脑组织产生严重损伤[17],并对生物体的神经、免疫、心血管和遗传系统产生毒性作用[18]。此外,PYRs还可影响成年女性卵巢功能[19]、降低男性精子的质量[20]、影响青少年听力水平[21]和学龄儿童认知水平[22],孕早期暴露于PYRs中还可能影响2 岁儿童的神经发育[23]等。而PYRs代谢产物3-PBA是一种抗雌激素类物质,具有内分泌干扰活性,也是一种多巴胺神经毒素,可能导致生物体帕金森病[24]。相关研究发现,1 mg/L的3-PBA可引起斑马鱼胚胎心包水肿和心率降低[25];尿液中的3-PBA可能与心血管疾病和冠心病的发病率增加有关[26],成年男性尿液中3-PBA水平与血清甲状腺素和总三碘甲状腺原氨酸水平呈负相关,影响甲状腺激素平衡[27];3-PBA也有明显的肝毒性,可通过调节半胱氨酸蛋白酶-3和B细胞淋巴瘤2(B-cell lymphoma-2,Bcl-2)诱导细胞凋亡[28]。同时3-PBA具有一定抗微生物活性,如果不能被及时降解,会抑制微生物的代谢活性,进一步阻碍母体农药的矿化降解,从而阻断该类农药彻底转化为无毒小分子物质,间接地使环境、农产品或食品中农药残留问题更加严峻。
2 丝状真菌降解PYRs和3-PBA的研究进展
丝状真菌一般指霉菌,是一种呈丝状、无光合作用的广泛分布于土壤、水域、空气及动植物体内外等自然环境中的真核微生物,包括子囊菌门、接合菌门和担子菌门。20世纪80年代中期,Science首次报道了可降解农药的白腐真菌[29],随后又发现了降解农药的新种曲霉属,直至近几年丝状真菌降解农药的研究才陆续被报道。
丝状真菌相较于其他微生物降解农药有以下几方面的优势[30]:1)生物量更大而且遗传特性更加稳定,含有更多蛋白质编码基因;2)它可在任何基质和恶劣的环境条件下生长,存在于北极、深海、动物及其遗骸、海藻、红树林和土壤中;3)含有包含内切葡聚糖酶、外切葡聚糖酶和β-葡糖苷酶在内的纤维素分解酶、木质素分解酶和漆酶(laccase,Lac)等胞外酶和细胞色素P450(cytochrome P450,CYP450)等胞内酶组成的独特氧化酶系统,可降解二苯醚类、芳香族类、氯酚类、杀虫剂及染料等物质[31]。因此,丝状真菌是农药降解的优势物种,并且许多丝状真菌被归类为公认安全的(generally recognized as safe,GRAS)微生物,在消减农产品及食品中农药残留方面有较好的应用前景。
丝状真菌降解农药可通过不同机制来完成[30],主要是矿化作用和共代谢作用。矿化作用是微生物以农药为唯一碳源和能源,使其彻底降解为水和二氧化碳;共代谢作用是微生物从其他底物获取大部分或全部碳源和能源后将同一介质中的农药进行降解,通常对农药的降解不彻底,会产生并积累毒性化合物,共代谢作用可降解顽固化合物如氯化烯烃、多环芳烃、多氯联苯、杀虫剂和药物等,以该方式进行降解的微生物广泛存在于自然界中[32]。
2.1 降解PYRs和3-PBA的丝状真菌
具有降解PYRs和3-PBA的微生物广泛存在于自然界中,目前已筛选到大量可降解PYRs和3-PBA的丝状真菌,表2和表3分别列出对PYRs和3-PBA具有降解能力的丝状真菌。由表2可知,降解PYRs的丝状真菌主要包括白腐真菌、曲霉属、散囊属、青霉属、地霉属、顶孢霉属、枝孢属、镰刀菌属等,其主要来源于土壤、农药厂污泥,其中枝孢菌(Cladosporiumsp.)HU[33]、曲霉菌(Aspergillussp.)PYR-P2[34]、镰刀菌(Fusariumsp.)TS-203及毛链孢菌(Monilochaetessp.)TS-205[35]对100 mg/L的PYRs降解率大于90%。降解3-PBA的丝状真菌相对较少,主要有曲霉属、散囊属、青霉属、根霉属等,其来源主要有黑茶、砖茶、酱醅及农药厂污泥,其中黑曲霉(Aspergillus niger)YAT1[36]、冠突散囊菌(Eurotium cristatum)ET1[37]、米曲霉(Aspergillus oryzae)M4[38]不仅对100 mg/L的3-PBA有较高的降解率,达到99%以上,并且它们还可以降解PYRs。
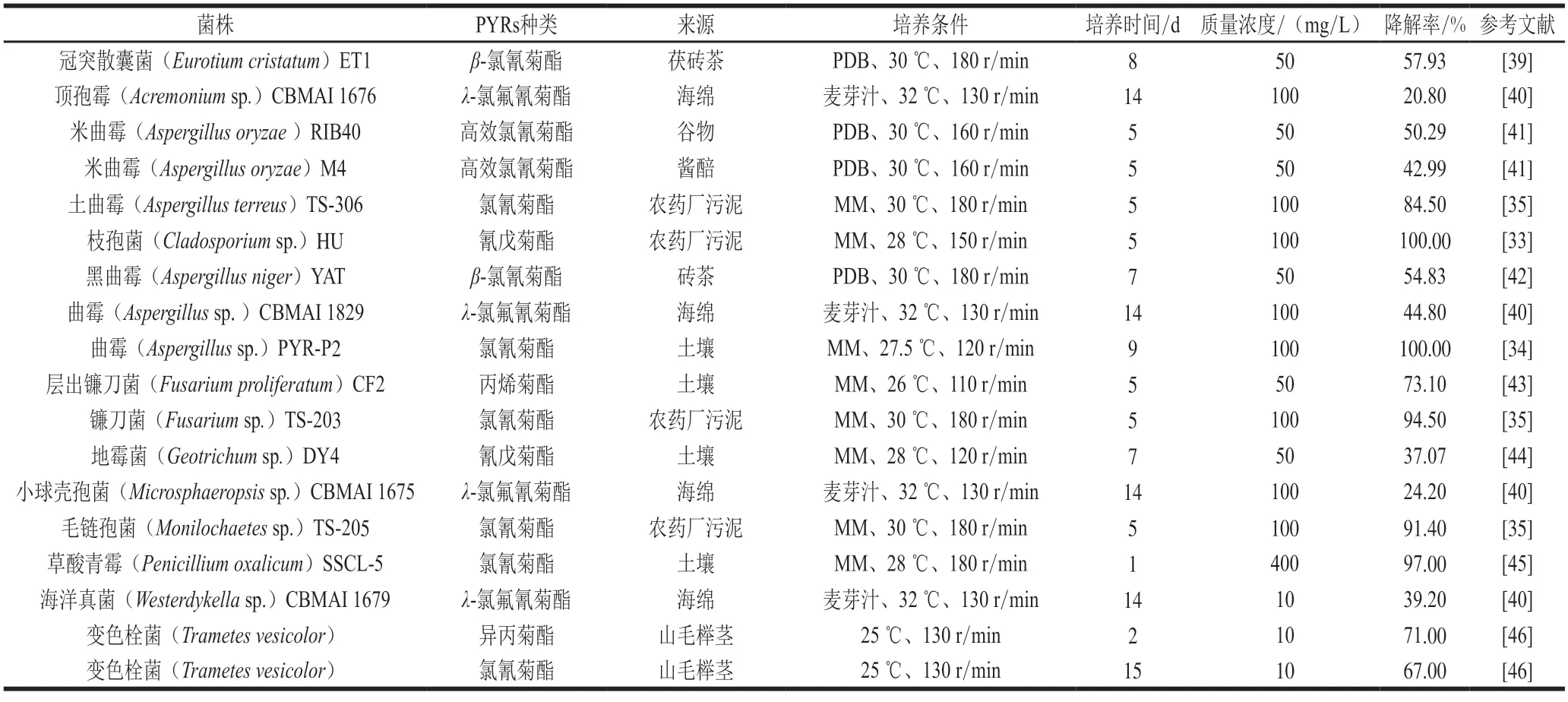
表2 降解PYRs的丝状真菌Table 2 Filamentous fungi used for the degradation of PYRs

表3 降解3-PBA的丝状真菌Table 3 Filamentous fungi used for the degradation of 3-PBA
单一微生物往往不具备矿化降解所需的酶系,加上母体农药产生的毒性代谢中间产物可能抑制微生物的生长,导致农药不能完全降解,因此筛选能够同时降解PYRs和3-PBA的菌株或者通过微生物共培养的方式来完成对PYRs和3-PBA的完全降解尤为重要。
2.2 丝状真菌对PYRs和3-PBA的降解途径
目前,微生物降解3-PBA途径已有研究,其中细菌对PYRs的降解大多是在羧酸酯酶、脂肪酶或者氨肽酶的作用下,使PYRs酯键断裂生成3-PBA,然后3-PBA在苯氧基苯甲酸双加氧酶的作用下,断裂二苯醚键生成苯酚和原儿茶酸,生成的苯酚和原儿茶酸进入三羧酸循环最终生成水和二氧化碳[49]。丝状真菌降解PYRs途径如图1所示(以氯氰菊酯为例),与细菌类似,即在酯酶作用下水解酯键生成二氯菊酸和α-氰基-3-苯氧基苄醇,后者自发转化为3-苯氧基苯甲醛,然后氧化生成毒性比母体农药更强的3-PBA[39,50]。3-PBA在降解初期可被还原生成毒性相对较低的3-苯氧基苄醇,随着3-PBA的降解和转化,3-苯氧基苄醇又被氧化为3-PBA,这一现象可看作丝状真菌的自转保护机制[41]。

图1 丝状真菌降解PYRs的可能途径Fig.1 Possible pathways of PYRs degradation by filamentous fungi
图2总结了丝状真菌降解3-PBA的两条途径。第一条途径是3-PBA先羟基化生成HO-3-PBA后再断裂醚键进行降解。Chen Shaohua[33]、Birolli[40]和Deng Weiqin[42]等在丝状真菌降解PYRs和3-PBA的体系中利用高效液相色谱(high performance liquid chromatography,HPLC)仪、气相色谱-质谱联用(gas chromatography-mass spectrometry,GC-MS)仪、液相色谱-质谱联用(liquid chromatography-mass spectrometry,LC-MS)仪在其代谢产物中检测到HO-3-PBA,推测在单加氧酶/羟化酶的作用下3-PBA可转化为水溶性更强的HO-3-PBA,在一些研究中发现HO-3-PBA也可进一步羟基化生成(HO)2-3-PBA[51],但羟基化位点不能确定。随后生成的HO-3-PBA在加氧酶的作用下继续断裂醚键生成苯酚、2,5-二羟基苯甲酸或对苯二酚、3-羟基苯甲酸等产物,然后进入下一步代谢生成水和二氧化碳。第二条途径与部分细菌降解3-PBA途径类似,即在苯氧基苯甲酸双加氧酶的作用下直接断裂醚键生成原儿茶酸和苯酚,如李金永等[37]在冠突散囊菌(Eurotium cristatum)ET1降解3-PBA特性研究中通过HPLC和GC-MS在代谢产物中检测到了苯酚和原儿茶酸,推测3-PBA可直接断裂醚键生成苯酚和原儿茶酸。此外,李金永等[47]还分析了产黄青霉(Penicillium chrysogenum)QH、米曲霉(Aspergillus oryzae)MAY、高大毛霉(Mucor mucedo)MHC、黑根霉(Rhizopus nigricans)GH降解3-PBA的代谢产物,发现4 种霉菌降解3-PBA产生的新物质存在差异,说明不同种类霉菌降解3-PBA途径存在一定的差异,还有待进一步研究。
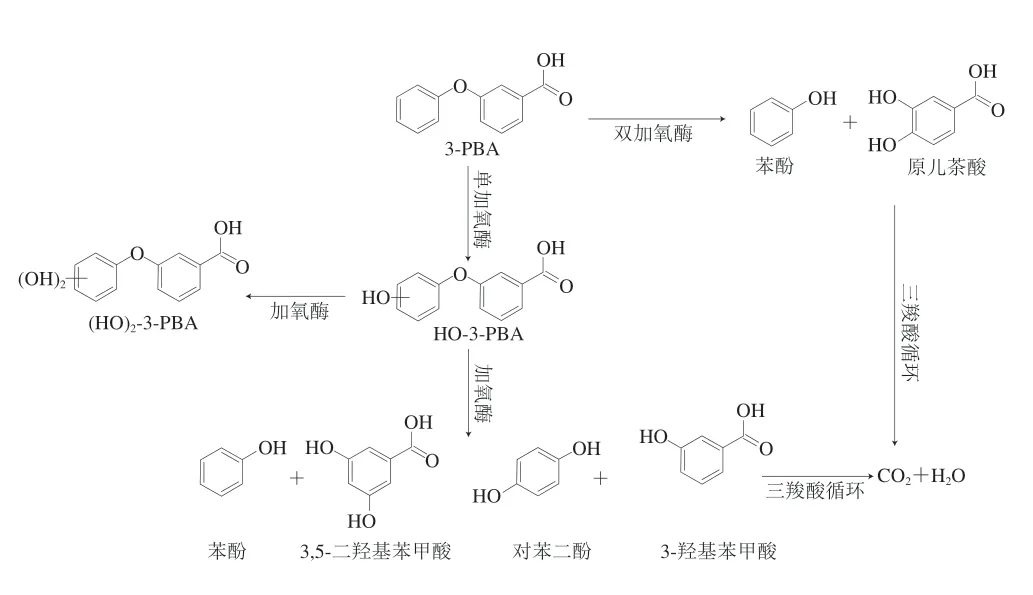
图2 丝状真菌降解3-PBA的可能途径[36-37]Fig.2 Possible pathways of 3-PBA degradation by filamentous fungi[36-37]
目前丝状真菌降解PYRs和3-PBA的代谢产物鉴定方法主要是利用HPLC、GC-MS、LC-MS,但这些方法对于复杂基质中的化合物难以进行准确定性,高分辨质谱(high-resolution mass spectrometry,HRMS)技术具有选择性强、良好的质量精度、高分辨率、高采集速率及高灵敏度等优点,不仅提高了对目标化合物检测的准确性,而且有助于识别可疑或未知化合物[52],被广泛应用于环境、食品安全等领域的检测分析,这为鉴定PYRs和3-PBA的代谢产物提供了一种新的方法。此外,还可结合核磁共振技术、傅里叶变换红外光谱技术,全方位、多视角对未知代谢产物进行结构分析鉴定。
2.3 丝状真菌的PYRs和3-PBA降解酶
2.3.1 PYRs降解酶
微生物对PYRs的降解主要是通过产生的酶来降解,这一过程涉及水解酶和氧化还原酶,水解酶主要有酯酶、脂酶、肽酶等,氧化还原酶主要有加氧酶、过氧化物酶等。目前对丝状真菌的PYRs降解酶的研究仅停留在酶的定位、降解性能以及纯化等方面。秦坤[53]提取了高效降解氯氰菊酯镰刀菌(Fusariumsp.)TS-203的胞外和胞内酶液,利用HPLC测定氯氰菊酯降解率,结果发现在10 min内胞内酶对100 mg/L氯氰菊酯降解率为59.8%,胞外酶为10.3%,确定了镰刀菌氯氰菊酯降解酶主要是胞内酶。此外,对氯氰菊酯胞内酶降解特性进行研究,得出该酶最适pH值为7.0,最适温度为30 ℃,且有较好的热稳定性和pH稳定性。Liang Weiqian等[54]通过凝胶过滤层析从黑曲霉(Aspergillus niger)ZD11中分离纯化了PYRs水解酶,该酶分子质量大约为56 kDa,最适温度为45 ℃,最适pH值为6.5,纯化的酶具有广泛的底物特异性,可降解具有结构类似羧酸酯的农药,如氯氰菊酯、氯菊酯、氰戊菊酯、溴氰菊酯和有机磷农药马拉硫磷,对氯菊酯有最高的酶活,对反式氯菊酯的比活力为31.1 U/mg,对顺式氯菊酯的比活力为29.3 U/mg。此外,该酶还可降解短中链脂肪酸的F-硝基苯酯。
大多数PYRs的降解酶属于水解酶家族的酯酶,在PYRs降解中起着关键的调节作用,现已从微生物、昆虫、动植物细胞中发现了不同的拟除虫菊酯降解水解酶[55],不同来源的PYRs水解酶的类型和特性虽然各不相同,但是这些酶的活性位点氨基酸具有共同的保守位点——包含1 个丝氨酸、组氨酸和谷氨酰胺的三联催化体,并且具有相似的催化机制,均为催化酯键水解[56]。
2.3.2 3-PBA降解酶
细菌的3-PBA降解酶大多是断裂醚键的双加氧酶或单加氧酶,如梁俊仕等[57]对来自不动杆菌(Acinetobactersp.)4-D的3-PBA降解关键酶基因d34进行克隆表达,经同源比对和酶活力验证,证实该基因编码的酶为邻苯二酚双加氧酶;Wang Chenghong等[58]在文新鞘脂菌(Sphingobium wenxiniae)JZ-1中发现一段可编码降解3-PBA的1’,2’-双加氧酶基因簇pbaA1A2B,可催化3-PBA生成3-羟基苯甲酸和儿茶酚,该基因是非组成型表达,受底物3-PBA的诱导,该基因簇编码的1’,2’-双加氧酶属于IV型Rieske非血红素铁芳香环羟基化加氧酶系统,由杂低聚加氧酶、[2Fe-2S]型铁氧还蛋白和谷胱肝肽还原酶型还原酶组成。此外,3-PBA的彻底降解还涉及苯酚羟化酶、邻苯二酚1,2-双加氧酶和原儿茶酸3,4-双加氧酶[3]。
目前关于丝状真菌3-PBA降解酶的研究较少,多为对降解菌株产降解酶条件的优化及对其降解酶性质的研究,如瑜志强等[59]对米曲霉(Aspergillus oryzae)M4产3-PBA降解酶进行研究,提取了米曲霉的胞内酶和胞外酶粗酶液,发现胞内酶比胞外酶对3-PBA有更强的降解能力,对胞内酶进行了酶学性质分析,结果发现pH值和温度可显著影响降解酶的酶活力和酶稳定性,且该酶在pH 7.0、30 ℃时有最高的酶活力。仅有少数研究报道了丝状真菌的3-PBA降解酶,如Zhao Jiayuan等[60]通过添加酶抑制剂和诱导剂对米曲霉M4降解3-PBA及其中间代谢产物的降解酶及途径进行了研究,结果表明CYP450、木质素过氧化物酶(lignin peroxidase,LiP)、Lac及双加氧酶参与了3-PBA及其中间代谢产物的降解,其中CYP450和LiP是将3-PBA转化为苯酚和没食子酸所需的酶,Lac和双加氧酶是将苯酚和没食子酸转化为长链烯酸或烯烃醛的酶;Deng Weiqin等[42]通过测定黑曲霉YAT对β-氯氰菊酯和3-PBA的降解产物及降解酶活力,推测双加氧酶参与了3-PBA、原儿茶酸和邻苯二酚的降解。
此外,3-PBA是二苯醚键结构类似物,据报道,二苯醚结构类似物如2-PBA、木质素、纤维素等可被Lac、锰过氧化物酶(Mn-dependent peroxidase,MnP)、LiP等胞外酶,CYP450胞内酶和各种双加氧酶等氧化还原酶降解[61],包括米曲霉在内的许多丝状真菌都有这些酶及编码基因[62],因此,可以推断这些氧化还原酶在丝状真菌降解3-PBA过程中起重要作用,其中丝状真菌CYP450与农药代谢关系密切,主要通过单加氧酶反应来催化农药的降解,常见反应包括羟基化、环氧化、双羟基化、O-脱烷基反应等[63]。Elisabet等[64]研究发现,单纯的胞内酶或胞外酶难以有效降解与3-PBA结构类似的木质素类化合物,微生物共代谢降解木质素类化合物需要胞内CYP450和胞外酶共同作用才能实现高效降解。下面将介绍丝状真菌中可能参与3-PBA降解的酶。
2.3.2.1 胞外酶
丝状真菌可分泌LiP、MnP和Lac等胞外酶。LiP是一系列含有Fe(III)-卟啉环(IX)血红素辅基的同功酶,不仅可以降解木质素,还能降解生态系统中的农药和抗生素等有机化合物[65],但天然LiP产量低,底物谱有限,耐受能力不强,降解有机污染物的效果不佳[66]。MnP是一种依赖Mn2+的含血红素的过氧化物酶,是一种非特异性酶,它作用底物广泛,可降解有机氯、有机磷等农药、含胺芳香族化合物和染料等化合物[67],如产自白腐真菌的MnP在3 d内可将30 mg/L的毒死蜱降解77.51%[68]。Lac是一种多铜氧化酶,普遍存在于植物和许多真菌中,其中真菌Lac广泛分布于白腐真菌、腐生真菌和菌根真菌中,尤以白腐真菌的研究和应用最广泛,是目前真菌领域中最重要的漆酶产生者[69]。Lac具有广泛的底物特异性,不仅可将木质素降解生成二氧化碳和水,还可对杀虫剂、染料和农药等难降解化合物进行降解,如轮纹韧革菌、朱红密孔菌产生的Lac在1 d内可降解90%土壤中0.3 mg/kg的嘧菌酯[70];重组毕赤酵母产生的Lac在香草醛介体的存在下在1 d内对25 mg/mL的毒死蜱降解率达98%[71]。丝状真菌产生的木质素降解酶系如LiP、MnP、Lac由于具有降解底物的非专一性,因此有广谱的生物降解性,对不同农药也有较好的降解效果,但在不同物质的刺激下产生的胞外木质素降解酶不同,因而对不同农药的降解能力和效果不同,对不同农药的降解机制也有待研究。
2.3.2.2 胞内酶CYP450
CYP450占所有I相外源性代谢酶的70%~80%[72],被认为是丝状真菌降解有毒有害物质过程中的关键酶。CYP450属于单加氧酶的一类,是一类分子质量在46~60 kDa、结构多样、功能多样的超基因家族酶,主要分布在内质网和线粒体内膜上,大多数属于膜蛋白。在进行物质代谢过程中,在氧化还原反应中发生电子转移,还原型烟酰胺腺嘌呤二核苷酸磷酸(triphosphopyridine nucleotide,NAD(P)H)是电子供体而底物是电子受体,从而发挥CYP450的一系列生物学功能。依据氧化还原伴侣的不同类型可以将CYP450催化系统分为5 类[73](图3):第一类是以CYP450、含铁硫簇(Fe2S2)的铁氧还原蛋白(ferredoxin,Fdx)以及含有一分子黄素腺嘌呤二核苷酸(flavin adenine dinucleotide,FAD)的铁氧还原蛋白还原酶(ferredoxin reductase,FdR)的三组分系统,原核生物和真核生物线粒体中的CYP450通常属于此类;第二类为双组分系统,大多数是真核生物(动植物及真菌等)来源的CYP450,其氧化还原伴侣为同时含有FAD和黄素单核苷酸(flavin mononucleotide,FMN)的CYP450还原酶(cytochrome P450 reductase,CPR),大多以膜蛋白的形式存在;第三类CYP450酶与CPR天然融合;第四类系统中CYP450结构域与含有Fe2S2/FMN的氧化还原伴侣结构域天然融合;第五类是自然界中存在少部分不需要氧化还原伴侣的CYP450酶,它们可以直接从NAD(P)H获取电子。

图3 CYP450催化系统类型[73]Fig.3 Types of CYP450 catalytic system[73]
Vasconcelos等[74]发现,海洋真菌(Olypocladiumsp.)CBMAI 1346对芘的降解主要由CYP450单加氧酶引发,它可与环氧水解酶结合将芘羟基化为4,5-反式二羟基芘后进行降解;Hata等[75]在白腐真菌(Phanerochaete sordida)YK-624消除双氯酚酸和甲芬那酸的研究中,利用质谱和核磁共振在代谢产物中检测到了羟基双氯酚酸和羟基甲酚那酸,并通过添加CYP450抑制剂1-氨基苯并三唑来抑制降解体系中的羟基双氯酚酸和羟基甲酚那酸的生成,说明白腐真菌中CYP450催化的羟基化反应可能参与双氯芬酸和甲芬那酸的降解反应,表明CYP450在难降解化合物的代谢中发挥核心作用[76]。丝状真菌中的部分编码CYP450的P450s基因具有降解环境污染物的能力[63],来源于子囊菌科的丝状真菌黑曲霉和构巢曲霉中的CYP53A基因可以使苯甲酸羟基化以及其他单取代苯甲酸衍生物形成羟基化产物,经过β-酮己二酸途径对有毒有害物质进行降解[77];Trippe等[78]克隆鉴定了黏束梗霉(Graphiumsp.)ATCC58400中的CYP52L1基因,功能上表征为环氧化的CYP450,通过CYP52L1基因沉默降低了黏束梗霉的氧化烷烃和醚的能力,说明CYP52L1基因参与了烷烃和醚的初始降解。
目前,已有大量研究证明丝状真菌CYP450酶系在降解农药中发挥重要作用,CYP450通过不同机制如羟基化、脱烷基化、环氧化、脱卤化等对农药进行降解,其中最主要的是羟基化反应,通过添加羟基的方式增加污染物的水溶性,形成不稳定的羟基化产物,进而生成共轭产物或者直接被矿化降解。
3 降解酶基因的筛选与验证
研究酶的传统方法是将酶从野生菌株的组织或细胞中提取出来并将其分离纯化,此法过程复杂,耗时长,难以大量生产。随着分子生物学技术的发展,对农药降解酶的研究不再局限于传统的分离纯化鉴定,目前常通过多种组学技术,如全基因组学、转录组学及蛋白组学等对降解过程涉及的酶及其编码的基因进行研究[79],但是目前对于丝状真菌代谢过程关键降解酶筛选技术尚不成熟,并且难度较大,关于丝状真菌降解PYRs及3-PBA过程的降解酶及其相关酶的编码基因这一领域的研究仍属空白,还有待进一步探索。
3.1 酶基因的筛选方法
3.1.1 基于基因组学筛选
基因组是生物体内包含的完整基因和染色体。基因组学是应用DNA重组、测序及生物信息学分析对基因的结构和功能进行分析。自2001年,模式丝状真菌粗糙脉孢菌基因序列被公布,曲霉、木霉等丝状真菌也相继完成全基因组测序[80]。全基因组测序可深入分析微生物基因组序列,通过基因序列比较分析可发现大量功能类似的基因。对于农药降解基因研究,可在已完成测序的基因组序列的基础上,通过序列比对寻找农药降解基因或相似基因,随着高通量测序技术的发展,全基因组测序为鉴定和发现农药降解酶基因及相似序列提供了一种高效、快捷的方法[81]。方连城[82]对毒死蜱降解菌南通嗜铜菌(Cupriavidus nantongensis)X1进行全基因组测序,通过GenBank数据库比对,确定了毒死蜱降解过程中的关键基因OPH以及毒死蜱降解产物3,5,6-三氯-2吡啶醇(3,5,6-trichloro-2-pyridinol,TCP)降解的关键基因TcpA,得到了毒死蜱在南通嗜铜菌XI中的代谢路径。马嘉雯[83]对高效降解三苯基锡的苏云金芽孢杆菌(Bacillus thuringiensis)GIMCC1.817进行全基因组测序,进行数据库注释比对,结合目标代谢产物分析,推测参与三苯基锡芳香环裂解的加氧酶主要是CYP450和脱氢酶。
3.1.2 基于转录组学筛选
转录组是指细胞在特定条件下转录的全部RNA的总和,是遗传信息和蛋白功能之间的纽带。转录组学可研究某一特定条件下,生物样本体内RNA序列的表达情况,是研究细胞表型和功能的重要手段,在许多领域中被广泛应用,对深入挖掘生物体内各反应的分子机理具有重大意义。2006年,Abe等[84]对A.oryzae基因组进行转录分析鉴别出新的代谢产物,为开发新型酶蛋白提供了一种新技术,随后转录组测序技术在丝状真菌领域中应用越来越广泛,技术也越来越成熟。通过转录组测序对基因进行基因本体(gene ontology,GO)功能富集、京都基因与基因组百科全书(Kyoto Encyclopedia of Genes and Genomes,KEGG)富集、基因表达量差异分析,进而进行功能和代谢通路分析,从而筛选出目标基因。通过对农药降解菌转录组的研究,可以探寻降解菌在农药作用下的转录调控机制,并进一步筛选鉴定农药降解关键酶及编码基因,也为发现新的农药降解酶及编码基因提供一种新颖且有效的技术方法。
Cheng Yi等[85]利用转录组学研究推导了红球菌(Rhodococcus erythropolis)D310-1对除草剂氯嘧磺隆降解的关键基因,对差异表达上调基因进行GO和KEGG注释以及实时荧光定量聚合酶链式反应(quantitative tealtime polymerase chain reaction,qPCR)验证,表明羧酸酯酶基因、CYP450基因和糖基转移酶基因在氯嘧磺隆生物降解过程中起关键作用。Zhang Cheng等[86]采用转录组测序技术分析了吉林克雷伯氏菌(Klebsiella jilinsis)2N3降解氯嘧磺隆的分子机制,预测硫代谢是降解过程中的关键途径,降解过程中羧酸酯酶、单加氧酶、糖基转移酶和CYP450的mRNA表达水平明显高于对照组,表明这些酶是降解过程中的关键酶。Long Zhengnan等[87]等对多菌灵降解菌-红球菌(Rhodococcussp.)CX-1进行了全基因组测序和转录组测序,提出了多菌灵降解的可能途径和机制,多菌灵首先在mhel基因编码的水解酶的作用下被水解生成2-氨基苯并咪唑,然后在hdx基因编码的羟化酶作用下生成2-羟基苯并咪唑,然后在mno、benA基因编码酶的作用下转化为儿茶酚,最后儿茶酚进入三羧酸循环进行降解最终生成H2O和CO2。Wang Beijia等[88]对降解双酚A的乳白原毛平革菌(Phanerochaete sordida)YK-624进行RNA测序分析该菌降解机制,对上调基因进行KEGG和GO富集分析,结果显示编码Lip和CYP450的基因表达量显著上调,表明Lip和CYP450可能参与了乳白原毛平革菌对双酚A的降解。
3.1.3 基于蛋白组学筛选
蛋白组学是探究细胞、组织和生物体蛋白质组的组成及变化规律的科学,可以分析降解过程中酶系组成和表达量,是对蛋白质组的表征,是理解基因功能的重要方法之一[89]。蛋白组学初期主要以通量低,灵敏度低的双向荧光差异凝胶电泳(two-dimensional fluorescence difference gel electrophoresis,2-DIGE)和十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulfate-polyacrylamide gel electrophoresis,SDS-PAGE)方法为主,随着HPLC技术和质谱技术的发展,基于LC-MS/MS的3D蛋白质组学逐渐成为主流方法,现在随着高精密度质谱的出现与成功应用,蛋白质组学已经进入4D的高通量时代[90]。
传统的农药微生物降解研究主要是对单一酶进行鉴定和表征,但是微生物降解是由蛋白质网络及其在细胞内的相互作用介导的复杂过程,使用蛋白质组学研究农药生物降解过程,可以确定降解过程的相关酶、主要代谢途径以及活性氧产生的氧化应激解毒机制。Liu Huan等[91]利用相对和绝对定量同位素标记结合液相色谱-串联质谱(isobaric tag for relative and absolute quantification-liquid chromatograph-mass spectrometer/mass spectrometer,iTRAQ-LC-MS/MS)技术研究了铜绿假单胞菌(Pseudomonas aeruginosa)SJTD-1对十八烷的代谢机制,鉴定出383 个烷烃反应蛋白,发现了编码参与烷烃羟基化的单加氧酶基因,主要包括烷烃羟化酶基因alKB2和单加氧酶基因almA。Otzen等[92]对降解己内酰胺的耶氏假单胞菌(Pseudomonas jessenii)GO3使用基于定量质谱的蛋白质组学方法鉴定了参与己内酰胺代谢的蛋白质和基因,确定了参与己内酰胺开环生成6-氨基己酸的ATP依赖性内酰胺酶和将6-氨基己酸转化为6-氧代己酸的转氨酶。刘晴[93]为了探究短密木霉(Trichodermta brevicompactum)降解米唑乙烟酸的蛋白质表达变化和相关代谢途径,对其进行蛋白质组学和转录组测序,随后将测序数据进行关联分析,筛选出TBU3981A和TBU1425AL两个基因作为短密木霉降解米唑乙烟酸的候选基因。近年来越来越多的研究将蛋白质组学方法应用于农药生物降解领域,这为全面深入研究微生物降解农药途径和降解机制提供了一种新的方法。
3.2 酶基因的功能验证
3.2.1 异源表达
在进行酶功能验证中最常规的方式就是克隆得到目的基因,构建表达载体以获得重组蛋白来检测酶活力,对酶的性质和功能进行研究。表达系统主要可分为原核表达系统和真核表达系统。表4列出了不同类型的异源表达系统、常用宿主细胞及表达的优缺点。原核表达系统宿主主要包括大肠杆菌和枯草芽孢杆菌,真核表达系统宿主主要包括酿酒酵母、毕赤酵母和黑曲霉、米曲霉等丝状真菌。

表4 几种常用的不同类型的异源表达系统Table 4 Several different types of commonly used heterologous expression systems
大肠杆菌是常用的原核表达系统的宿主,具有操作简单、技术成熟、周期短、表达量大等优点,但是对来源于真核生物的基因在进行表达时常出现蛋白质无法正确折叠,缺少糖基化修饰等问题,形成不溶的无活性的包涵体[94]。如真核CYP450大多数位于线粒体或内质网的膜蛋白上,难以在大肠杆菌中实现可溶性表达,这主要是因为真核CYP450的N端疏水性对蛋白质在细胞内的定位起着重要指导作用,这些序列可被识别,并转移至真核生物内质网或原核生物的细胞质膜,辅助其正确表达,而大肠杆菌缺乏细胞器膜结构,无法提供真核CYP450正确锚定位置,导致真核CYP450无法在大肠杆菌中进行正确表达。解决方法主要有N端序列修饰与分子伴侣共表达,降低诱导温度,密码子的优化,培养时添加醇类、蔗糖等蛋白可溶性添加剂,这些是实现在大肠杆菌中可溶性表达的有效策略[97]。
枯草芽孢杆菌属于GRAS微生物,作为原核表达宿主具有良好的性能,包括无明显的密码子偏好性、对发酵培养基要求简单、容易进行高密度发酵等,使其成为食品、饲料等行业中的理想表达宿主[99]。但是枯草芽孢杆菌在表达异源蛋白时,自身分泌的多种酶可能会将重组蛋白降解,存在表达的异源蛋白不稳定的缺陷[100]。
毕赤酵母含有醇氧化酶(alcohol oxidase,AOX)启动子,可用甲醇诱导调控外源基因的表达,既可实现胞内表达,也可实现胞外表达,与酿酒酵母相比,发酵产物不产生乙醇,不会对酵母生长有影响,大大提高了表达效率,适合大批量发酵生产外源蛋白。
黑曲霉和米曲霉也属于GRAS微生物,作为丝状真菌表达宿主,可进行高效表达、高分泌及糖基化修饰和二硫键修饰等多种翻译后加工,使得许多高附加价值的蛋白都实现了高效表达,在工业上被广泛应用[101]。但是丝状真菌作为表达宿主时也会出现异源蛋白被降解的情况,因此需要抑制丝状真菌自身的蛋白酶系统,减少重组蛋白酶的降解[102]。
大肠杆菌虽然是最简单和最常用的表达系统,但是在表达真核基因时可能出现酶活性较低或者形成无活性包涵体的情况,并且表达的酶分泌在胞内,后续提取酶的过程相对较为复杂。毕赤酵母表达系统是目前研究最透彻、基因操作技术较成熟及应用最广泛的真核表达系统,能够稳定地表达外源蛋白,并且可实现胞外分泌表达,是表达真核基因的一个很好选择。目前,已有较多丝状真菌酶基因实现了在毕赤酵母中的高效表达,如来源于如黑曲霉的果胶酯酶基因[103]、烟曲霉Z5中内切木聚糖酶和乙酰木聚糖酯酶基因[104]、米根霉的脂类水解酶基因[105]、米曲霉中的裂解性多糖单加氧酶基因[106]、白腐真菌的漆酶基因[107]以及真核CYP450基因[108]等。虽然丝状真菌表达系统蛋白质胞外分泌效率高、表达量大、分泌产生的外源蛋白有优良的天然活性,但在实际操作及应用中还存在许多问题,如背景复杂的宿主细胞分泌产生的外源蛋白酶容易被自身分泌的酶降解,一些异源蛋白在丝状真菌中无法实现表达以及大量表达,遗传转化操作相对困难[109],因此还需要对宿主细胞及蛋白表达元件进行优化改造,以期获得高生长速率、便捷遗传转化、高效率蛋白质合成以及低分泌背景的丝状真菌[110]。
3.2.2 基因敲除
基因敲除是研究丝状真菌基因功能的重要方法之一,可直接对基因功能进行验证,其原理是利用同源重组技术定点置换目的基因,通过抑制目的基因的正常表达、检测基因缺失菌株各项生理指标的变化,推断该基因的生物学功能[111]。基因敲除步骤主要包括敲除载体的构建、敲除载体的转化、目的敲除子的筛选及转化子的鉴定,传统的丝状真菌遗传转化方法主要有农杆菌介导的转化、基因枪转化、电转化及原生质体转化[112],其中农杆菌介导的转化方法转化效率高、转化子稳定遗传,是目前最常用的转化方法。基因敲除技术虽然是研究基因功能和结构的最直接最有效的方法之一,但是目前对丝状真菌的基因敲除技术还存在一些困难,主要包括获得所需打靶载体费时费力、需要较长的同源序列、发生同源重组的频率低和打靶效率低[113]。随着基因编辑技术的发展,丝状真菌简单、快捷、高效率遗传转化操作体系逐渐建立起来,其中成簇的规律间隔的短回文重复序列系统(clustered regularly interspaced short palindromic repeats-associated protein 9,CRISPR/Cas9)操作简单、定位精确、转化效率高,在各研究领域迅速发展[114],这对研究丝状真菌功能基因、代谢调控、代谢产物具有重要意义和价值。
4 结语
对于食品中农药残留的消减,保证菌株本身安全性及农药降解产物无毒无害是目前亟待解决的问题。因此,从食品原料或发酵食品中筛选降解菌株,揭示其降解途径并阐明降解机理,判断菌株对农药的降解否完全、降解产物是否无毒,对食品中PYRs和3-PBA的消减具有重要意义。目前已筛选到降解PYRs和3-PBA的丝状真菌,并对其降解特性和降解途径进行了研究,但是对PYRs和3-PBA降解过程的相关酶、编码基因及其降解机制方面的研究尚属空白。本文通过综述丝状真菌降解PYRs和3-PBA的研究进展,提出今后的研究方向:1)降解PYRs和3-PBA的丝状真菌来源广泛,但大多来自被农药污染的土壤和水体,菌株安全性难以保障,因此筛选食品来源的高效降解菌对食品中残留PYRs和3-PBA的消减有重要意义;2)丝状真菌降解PYRs和3-PBA途径大多是通过HPLC、LC-MS、GC-MS等对其降解产物进行分析,存在难以对降解产物进行准确定性的问题,可借助HRMS技术、红外光谱和核磁共振技术等对降解产物进行分析从而推断其降解途径;3)为阐明丝状真菌降解PYRs和3-PBA的机制,需要对降解过程中的酶及其编码基因进行研究,随着测序技术的发展,可以借助基因组学、蛋白质组学、转录组学等方法挖掘降解过程中涉及的酶及其编码基因从而阐明降解机制;4)对筛选的关键基因利用食品级宿主枯草芽孢杆菌或米曲霉和黑曲霉等丝状真菌构建基因工程菌并获得重组酶,为农产品中PYRs和3-PBA残留消减应用提供参考。
