电解水实验正负极体积比异常的实验探究及优化
2023-11-06郭玲凤
郭玲凤
(江苏省南通中学附属实验学校 江苏 南通 226500)
一、问题的提出
《义务教育化学课程标准(2022年版)》将“水的组成及变化的探究”作为学生必做实验,现行各版本九年级化学教科书都编排了电解水实验,旨在通过正负极产生的两种气体成分推知水的组成,再结合正负极气体的体积比为1∶2推出水分子的构成。已有研究利用原装J2606型霍夫曼水电解器或者自制水电解器对电极、电压、电解液类别及浓度等实验条件进行了探究[1-2],也有老师设计新型水电解器将水的电解与生成物氢气的点燃和检验合二为一[3],从而证明水的组成。但日常实验中发现,正负极产生气体的体积比常常小于1∶2。教学时大多教师一般会用氧气、氢气的溶解度差异进行分析和解释,那是不是这个原因呢?如何优化实验设计以减小实验误差呢?
二、正负极产生气体体积比异常的探究
1.溶解度影响因素的分析
查阅资料可知,在20 ℃、1个标准大气压下,1体积水中分别可溶解约0.018 体积的氢气和0.031 体积的氧气。30 mL霍夫曼水电解器(图1)两个支管的实际容积均为40 mL,计算可得溶解的氢气和氧气的体积分别约为0.72 mL和1.24 mL,理论差值约为0.5 mL。
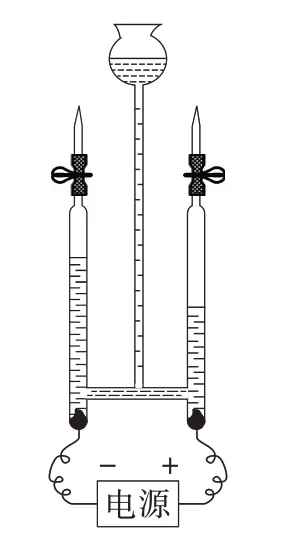
图1 常用的霍夫曼水电解器
2.实验探究
选择石墨作为电解水的电极,分别选用10%硫酸钠溶液、10%氢氧化钠溶液作为电解质溶液进行实验。实验3次的结果皆发现两极产生的气体体积差远远超过理论差值,为了证实非实验的偶然性,反复多次实验,结果几乎一致。实验数据如表1所示。
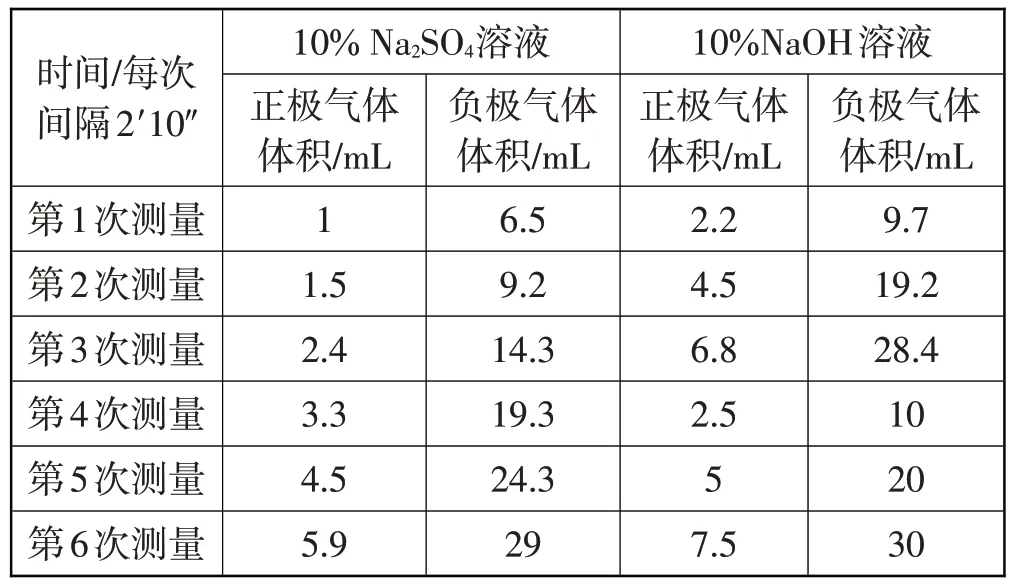
表1 用石墨作电极电解水
多次测量数据表明,两极气体体积差仍然超过理论差值且相同时间电解氢氧化钠溶液比电解硫酸钠溶液所获得的气体体积大,两极气体体积偏差相对较大。为了排除不是因为溶解能力而导致的差异,分别先电解两种溶液一段时间使其形成气体的饱和溶液后,再继续电解,发现两极气体的体积差仍偏大,且理论差值远大于0.5 mL,如表2 所示。显然,无法用氢气、氧气溶解于水中的体积大小给出合理解释。
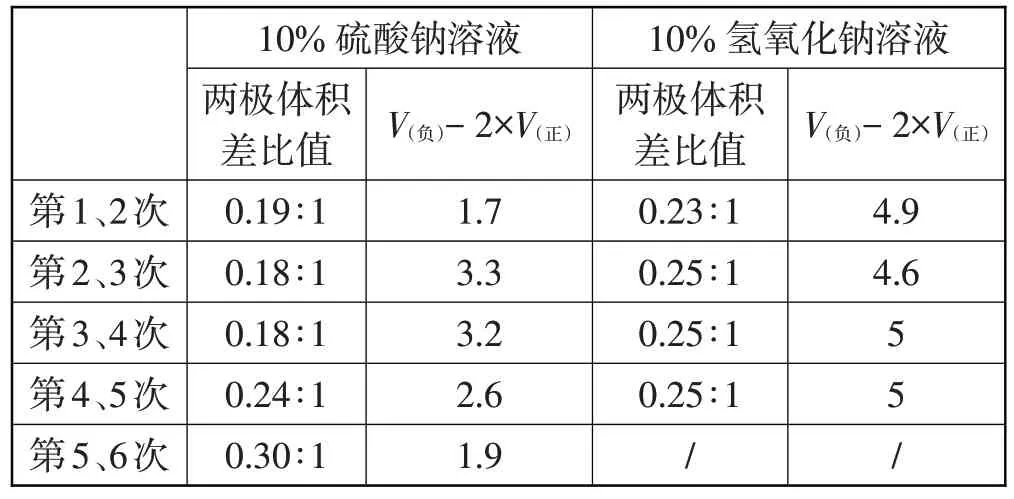
表2 用石墨作电极电解水气体体积差值比较
通过比较电解两种溶液过程中气体体积变化差值,我们还发现,电解硫酸钠溶液气体体积比变化不规律,而电解氢氧化钠溶液气体体积比逐渐趋于稳定,之后保持在0.25∶1。再反复进行多次实验,数据关系与上表相符。
已有研究文献认为,石墨作为电解水的电极材料时,正极的石墨与电解生成的一部分氧气发生了氧化,产生少量二氧化碳,导致氢气与氧气的体积比高于2∶1。钱莉、丁伟等利用手持技术探究用石墨作电极电解水也同样发现氧气体积偏小,认为,“氧气体积偏小的原因是阳极产生氧气的过程生成强氧化性的自由基,这些自由基与石墨进一步反应形成二氧化碳;另外,石墨电极的确会吸附气体产生误差,但其吸附性不是造成氧气体积偏小的原因,因为石墨对氢气的吸附能力强于氧气”[4]。
为了进一步证明,我们将石墨电解硫酸钠溶液正极所产生的气体通入澄清石灰水中,石灰水变浑浊,说明正极气体中的确含有二氧化碳;将石墨电解氢氧化钠溶液正极产生气体通入澄清石灰水中,石灰水不变浑浊,再将正极电解液加入澄清石灰水中,石灰水变浑浊。这是因为氢氧化钠溶液吸收了产生的二氧化碳气体,产生碳酸根离子。通过对实验数据进行计算发现,石墨电解氢氧化钠溶液时约一半的氧气转化为二氧化碳。
三、电解水实验再设计
基于上述实验结果及相关理论解释,除石墨电极外,其他活泼金属作电极也应该会发生氧化作用。为证实这一猜想,我们用铁钉、回形针、保险丝等常见金属材料进行电解水实验,气体体积变化与理论差值差距也很大,且规律不明显。
为避免较活泼电极对实验结果的影响,我们仍然选用霍夫曼电解器,用不易与氧气反应的铂丝作电极,分别电解10%硫酸钠溶液和10%氢氧化钠溶液多次,并对正负极气体体积差进行分析,所得数据如表3、表4所示。
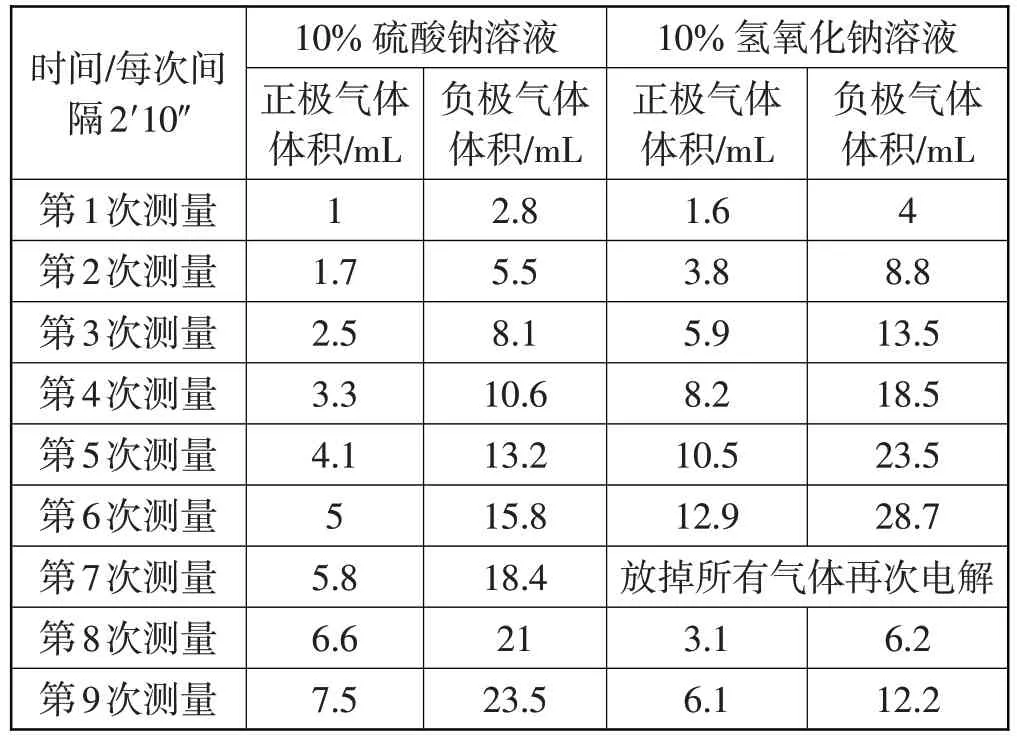
表3 用铂丝作电极电解水实验
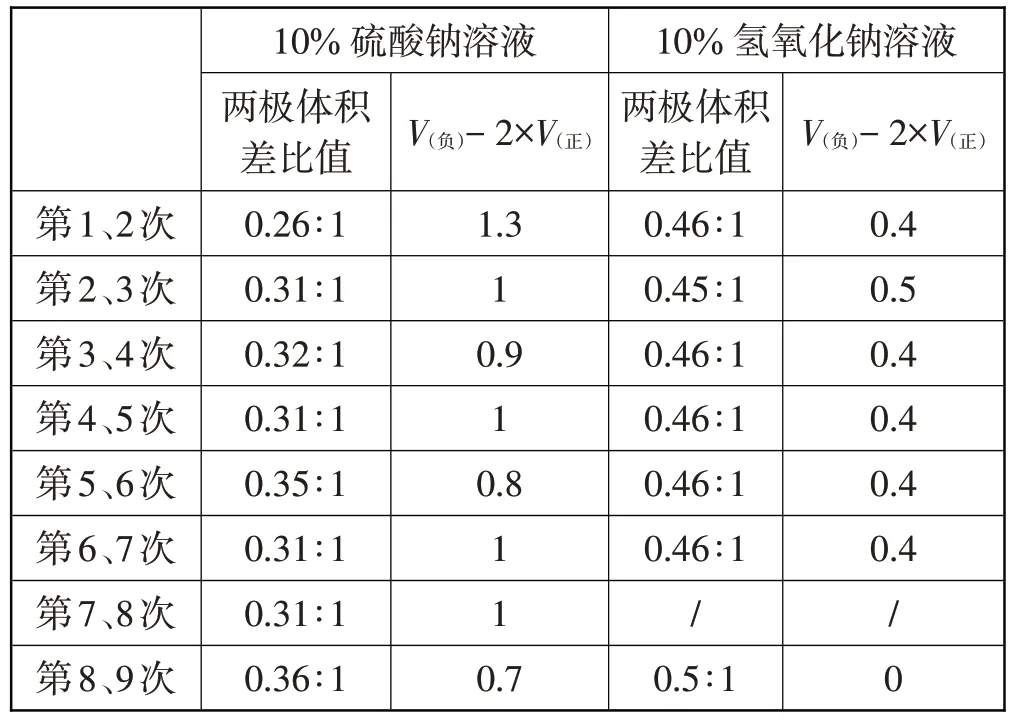
表4 用铂丝作电极电解水气体体积差值比较
通过这两组数据的比较可见,使用铂丝作电极进行电解时,正、负两极产生气体的体积比接近1∶2。选用硫酸钠作电解质时,由于正极附近的硫酸根离子也会失去电子,形成过二硫酸根离子,从而导致正极产生的氧气偏小,而且相对来说速率偏慢,不适合课堂演示。
为了解决氧气比氢气更易溶于水使得正负两极体积比低于1∶2的问题,可先将氢氧化钠溶液电解一段时间,让两种气体形成各自的饱和溶液,再继续电解,发现电解所得到的气体体积比恰好为1∶2,如表4所示第8次和第9次电解10%NaOH 溶液的数据。反复多次实验,数据与理论相符。
四、实验结论与反思
综上可知,用电解法测定水的组成时,用铂丝作电极,氢氧化钠溶液作电解质溶液较为合适。实验时,预先将氢氧化钠溶液电解约5 min,待形成氧气和氢气的饱和溶液后,放掉气体,课堂中再实验可获得理想的实验结果。夏天室内气温较高时,选择10%氢氧化钠溶液作为电解质溶液比较合适。当秋冬季室内气温较低,用10%氢氧化钠溶液作为电解质溶液速率较慢,用15%氢氧化钠溶液进行实验,速率较为适中。所以选择氢氧化钠溶液浓度时,要考虑周围环境温度。
使用霍夫曼电解器进行电解水实验,操作简单,耗时少,现象明显,适合作为学生的分组实验。上述实验过程,也可以设计为学生的课后探究活动。引导学生进行对比实验,分析数据、查阅文献、推理原因、进行实验的再设计优化。这种真实的实验探究活动,能帮助学生初步形成化学实验探究的一般思路与方法,知道科学探究是获取科学知识、理解科学本质的重要途径,培养学生基于实验事实进行证据推理的能力[5]。
致谢:本文在写作过程中还得到了江苏省特级教师李德前的指导,谨表谢意。
