CdS/Fe2S3复合物的制备及其光芬顿催化降解环丙沙星
2023-11-04杨在卿倪晓玺孙亚鑫孙智慧李成林沈世高刘菲徐东彦
杨在卿,倪晓玺,孙亚鑫,孙智慧,李成林,沈世高,刘菲,徐东彦
(青岛科技大学 化工学院,山东 青岛 266042)
抗生素是世界上用量最大、使用最广泛的药物之一。在各种抗生素中,氟喹诺酮类抗生素由于具有广谱抗菌性、抗菌能力强、吸收效果好和价格低廉等优点而被广泛使用[1]。然而,这类抗生素化学结构稳定,大多无法被人体和动物体完全吸收,而是随新陈代谢排出体外[2]。随着抗生素在水和土壤等环境中累积而导致天然细菌种群中抗生素耐药性的产生与传播,环境抗生素污染对生态系统和人类健康的威胁逐渐引起了人们的广泛关注。寻找一种能够高效降解抗生素的技术对于解决抗生素类环境污染问题具有重要意义[3]。
芬顿催化技术是高级氧化工艺中最为经济有效的水处理方法之一。传统均相芬顿技术利用H2O2与Fe2+反应生成具有高氧化活性的羟基自由基(·OH),以非选择性的方式高效地降解有机污染物。然而,均相芬顿反应存在诸如H2O2消耗高、适宜pH范围窄及产生大量氢氧化铁污泥等缺点[4]。因此,基于氧化铁和负载于各种载体上的铁基非均相催化剂的类芬顿反应受到越来越多的关注。但固相催化剂中Fe3+与H2O2反应生成·OH的反应速率显著低于均相芬顿反应[5]。为改善非均相芬顿反应效率,光芬顿技术应运而生,开发高效、稳定、能以可见光或天然日光作为驱动光源的非均相光芬顿催化剂成为高级氧化领域的研究热点[6-8]。研究发现,使用CdS改性对于提高铁基非均相催化剂的光芬顿催化活性有显著效果。例如,Shi等人[9]通过一锅涂层蚀刻工艺合成核壳结构Fe3O4@void@CdS纳米颗粒,具有良好的单分散性和约15 nm的均匀CdS壳层。该复合材料在可见光照射下,在4.5~11的宽pH值工作范围内,对亚甲基蓝的降解表现出优异的光Fenton活性。Zhang等人[10]通过煅烧-水热法制备了核壳CdS/Fe3O4@nitrogen掺杂多孔碳催化剂,用于光芬顿催化降解RhB,75 min内降解率可达92%。
以醋酸镉、硝酸铁、硫化钠为原料,在室温下制备了CdS/Fe2S3非均相光芬顿催化剂,并构建了可见光驱动的非均相光芬顿反应体系,用以降解环丙沙星(CIP)。本研究重点考察了Cd/Fe物质的量比和反应条件对催化剂性能和光芬顿降解效率的影响。
1 实验材料和方法
1.1 材料
二水合醋酸镉(Cd(CH3COO)2·2H2O),上海阿拉丁生化科技股份有限公司生产;九水合硝酸铁(Fe(NO3)3·9H2O)、甲醇、聚乙烯吡咯烷酮(PVPK30)、过氧化氢,国药集团化学试剂有限公司生产;九水合硫化钠(Na2S·9H2O),上海麦克林生化科技股份有限公司生产;实验中所用水为去离子水。
1.2 CdS/Fe2S3材料的制备
将一定量的Cd(CH3COO)2·2H2O和Fe(NO3)3·9H2O(共4 mmol)溶于30 mL甲醇中得到溶液A;在50 mL甲醇中溶解0.5 g PVPK30并移取5 mL加入到溶液A中得溶液B。将5 mmol Na2S·9H2O溶解于30 mL甲醇中,之后缓慢滴入到溶液B中并搅拌5 h,再用循环水式多用真空泵进行抽滤,最后放入60 ℃的烘箱中干燥8 h即得CdS/Fe2S3催化剂。分别制备了Cd、Fe物质的量比为8∶2、6∶4、4∶6、2∶8的CdS/Fe2S3光芬顿催化剂,并标记为CdS/Fe2S3-1、CdS/Fe2S3-2、CdS/Fe2S3-3和CdS/Fe2S3-4。
1.3 光芬顿实验
催化剂的性能评价在多通道光催化反应系统(PCX50C)中进行。将10 mg不同Cd/Fe物质的量比的CdS/Fe2S3催化剂分散于40 mL的20 mg/L CIP溶液中,溶液经超声后倒入石英瓶中并放置于多通道光催化反应系统中,经过20 min的暗反应之后向溶液中移入50 μL的30%过氧化氢,然后在300 W氙灯和420 nm滤光片下照射进行光芬顿降解实验。每隔10 min用注射器取3 mL上清液并用孔径为0.45 μm的滤膜过滤,通过紫外可见分光光度计(上海元析UV-8000)测定CIP在267 nm最大吸收波长下的吸光度。
1.4 自由基捕获实验
使用乙二胺四乙酸二钠(EDTA-2Na)作为光生空穴(h+)的淬灭剂,叔丁醇(TBA)、苯醌(BQ)和L-组氨酸(L-His)分别作为·OH、超氧阴离子自由基(·O2-)和单线态氧(1O2)的淬灭剂。
2 实验结果与讨论
2.1 Cd/Fe物质的量比对催化剂性能的影响
在初始溶液pH值为7的条件下,考察Cd/Fe物质的量比对光芬顿降解CIP效果的影响。如图1所示,当体系中仅存在光照或H2O2时,CIP降解率都随着Cd/Fe物质的量比的增大而增加。然而,反应体系中的CIP降解效率都处于较低的水平,可见光照射60 min后CIP的最佳去除率仅有60%,芬顿体系中CIP的最佳去除率也仅有77%。从图1c中可以看出,在可见光照射与H2O2同时存在的条件下,CdS/Fe2S3-1催化剂的CIP降解率在10 min内达到了80%,60 min后降解率达到了95%。以上实验结果表明,CdS与Fe2S3的复合有助于充分利用光-芬顿的协同效果,改善降解CIP的性能。在该体系中,利用可见光激发CdS产生光生e-和空穴(h+),光生e-从CdS迁移至Fe2S3,促进了Fe(III)/Fe(II)的循环,从而加速H2O2产生·OH[11]。另一方面,光生e-和h+的有效分离强化了h+的直接氧化作用,从而使催化效率得到提高。

(a)光照;(b)H2O2;(c)光照+H2O2
2.2 催化剂投加量和溶液pH值对CIP降解效果的影响
催化剂投加量对CIP降解率的影响如图2a所示。可以看出,当催化剂投加量从0.125 g/L增加到0.25 g/L时,反应60 min后CIP降解率由73%增加95%。这是由于反应体系中固液接触界面随着催化剂投加量增加而增大,活性位点增多,可见光利用效率更高,单位时间内可以产生更多的光生空穴和·OH;同时,催化剂投加量的增加也有利于反应物的吸附。而当催化剂投加量继续增加时,CIP降解率并没有明显提升,说明此时体系中H2O2的浓度成为主要影响因素。溶液pH值对CIP降解率的影响如图2b所示。可以看出,CdS/Fe2S3在较宽的pH值范围内均显示出了良好的催化活性。但体系中CIP的降解率随着pH值的增大而呈现下降趋势。当pH值=3时,体系中CIP的降解率在15 min内达到了100%。在此过程中,催化剂中的Fe3+被来自CdS的光生电子还原为Fe2+,进而与H2O2反应生成了具有强氧化性的·OH;同时又重新生成Fe3+继续参与芬顿氧化进程,实现了Fe(III)/Fe(II)的氧化还原循环。而CdS受到可见光激发产生的具有强氧化性的光生空穴则继续参与有机物的分解。随着pH值的增大,体系中游离的Fe(III)/Fe(II)可能会导致Fe(OH)2和Fe(OH)3污泥的形成,从而抑制·OH的产生,降低芬顿体系的氧化能力[12]。而在过酸条件下,Fe会在溶液中大量浸出,从而增加催化剂的损耗,综合考虑降解效果和催化剂Fe溢出的情况,本实验中选用pH值=7作为最佳反应条件。

(a)催化剂投加量;(b)pH值
2.3 自由基捕获实验
从图3中可以看出,在投入BQ和L-His后,CIP的降解率出现了小幅度下降,分别由95%下降至91%和85%,这说明在该体系中,·O2-和1O2并未作为主要的氧化活性物种参与到CIP的降解。但当在体系中加入EDTA-2Na对光生空穴进行淬灭后,CIP的降解效率显著下降至28%,这是因为EDTA-2Na不仅限制了光生空穴直接参与有机物的氧化,同时也对空穴本身捕获H2O生成·OH有着极大的抑制效果。另外,在加入TBA淬灭·OH后,对体系达到了最大的抑制效果,这是由于TBA除了抑制芬顿反应中H2O2产生的·OH,还作用于空穴捕获H2O生成的·OH。自由基捕获实验表明,在该体系中,活性物种的贡献程度顺序依次为·OH >h+>1O2>O2-,其中·OH和h+对CIP的降解起着最重要的作用。
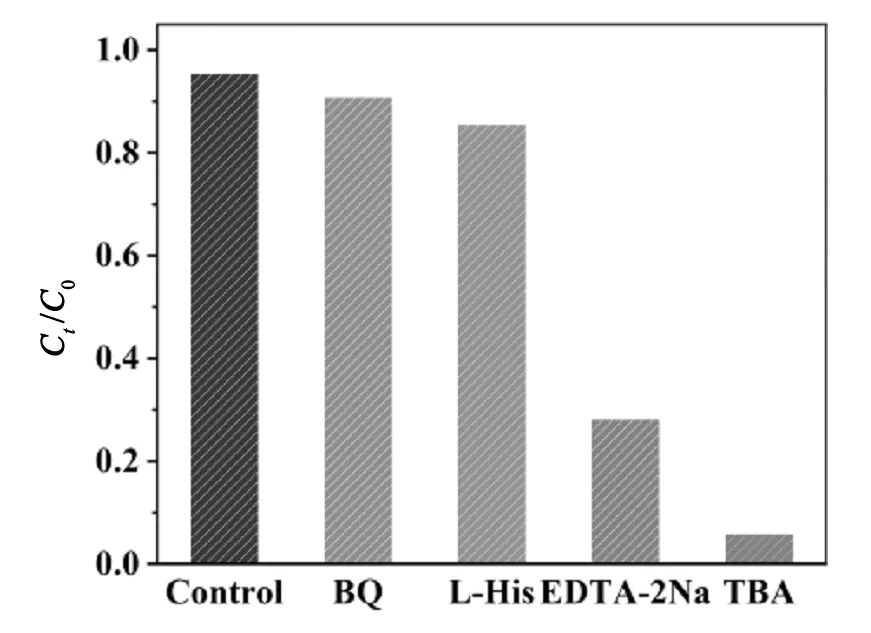
图3 光芬顿体系中不同自由基对CIP降解的影响
2.4 催化剂稳定性评价
为了考察催化剂在CIP降解中的循环使用性能,进行了三次循环实验。如图4所示,经过三次循环实验后,CIP的降解率由95%降至85%。由于催化剂使用量较少,回收过程中的损失不可避免,这是导致CIP降解率下降的主要原因。

图4 CdS/Fe2S3催化剂循环实验
3 结论
在室温下合成了CdS/Fe2S3催化材料,在可见光光芬顿体系中显示出了良好的降解环丙沙星性能。在Cd/Fe物质的量比为8∶2、初始pH值为7、催化剂质量浓度为0.25 g/L反应条件下,CIP在60 min内的降解率可以达到95%。自由基捕获实验表明,在光芬顿降解环丙沙星的过程中,·OH是主要活性物种,h+起着非常重要的作用。
