尼可地尔鼻腔给药制剂的处方前研究
2023-11-03杨蕾彭俊文谷福根内蒙古医科大学药学院呼和浩特010110内蒙古医科大学附属医院呼和浩特010050
杨蕾,彭俊文,谷福根*(1.内蒙古医科大学药学院,呼和浩特 010110;.内蒙古医科大学附属医院,呼和浩特 010050)
尼可地尔是一种新型硝酸酯类化合物,同时也是一种钾离子通道开放剂,通过双重机制改善心肌缺血,可用于冠心病及各类心绞痛治疗[1-2]。与传统硝酸类抗心肌缺血药相比,它具有疗效确切、不良反应少、耐受性好等特点,是目前临床抗心肌缺血首选药物之一[3]。尼可地尔现上市剂型有口服片剂与注射剂。前者吸收起效缓慢、生物利用度低,不适用于心绞痛的紧急治疗,后者属于侵入性给药,会给患者带来一定痛苦,且需协助用药,用药依从性差,此外,给药前需要配药、消毒等操作,易延误疾病的治疗。鼻腔给药具有给药方便、吸收起效快、生物利用度高等特点,作为快速治疗重要手段,已成为部分镇痛药、退热药、癫痫与偏头痛治疗药的理想给药途径而受到国内外高度关注,也是目前制剂领域研究的热点[4-5]。另外,尼可地尔熔点低、使用剂量小,且相对分子量低,这些性质均符合鼻腔给药的基本要求。药物溶解度、溶液化学稳定性是制备溶液型鼻腔给药必须要考虑的主要因素,而药物油水分配系数的大小又与其经鼻黏膜吸收难易程度密切相关[6]。鉴于尼可地尔在结构上属于具有硝酸酯侧链的烟酰胺类化合物,故pH值可能对其溶液化学稳定性、油水分配系数及溶解度有重要影响;此外,为进一步改善药物经鼻黏膜吸收,鼻腔制剂处方中常需加入吸收促渗剂,因而有必要筛选尼可地尔经鼻黏膜吸收的理想促渗剂。基于上述分析,本文将完成尼可地尔鼻腔给药制剂的处方前研究工作,旨在为今后研制该药物溶液型鼻腔给药新制剂提供重要理论依据。
1 材料
1.1 仪器
LC-20AT高效液相色谱仪(包括SPD-20A紫外-可见检测器,日本岛津公司);TP-6智能透皮试验仪(天津市鑫洲科技有限公司);PHS-3C型pH计(上海仪电科学仪器有限公司);AB265-S型电子分析天平(瑞士梅特勒·托利多公司);KQ5200E型超声波清洗器(昆山市超声仪器有限公司);Arioso UP 900型超纯水器(韩国Human公司);101型电热鼓风干燥箱(北京市永光明医疗仪器厂)。
1.2 试药
尼可地尔对照品(纯度:99.5%,批号:k1710021,上海阿拉丁生化科技股份有限公司);HP-β-CD(纯度:98%,山东新大精细化工有限公司);SBE-β-CD(纯度:99%,山东新大生物科技有限公司);DM-β-CD(纯度:98%,山东滨洲智源生物科技有限公司);正辛醇(AR,天津市化学试剂有限公司,批号:20200401);生理盐水(批号:2104153404,石家庄四药有限公司);水为双蒸水,甲醇、乙腈均为色谱纯,其余试剂均为分析纯。
2 方法与结果
2.1 尼可地尔含量测定方法建立
2.1.1 色谱条件[7]色谱柱:InertSustain C18色谱柱(250 mm×4.6 mm,5 μm);流动相:甲醇-水(48∶52);流速:1.0 mL·min-1;检测波长:254 nm;柱温:36℃;进样量:10 μL。
2.1.2 专属性试验 以50%甲醇溶液为溶剂,配制质量浓度为80 μg·mL-1的尼可地尔溶液。取上述尼可地尔溶液适当体积于10 mL具塞刻度试管中,分别以0.1 mol·L-1盐酸溶液、0.01 mol·L-1氢氧化钠溶液、0.5%过氧化氢溶液稀释至刻度,摇匀,然后置于80℃恒温条件下放置,分别于适当时间取样,进样分析,其中,以0.1 mol·L-1盐酸溶液、0.01 mol·L-1氢氧化钠溶液所制样品,需在进样前以相同浓度碱或酸溶液进行中和。结果见图1,在该色谱条件下,尼可地尔与其降解产物能够很好地分离,表明该分析方法专属性强;此外,尼可地尔溶液在酸性及碱性条件下均不稳定,但在强氧化条件下较稳定。
2.1.3 标准曲线的制备 精密称取尼可地尔对照品适量,以50%甲醇溶液为溶剂,制得质量浓度为500.0 μg·mL-1的尼可地尔储备液。将上述尼可地尔储备液,以50%甲醇稀释不同倍数,分别制得质量浓度为 2.5、5.0、10.0、20.0、40.0、60.0、80.0 μg·mL-1的尼可地尔系列对照品溶液。进样分析,记录药物色谱峰面积。以尼可地尔质量浓度(C,μg·mL-1)为横坐标,峰面积(A)为纵坐标,求得回归方程为:A=3255.5C-1713.7(r=0.9997),表明尼可地尔在2.5~80.0 μg·mL-1内与峰面积呈现良好的线性关系。
2.1.4 精密度试验 分别取5.0、20.0、60.0 μg·mL-1的尼可地尔对照品溶液,日内重复测定5次,连续测定5 d,计算方法的日内及日间RSD值。结果该方法的日内RSD在0.23%~0.63%,日间RSD在0.60%~1.6%(n=5),表明该方法的精密度良好。
2.1.5 回收试验 配制5.0、20.0、60.0 μg·mL-1尼可地尔对照品溶液,每个浓度各5份,进样分析,记录尼可地尔峰面积,并根据随行标准曲线方程,计算方法的回收率。结果低、中、高浓度尼可地尔的回收率分别为103.12%、96.72%、98.52%,RSD分别为0.92%、0.67%、0.39%,表明该方法的准确度较高。
2.1.6 检测限与定量限 将标准曲线下尼可地尔最低浓度对照品溶液逐步稀释,以信噪比S/N=3时,药物浓度作为方法的检测限,以S/N=10时,药物浓度作为方法的定量限。结果该方法的检测限为0.05 μg·mL-1,定量限为0.15 μg·mL-1。
2.2 尼可地尔溶液化学稳定性研究
按照《中国药典》2020年版四部中“缓冲液”项下方法,分别配制pH值为2.0、4.5、6.0、7.0、8.0、10.0、12.0的系列缓冲液。
精密称取尼可地尔适量,加50%甲醇溶液溶解,制得质量浓度为1000.0 μg·mL-1的尼可地尔储备液。取尼可地尔储备液,加蒸馏水稀释,制得质量浓度为80.0 μg·mL-1的尼可地尔溶液。取尼可地尔溶液1 mL置于10 mL试管中,分别加入上述不同pH值系列缓冲液至10 mL,摇匀,密封,于80℃恒温条件下放置,分别于0、2、4、8 h取样,放冷至室温,进样分析,测定反应液中尼可地尔的浓度并计算药物降解百分率,结果见图2。可见,尼可地尔溶液随着介质pH的增加,其降解百分率总体呈现上升趋势;且随着加热时间的延长,药物的降解百分率也随之增加。此外,在pH 2.0的强酸条件下药物溶液的降解速度最慢,而pH值在4.5~8.0时药物溶液的降解速度较pH 2.0时明显增大,但在此pH值范围内,不同pH值下药物降解速度基本相似,而尼可地尔溶液在pH 10.0及以上强碱性条件下,其降解速度显著加快,化学稳定性最差,如在pH值为12时,2 h内药物已基本降解完全。

图2 尼可地尔溶液在不同pH条件下的降解曲线(n=3)Fig 2 Degradation curves of nicorandil solution under different pH conditions(n=3)
2.3 尼可地尔油水分配系数的测定
2.3.1 油水平衡时间测定 配制pH值分别为2.0、4.5、6.0、7.0、8.0、10.0、12.0的系列缓冲液作为水相,以经过水饱和的正辛醇作为油相。
取质量浓度为1000 μg·mL-1的尼可地尔储备液,分别加入不同pH值水相进行稀释,制得质量浓度为32 μg·mL-1的尼可地尔系列水相溶液。取尼可地尔水相溶液10 mL,置于具塞锥形瓶中,加入相同体积油相,密塞,于25℃恒温振荡器中振荡,分别于0、20、40、60、120、180 min在水相中取样,再用0.45 μm微孔滤膜过滤,取续滤液,进样分析,测定水相中尼可地尔的浓度。实验结果可见,当恒温振摇120 min时,不同pH值水相中尼可地尔的浓度已达恒定,故将该药物在油相、水相中分配平衡时间设为120 min。
2.3.2 油水分配系数的测定 将不同pH值药物水相溶液与相同体积油相混合,在25℃恒温振荡器中振荡120 min后,在水相中取样,同法处理后进样分析,测定不同pH值水相中药物的浓度。根据公式:P=(C0-Cw)/Cw,计算不同pH下药物的油水分配系数P。式中,C0是水相中药物初始浓度,Cw是分配平衡后水相中药物浓度。结果测得,尼可地尔在正辛醇-水中的P值为2.31,而药物在正辛醇/不同pH值缓冲液中尼可地尔的P值变化,见图3。可见,尼可地尔的P值随着pH值增大而呈波动式增加,在pH值为6.0时,P值出现一定程度下降,而后又逐渐增大。

图3 尼可地尔的P值随pH变化的曲线(n=3)Fig 3 P change curve of nicorandil under various pHs(n=3)
2.4 溶解度的考察[8]
分别取适当体积水、丙二醇、PEG400及pH值分别为2.0、4.5、6.0、8.0 磷酸盐缓冲液,置于0.5 mL EP管中,均加入过量尼可地尔,超声处理,观察药物溶解情况,直至药物不再溶解。然后,将样品置于25℃恒温振荡器中继续振摇72 h,使药物溶解达饱和状态。将EP管以10 000 r·min-1离心10 min,取上清液以0.45 μm微孔滤膜过滤,取续滤液以50%甲醇溶液稀释适当倍数后,进样分析,计算尼可地尔在不同溶剂中的溶解度,结果见表1。可见,在pH值2.0~8.0内,尼可地尔的溶解度随介质pH的增加而总体呈减小趋势,而其在丙二醇中的溶解度与在水中的溶解度基本相似,在PEG400中的溶解度却较小。

表1 尼可地尔在不同溶剂中的平衡溶解度(n=3)Tab 1 Equilibrium solubility of nicorandil in different solvents(n=3)
2.5 促渗剂的筛选
以鼻腔给药制剂中使用广泛、安全性高的3种β-CD水溶性衍生物DM-β-CD、HP-β-CD、SBE-β-CD为候选促渗剂[9],筛选尼可地尔鼻用制剂的最佳促渗剂。
取新宰杀羊鼻黏膜,采用Franz立式扩散池法,完成药物渗透性试验。试验时,将鼻黏膜剪成适宜大小,固定于扩散池接口处,黏膜侧朝向供给池,以生理盐水为接收液,在供给池内加0.1%尼可地尔供试液1.0 mL,内含5%β-CD水溶性衍生物,水浴温度设为34℃,搅拌速率为300 r·min-1,分别于20、40、60、90、120、180 min,从接收池中取样1.0 mL,并立即补充同体积等温生理盐水。按“2.1.1”项下色谱条件,测定样品中尼可地尔的浓度。样品中尼可地尔的定量方程为:A=2883.9C+2199(r=0.9999),尼可地尔在0.2~80.0 μg·mL-1与峰面积呈良好线性关系。方法的日内精密度在0.18%~0.72%,日间精密度在0.41%~2.3%(n=5)。
依据药物累积渗透量(Qn,μg·cm-2)计算公式[10]:计算不同时间尼可地尔的累积渗透量。式中,V0为接收液体积,Cn为第n个取样点的药物浓度,Vi为第i次取样体积,Ci为第i次取样接收液中药物浓度,A为有效透皮面积,以Qn对时间t作图,绘制尼可地尔经鼻黏膜的渗透曲线,结果见图4。可见,5%SBE-β-CD对尼可地尔经鼻黏膜吸收的促渗作用最强,5%HP-β-CD的促渗作用次之,而5%DM-β-CD却抑制药物的鼻黏膜渗透。
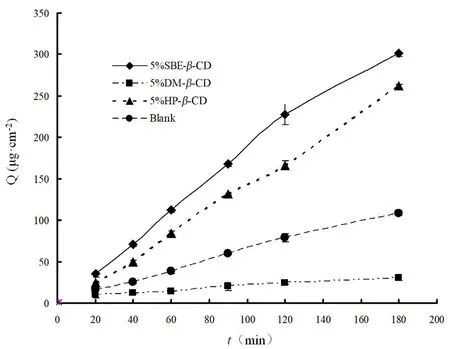
图4 不同促渗剂对尼可地尔经离体羊鼻黏膜渗透量的影响(n=3)Fig 4 Effect of different absorption enhancers on the permeation amount of nicorandil via in vitro sheep nasal mucosa(n=3)
因此,确定了SBE-β-CD为最佳促渗剂,进一步考察其浓度对促渗效果的影响,方法同前。分别考察了1.0%、3.0%、5.0%、7.0% SBE-β-CD对尼可地尔的促渗作用,结果见图5。可见,当SBE-β-CD 浓度较低时,随着浓度的增加,其促渗作用随之增加,当浓度为5.0%时,其促渗效果达到最大,此后,随着浓度增加,其促渗作用下降。因此,5.0%SBE-β-CD作为尼可地尔鼻腔给药制剂的最佳促渗剂。

图5 SBE-β-CD浓度对尼可地尔经离体羊鼻黏膜渗透的影响(n=3)Fig 5 Effect of SBE-β-CD concentrations on permeation amount of nicorandil via in vitro sheep nasal mucosa(n=3)
3 讨论
本文首先建立了HPLC法测定尼可地尔含量的方法,该方法专属性强、操作简单、线性范围大、精密度与准确度良好。因尼可地尔结构上属于硝酸酯类化合物,具有易水解的特性,其溶液化学稳定性易受介质pH的影响。尼可地尔溶液稳定性研究结果显示,药物溶液在强酸性pH条件下稳定性最好,在弱酸性与中性pH下稳定性次之,而在强碱性pH下稳定性最差,这是由于在碱性条件下,尼可地尔易发生专属性碱催化水解反应,生成降解产物N-(2-羟乙基)-烟酰胺的缘故,该结果与文献报道基本一致[11-12]。
有研究证实,当药物油水分配系数为-1<logP<2,在此范围内药物通过被动扩散较易透过细胞膜[13]。本文测定结果显示,在pH 4.5~12内,尼可地尔的P值在2.2~4.5,其logP大致在0.33~0.65,在正辛醇-水中的logP为0.36,均处于药物最佳吸收范围内,预期经鼻腔黏膜较易吸收。尼可地尔的P值随pH值增大而呈波动式增加,其原因可能是由于其结构上同时含有酰胺基与吡啶环,使药物总体呈现弱碱性,导致其P值随pH值的变化不同于一般弱碱的变化规律[14-15]。
其次,本文采用饱和溶液法测定了尼可地尔溶解度,发现在强酸性pH条件下,该药物的溶解度最大,随着介质pH值增大,药物溶解度总体呈逐渐下降趋势,这可能是由于尼可地尔属于弱碱性化合物,在强酸性pH值下,有部分药物发生解离,以离子形式存在,从而增加药物的溶解度,而随着介质pH值逐渐增加,绝大部分药物以分子形式存在,故溶解度明显降低。此外,还发现尼可地尔在丙二醇中的溶解度与其在水中相似,均远大于在PEG400中的溶解度。鉴于尼可地尔上市口服片剂的规格为5 mg,而人单侧鼻孔每次给药体积范围应为100~200 μL[16],本文测得该药物在常温下水中的溶解度大于70 mg·mL-1,完全可满足制备溶液型鼻用制剂要求,因此,可考虑以水作为制备尼可地尔鼻腔制剂的理想溶剂。
最后,离体鼻黏膜渗透性试验结果发现,候选的3种促渗剂中,HP-β-CD与SBE-β-CD均可明显促进尼可地尔的经鼻黏膜吸收,但后者促渗效果更好;相反,DM-β-CD则表现为明显抑制该药物经鼻黏膜的渗透作用,产生这一现象的原因尚不明确,可能与β-CD母体结构上取代基的不同有关。此外发现,不同浓度SBE-β-CD的促渗作用大小顺序为:5.0%SBE-β-CD>7.0%SBE-β-CD≈3%SBE-β-CD>1.0%SBE-β-CD,表明SBEβ-CD对尼可地尔的促渗效果具有一定程度的浓度依赖性:在低浓度时,促渗作用随其浓度增加而增强,当浓度达到5%时,其促渗效果最大,进一步提高SBE-β-CD的浓度,其促渗作用不再增加,这一现象与文献报道结果类似[17]。
人体鼻腔正常生理pH值范围为5.5~6.5,平均值为6.4[18],综合考虑尼可地尔溶液化学稳定性、油水分配系数、溶解度和对鼻黏膜可能产生的刺激性,制备该药物鼻腔制剂的pH值应控制在6.0~6.5为宜,而其最佳促渗剂为5.0%SBE-β-CD。后续将通过体内药动学研究来验证制剂在体内吸收以及生物利用度情况。
