一种改善磁微粒化学发光项目CA72-4产品性能的方法
2023-11-02陈永奇逯阵毫马明李静雯王玉堂
陈永奇,逯阵毫,马明,李静雯,王玉堂
(郑州安图生物工程股份有限公司,河南 郑州 450016)
癌症抗原72-4(CA72-4)法是一种检测肿瘤相关糖蛋白72(TAG-72)的免疫分析法,该抗原被发现是在某些肿瘤细胞群中表达的抗原[1-3]。抗原被鉴定为220~400 kDa 黏蛋白型糖蛋白[1,4]。抗体B72.3 最初是用转移到肝脏的乳腺肿瘤的膜富集细胞提取物制备的,并已被证明能与TAG-72[3]反应。CC49 是TAG-72 特异性抗体。CC49 抗体和B72.3 抗体分别识别TAG-72 的Galβ(1-3)唾液酸-tn和唾液酸-tn 糖链表位[5-6]。有趣的是,CA72-4 在恶性胃癌、卵巢癌、结直肠癌和胰腺癌患者的血清或血浆中含量升高,并被用于监测胃肠道和黏液性卵巢癌患者[1,7-9]。血液测试可以为临床医生提供各种疾病迹象的信息。由于血液检测的结果提高了诊断的准确性,诊断测定显示准确的测量值对于临床决策至关重要。直到20 世纪40 年代,标本都是用肉眼和人工检测的。每次测试都很耗时,测试的准确性取决于技术人员的技能水平。20 世纪50 年代,随着美国制造商自动分析仪的出现,全面的检测自动化开始了。自动化技术的进步缓解了准确性和速度的问题。如今,全国医疗机构(医院和临床检验中心)的实验室都有相当数量的标本,并在24 h 内进行检测。免疫化学方法在医学实验室中被常规使用。电化学发光免疫分析(ECLIA)法和化学发光免疫分析(CLIA)法因其灵敏度高、背景低、操作简单而广泛应用于自动化分析仪中。然而,这两种方法都受限于免疫化学反应对各种干扰的敏感性,如血清中的自体抗体、抗动物IgG 的嗜异抗体、交叉反应、溶血、高脂血症和高胆红素血症。本文基于化学发光免疫分析法,采用一些手段排除交叉反应等干扰,提高检测准确性。
1 材料和方法
1.1 材料
1.1.1 主要试剂 小牛血清白蛋白(BSA)(Sigma公司,雅为生物公司等),鱼明胶(Sigma 公司)磁微粒(Merck 公司,羧基磁珠,100 mg/mL);包被抗体(郑州伊美诺生物技术有限公司);酶标抗体(郑州伊美诺生物技术有限公司);1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐 EDC(Sigma 公司);N-羟基丁二酰亚胺 NHS(Sigma 公司);磁微粒偶连缓冲液0.1 mol/L pH=7.4 MES buffer;磁微粒稳定液:缓冲液0.1 mol/L pH=7.4 PBS buffer;酶结合物稳定液:缓冲液0.1 mol/L pH=7.4 PBS buffer;乙醇胺(Aladdin 公司);高碘酸钠(Sigma公司);氰基硼氢化钠(Sigma 公司);精氨酸(Sigma 公司)。
1.1.2 主要仪器 全自动化学发光测定仪AutoLumo A2000 Plus(安图生物);电热恒温培养箱(上海跃进医疗器材有限公司);振荡器(TOPSCIEN 公司)。
1.2 研究方法
1.2.1 磁微粒试剂包被方法 在4 mL 玻璃瓶中分别加入0.1 mL 10%质量浓度羧基磁珠,1 mL 偶连缓冲液,震荡5 min 后磁分离,将上述操作重复3 遍进行清洗,而后分别加入0.3 mL 0.1 mol/L EDC 溶液与0.3 mL 0.1 mol/LNHS 溶液(注:以偶连缓冲液进行溶解),室温震荡反应1 h;洗2 次后加入0.9 mL 磁微粒偶联缓冲液和0.6 mg CA72-4抗体,并室温震荡反应2 h。最后加入乙醇胺60 μL 继续反应30 min,使用磁微粒稳定液(根据不同方案,向磁微粒缓冲液中加入不同的稳定剂,稳定剂浓度为10 mg/mL),磁分离清洗3 次后定容至9 mL,2~8 ℃储存。
1.2.2 酶结合物配制方法 配制酶结合物稳定液,根据不同方案,向从酶结合物缓冲液中加入不同的稳定剂,稳定剂浓度为10 mg/mL;再向上述配置好的稳定液中加入酶结合物,终浓度为1 μg/mL。充分混匀,2~8 ℃储存。
1.2.3 测试模式 由机器按照上机文件进行测试,每次加入50 μL 校准品(浓度值为0 μIU/mL、5 μIU/mL、50 μIU/mL、100 μIU/mL、150 μIU/mL、300 μIU/mL)、20 μL 磁珠混悬液和100 μL 酶结合物以及100 μL 底物。具体过程使用A2000plus 仪器进行检测,除磁珠混悬液其余均使用该公司在售试剂盒内组分。
1.2.4 检测指标 稳定性指标:目前IVD 行业对化学发光试剂盒的稳定性的共识为在37 ℃下放置7 d 约等于试剂条件下在2~8 ℃存放8~12 个月,计算浓度点相对光单位(RLU)下降率ROD(%)=ABS(RLU37℃7d/RLU2~8℃-1)×100%,ROD 均 值为校准品各值的平均值,目前业内公认ROD 值小于10%为合格标准。
1.2.5 BSA 去糖基化方法 将BSA 用纯化水配成50 mg/mL,充分搅拌,待其完全溶解后,向其中加入高碘酸钠和精氨酸,高碘酸钠及精氨酸的终浓度均为5 mg/mL,避光反应3 h。向其中加入氰基硼氢化钠,终浓度为5 mg/mL,过夜反应。用PBS 缓冲液透析,过夜,透析液:PBS 缓冲液液>1∶50。
2 结果
2.1 不同稳定剂对产品性能影响的结果
将鱼明胶、BSA 加入稳定液(10 mg/mL)中,上机验证产品CA72-4 反应性,结果如表1 所示。
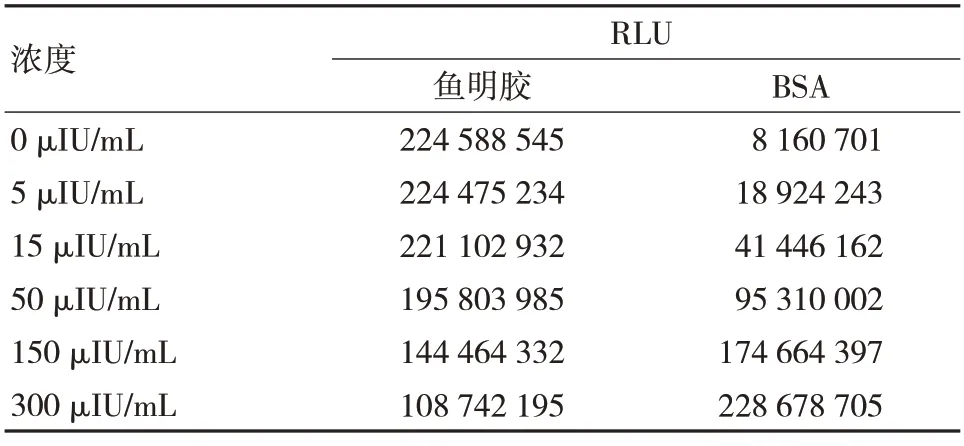
表1 不同稳定剂对产品性能影响的结果比较
2.2 不同厂家BSA 对产品性能影响的结果
将不同厂家BSA 加入到稳定液中(10 mg/mL),上机验证产品CA72-4 反应性,结果如表2 所示。

表2 不同厂家BSA 对产品性能影响的结果
2.3 去糖基化BSA 对产品性能影响的结果
将上述提到效价较优的BSA 进行去糖基化,加入到稳定液中,且对该产品进行稳定性考核,其结果如表3 所示。
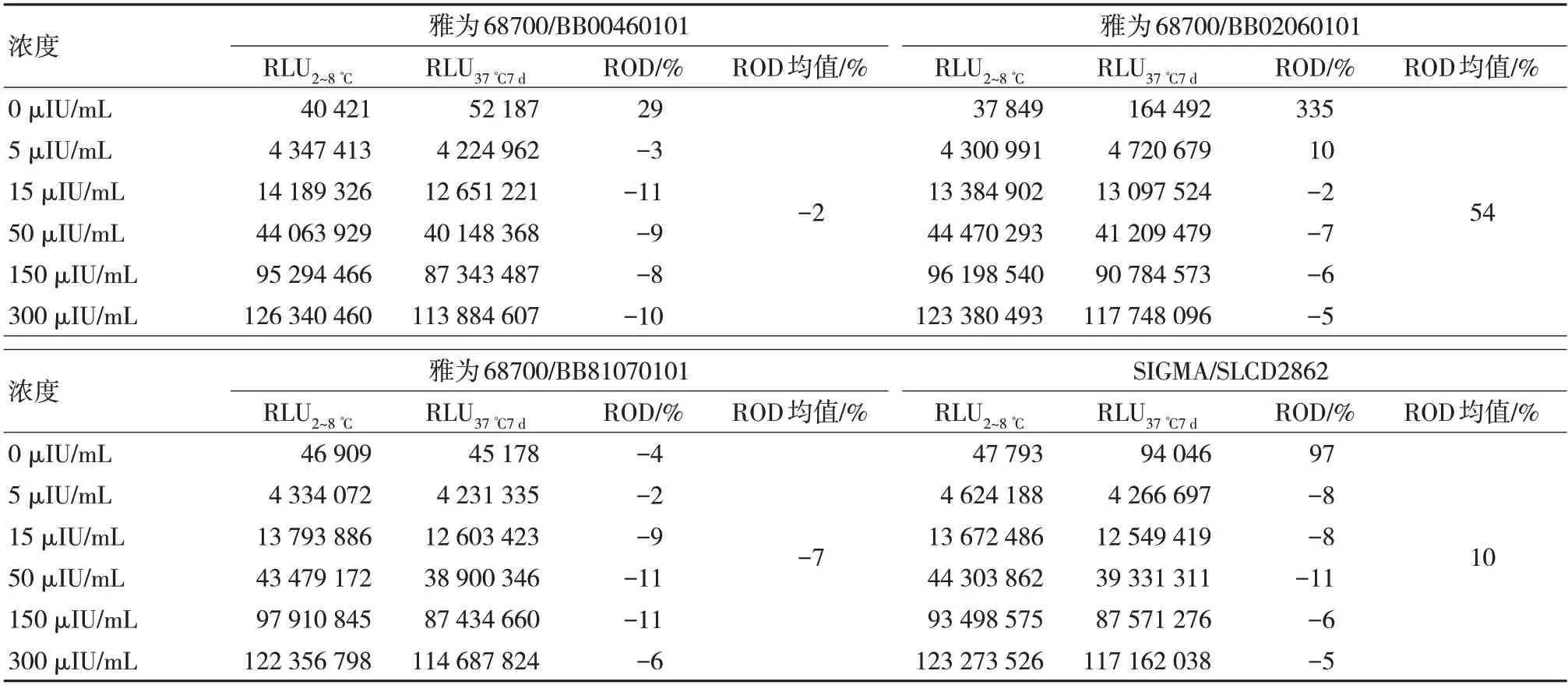
表3 去糖基化BSA 对产品性能影响的结果
通过表2 和表3 数据进行对比,将BSA 去糖基化之后,本底有所降低,高浓度RLU 略微降低,但是泽龙20190739 批号的BSA 出现异常。除此之外,其它进行7D 热加速稳定性考核,仅个别去糖基化BSA 作为稳定剂本底会升高,其它均较优。满足项目需求。
3 讨论
本文通过筛选常用的两种稳定剂,确定BSA对RLU 影响较小,但是本底高。后期,笔者又对不同厂家的BSA 进行筛选,发现不同厂家BSA 对产品性能影响差异较大,综合分析,可能是BSA上的糖基于抗体发生了交叉反应,因此本文对BSA 进行去糖基化,最终通过热加速稳定性考核,本底降低,满足项目需求。
