肾移植受者早期霉酚酸暴露量估算模型研究Δ
2023-10-28张寒娟丁建强韩文超陈永妍王高彪丁蕊袁冬冬郑州市第七人民医院药学部郑州45006武警河南总队医院药学部郑州45005
张寒娟 ,丁建强 ,韩文超 ,陈永妍 ,王高彪 ,丁蕊 ,袁冬冬 (.郑州市第七人民医院药学部,郑州 45006;.武警河南总队医院药学部,郑州 45005)
吗替麦考酚酯(mycophenolate mofetil,MMF)作为新型抗代谢免疫抑制剂在器官移植中被广泛应用,其口服吸收后,可迅速水解为次级代谢产物——霉酚酸(mycophenolic acid,MPA)[1—2]。MPA的血药浓度-时间曲线下面积(area under the plasma concentration-time curve of MPA,MPA-AUC)与其临床疗效和药物不良反应(adverse drug reaction,ADR)密切相关,但不同受者服用相同剂量的MMF,其MPA-AUC个体差异可达10倍[3]。MPA在代谢过程中存在肝肠循环现象,导致其谷浓度难以反映真实的治疗效应,目前临床多推荐MPA-AUC0-12h作为MMF的治疗药物监测指标[4]。但是测定一个完整12 h给药间隔的AUC,往往存在采样点密集、受者依从性差等缺陷[5],因此,MPA血药浓度监测通常采取有限采样(limited sampling strategy,LSS)法,即利用1~4个采样点预估MPA-AUC0-12h,操作方便、更具临床可行性[6—7]。目前关于肾移植受者估算MPA-AUC0-12h模型的研究大多为肾移植术后稳定期受者[8],但由于早期受者合并用药较多、生理指标未完全恢复等,移植早期反而更易出现MPA暴露量不足(MPA-AUC0-12h<30 mg·h/L)的情况,且患者的药动学特征可能与稳定期受者存在差异,因此建立肾移植受者早期的MPA-AUC0-12h估算模型非常必要[9—10]。为此,本研究纳入了肾移植术后15 d的受者,采用LSS法建立了肾移植受者早期MPA暴露量的估算模型,旨在为临床监测MPA的暴露量提供参考。
1 对象与方法
1.1 研究对象
选取2021-2022年在郑州市第七人民医院首次接受肾移植手术的患者。本研究方案通过郑州市第七人民医院医学伦理委员会审查批准(批件编号为2021-05-001),并且所有参与本试验的患者在试验前均被告知试验目的和内容,并签署知情同意书。
本研究的入选标准为:(1)术后接受MMF+他克莫司+甲泼尼龙三联免疫抑制治疗方案;(2)1周内MMF给药剂量无变化;(3)可以获得完整的药动学参数。
本研究的排除标准为:(1)有肝炎或肝功能异常受者;(2)同时服用含有氢氧化镁或氢氧化铝等抗酸剂或考来烯胺等可能影响MPA吸收及肝肠循环的药物者;(3)有活动性消化道溃疡者,存在严重免疫抑制药相关药物不良反应者,尤其是胃肠道反应者;(4)近期发生临床确诊的急性排斥反应或感染者。
1.2 免疫抑制治疗方案
所有参与试验的肾移植受者均采用三联免疫抑制方案:MMF+他克莫司+甲泼尼龙:术后首日开始口服吗替麦考酚酯分散片(杭州中美华东制药有限公司,国药准字H20052083,规格0.25 g)500 mg,q12 h,术后3 d调整剂量为750 mg,q12 h;术后2 d左右开始口服他克莫司胶囊(杭州中美华东制药有限公司,国药准字H20084514,规格1 mg)1 mg,q12 h,并根据他克莫司血药浓度调整剂量;术前、术后第1天、术后第2天给予兔抗人胸腺细胞免疫球蛋白(Genzyme Polyclonals S.A.S.,国药准字J20150136,规格25 mg/瓶)25 mg,qd(亲属肾移植除外);术后第1天静脉滴注注射用甲泼尼龙琥珀酸钠(Pfizer Manufacturing Belgium NV,国药准字HJ20170197,规格4 mg)500 mg qd,术后第2天调整剂量为250 mg,qd,术后第3天起改为口服甲泼尼龙片(Pfizer Italia Srl,国药准字H20150245,规格4 mg)8 mg,qd维持。
1.3 检测仪器与试剂
本研究所用主要仪器包括2D-LC-UV全自动二维液相色谱-紫外检测系统[由FLC2420全自动二维液相色谱耦合仪(湖南德米特仪器有限公司)以及液相色谱LC-20AT部件(日本岛津公司)构成]、XW-80A型涡旋混合仪(上海琪特分析仪器有限公司)、TDZ4-WS型低速离心机(湖南湘仪实验室仪器开发有限公司)、Mini-15K微型高速离心机(杭州奥盛仪器有限公司)。
Aston SC2T(3.5 mm×50 mm,5 μm)色谱柱、Aston SBR(3.0 mm×10 mm,5 μm)色谱柱、Aston SBX4(4.6 mm×150 mm,5 μm)色谱柱、MPA质控品(批号20210922)、MPA校准品(批号20191120)、ORG-2去蛋白剂(批号20210705)、MPA-1A移动相、MPA-2A移动相均购于湖南德米特仪器有限公司;试验用水为怡宝纯净水。
1.4 血样采集方法
待受者服用MMF达到稳态后,于术后第15天采集当日服药前以及服药后0.5、1.0、1.5、2.0、3.0、4.0、6.0、8.0、12.0 h的血样,置于乙二胺四乙酸抗凝管中,以3 000 r/min离心5 min,取上清液放于-20 ℃冰箱中,待测。
1.5 血药浓度测定方法
本研究采用本课题组已建立的全自动二维液相色谱法测定人血浆中MPA的浓度[11]。取血浆400 μL,加至含1 000 μL ORG-2去蛋白剂的1.5 mL聚丙烯管中,涡旋混匀后,置于高速离心机中,以14 500 r/min离心10 min,取上清液,置于1.5 mL进样瓶中,待测。色谱条件如下:一维色谱柱为Aston SC2T(3.5 mm×50 mm,5 μm),一维流动相为MPA-1A移动相,流速为0.8 mL/min;转移柱为Aston SBR(3.0 mm×10 mm,5 μm),流动相为纯净水;二维色谱柱为Aston SBX4(4.6 mm×150 mm,5 μm),二维流动相为MPA-2A移动相;各色谱柱柱温均为40 ℃,紫外检测波长为304 nm,采用等度洗脱,进样量为200 μL。经检验,MPA在0.32~25.03 μg/mL线性范围内呈良好的线性关系;该方法的各项方法学指标均符合生物样品测定要求。
1.6 分析指标与统计学方法
采用SPSS 21.0软件录入数据,数据以±s表示;使用WINNOLIN软件进行药动学分析,计算给药前血药浓度(c0)、药峰浓度(cmax)、药峰时间(tmax)、半衰期(t1/2)、AUC0-12h;使用SPSS 21.0软件进行统计分析,采用多元逐步回归法,分析各个时间点MPA浓度(任意一点或多个时间点)与AUC0-12h的相关性,根据各个时间点的相关系数(R2),逐步回归分析得到R2较大的简化计算公式。再按下列公式计算相对预测误差(relative prediction error,RPE)、相对预测误差绝对值(absolute relative prediction error,ARPE)、平均相对预测误差(mean relative prediction error,MRPE):RPE(%)=(AUC预测值-AUC实测值)/AUC实测值×100%,ARPE(%)=|RPE|,MRPE(%)=1/n∑ARPEi(i指患者编号);使用拟合曲线评价MPA简化计算公式与MPA-AUC0-12h的拟合情况;使用GraphPad Prism 8.0软件中的Bland-Altman方法评价简化计算公式预测值与经典药动学方法之间的一致性,使用x±1.96SD(SD即标准差)来绘制上下限的线表示数据的离散程度,覆盖95%的数据[12]。
2 结果
2.1 受者基本资料
本研究纳入肾移植受者20名,其中男性17例(占85.0%),女性3例(占15.0%);平均年龄(36.00±7.83)岁,平均体重(66.17±7.41)kg,体重指数(22.53±2.40)kg/m2。他克莫司的谷浓度为(7.93±1.71)ng/mL、峰浓度为(18.24±5.43)ng/mL,白蛋白水平为(40.94±2.62)g/L,血肌酐水平为(97.80±24.47)μmol/L。
2.2 MPA的药动学特征
20例肾移植受者的MPA-AUC曲线(图1)显示,部分受者曲线出现双峰现象,MPA的c0、cmax、tmax变异度相差较大。MPA的药动学参数(表1)如下:c0为(1.53±0.84)μg/mL,cmax为(12.07±5.97)μg/mL,t1/2为(5.41±3.67)h,tmax为(1.58±0.75)h,fAUC0-12h(按经典药动学方法计算出的AUC0-12h)为(33.95±13.40)μg·h/mL。

表1 20例肾移植受者体内MPA药动学参数

图1 20例肾移植受者体内MPA-AUC曲线图
2.3 多元回归模型的分析结果
将单个时间点的MPA血药浓度与fAUC0-12h进行相关性分析,结果(表2)显示,单一时间点的MPA血药浓度与fAUC0-12h相关性均较低(R2=0.008~0.826),其中,c0与fAUC0-12h的相关系数R2仅为0.186,6.0、8.0 h时的MPA血药浓度与fAUC0-12h的相关性最高,R2分别为0.792、0.826。
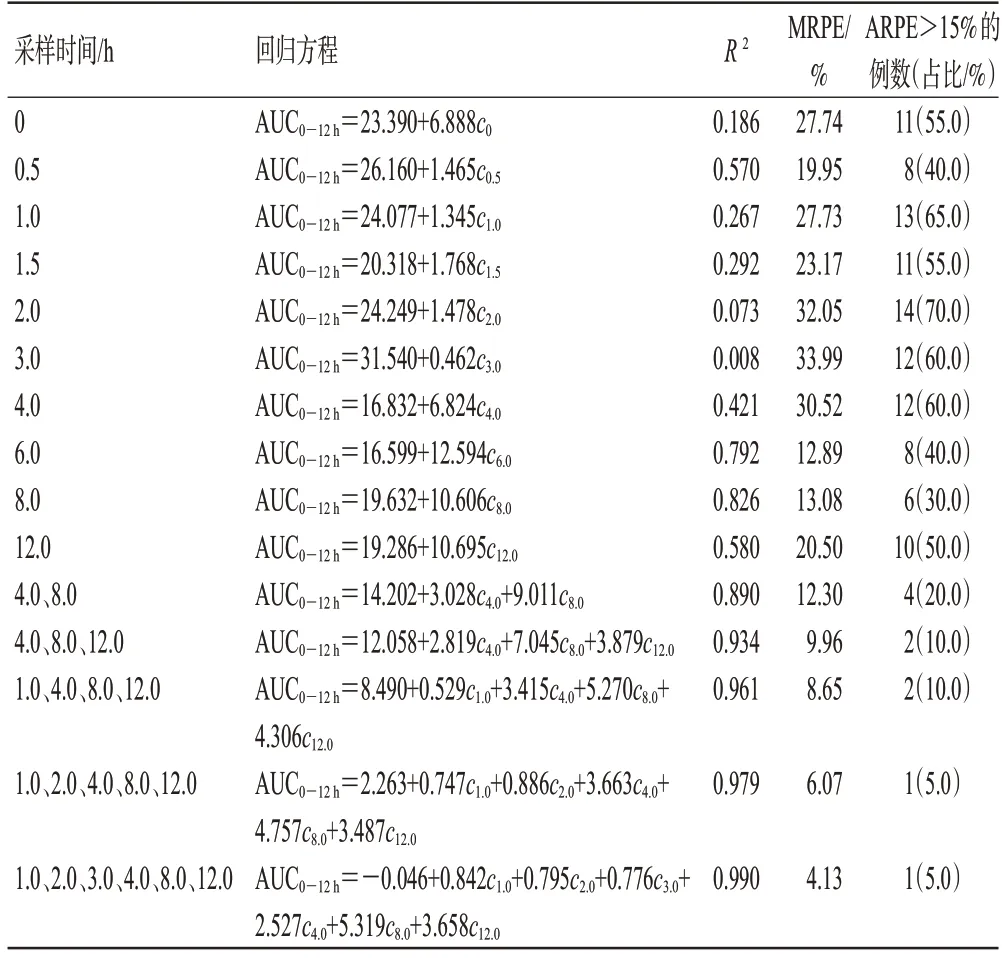
表2 MPA-AUC0-12 h简化计算公式及相关参数
进一步将MPA多个时间点血药浓度与fAUC0-12h通过多元线性逐步回归分析拟合简化计算公式,结果(表2)显示,多个时间点的MPA血药浓度所拟合出的简化计算公式的R2明显高于单个时间点,且公式纳入的采样点越多,拟合出的简化计算公式的R2就越高。考虑到检测成本和受者的依从性,以2~4个时间点作为采样点较为合适。经分析,“4.0、8.0、12.0 h”三点采样和“1.0、4.0、8.0、12.0 h”四点采样这两种采样时间点组合的R2分别为0.934、0.961,MRPE分别为9.96%、8.65%,ARPE>15%的比例均为10%,R2均高于“4.0、8.0 h”两点采样(R2为0.890),MRPE和ARPE>15%的比例均低于“4.0、8.0 h”两点采样(MRPE为12.30%,ARPE>15%的比例为20%)。可见,三点采样和四点采样的预测精度相当,均优于两点采样。考虑到采样时间点越少操作越方便,受者越易接受,故本研究最终选择“4.0、8.0、12.0 h”三点采样的MPA血药浓度用于预测AUC0-12h,其拟合出的计算公式为AUC0-12h=12.058+2.819c4.0+7.045c8.0+3.879c12.0,预测的AUC0-12h与fAUC0-12h相关性较好,R2为0.934。Bland-Altman分析结果(图2)显示,上述计算公式预测的AUC0-12h与fAUC0-12h一致性较好,有19例(占95.0%)在x±1.96SD范围内。

图2 MPA的预测AUC0-12 h与fAUC0-12 h的一致性考察结果
3 讨论
MMF是器官移植术后三联免疫抑制方案中常用的免疫抑制剂,其代谢产物MPA的体内代谢过程易受年龄、体重、基因以及合用药物等多重因素的影响,导致受者的个体差异大。应用治疗药物监测评估MPA体内暴露量,以提高药物疗效,减少不良反应,是十分必要的。目前,LSS法因其采样点少、监测成本低、受者痛苦少以及预测精度良好等优势,已成为临床MPA-AUC0-12h监测的常用策略。
由以往关于LSS法估算实测AUC的研究可见,LSS法估算模型常因不同给药剂量、剂型、给药方案、药物监测方式以及不同受者人群的影响,导致拟合出的简化计算公式差别较大[8—10,13]。若要拟合出更为精准的简化计算公式,需对研究过程的条件和检测结果作出更准确的限定。在合并用药方面,本研究选择了合用他克莫司的受者人群,他克莫司对MPA的体内暴露量影响较环孢素更小,有利于提高拟合结果的预测精度。相比于以往研究通常采用的留置针采血的方式,本研究采用小针多次采血的方式,能保证各时间点MPA血药浓度的真实可靠——因为留置针中会有部分冲管液,如果直接从留置针取血,冲管液会混到血样中,稀释药物浓度,致使检测值偏低。此外,目前报道的MPA浓度检测方法有高效液相色谱法、均相酶免疫分析法等,本研究采用的是本课题先前建立的全自动二维液相色谱法,该方法操作简便、成本低、准确度高。
本研究针对采用MMF(750 mg,q12 h)+他克莫司+甲泼尼龙三联免疫抑制方案的受者,监测其不同时间点MPA的血药浓度,基于LSS法拟合估算了MPAAUC0-12h的预测模型。结果发现,MPA的tmax为(1.58±0.75)h,部分受者出现了双峰现象,说明MPA存在肝肠循环;fAUC0-12h为(33.95±13.40)μg·h/mL,个体间差异较大。通过分析单一时间点MPA的血药浓度与fAUC0-12h的相关性发现,相关性均较差,其中,c0与fAUC0-12h的相关性R2仅为0.186,c8.0与fAUC0-12h的相关性最高,R2为0.826,ARPE>15%的占比仅为30.0%,预测精度仍较低。这一结果证实,仅通过测定c0或任一单一时间点的MPA浓度无法准确反映MPA的体内暴露量。本研究又采用多元线性逐步回归分析拟合出了基于LSS法估算MPA-AUC0-12h的简化计算公式,经验证,使用“4.0、8.0、12.0 h”三点采样的血药浓度估算MPAAUC0-12h的效果较好,预测值与fAUC0-12h有很好的相关性及一致性,ARPE在临床可接受范围内,简化计算公式为:AUC0-12h=12.058+2.819c4.0+7.045c8.0+3.879c12.0。若采用两点采样法,尽管减少了采血次数,但预测精度明显降低;若增加采样点,拟合出的简化计算公式预测精度虽然更高,但是这样势必会造成采样次数太多、时间较长,不利于临床应用。
本研究建立了肾移植受者早期服用MMF合并他克莫司时体内MPA-AUC0-12h的估算模型,通过控制入组受者类型(均为移植术后早期受者)、MMF剂型和用量以及使用更准确的检测方法等,使拟合出的MPAAUC0-12h简化计算公式更具有针对性,能够为临床提供更加精准的MPA-AUC0-12h估算结果。但本试验也存在一定不足,如本研究纳入的样本量较少,拟合出的简化计算公式仍需经大样本数据的优化和验证。今后,本课题组将进一步扩大样本量进行相关研究。
