妊娠合并主动脉夹层的临床及遗传学分析
2023-10-25张可莹李小燕刘旭霞王月丽李同勋张晓萍
张可莹,李小燕,刘旭霞,王月丽,李同勋,刘 爱,张晓萍
(1.首都医科大学附属北京妇产医院/北京妇幼保健院输血科,北京 100026;2.首都医科大学附属北京安贞医院,北京市心肺血管疾病研究所,心血管重塑相关疾病教育部重点实验室,北京 100029;3.首都医科大学附属北京安贞医院超声心动二部,北京 100029;4.首都医科大学附属北京安贞医院冠心病外科中心一病区,北京 100029)
急性主动脉夹层(acute aortic dissection,AAD)是妊娠期间的罕见事件,发病率低,但其发作时间短而凶险,母子死亡率高[1]。妊娠已被认为是AAD的诱发因素之一。孕妇突发背痛、上腹部疼痛等都需要引起注意,超声作为识别和诊断妊娠合并AAD的有效手段,能及时准确诊断,从而为挽救孕妇生命争取手术时间[2]。在手术治疗时,需要同时考虑抢救孕妇和胎儿,大大增加了手术的难度[3]。
为了减少妊娠合并AAD的发生,临床上需要准确诊断并及早发现[4-5]。据报道,在患有罕见遗传病的女性患者,如马凡综合征(Marfan syndrome,MFS)、特纳综合征(Turner syndrome,TS)、Ehlers-Danlos 综合征(Ehlers-Danlos syndrome,EDS)、Loeys-Dietz 综合征、家族性胸动脉瘤(familial thoracic aortic aneurysm,FTAA),发生妊娠合并AAD的风险更高[3,6-8]。有研究发现,未怀孕的马凡综合征女性患者的主动脉扩张速度大约每年0.38mm,在怀孕期间扩张速度每个月增加0.3mm,分娩后主动脉扩张率的增加有所下降,但仍高于怀孕前速度[9]。因此,提前对患有这些综合征患者的妊娠过程进行监控,能减少这一部分妊娠合并AAD的发生[5,8]。妊娠高血压也增加了AAD的风险。近年来,多项研究关注了妊娠合并AAD的临床诊疗管理,但针对上述综合征引起的妊娠合并AAD的遗传基础关注较少。
本研究对临床表型疑似马凡综合征的5例妊娠期女性,利用全外显子基因检测(whole-exome sequencing,WES)其可能携带的致病突变,对患者的临床特征、妊娠合并AAD诊疗方案及母婴结局进行了随访。确认了马凡综合征的致病基因变异,避免了妊娠合并AAD导致猝死的发生,为患者家族的优生优育和遗传咨询提供依据。
1 研究对象与方法
1.1 研究对象
研究对象为2016年1月至2022年1月由外院转诊至北京安贞医院的5名妊娠患者(孕8~38周),均具有疑似马凡综合征患者的体征:身材瘦长,手指及足趾细长,胸廓畸形呈鸡胸,近视。患者的基本情况见表1。本研究遵循《赫尔辛基宣言》,通过了首都医科大学附属北京安贞医院伦理委员会批准(20220225),所有受试者及其监护人均签署了知情同意书。

表1 患者基本特征Table 1 Basic information of patients
1.2 方法
1.2.1 基因组DNA的提取
取患者2mL外周静脉血(EDTA抗凝),采用全血DNA提取试剂盒提取基因组DNA,测定DNA浓度及纯度达到建库要求。
1.2.2 全外显子测序
使用NEBNext Ultra DNA 文库制备试剂盒(NEB公司)构建基因组DNA文库,使用 NimbleGen SeqCap EZ v3.0试剂盒进行全外显子捕获,质检合格后用Illumina x10进行高通量测序。原始测序数据进行去接头和质控后,比对人类参考基因组hg19,获得单核苷酸多态(single-nucleotide polymorphism,SNP)和插入缺失(insertion/deletion,InDel)。所有单核苷酸变异(single nucleotide varients,SNV)在dbSNP数据库、千人基因组等数据库的频率信息,并对变异的位置信息、类型、保守性等进行预测。Sanger测序验证变异位点。
1.2.3 功能预测及注释
使用在线预测软件Mutation taster对变异位点致病性进行预测。根据美国医学遗传学与基因组学学会(American College of Medical Genetics and Genomics,ACMG)遗传变异分类标准与指南及中国2017版《遗传变异分类标准与指南》对基因变异进行分类。
1.2.4 临床分析
随访5名患者,对其妊娠合并AAD的孕周及妊娠结局进行总结。
2 结果
2.1 全外显子基因测序结果
外显子测序结果经过筛选,并比对与遗传性主动脉疾病相关的FBN1(fibrillin-1)、SMAD3、TGFBR1、TGFBR2、TGFB2、TGFB3、COL3A1、ACTA2、MYH11、MYLK、PRKG1、LOX共12个基因所包含的变异位点,在clinvar中找到已有的FBN1基因变异为4 202个,在这5名患者上发现的杂合变异位点信息见表2。以1号患者的杂合变异为例,FBN1 基因的第63号外显子上的7 754位核苷酸由T变为C,引起蛋白的2 585位氨基酸由异亮氨酸(isolecine,I)变为苏氨酸(threonine,T)。所有致病位点经过sanger测序验证。
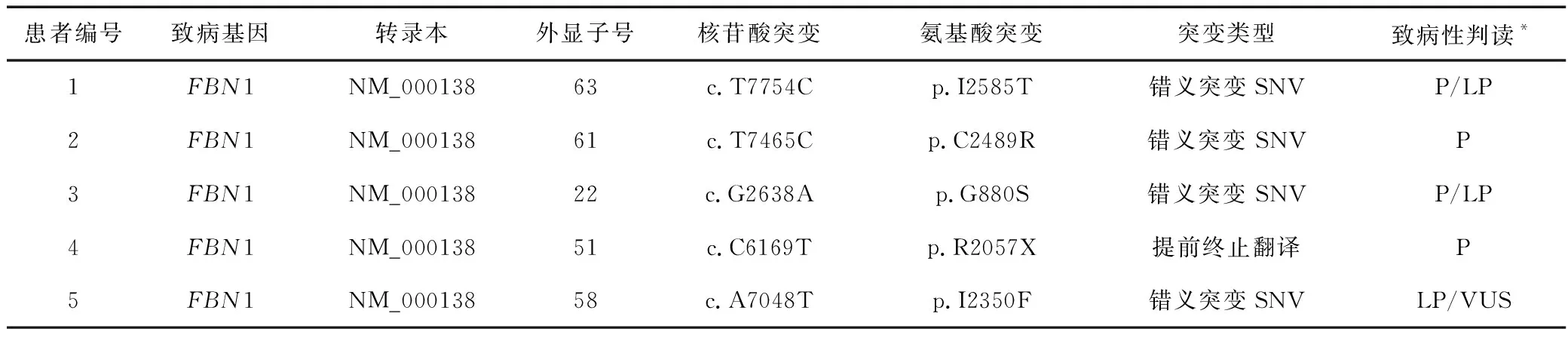
表2 患者基因检测结果Table 2 Genetic testing results of patients
2.2 变异位点功能预测及注释
表2中的5个核苷酸突变位点在dbSNP、ExAC、ESP6500等数据库中均未见频率报道,显示变异不是常见良性变异。4名患者(第1、2、3、5号)的FBN1变异为错义突变(missense SNV),不改变FBN1蛋白长度,只改变1个氨基酸。第4号患者的突变为外显子提前终止翻译(stopgain),引起FBN1蛋白长度变短。FBN1基因的提早终止翻译,患者的表型会更加严重。早孕期的基因诊断,能确认患者的遗传性疾病,同时也能在临床上对后续妊娠情况增加关注,并对主动脉直径、血压等相关指标进行持续关注,对后续妊娠的健康发展提供指导意义。
2.3 家系分析
通过对妊娠患者的致病基因变异分析后,经患者要求,对其家系进行一代测序验证,明确其家族成员携带致病变异的情况,见图1。患者1为独生女,其致病突变遗传自母亲,患者1的第一胎女儿未携带致病突变。患者2遗传自父亲,患者2的弟弟未携带致病突变。患者3的突变遗传自母亲,其母亲2008年死于主动脉夹层,患者3之子携带FBN1 c.G2638A的致病变异,后期要定时随访其主动脉宽度改变。患者4遗传自母亲,其有一哥哥早年猝死,其姐姐健康。患者5的突变FBN1 c.A7048T遗传自父亲。

注:在本研究中被检测的患者用箭头表示,虚线圆圈为妊娠患者。图1 患者家系图Fig.1 Familial pedigree of patients
2.4 临床分析结果
根据前期的遗传诊断,5名患者转诊至心血管科进行主动脉直径观察,并对患者后续主动脉发展和妊娠结局进行了随访和总结。主动脉夹层分为A型和B型,A型主要累及升主动脉,较B型更为凶险。患者1、2、3的AAD为A型动脉夹层,心脏B超检测妊娠合并AAD患者手术前的主动脉窦部(aortic sinus,AoS)直径、左室舒张末期内径(left ventricular end-diastolic diameter,LVEDD)、心脏射血分数,整体反映出患者的心脏功能,主动脉窦增宽,射血分数减低不明显。患者1、2、3发生AAD是在孕晚期(孕37~38周),同时进行剖宫产和主动脉根部置换术,手术成功并康复,婴儿体重分别为3.52、3.21、3.89kg,发育正常。患者4孕16周时的主动脉夹层向远端延续,累及降主动脉全程,已危急生命;升主动脉直径为42mm,主动脉弓部直径为23.7mm,降主动脉上胸段直径约24mm,夹层撕裂范围大,心脏射血分数减低至43%,左室舒张功能减退;孕17周时,胎儿超声检查发现双顶径3.2cm,股骨长1.8cm,头围12.1cm,腹围10.5cm,羊水深度4.9cm,有胎心和胎动。经多学科联合诊疗及家属综合考虑,先进行主动脉置换术(升主动脉+全弓+降主动脉替换术),后进行剖宫取胎术终止妊娠。患者5在孕早期(孕8周)已发生AAD,先终止妊娠,再进行主动脉根部置换术。见表3。

表3 患者疾病相关临床特征Table 3 Clinical characters of patients
3 讨论
3.1 马凡综合征的临床特征及遗传特点
马凡综合征是一种结缔组织的常染色体显性遗传病,主要以心血管、眼部和骨骼系统疾病为特征。体貌特征主要表现为身材瘦长、蜘蛛指及足趾细长;胸廓畸形呈鸡胸;脊柱侧弯;近视[10]。心血管系统受累的疾病主要为主动脉瘤、瓣膜病变、左心室扩大和心力衰竭[10]。马凡综合征的致病基因是FBN1,该基因包含66个外显子,编码2 871个氨基酸[10-11]。随着二代测序技术的发展,人们对马凡综合征的遗传学机制有了更清晰的认识,目前能通过基因检测来精准判断并确认马凡综合征患者的基因型。目前已经发现的FBN1致病突变超过2 000种,分布于FBN1基因的各个外显子,没有明显的热点区域,这些突变解释了90%左右的马凡综合征[10-11]。
3.2 妊娠增加了主动脉夹层的破裂风险
怀孕会增加马凡综合征女性主动脉夹层的风险,Liu 等[3]报道总结发现12例妊娠合并主动脉夹层的患者中有4人是马凡综合征患者。马凡综合征患者在妊娠前需要评估妊娠风险并进行孕前咨询,多学科医疗团队需要参与孕前评估,包括心脏病专家、遗传学家和妇产科医生[12]。多学科评估的内容应包括家族史、体格检查和主动脉成像的检查[13]。国外报道建议马凡综合征女性患者怀孕前使用磁共振成像(nuclear magnetic resonance imaging,MRI)对整个主动脉进行成像,全面检查其主动脉的生理状态。女性马凡综合征患者的主动脉根部直径>45mm,应考虑在孕前选择性接受主动脉根部置换术[13]。
3.3 疑似马凡综合征的妊娠患者有必要进行基因检测
在本研究中,我们在患者孕早期,通过体貌特征怀疑患者患有马凡综合征,通过全外显子测序确认其致病位点,并进一步对其家系进行分析。我们发现4个家系的致病变异均为致病或疑似致病位点,检出成功率较高。患者1家系的致病变异FBN1 c.T7754C是致病/可能致病,在clinvar上有相同变异位点的不同变异;患者2家系的致病变异FBN1 c.T7465C是已经经过确认的致病突变;患者3的致病变异FBN1 c.G2638A 是致病/可能致病,在clinvar上报道过相同变异;患者4的致病变异FBN1 c.C6169T 是移植致病变异;患者5的变异FBN1 c.A7048T是可能致病/意义不明确的,在clinvar上没有相同变异报道,但该位点在家系内与疾病共分离,因此该位点为可能致病变异。
我们在基因检测获得明确结果后,对患者及其家属进行了遗传学相关的知识教育,讨论怀孕过程中可能发生AAD的母体和胎儿风险。提前告知患者AAD的临床症状如胸痛、背痛等,如出现症状应立即就医。同时教育患者马凡综合征的遗传特性,即孩子有50%的几率遗传该致病变异。虽然这些健康教育不能阻止妊娠合并AAD的发生,但能让患者意识到妊娠过程可能遇到的危险,并提前到心内科就诊,监测主动脉的变化。最终,有3名患者在妊娠晚期发生AAD并及时救治,通过剖宫产分娩出孩子,母子平安。有2名患者在孕中期或孕早期出现AAD,通过手术恢复。我们的研究有效地预防了妊娠合并AAD猝死的发生,对患者的马凡综合征进行了精准诊断,为患者的后续治疗选择提供了遗传依据,并为临床诊疗提供了基础。
