烧结烟气臭氧梯级氧化吸收工艺硫氮平衡研究
2023-10-24赵瑞壮郜国平刘霄龙朱廷钰
赵瑞壮,邹 洋,郜国平,刘霄龙,朱廷钰
(1.河北创洁环保工程有限公司,河北 石家庄 050000;2.中国科学院过程工程研究所,北京 100190)
在钢铁生产过程中,烧结工序是大气污染排放量最大的工序,其SO2、NOx、二英排放量分别占整个钢铁行业排放总量的70%、48%和90%左右[1]。因此,在传统的烧结—高炉—转炉长流程钢铁生产结构中,钢铁超低排放普遍聚焦在烧结工序,从烟气污染物治理技术研发和应用上更是重点围绕脱硝来开展。随着钢铁行业超低排放限值的提出,烧结烟气已成为大气污染物治理的重要目标,研发出高效、低耗的烧结烟气硫硝治理技术已经成为当务之急,也是缓解大气污染的最有效的途径之一。
目前,烧结烟气的硫硝治理工艺主要有SCR脱硝+半干法脱硫工艺[2-5]、活性炭吸附工艺[6-8]、臭氧氧化吸收工艺[9-12]等。针对我国目前大多数烧结机已安装脱硫环保设施的现状,同时结合烧结烟气的工况特点以及综合考虑投资运行费用和场地等制约因素,臭氧氧化吸收工艺被认为是非常适用于烧结烟气的硫硝控制技术之一。十三五期间,相关科研单位在河钢唐钢240 m2烧结机末端烟气现有“密相干法脱硫+布袋除尘”净化系统的基础上,共同研发了烧结烟气臭氧梯级氧化吸收工艺,其工程应用表明,烧结烟气经过臭氧梯级氧化吸收净化后,SO2和NOx排放质量浓度分别低于10mg/m3和30mg/m3,满足超低排放限制指标要求。
烧结烟气中NO组分占所有NOx的90%以上,且由于NO物性特征难以直接与碱性吸收剂进行反应实现NOx的脱除,因此通常将NO转化为较容易与碱性吸收剂发生反应的其它含“N”化合物,再进一步进行脱除。臭氧氧化-吸收技术工艺原理即是将NO氧化为更容易吸收的高价态NOx(如:NO2和N2O5等),再与SO2共同在脱硫塔中发生吸收反应进行脱除。通常认为,NOx与吸收剂发生化学反应后生成亚硝酸盐和硝酸盐;然而,SO2与吸收剂发生化学反应后生成的亚硫酸盐也有可能将亚硝酸根还原成N2。
本文对该工艺技术的硫氮平衡展开深入研究,通过对净化系统入口和出口烟气量以及烟气中的SO2、NOx质量浓度和设备运行时间进行监测记录,计算得到净化系统中S、N输入总量,再根据系统排出吸收剂总量可计算得到理论上脱硫废灰中S、N元素的质量分数,进而得到S、N元素平衡率,分析数据可得系统输入和输出的S、N元素基本达到平衡的条件;最后根据XRD结果,进一步对吸收产物进行分析,明确该工艺技术中NOx的主要吸收路径和原理。
1 工程应用和检测分析情况
1.1 工艺概况
本文以河钢唐钢240 m2带式烧结机配套的净化设施作为研究对象,该系统采用的净化工艺为“臭氧梯级氧化+密相干塔吸收+布袋除尘”,其工艺流程如图1所示。由图1可知,烧结烟气经A、B烟道分别进入A、B净化系统进行处理后,汇合在一起,由烟囱排出。其中臭氧梯级氧化吸收技术的工艺原理:烧结原烟气在脱硫主塔前烟道内NO被第一、二级臭氧分布器喷入的O3初步氧化为高价态NOx,之后进入脱硫塔与吸收剂进行反应吸收;主塔内未进行反应吸收的NOx被脱硫主、副塔之间设置的第三级臭氧分布器喷入的O3进行氧化,在后端的脱硫副塔、布袋除尘器内与吸收剂进行进一步反应吸收,最后达标烟气由烟囱排放。整个系统共有5个烟气监测点,分别是A系统原始烟气监测点和脱硫脱硝后监测点、B系统原始烟气监测点和脱硫脱硝后监测点、烟囱总排口监测点。

图1 臭氧梯级氧化吸收工艺Fig.1 Ozone cascade oxidation absorption process
1.2 样品选取
从新鲜吸收剂中采集的样品记为样品1(确定吸收剂本身的S、N元素质量分数);A、B净化系统运行稳定期间,第一日从A系统脱硫脱硝后排出的吸收剂中所采样记为样品2;第一日从B系统脱硫脱硝后排出的吸收剂中所采样记为样品3;第二日从A系统脱硫脱硝后排出的吸收剂中所采样记为样品4;第二日从B系统脱硫脱硝后排出的吸收剂中所采样记为样品5。从相同钢铁企业(烧结生产原料和污染物吸收剂品质基本一致)不同烧结机配套的“SCR脱硝+循环流化床脱硫+布袋除尘”净化系统中排出的吸收剂中所采样记为样品6(对比不同净化工艺的吸收产物)。
1.3 检测方法及仪器
净化系统入口和出口烟气中的SO2、NOx质量浓度由CEMS在线监测系统进行实时监测,系统排出的吸收剂总量由中控室生产人员详细记录。样品中S、N元素质量分数分别采用元素分析法(vario EL cube型元素分析仪)和离子色谱法检测(DX-600型离子色谱仪)进行分析检测。另外,通过XRD(Rigaku SmartLab 9 kW 离子色谱仪X射线衍射仪)对各组样品进行物相分析,并采用碘量法对样品中CaSO3的质量分数进行滴定分析。
1.4 S、N平衡率的计算
净化系统S、N平衡率是指系统排出吸收剂实际检测的S、N元素质量分数与根据系统进出口SO2、NOx质量浓度计算的吸收剂S、N元素应有质量分数的比值。烟气中的S、N元素进入净化系统中发生吸收反应后,大部分以固体的形式留在脱硫废灰中从系统排出,剩余小部分未被吸收的S和N元素随烟气从烟囱排出。根据净化系统入口和出口烟气量、污染物质量浓度和运行时间,可计算净化系统中S、N输入总量,再根据系统排出吸收剂总量可计算得到理论上脱硫废灰中S、N元素的质量分数。具体计算公式如下。
式中:mS为系统输入S元素总量,kg;C1S、C2S分别为系统入、出口的SO2质量浓度,kg/m3;Q为烟气流量(标况),Nm3/h;T为系统运行时间,h;M1S、M2S分别为SO2、S的相对摩尔质量,g/mol;w1S为排出吸收剂中S元素应有质量分数,%;ma为排出吸收剂总量,kg;ηS为系统S元素平衡率;w2S为排出吸收剂采集样品中检测的S元素质量分数,%;mN为系统输入N元素总量,kg;C1N、C2N分别为系统入、出口NOx质量浓度,kg/m3;M1N、M2N分别为NO2、N相对摩尔质量,g/mol;w1N为排出吸收剂中N元素应有质量分数,%;ηN为系统N元素平衡率;w2N为排出吸收剂采集样品中检测的N元素质量分数(烟气中NOx质量浓度以NO2计),%。
2 结果与讨论
2.1 净化系统硫氮平衡分析
2.1.1 净化系统运行情况
针对臭氧梯级氧化吸收净化系统,运行参数主要包括净化系统入口和出口SO2和NOx质量浓度、烟气流量以及系统排出吸收剂总量,生产运行稳定期间的相应参数如表1所示。净化系统共有5个监测点,相较于其它监测点,烟囱烟气流量最稳定、波动较小。因此,选择烟囱的流量作为烟气的流量进行计算。A、B净化系统入口和烟囱出口的SO2、NOx质量浓度在一定范围内波动,选取中间值作为入口和出口的质量浓度进行计算分析。
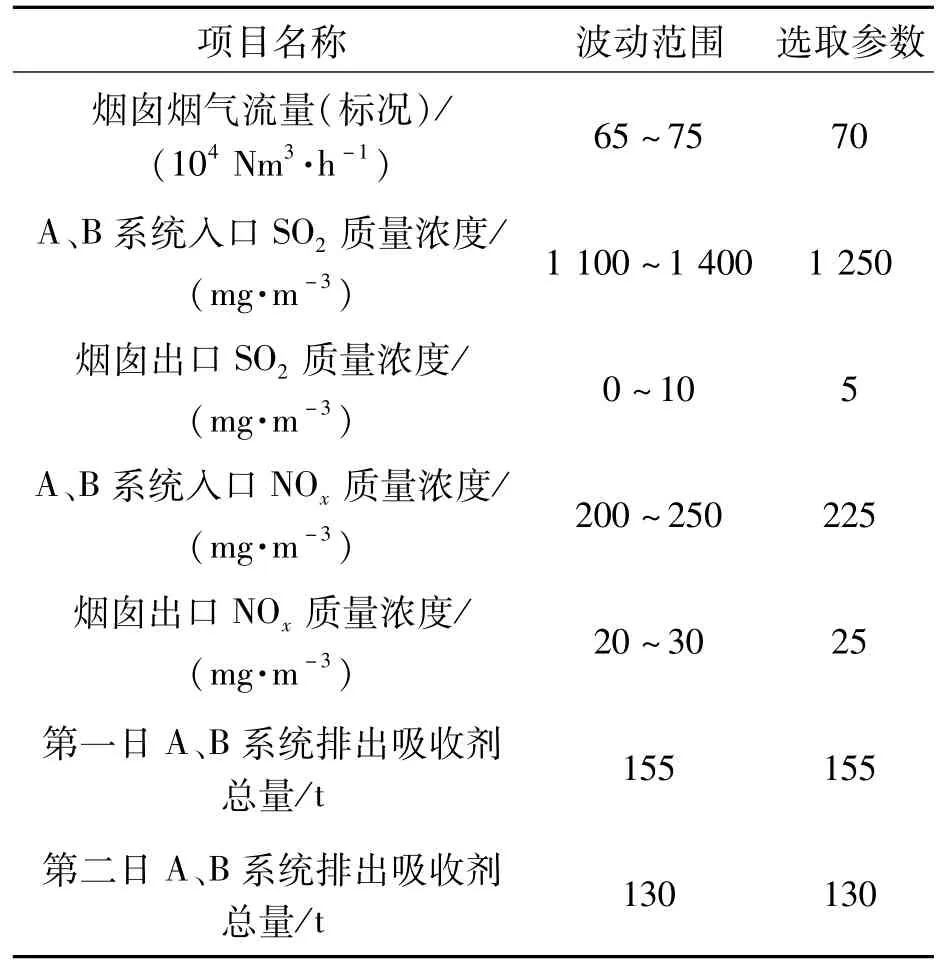
表1 系统运行参数Table 1 System operation parameters
2.1.2 系统输入S/N元素总量及排出吸收剂中S/N应有质量分数
根据臭氧梯级氧化吸收净化系统运行参数:烟囱烟气流量、净化系统入口和烟囱出口的SO2和NOx质量浓度、运行时间,代入式(1)和(4),计算得出系统生产运行24 h,A、B系统输入S元素总质量为10 458 kg,输入N元素总质量为1 022.61 kg。
第一日A和B系统排出吸收剂155 t,代入公式(2)和(5),排出吸收剂中S元素应有质量分数为6.75%,N元素应有质量分数为0.66%。第二日A和B系统排出吸收剂130 t,代入公式(2)和(5),排出吸收剂中S元素应有质量分数为8.04%,N元素应有质量分数为0.79%。生产运行两日,A、B系统输入S元素总质量为20 916 kg,输入N元素总质量为2 045.22 kg。两日系统排出吸收剂共计285 t,排出吸收剂中S元素应有质量分数为7.33%,N 元素应有质量分数为0.72%。
2.1.3 系统S/N元素平衡率计算
对所选取的样品进行元素质量分数检测,检测结果如图2所示。S元素质量分数是通过元素分析仪直接检测得出,样品中的S元素经高温氧化燃烧生成SO2,并在载气的推动下,进入分离检测单元;S元素的氧化物经吸附-脱附柱的吸附解析作用,S被分离测定。N元素质量分数是通过离子色谱测量样品中的硝酸盐和亚硝酸盐的含量确定的。从检测结果可知,样品1新鲜吸收剂中含有少量的S、N元素;样品2、3相比样品4、5中S元素和N元素质量分数均相对要少一些,这与系统运行时长有直接关系;对于在A、B不同系统同一周期采集的样品2和样品3、样品4和样品5中的S/N元素质量分数还是比较接近的。其中,样品3的N元素质量分数与其它样品相差较大,这可能是与净化系统入口NOx的质量浓度波动或选取的样品自身未能充分参与吸收反应有关系。
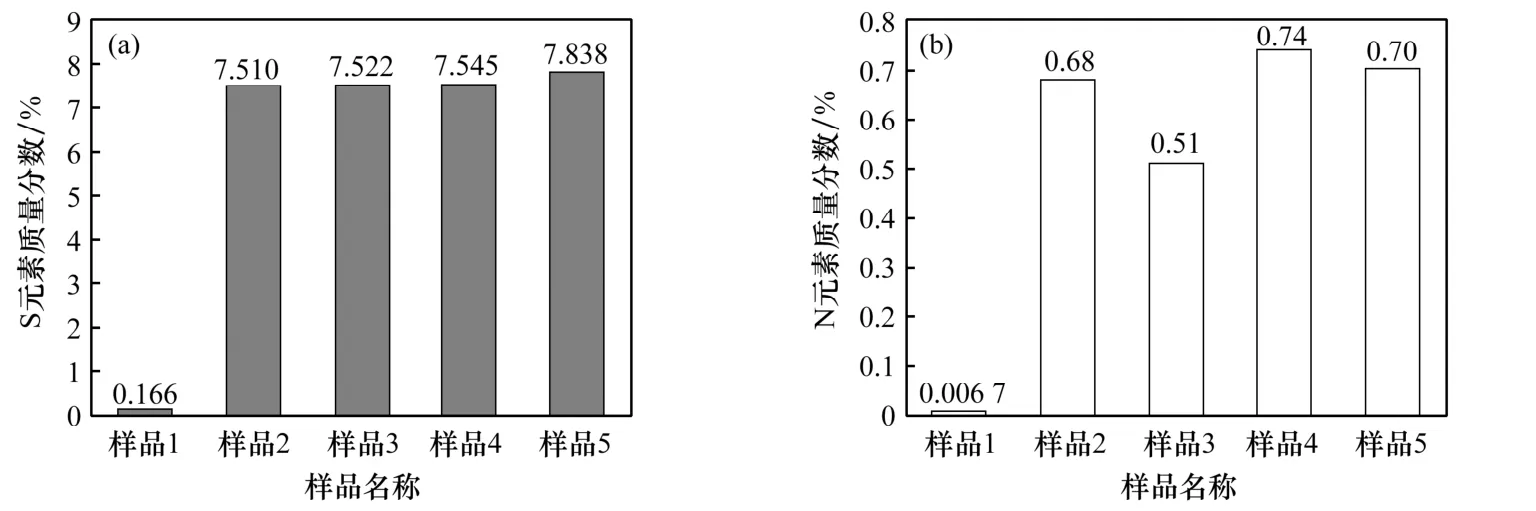
图2 样品中S和N元素的质量分数Fig.2 Nass fraction of S element and N element in the sam p le
根据样品实际检测的元素质量分数和计算的元素应有质量分数,代入公式(3)和(6),计算出系统S/N元素平衡率如图3所示。由图3可知,系统S/N元素平衡率大于89%,系统输入和输出的S元素和N元素基本达到平衡。其中,第一日的S平衡率为108.94%,输出的S元素大于输入,这可能是第一日系统实际入口的SO2质量浓度比选定的质量浓度相对要高,导致计算的S元素应有质量分数偏小。对于系统N元素平衡率,第一、二日以及两日平均的平衡率都在90%左右,这说明烟气中的NOx被吸收后,主要以硝酸盐和亚硝酸盐的形式保留在吸收剂中,即输入的N元素很少或没有以N2的形式从系统中输出。N元素未达到完全平衡主要原因分析:由于烧结生产工况波动性较大,A、B系统入口烟气量和NOx质量浓度参数变化等的不确定性,导致选定参数计算的N元素总量比实际输入的N元素总量可能偏高。
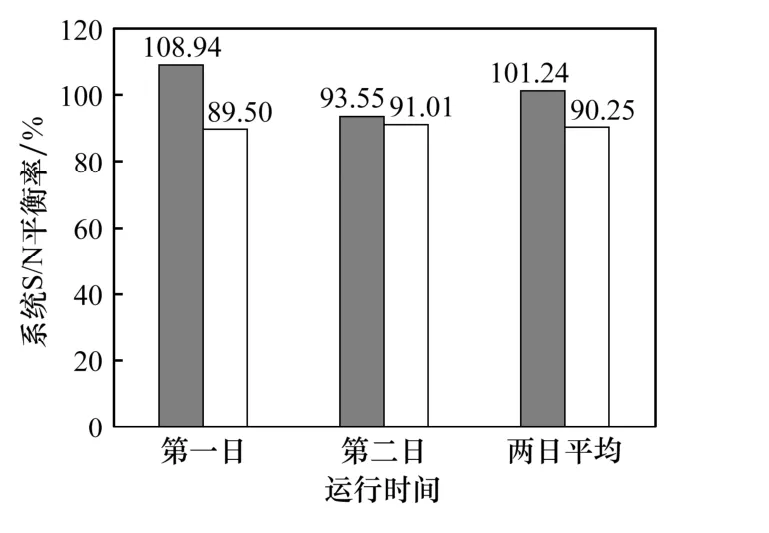
图3 系统S/N元素平衡率Fig.3 S/N elem ent balance rate of the system
2.2 吸收产物分析
梯级氧化吸收工艺是利用臭氧先将烟气中的NO氧化为NO2,然后在脱硫塔内进一步氧化为N2O5,再通过吸收剂与SO2一并吸收。相对于“SCR脱硝+半干法脱硫”技术,臭氧梯级氧化吸收工艺在脱硫塔内不仅同时吸收脱除NOx,还同时存在氧化反应。因此,有必要对吸收后的产物进行进一步分析,并与“SCR脱硝+半干法脱硫”技术排出的吸收剂进行了对比分析。
首先,对样品进行XRD物相分析,其检测图谱如图4所示。由图4可以看出:臭氧梯级氧化吸收工艺排出的吸收剂样品2到样品5检测出的主要组分为CaSO3、CaSO4和Ca(OH)2,而“SCR脱硝+半干法脱硫”排出吸收剂样品6中检测出的组分为CaSO3和Ca(OH)2。新鲜吸收剂的主要成分是Ca(OH)2,吸收SO2后生成CaSO3,CaSO3氧化后会进一步生成CaSO4。臭氧梯级氧化吸收工艺的脱硫塔内存在强氧化剂臭氧,能较快地将CaSO3氧化为CaSO4; “SCR脱硝+半干法脱硫”工艺在脱硫塔内虽然存在氧气,但CaSO3被氧化为CaSO4的反应速率很慢,使得副产物脱硫灰中的CaSO4质量分数非常少,以至于样品6中没有明显检测到CaSO4组分。
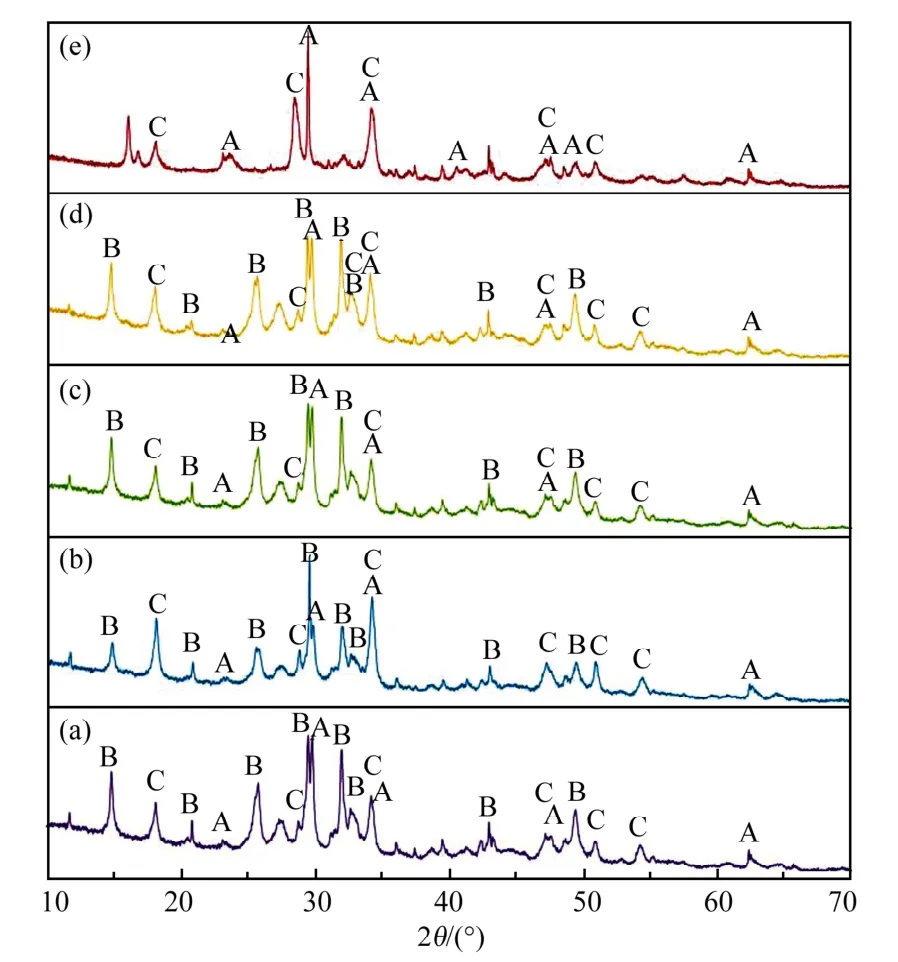
图4 XRD检测图谱Fig.4 XRD detection map
为进一步对比两种不同净化工艺副产物的差别,同时对样品CaSO3质量分数进行测量分析,结果如图5所示。由图5可以看出,样品2到样品5的CaSO3质量分数明显要低于样品6,结合图4的XRD图谱,这说明臭氧梯级氧化吸收工艺在吸收过程中产生的CaSO3大量被氧化为CaSO4,从而导致样品中的CaSO3质量分数减少。
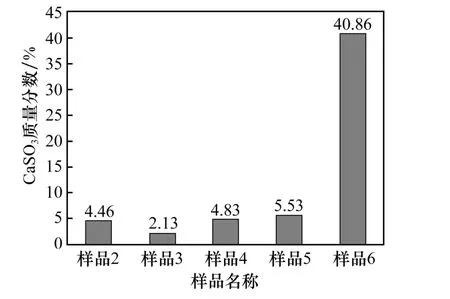
图5 吸收剂中的CaSO3质量分数Fig.5 CaSO3 mass fraction in absorbent
3 结 论
本文通过研究钢铁烧结烟气臭氧梯级氧化吸收工艺在工程实践应用中的硫硝平衡,明确了该工艺脱硫脱硝过程中硫元素和氮元素的去向,厘清了脱硫塔内复杂组分中NOx吸收反应的主要路径或原理。得到如下结论:
(1)臭氧梯级氧化吸收净化系统排出的吸收剂样品 S平衡率为101.24%,N 平衡率为90.25%,排除生产波动导致选取参数误差的计算结果影响外,可以确定臭氧梯级氧化吸收工艺的S、N元素输入和输出基本平衡,去向明确。
(2)臭氧梯级氧化吸收工艺排出的吸收剂中CaSO3质量分数要明显低于“SCR脱硝+半干法脱硫”工艺,即提高了脱硫副产物中的CaSO4组分质量分数,从当前脱硫副产物主要应用于建材等行业角度去综合考虑,相当于臭氧梯级氧化吸收工艺有助于提高脱硫副产物的再利用品质。
