原位DRIFTS在SCR过渡金属催化剂研究中的应用进展
2023-10-19张兴华王宽岭王学海
张兴华,王宽岭,王学海,李 龙
(1. 中石化(大连)石油化工研究院有限公司,辽宁 大连 116045;2. 中国昆仑工程有限公司 大连分公司,辽宁 大连 116045)
氮氧化物(NOx)涵括NO、NO2、N2O4等组分,来源于炼油化工、船舶重卡运输、垃圾焚烧等行业的诸多尾气排放过程。对于炼油化工行业而言,尾气中的NOx大多以NO的形式存在,而选择性催化还原(SCR)工艺是应用历史较长、前景较广且性价比较高的脱硝技术。该技术是指在催化剂介入下,NH3选择性地将NOx(一般指NO)还原为N2的过程[1]。SCR反应的通用方程式为4NH3+4NO+O2→4N2+6H2O。若SCR体系中无O2时,反应遵循标准SCR反应4NH3+6NO→5N2+6H2O;若体系中富氧时,反应遵循快速SCR反应4NH3+2NO+2NO2→4N2+6H2O。快速SCR反应速率比标准SCR高约1个数量级[2]。
SCR工艺研究的核心在于催化剂的迭代研发。目前,SCR催化剂可分为贵金属催化剂、分子筛催化剂、过渡金属催化剂等几类,其中过渡金属催化剂的工业化应用前景较广,对其的研究也较为系统。适宜的酸度和良好的氧化还原性能是过渡金属催化剂高效吸附和活化NH3和NO的两大重要因素,而原位漫反射红外傅里叶变换光谱(原位DRIFTS)技术是原位表征NH3和NO吸附和活化过程的普适手段。原位DRIFTS通常由配气系统、光谱采集系统以及吸附-反应系统构成,可无损地对催化剂表面物种进行在线追踪与表征,并以此来分析催化反应路径[3]。对于SCR过程,研究者通常先考察变温条件下NH3和NO(NO+O2)分别持续通入时在催化剂表面的吸附脱附过程,着重关注某工况下气体的吸附位点变化及中间体的转化路径;接下来即可进行SCR反应研究,即先通入第一类反应气体至饱和并摄谱,再通入第二类反应气体,在程序升温的准稳态吸附-反应过程中考察反应气体吸附峰(包括倒峰,主要来自于中间产物的分解)的生消,并分析催化反应路径。同时,借助XRD、BET、TG、SEM、TEM、XPS、XRF、RS、NH3-TPD等分析手段对催化剂性能进行综合表征,从诸多方面来印证、探讨催化剂的SCR反应机理。利用原位DRIFTS进行SCR反应机理的研究是高效而广泛的,通过探索催化剂表面物化过程可以从理论层面指导催化剂的合成和优选。
本文概述了4类SCR过渡金属催化剂的研发现状,归纳了原位DRIFTS在NH3和NO吸附转化过程研究中的应用进展,总结了不同种类过渡金属催化剂体系的SCR反应机理及路径,并对原位DRIFTS在SCR研究中的应用前景进行了展望。
1 SCR过渡金属催化剂
1.1 钒基催化剂
钒基催化剂是最早且广泛应用于工业SCR工艺的过渡金属催化剂,有多聚钒物种存在或金属掺杂的钒基催化剂因其高脱硝率和SO2耐受性而受到研究者的广泛关注[4]。其中,VMo(W)Ti系催化剂是性能稳定且应用成熟的商用催化剂[5],但因其活性温度范围窄(300~400 ℃)、副反应易发而仍有研发改进空间。研究者常通过掺杂CeO2(提高储释氧性)、Fe2O3(增加磁性)、ZrO2(提高热稳定性)、TiO2(提高表面活性组分的分散性和N2选择性)等助剂来提高钒基催化剂的SCR性能[6-7]。此外,研究者也通过改进合成方法、减小粒子尺寸、暴露特定晶面、调变载体结构等方式进一步解决钒基催化剂活性温度范围窄、易硫中毒等弊端[8]。然而,钒基催化剂的发展前景并不被看好,这是因为其低温段活性低和具有生物毒性的劣势尚不能从根本上得到解决。
1.2 铁基催化剂
地壳中含有储量丰富的铁资源,自20世纪80年代起的研究表明,氧化铁颗粒(包括α-Fe2O3和γ-Fe2O3)、铁溶胶物质及复合铁氧化物均有较好的中高温(>250 ℃)SCR脱硝性能,这归功于铁元素良好的氧化还原能力和热稳定性[9-10]。然而铁基催化剂的低温SCR活性短板明显,工业应用空间有限,研究者多采用修饰或掺杂金属(如Mo、W、Ce等)氧化物助剂的方式调节其低温活性[9]。将铁元素掺杂到其他金属基催化剂体系中也会对SCR活性产生正向影响,这是因为铁元素作为助剂可有效降低催化剂的结晶度和晶体尺寸、增加氧空穴数量、有利于氧化中间体形成等[11]。此外,铁基纳米催化剂近年来发展迅速,催化剂表面的纳米针结构和均匀的组分分布使其在200~350 ℃的NO转化率和N2选择性均可达90%以上[12]。
1.3 铈基催化剂
同铁元素一样,铈元素储量丰富、无生物危害性,不稳定的外电子层结构使之具有优异的氧化还原活性、良好的储释氧能力和灵活的电荷平衡性能,故铈基催化剂被认为是钒基催化剂的有力替代品。尽管单独CeO2催化剂的反应活性有限、抗硫抗水性不佳且N2选择性较差,但大量研究表明,向铈基催化剂中掺杂助剂组分(如Fe、Cu、W、Mo、Nb、Zr、Al、Sb、Co、无机盐离子等)可大幅提升其催化性能[13-17]。助剂掺杂不仅可以提高铈基催化剂的储释氧性能,还能细化氧化物晶粒,增加其比表面积,提升其氧化还原活性和酸性位点数量。在目前的低温SCR催化剂中,铈元素仍主要以改性剂和助催化剂的形式参与体系,其作用主要是通过提升体系氧化还原性能促进反应活性中间体的生成。
1.4 锰基催化剂
钒、铁、铈基催化剂的活性温度范围集中在中高温段,锰基催化剂则在低温段具有突出的SCR反应活性。锰元素具有3d44s2的外层电子结构,多变的化学价态和优异的氧化还原性能是其具有良好SCR低温反应活性的根本原因[18]。KAPTEIJN等[19]报道了不同晶相锰氧化物的脱硝活性强弱顺序为MnO2>Mn5O8>Mn2O3>Mn3O4。锰基催化剂的抗硫性和N2选择性较差,掺杂过渡金属或稀土元素可以改善。GAO等[20]制备了一系列MMnCeOx(M为Cu、Cr、Fe、Sn等)锰基三元复合氧化物催化剂,发现助剂的掺杂显著提高了催化剂的SCR性能,这是因为有助剂掺杂的催化剂固溶体结构不仅有更大的比表面积,且更易形成活性氧物种,促进了快速SCR反应的进行。另外,一大类具有特殊构型的锰基催化剂也在实验室研发中,主要包括钙钛矿型、尖晶石型催化剂以及其他具有特殊微观形貌的催化剂,此类催化剂通常具有更多的活性晶面、表面活性氧物种和酸性位点,因而理论上具有更为卓越的SCR性能。
上文对目前研发和应用最为广泛的4类过渡金属SCR催化剂进行了概述,研究者通常在合成并评价其性能后,结合原位DRIFTS等手段从微观层面对反应过程加以理解和阐释,下文将着重讨论。
2 SCR催化剂上的吸附物种
利用原位DRIFTS对SCR反应中NH3及NO+O2的吸附位点进行表征是探求反应路径的首要步骤,表1和表2分别整理了NH3及NO+O2在各类过渡金属催化剂上吸附时的原位DRIFTS峰位。
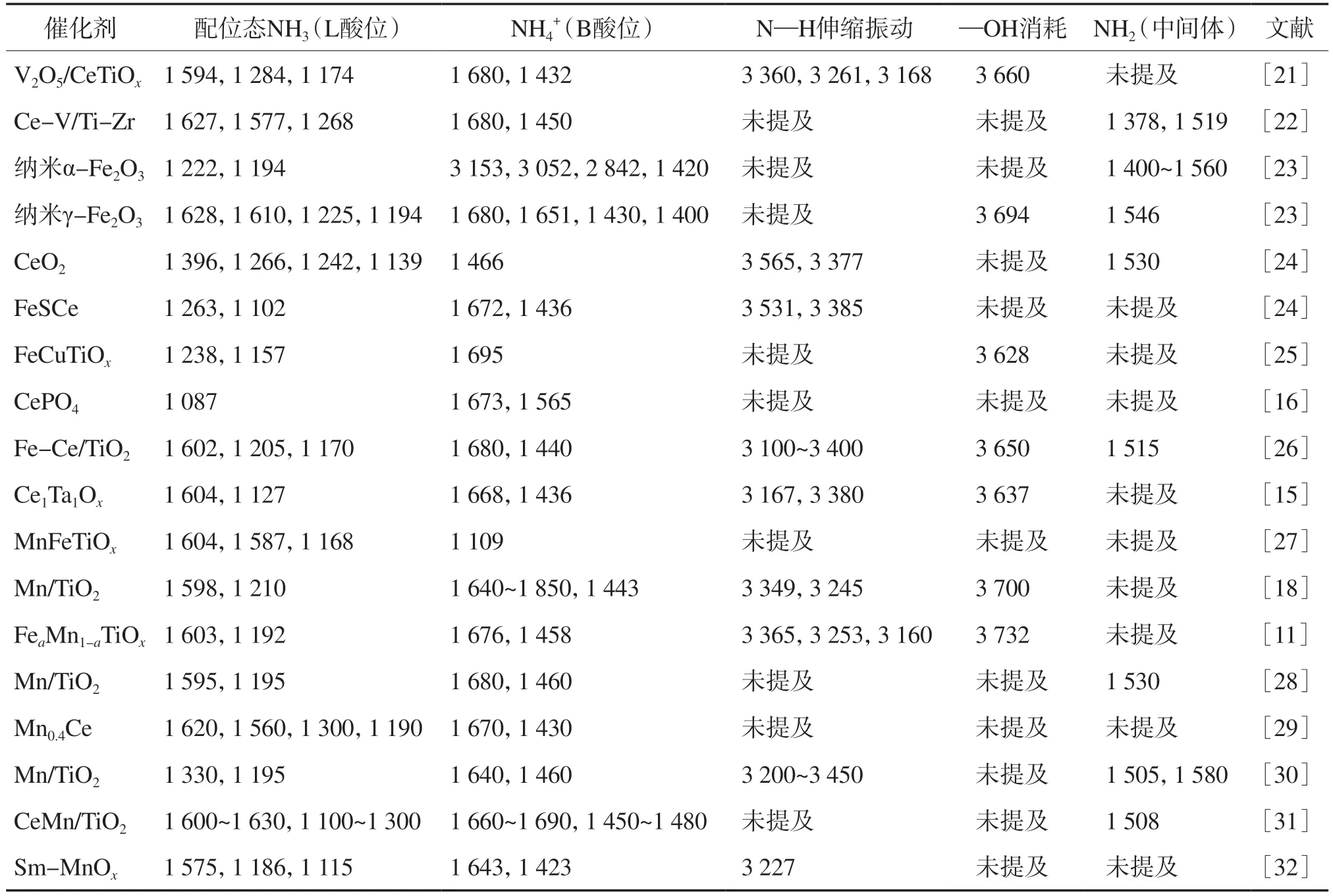
表1 NH3在不同过渡金属催化剂上吸附时的原位DRIFTS峰位 波数,cm-1

表2 NO+O2在不同过渡金属催化剂上吸附时的原位DRIFTS峰位 波数,cm-1
2.1 NH3的吸附
如表1所示,作为反应中还原性气体的NH3一般会以两类形态吸附在催化剂表面并参与反应,一类是以NH4+的形式吸附在催化剂B酸位的—OH(羟基)上,一类是以配位态NH3的形式(包括氨基、亚氨基等)吸附在L酸位的未饱和阳离子上。图1具体表征了NH3吸附在L酸位的几类形式及其转化过程[33]。不同体系中L/B酸位点上氨物种参与反应的程度有较大差异:SJOERD KIJLSTRA等[34]在Mn/Al2O3二元复合氧化物催化剂体系的研究中发现,吸附于L酸位的氨基可同时与气相NO和吸附相NO2物种发生反应,但吸附于B酸位上的NH4+为惰性反应物种;SMIMIOTIS等[35]的研究结论则与之相反,发现在Mn/SiO2表面NH3主要以NH4+的形式参与了反应,这说明同金属基的不同载体形态对NH3的吸附和活化程度有显著影响。此外,金属的前驱体形态也是重要影响因素:ANGELES LARRUBIA等[33]的研究表明,当催化剂活性组分为Fe2O3时,吸附于L酸位的氨物种是主要反应物;有研究者则发现,前驱体为Fe2(SO4)3时,B酸位点对催化剂的活性、选择性及稳定性起更重要的作用[36]。对于原位DRIFTS而言,除B和L酸位的氨物种峰外,NH3吸附时消耗催化剂表面—OH形成的倒峰、NH3被过氧化过程中出现的中间体及副产物峰等也是常见峰。

图1 NH3吸附在L酸位的几类形式及其转化过程
温度是影响催化剂NH3吸附性能的重要因素。B酸位上的NH4+在高温下易发生热分解、脱附,这对中低温SCR反应是有利的[11];而L酸位上的氨物种常体现出随温度升高而吸附性增强的特征。有研究也发现,V2O5/TiO2催化体系中,随温度升至500 ℃,L酸位吸附性先增强后略微降低,B酸位吸附性则不断弱化,直至不再吸附[21];但也有少量研究观察到L酸位吸附性在高温下显著弱化的现象[29]。总体而言,当温度低于300 ℃时,催化剂上的B酸位和L酸位都会吸附氨物种;当温度高于300 ℃时,催化剂以L酸位吸附为主,且高温会导致B酸位向L酸位的转化[29]。值得注意的是,恒定温度下位于L、B酸位上的NH3吸附物种谱峰会有红移的现象,这分别反映了NH3和NH4+物种的脱氢过程[22]。除温度外,催化剂的载体形态(如Ti纳米管的应用)、多种活性金属组分的协同、无机阴离子(如SO42-、PO42-)的修饰也可以丰富催化剂表面的酸性位点,拓宽催化剂对NH3吸附和活化的温度范围[36]。另外,H2O的存在可能会将L酸位转化为B酸位,这对NH3的吸附有轻微的正向作用[30],但H2O引起催化剂表面硝酸盐物种(NO吸附物种)的锐减是导致SCR反应钝化的主要原因[9]。SO2也可促进B酸位的生成,但也易与NH4+结合形成惰性铵盐[37]。
2.2 NO的吸附
相较于NH3,NO在催化剂上的吸附形态更为多样,常见的物种包括NO2和(亚)硝酸盐(单齿(亚)硝酸盐、桥式(亚)硝酸盐、双齿(亚)硝酸盐及桥式硝基亚硝酸盐)等,如图2所示。NO的吸附构型可影响(亚)硝酸盐物种的生成过程和反应性,而吸附构型主要与催化剂表面是否存在O空位,N、O原子与过渡金属成键方式等因素相关,可通过密度泛函理论推得。另外,由于体系中O2或NO吸附程度的不同,吸附态NO2的生成路径也不止一种[18],这些都充分反映了SCR体系的复杂性。多数体系中,吸附态NO2、亚硝酸盐及单齿硝酸盐性质活泼,可直接与NH3吸附物种进行SCR反应,吸附态NO2也被认为是发生快速SCR反应的关键物种。尽管桥式硝酸盐也能够部分被活性氧氧化为NO2参与反应,但其同双齿硝酸盐一样具有较好的热稳定性。事实上,硝酸盐(特别是双齿及桥式硝酸盐)的脱附温度可用来表征催化剂性能的优劣。高温下仍稳定存在且占据反应活性位的硝酸盐类物种可导致SCR活性的下降。

图2 NO在催化剂上常见的吸附形态
不同硝酸盐物种间会互相转化,如NH3可能会促进双齿和桥式硝酸盐变为单齿硝酸盐,同时伴随NH2物种的生成,最终单齿硝酸盐和NH2作为主要活性物种完成SCR反应。此过程主要与催化剂活性组分相关[19]。硝酸盐物种也会和NO发生可逆反应,生成亚硝酸盐和NO2,可促进中低温反应的进行[21]。反应体系中的O2也能够促进NO的吸附和转化,以及氧化亚硝基类物种[38],富氧体系中单齿硝酸盐及双齿硝酸盐的生成会有所强化。除这些组分外,活性中间体和副产物的生消也不容忽视,中间体的种类一定程度上可表征催化剂对NO的活化能力,而副产物则可推导SCR反应的微观过程。如副产物N2O可来源于吸附态NO的分解、NH3的深度脱氢及中间产物NH2NO的两步脱氢等过程,结合体系中的其他组分可进一步窥探反应机理。此外,某些体系中NO的弱吸附相或气相也可作为SCR的关键反应组分[9]。
调节NO吸附位点的方式多样且有效。FRANCE等[39-41]分别将Ce、W、Ti作为助剂引入到铁基催化剂中,调节了NO吸附位点和化学吸附表面氧的比例,从而有效促进了快速SCR反应的进行。有研究表明,P的添加亦可促进亚硝酸盐和NO2间的转化[42]。此外,金属掺杂能够提升SCR性能的原因还在于其抑制了惰性硝酸盐的生成过程[3]。有研究表明,将Fe掺杂到锰基催化剂后,Mn4+/Mn3+和Fe3+/Fe2+的占比会影响催化剂的电子转移速率和方向,它们分别对硝酸盐的生成速率和类型起重要作用;在Fe和Mn离子的协同作用下,单齿硝酸盐更易生成,双齿硝酸盐的生成受到抑制,从而提升了SCR性能[1]。ZHANG等[16]则关注了硫酸改性的铈基介孔材料催化剂上硝酸盐的生消过程,发现通过平衡催化剂表面的碱性物种,减少电子向吸附态NO2的流动,从而抑制硝酸盐的生成。此外,利用原位DRIFTS来表征催化剂的失活过程也精确明晰。如ZHANG等[30]通过原位DRIFTS发现,当Mn/Ti催化剂无助剂修饰时,SO2与NO、NH3间的竞争吸附导致了活性位点的锐减;而将Ho元素引入体系后,SO2对NO的竞争吸附变小,对NH3的吸附和活化几乎无影响,这使得催化剂的性能大幅提升。GAO等[20]的研究也同样证实,用Ni/Co修饰锰基催化剂可以调控SO2和NO的竞争吸附,促进更多单齿硝酸盐的生成,以诱导反应正向进行。
3 SCR反应的路径及机理
基于原位DRIFTS对反应中间体和产物等的观测和分析,SCR反应路径及机理已有大量成熟研究,并已做出多种假说和论证,总体而言可分为两类,即E-R机理和L-H机理。E-R机理:NH3先吸附于催化剂表面的L酸位上形成吸附相氨基,再与气相或弱吸附相NO作用生成活性中间体,最后裂解为N2和H2O,该机制发生的要素在于L酸性位上吸附的NH3结合了催化剂表面的氧元素,促进了中间产物氨基的生成。L-H机理:NH3和NO同时吸附于催化剂表面,两者分别以NH4+和硝酸盐物种或NO2的吸附态形式结合生成不稳定中间体,继而裂解为最终产物。两类反应均发生在催化剂表面。图3以Ti-Fe基催化剂为例构建了两类机理的反应路径[43]。通常,当体系在中低温段时反应以L-H机理为主导,当体系在中高温段时反应以E-R机理为主导,反应以何种机理为主导主要取决于某温度下催化剂是否能够对NO形成吸附和活化。
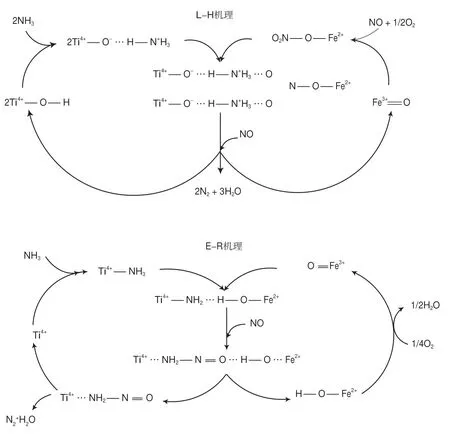
图3 SCR反应的两类机理示意(以Ti-Fe基催化剂为例)
前言中提到当反应体系中有过量O2或NO2时,体系会发生快速SCR反应[2]。图4以V-Ti基催化剂为例,详析了标准和快速SCR反应的异同[43]。如图4所示,两类反应的还原部分是一致的,即NH3和NO先后吸附到催化剂表面并形成NH2NO中间体,但在再氧化的过程中,标准SCR反应为NO和O2分别吸附至催化剂表面生成NO2,快速SCR反应则直接吸附NO2进行SCR再氧化。H2O的脱附、NO的氧化分别是标准SCR反应和快速SCR反应的速率决定步骤。于快速SCR反应而言,原位DRIFTS还只能观察到催化剂表面硝酸盐物种的迁移转化,难以捕捉到中间物种及NO2的变化。
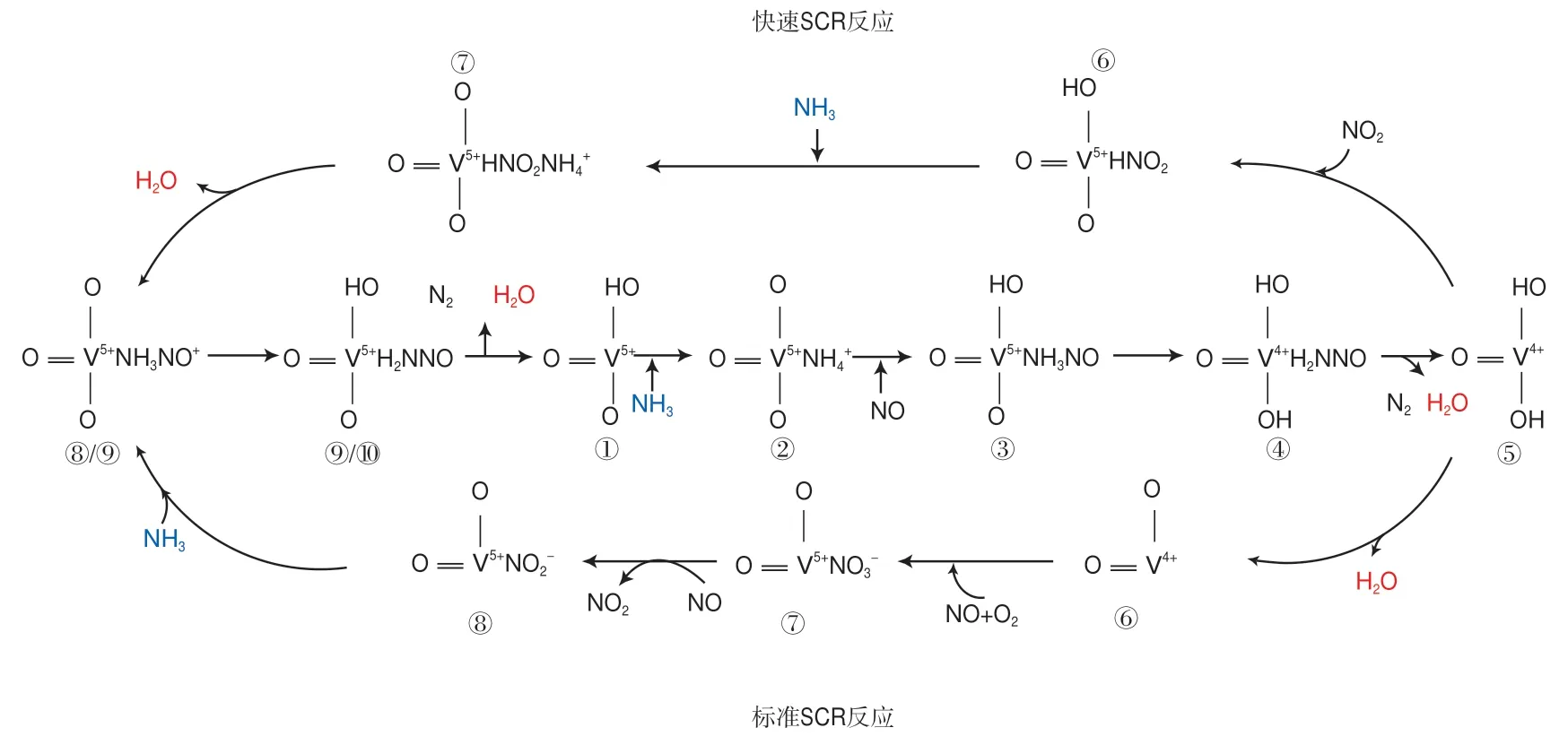
图4 标准和快速SCR反应的机理示意(以V-Ti基催化剂为例)
对于4类SCR过渡金属催化剂而言,催化过程整体上皆遵循L-H或E-R机理的反应路径,但体系中的酸位吸附、气体活化、电子转移、中间体生消、副产物形成等过程千差万别。以钒基催化剂来说,多项研究表明其在中高温下遵循E-R机理;但也有研究认为,NH3首先吸附于V5+—OH的B酸位上,活化于V5+=O键上,形成活化氨分子,与NO结合后分解为N2和H2O,正如图4还原部分所示,该过程遵循L-H机理[43]。对于铁基氧化剂而言,中高温的SCR机理是研究焦点,低温催化机理仅有少量报道。LIU等[9]和YANG等[12]均发现,对于Fe-Ti基催化剂体系:当温度低于200 ℃时,SCR反应服从L-H机理,NO被Fe3+催化氧化形成的单齿硝酸盐吸附于催化剂表面,这是反应速率决定步骤;当温度高于300 ℃时,反应服从E-R机理,NH3被Fe3+催化失氢,与被活化的NO结合形成NH2NO,这是反应速率决定步骤。有Mn掺杂的低温铁基催化剂亦服从L-H机理,NH4+可与桥式和单齿硝酸盐物种结合形成NH4NO3,NO还原NH4NO3是反应速率决定步骤[5]。对于锰基催化剂,一般认为,低温下吸附态NO被Mn4+氧化形成单齿硝酸盐Mn3+-ONO,与NH3结合后经脱水、氧化还原生成N2,添加助剂可加速氧化还原过程;但ZHANG等[44]的研究表明,低温MnZrTi体系中氧为反应气体吸附活化和元素间电子转移的重要媒介,NH3则与双齿硝酸盐和单齿硝酸盐发生SCR反应。另外也有研究表明,铈基催化剂与锰基催化剂一致,在低于200 ℃时E-R和L-H机理可同时存在。目前,锰基催化剂的低温SCR机理尚不完全明确,还有待进一步的探究与归纳。
基于原位DRIFTS对反应位点的表征和分析可帮助研究者在微观层面明确影响SCR催化剂活性和寿命的原因。如WO3的掺杂可显著增加钒基催化剂的B酸位[7];Cu的掺杂可增加催化剂的活性氧物种和L酸位[6];F的掺杂则可取代钒基催化剂表面的部分晶格氧,大幅促进低温下对NO的吸附与活化[45]。金属元素掺杂还能够调控硝酸盐物种的生成与解吸,如Ce的掺杂会加速过渡金属元素的氧化还原循环,进而产生更多的NO2和单齿硝酸盐物种。XIN等[46]则将Mo原子掺杂到Fe2O3晶格中,观测到L酸位的增多和低温活性的显著提高。曹政等[47]将Sb掺杂至钒基催化剂中促进了惰性副产物硫酸铵盐的分解和解析。总体而言,研究者着眼于调节催化剂的酸位点和氧化还原循环过程,将催化剂制备和原位DRIFS的研究结合起来形成构效关系,力求避免副反应的发生,以达到优化SCR催化剂性能的目的。
4 结语
原位DRIFTS技术应用于SCR反应机理的研究已日趋成熟,应用价值和潜能巨大。基于原位DRIFTS技术可遴选出影响催化剂SCR活性的要素,这些要素包括体系中NH3和NO在催化剂上的吸附方式、物种间的活化转化、中间体及(副)产物的生消过程等,这对针对性合成具有特殊结构和形貌的高活性催化剂具有重要指导作用。基于此,对原位DRIFTS的应用前景做如下展望。
a)采用如CO、CH4等作为SCR反应还原类气体是研究方向之一,这些气体在高抗硫性、宽活性温度范围等方面引人关注,但同时也存在极易与O2反应造成脱硝性能下降等较大缺陷,而基于原位DRIFTS在此方面的研究仍不充分。原位DRIFTS可靶定该类反应过程中的活性位点,掌握吸附物种的性质及影响因素,对其调控或抑制,以促进SCR反应的高效进行。
b)将原位DRIFTS与其他技术联用或互证,进一步量化SCR反应,发掘其本质特性。这包括对反应动力学、反应能、过渡态及活化能的模拟计算,对催化剂微观结构和电子配位环境的精准表征,对反应物种进行同位素标定等。不同技术间既相互联系,也彼此印证。
c)反应活性中间体的捕捉和定性是窥探SCR反应机理的关键一环,而原位DRIFTS在此方面的性能还有待突破,构建更稳定细密的实验系统、开发更卓越高效的采集系统是未来该领域的着力点。研究需着眼于观测更多的基元反应,确定氧化还原循环的活性中心,从机理层面明确H2O及SO2使催化剂失活的原因。
