基于席夫碱的四种Zn2+荧光探针的合成及其性能
2023-10-19邓绍文李中燕
何 薇 龚 兰 邓绍文 李中燕 袁 霖
(湖南科技学院化学与生物工程学院,永州 425199)
0 引 言
锌离子具有良好的配位能力,广泛存在于人体细胞和体液中,是人体必需的微量元素之一,在人体内的含量仅次于铁。Zn2+在基因表达、机体免疫和神经传输等新陈代谢活动中发挥着重要作用[1-3]。人体内Zn2+代谢紊乱,往往会导致酶活性失调、基因表达错误、细胞凋亡、神经传递受阻等生理紊乱现象,Zn2+浓度过低会引起消化不良、食欲不振,而Zn2+浓度过高则会导致一些毒性症状和神经退行性疾病,如帕金森病、癫痫等[4-6]。因此,Zn2+的识别、检测对人体疾病的诊断与环境中Zn2+污染的监测具有重要意义。
目前,与大多数传统分析方法相比,荧光探针法具有灵敏度高、选择性好、作用迅速、操作简单、可实时监测等诸多优点,因此在分析化学、生物化学和医药科学等多个领域里得到普遍应用[7-13]。目前报道的大多数Zn2+荧光探针的分子量一般较大,合成步骤多,结构相对复杂,有的探针水溶性较差,这些因素限制了荧光探针的实际应用范围[14-17]。因此通过简单的反应制备出水溶性好的小分子Zn2+荧光探针仍然具有重要意义。此外,席夫碱型荧光探针由于其合成条件温和且具有良好的配位能力而得到化学工作者的广泛关注[18-19]。
我们以乙二胺与水杨醛及其衍生物为原料设计合成了4 种新型的席夫碱荧光探针L1~L4(Scheme 1),并通过光谱实验研究了探针对Zn2+的选择性识别、检测。
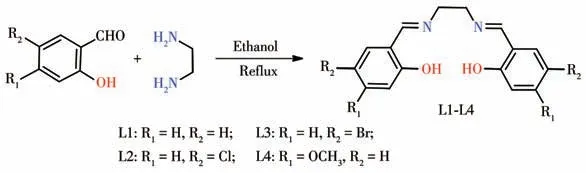
Scheme 1 Synthesis of probes L1-L4
1 实验部分
1.1 仪器与试剂
主要仪器有AVANCE ⅢHD 400 MHz核磁共振波谱仪(德国Bruker公司)、AVATAR-360傅里叶变换红外光谱仪(美国Niconet 公司)、RF-6000 荧光分光光度计(日本岛津公司)、UPH-III-10TN 超纯水机(四川优普超纯科技有限公司)。
水杨醛、取代水杨醛、乙二胺、乙醇及所用金属离子的相应盐酸盐或硝酸盐,均为分析纯,购于上海泰坦科技股份有限公司。实验用水为超纯水。
1.2 探针L1~L4及配合物L2-Zn2+的合成及表征
探针的制备如Scheme 1 所示。称取水杨醛或取代水杨醛(2 mmol)、乙二胺(60 mg,1 mmol),加入到15 mL 无水乙醇中,然后加热回流2 h 左右,用薄层色谱法(TLC)监测反应进程,反应期间会产生大量固体。反应完全后,旋蒸除去溶剂,加入少量冰乙醇洗涤,抽滤,烘干,即可得到目标产物。
将探针L2(169 mg,0.5 mmol)和醋酸锌(183 mg,1 mmol)加入到乙醇(20 mL)中,加热回流2 h,然后冷却至室温,静置5 d 左右析出淡黄色晶体,即配合物L2-Zn2+。
L1:淡黄色固体,产率88%。1H NMR(CDCl3,400 MHz):δ13.153(s,2H),8.257(s,2H),7.205(t,J=15.588 Hz,2H),7.143(d,J=9.113 Hz,2H),6.867(d,J=8.279 Hz,2H),6.769(t,J=14.921 Hz,2H),3.833(s,4H)。13C NMR(CDCl3,101 Hz):δ165.444,159.921,131.342,130.443,117.637,117.559,115.882,58.672。FTIR(KBr,cm-1):3 444,2 905,1 634,1 483,1 277,1 034,827,706。元素分析按C16H16N2O2的计算值(%):C 71.62,H 6.01,N 10.44。实验值(%):C 71.23,H 5.83,N 10.23。HRMS(m/z):计算值269.129 0 [M+H]+;实验值269.127 3。
L2:淡黄色固体,产率92%。1H NMR(CDCl3,400MHz):δ13.060(s,2H),8.220(s,2H),7.157~7.190(m,2H),7.134(d,J=2.499 Hz,2H),6.833(d,J=8.766 Hz,2H),3.882(s,4H)。13C NMR(CDCl3,101 MHz):δ164.385,158.508,131.319,129.539,122.280,118.228,117.555,58.568。FTIR(KBr,cm-1):3 444,2 940,1 634,1 483,1 277,1 034,706,644。元素分析按C16H14Cl2N2O2的计算值(%):C 56.99,H 4.19,N 8.31;实验值(%):C 56.70,H 4.01,N 8.14。HRMS(m/z):计算值337.051 1[M+H]+;实验值337.049 1。
L3:淡黄色固体,产率93%。1H NMR(CDCl3,400MHz):δ13.059(s,2H),8.225(s,2H),7.159~7.191(m,4H),7.137(d,J=2.320 Hz,2H),6.833(d,J=8.762 Hz,2H),3.887(s,4H)。13C NMR(CDCl3,101 MHz):δ164.295,158.990,134.129,132.526,118.854,118.012,109.156,58.562。FTIR(KBr,cm-1):3 426,2 933,1 634,1 474,1 276,1 127,1 033,826。元素分析按C16H14Br2N2O2的计算值(%):C 45.10,H 3.31,N 6.57;实验值(%):C 45.00,H 3.19,N 6.39。HRMS(m/z):计算值426.948 0[M+H]+;实验值426.946 1。
L4:淡黄色固体,产率89%。1H NMR(CDCl3,400MHz):δ13.780(s,2H),8.425(s,2H),7.273(d,J=8.570 Hz,2H),6.398(d,J=1.920 Hz,1H),6.376(d,J=1.869 Hz,1H),7.134(d,J=1.779 Hz,2H),3.824(s,4H),3.743(s,6H)。13C NMR(CDCl3,101 MHz):δ166.305,165.723,163.711,133.645,112.418,106.316,101.458,57.731,55.713;FTIR(KBr,cm-1):3 444,2 973,1 621,1 444,1 285,1 025,852,581。元素分析按C18H20N2O4的计算值(%):C 65.84,H 6.14,N 8.53;实验值(%):C 65.65,H 6.00,N 8.39。HRMS(m/z):计算值329.150 1[M+H]+;实验值329.149 0。
L2-Zn2+:淡黄色固体,产率90%,1H NMR(DMSOd6,400 MHz):δ8.42(s,2H),7.34(d,J=2.8 Hz,2H),7.21(dd,J=9.0,2.8 Hz,2H),6.58(d,J=9.0 Hz,2H),3.72(s,4H)。13C NMR(101 MHz,DMSO-d6):δ170.03,167.68,133.48,132.91,125.01,120.36,115.38,56.49,56.12,19.03。FTIR(KBr,cm-1):3 451,2 970,2 920,1 641,1 560,1 460,1 420,1 300,1 171,1 090,1 050,947,819,709。元素分析按C16H14Cl2N2O3Zn 的计算值(%):C 45.91,H 3.37,N 6.69;实验值(%):C 45.65,H 3.13,N 6.59。
1.3 光谱性质测试
将探针L1~L4 溶于乙醇制得探针储备液(2 mmol·L-1),配制金属离子(Na+、K+、Ag+、Ca2+、Ba2+、Co2+、Ni2+、Pb2+、Zn2+、Cu2+、Sn2+、Cd2+、Fe3+、Cr3+、Al3+)储备液(2 mmol·L-1)用于金属选择性的检测。将4-羟乙基哌嗪乙磺酸(Hepes)溶于超纯水中制备0.1 mg·mL-1的溶液,并用稀HCl 和NaOH 调节至pH=7.54,作为缓冲溶液。检测体系为EtOH-H2O(9∶1,V/V,pH=7.54)。
荧光滴定实验:移取20 μL探针储备液(2 mmol·L-1),加入适量的Zn2+缓冲溶液,然后加入乙醇定容至2 mL,荧光光谱测定条件为:λex=362 nm,λem=400~600 nm,激发/发射狭缝宽度为3 nm/3 nm。
1.4 单晶X射线衍射
选取尺寸为0.42 mm×0.36 mm×0.32 mm 的配合物L2-Zn2+的晶体置于玻璃毛细管上,使用Bruker SMART APEX ⅡCCD衍射仪,在室温下以石墨单色化的MoKα辐射(λ=0.071 073 nm)和φ-ω扫描技术在一定θ范围内收集晶体的强度数据。原始数据经集成到SHELX 程序并用SAINT 程序校正,全部数据经Lp 因子和多重扫描吸收校正后,使用Olex2 软件和SHELXS程序解出晶体分子结构,用SHELXL程序[20]对全部非氢原子坐标及其各向异性热参数进行全矩阵最小二乘法精修至收敛。氢原子均为理论加氢并在结构精修中确定氢原子的位置和热参数。相应的晶体学数据见表1,部分键长和键角见表2。
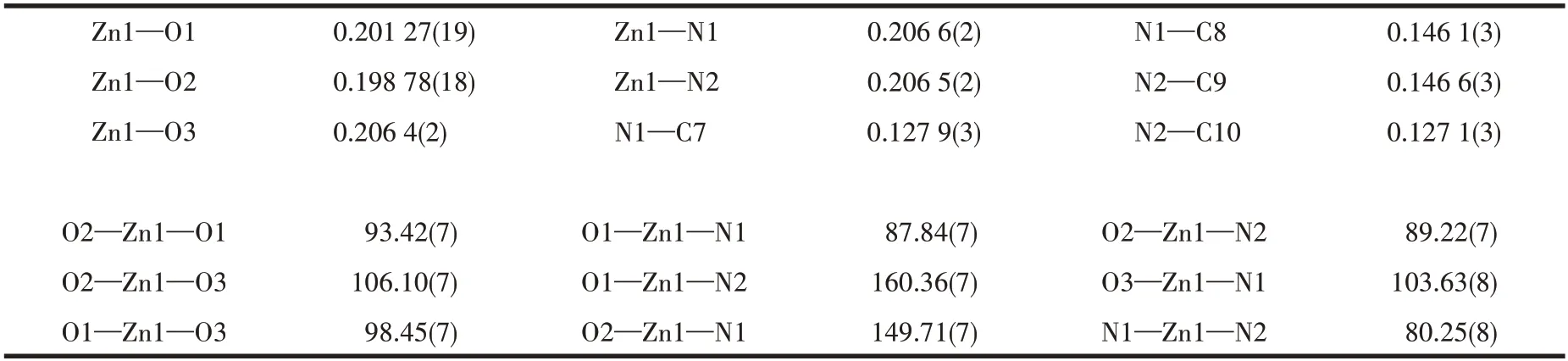
表2 配合物L2-Zn2+的部分键长与键角Table 2 Selected bond lengths(nm)and bond angles(°)of complex L2-Zn2+
CCDC:2247372。
2 结果与讨论
2.1 探针L2与L2+Zn2+的UV-Vis吸收光谱
探针L2分子中C=N键中的N原子和酚羟基中的O 原子容易与Zn2+结合,使得分子刚性增强,从而引起探针L2 光谱性质的变化。在EtOH-H2O(9∶1,V/V,pH=7.54)中对L2 的UV-Vis 光谱性质进行了研究,如图1所示。加入等量的Zn2+后,L2在332 nm处产生了一个新的吸收峰,说明L2 与Zn2+发生了配位。
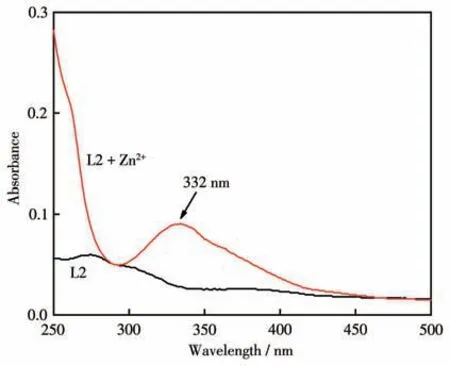
图1 L2与L2+Zn2+的UV-Vis吸收光谱Fig.1 UV-Vis absorption spectra of L2 and L2+Zn2+
2.2 探针与Zn2+的荧光光谱
考察了探针L1~L4对Zn2+的荧光响应性,如图2所示。结果表明,探针本身几乎没有荧光,随着Zn2+的加入,4 种探针的荧光强度显著增强,这可能是探针与Zn2+的螯合使得探针分子中C=N 的异构化受阻,同时增加了分子的刚性,产生了螯合型荧光增强的效果,据此可对Zn2+进行识别检测。其中探针L2 的荧光强度最强,发出亮蓝色荧光(图2 插图),因此选择L2为代表研究探针对Zn2+的识别性能。
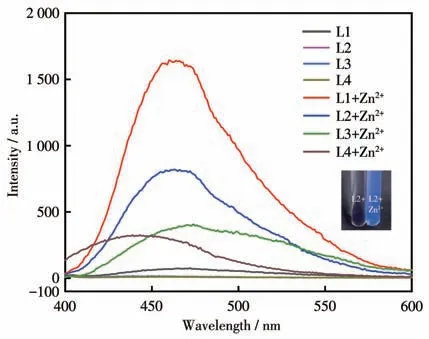
图2 L1~L4对Zn2+的荧光响应Fig.2 Fluorescence response of L1~L4 to Zn2+
2.3 探针L2与Zn2+的荧光滴定实验
如图3所示,随着Zn2+的加入,探针L2在464 nm处的荧光强度显著增强。荧光滴定实验(图3和4)表明,在0~30 μmol·L-1范围内,随着加入的Zn2+浓度的升高,体系的荧光强度不断增强,而且体系的荧光强度与Zn2+的浓度在0~30 μmol·L-1范围内具有良好的线性关系,相关系数为0.993 76,检出限为92.15 nmol·L-1,远低于国标GB5749-2006《生活饮用水卫生标准》[20]规定的饮水中Zn2+含量的限量值1.0 mg·L-1(约15 μmol·L-1)。实验数据表明探针L2 可以对Zn2+进行高效地识别、检测。同时,根据荧光滴定结果,如图5 所示,利用Benesi-Hildebrand 方程计算得出探针L2与Zn2+的结合常数为2.66×104L·mol-1。
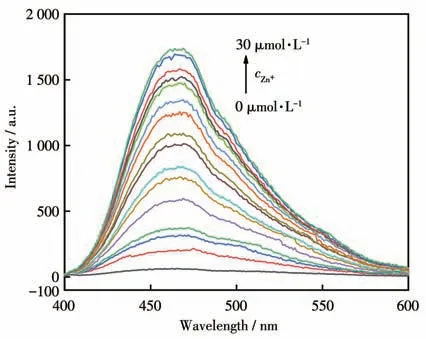
图3 不同浓度Zn2+存在时L2的荧光光谱Fig.3 Fluorescence spectra of L2 in the presence of Zn2+with different concentrations
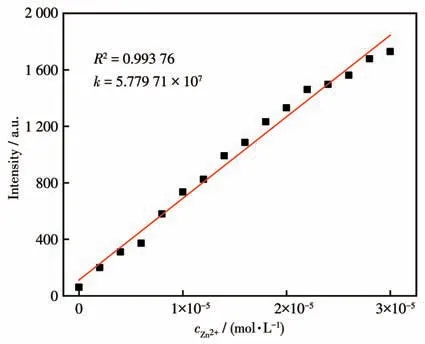
图4 Zn2+浓度与L2荧光强度的线性关系Fig.4 Linear relationship between the concentration of Zn2+and the fluorescence intensity of L2
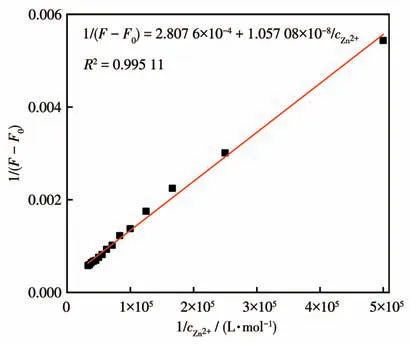
图5 L2与Zn2+的荧光滴定数据的Benesi-Hildebrand图Fig.5 Benesi-Hildebrand plot from fluorescence titration data of L2 with Zn2+
2.4 探针L2识别Zn2+的响应时间
用荧光光谱法研究探针L2 识别Zn2+的响应时间,结果如图6所示。前59 s是探针L2溶液,溶液无荧光变化。在59 s 时加入Zn2+溶液,体系的荧光强度迅速增强,在6 s 内荧光几乎达到最强且基本稳定。这表明L2可以作为Zn2+的快速识别荧光探针。
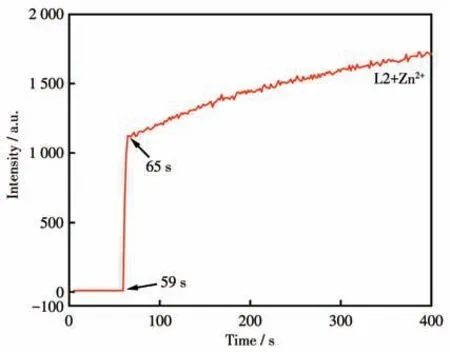
图6 L2加入Zn2+后在464 nm处荧光强度随时间的变化Fig.6 Change of fluorescence intensity at 464 nm of L2 with time after adding Zn2+
2.5 pH值对荧光光谱的影响
溶液的pH 值对探针L2 及L2+Zn2+的荧光光谱的影响结果如图7 所示,探针L2 本身的荧光强度非常弱,而且在5.5~8.5 的pH 范围内,探针L2 的荧光强度几乎没有变化。但是pH 对L2+Zn2+体系的荧光强度影响比较明显,在pH=6.7~8.0 时体系荧光强度较大且基本不受溶液酸碱度的影响,当pH<6.7 或pH>8.0 时荧光强度会迅速下降。这可能是由于体系酸性增强时会引起C=N 基团的分解,降低识别基团的有效浓度,而碱性增强时会导致体系中的Zn2+形成Zn(OH)2,降低体系中游离Zn2+的浓度,二者都不利于探针L2 与Zn2+的结合,均会导致体系荧光强度的降低。L2+Zn2+体系在pH=7.54 时荧光强度最强,故选择7.54为测试的最佳pH值。
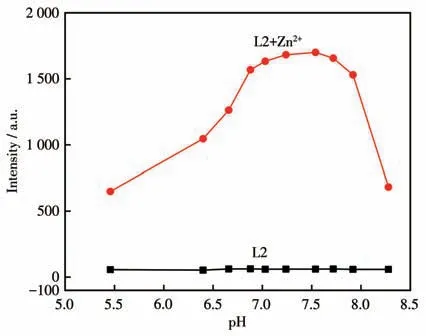
图7 pH对L2和L2+Zn2+体系荧光强度的影响Fig.7 Effect of pH on the fluorescence intensities of L2 and L2+Zn2+system
2.6 离子选择性和抗干扰性
考察了采用探针L2 检测Zn2+的选择性。如图8所示,在含有10 μmol·L-1探针L2 的EtOH-H2O(9∶1,V/V,pH=7.54) 体系中分别加入20 μmol·L-1的Na+、K+、Ag+、Ca2+、Ba2+、Co2+、Ni2+、Pb2+、Zn2+、Cu2+、Sn2+、Cd2+、Fe3+、Cr3+和Al3+,只有Zn2+能使探针L2的荧光强度显著增强,表明探针对Zn2+有特异性响应。进一步考察了共存离子的影响,除了Cu2+和Co2+,其它离子对体系荧光强度的影响不明显,这表明探针L2在上述共存离子存在下可以有效地选择性识别和检测Zn2+。在实际测试中可以加入Cu2+和Co2+掩蔽剂再进行离子检测。
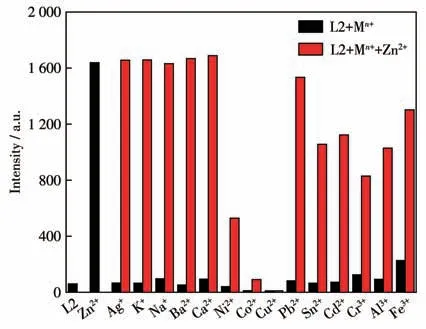
图8 L2(10 μmol·L-1)对金属离子(20 μmol·L-1)的选择性以及Zn2+ (20 μmol·L-1)与其它金属离子(20 μmol·L-1)共存时,L2在464 nm处的荧光强度Fig.8 Selectivity of L2 for metal ions and the fluorescence intensity of L2 at 464 nm when Zn2+coexists with other metal ions
2.7 探针L2与Zn2+的结合模式
为了探究探针L2 与Zn2+的结合模式,我们首先利用等物质的量连续变换法测定了L2 与Zn2+的Job曲线,结果如图9所示,可以推测探针L2与Zn2+的结合比为1∶1。
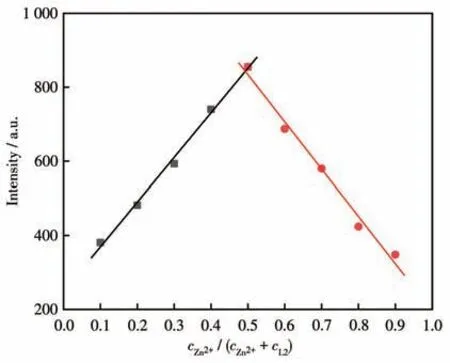
图9 探针L2与Zn2+相互作用的Job曲线Fig.9 Job′s plot for interaction between L2 and Zn2+
核磁滴定结果也验证了这一推测。在L2(0.3 mmol)的DMSO-d6溶液里加入0.15 mmol 和0.3 mmol的醋酸锌,测定其1H NMR谱的变化,结果如图10所示。从图10 中可以看出,随着Zn2+的加入,L2 上酚羟基的质子峰(H1)逐渐消失,发生去质子化,亚胺的质子峰(H2)、苯环上的质子峰(H3、H4、H5)均向高场发生移动,这说明探针分子中的N 原子和O 原子均与Zn2+发生了配位。当加入与L2 等量的Zn2+时,H1完全消失,H2~H5 完全移向高场,说明L2 与Zn2+的结合比为1∶1。
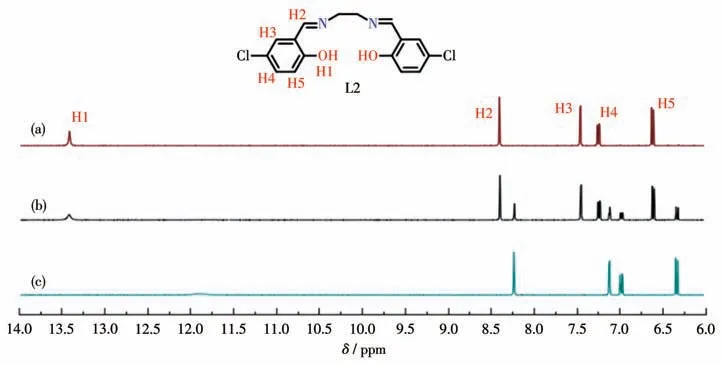
图10 (a)L2、(b)L2(0.3 mmol)+Zn2+(0.15 mmol)、(c)L2(0.3 mmol)+Zn2+(0.3 mmol)的1H NMR谱图Fig.101H NMR spectra of(a)L2,(b)L2(0.3 mmol)+Zn2+(0.15 mmol),(c)L2(0.3 mmol)+Zn2+(0.3 mmol)
同时,我们培养了配合物L2-Zn2+的晶体,分子结构如图11 所示。L2-Zn2+的晶体结构表明Zn2+通过探针L2 的N 原子与O 原子、以及一个水分子的O原子形成了金属配合物。原子O1、C1、C6、N1 和相邻苯环几乎在一个平面上,命名为P1,原子N2、C10、C11、C12、O2 和相邻苯环也几乎在一个平面上,命名为P2,P1 和P2 的二面角为6.999(4)°。Zn2+与相连的N 和O 原子呈变形四方锥体。同时,分子结构表明探针L2 中的酚羟基发生了去质子化,L2与Zn2+的配位比为1∶1,这与等物质的量连续变换法与核磁滴定实验的推测结果一致。
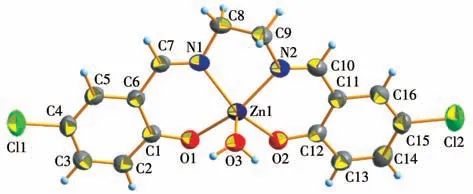
图11 L2-Zn2+的50%概率晶体结构椭球图Fig.11 Crystal structure of L2-Zn2+shown as ellipsoids with 50%probability
此外,我们还利用Gaussian16 B3LYP/6-31G(d,p)计算了L2 和L2-Zn2+的能量优化轨道[21](图12)。结果表明,L2-Zn2+配合物的HOMO 和LUMO 的能量差为3.74 eV,低于L2 的HOMO 和LUMO 的能量差(4.31 eV),说明探针分子L2与Zn2+发生了配位。
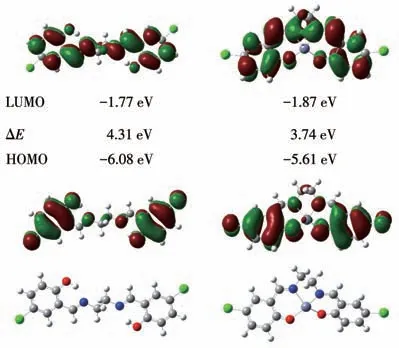
图12 探针L2和配合物L2-Zn2+的优化结构和HOMO/LUMO能量Fig.12 Optimized structures and HOMO/LUMO energies of probe L2 and complex L2-Zn2+
根据上述实验结果,我们推测L2 对Zn2+可能的识别机理如Scheme 2 所示。L2 中存在C=N 双键异构化,同时苯酚上的—OH 基团和相邻的—CH=N—组合在一起,两者导致了激发态分子内质子转移(excited-state intramolecular proton transfer,ESIPT)过程,加剧了激发态下的非辐射跃迁,使探针L2 本身几乎没有荧光。加入Zn2+后,探针L2 识别基团的空腔与Zn2+刚好匹配,L2 与Zn2+发生配位,阻止了探针分子中C=N 的异构化,同时增加了分子的刚性,产生了螯合型荧光增强(chelation-enhanced fluorescence,CHEF)的效果;另外,L2 与Zn2+配位后,ESIPT过程被抑制,产生荧光响应[22]。
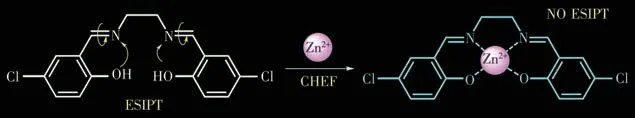
Scheme 2 Fluorescence enhancement mechanism for L2 to recognize Zn2+
2.8 水样中Zn2+的检测
运用本文中的实验方法检测了自来水和湘江河水中的Zn2+,结果见表3。2 种实际水样中Zn2+的加标回收率分别为100.4%~102.7% 和101.0%~103.3%,相对标准偏差(RSD)分别为1.20%~1.68%和1.56%~2.52%,说明L2 在实际水样中识别检测Zn2+的准确度高,具有良好的应用前景。
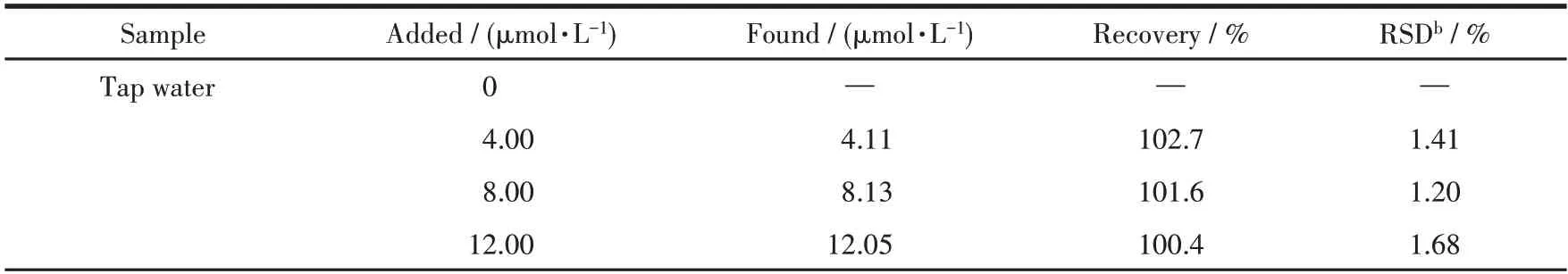
表3 自来水和河水中的Zn2+的检测Table 3 Determination of Zn2+in tap water and river water samples
3 结 论
以乙二胺与水杨醛及其衍生物为原料,通过简单的反应合成了4 种新型的席夫碱类荧光探针L1~L4,其中探针L2 对Zn2+表现出出色的选择性和灵敏度。在365 nm 紫外灯下,探针L2与Zn2+可形成配合物,引起体系荧光增强,发出明亮的蓝色荧光,因此,探针L2 可以实现可视化检测Zn2+,其检出限为92.15 nmol·L-1。探针L2 对Zn2+检测的机理为CHEF 效应和ESIPT 效应。通过Job 曲线、核磁滴定实验、DFT 理论计算和单晶结构研究发现,探针L2与Zn2+形成了1∶1 的配合物,探针L2 中的亚胺中的N 原子与酚羟基中的氧原子参与了L2 与Zn2+的配位。此外,水样中Zn2+的检测实验表明该探针在检测实际水样中的Zn2+浓度具有潜在的应用价值。
