车前子及其炮制品色度值、UPLC指纹图谱及体外抗氧化活性的差异研究
2023-10-19程钰洁邱彩月洪婉敏卢彭信汪凯东张志鹏
程钰洁,邱彩月,洪婉敏,卢彭信,汪凯东,徐 杰,张志鹏
车前子及其炮制品色度值、UPLC指纹图谱及体外抗氧化活性的差异研究
程钰洁,邱彩月,洪婉敏,卢彭信,汪凯东,徐 杰,张志鹏*
广东一方制药有限公司,广东省中药配方颗粒企业重点实验室,广东 佛山 528244
分析车前子及其不同炮制品的指纹图谱、色度值及抗氧化活性的差异,探讨其化学成分与抗氧化作用的谱效关系。采用分光测色仪测定色度值,采用UPLC法建立车前子及其不同炮制品指纹图谱,采用ABTS法测定抗氧化活性,结合相似度评价、方差分析、主成分分析(principal component analysis,PCA)、层次聚类分析(hierarchical cluster analysis,HCA)、正交偏最小二乘-判别分析(orthogonal partial least squares-discriminant analysis,OPLS-DA)等多元统计方法分析车前子及其炮制品的差异;运用偏最小二乘回归法(partial least squares regression method,PLSR)和灰色关联度分析法(grey relation analysis,GRA)分析车前子及其不同炮制品化学成分与抗氧化活性的谱效关系。建立的车前子UPLC指纹图谱标定了19个共有峰,炒车前子和盐车前子标定了27个共有峰,合计标定了34个色谱峰,并对其中13个色谱峰进行了指认。多元统计分析表明,车前子与不同炮制品间存在显著差异,PCA与HCA可将车前子生品与炮制品分为2类,OPLS-DA筛选出10个差异性标志成分。车前子炮制前后的粉末色度值Δ*>6,可被肉眼识别,但不同炮制品间粉末颜色差异不明显。抗氧化活性结果表明,车前子炮制后抗氧化作用增强,不同炮制品间差异不大。相关性分析表明,共有峰的峰面积值对色度值有一定影响,对*值的影响较小,对*值、*值影响较大;PLSR与GRA分析表明,有11个共有峰表征的化学成分与车前子及其炮制品的抗氧化活性关联较大,其中包括原儿茶酸、木通苯乙醇苷B与野漆树苷。建立的UPLC指纹图谱及色度值、抗氧化活性的测定方法,可用于车前子及其不同炮制品的鉴别及质量分析,指纹图谱-体外抗氧化活性的谱效关系研究,可为车前子炮制机制的研究提供参考。
车前子;炮制;UPLC;指纹图谱;色度值;抗氧化活性;谱效关系;ABTS法;主成分分析;层次聚类分析;正交偏最小二乘-判别分析;灰色关联度分析法;异毛蕊花糖苷;车前草苷D;野漆树苷;京尼平苷酸
车前子是车前科车前属植物车前L.或平车前Willd.的干燥成熟种子,始载于《神农本草经》,具有清热利尿通淋、渗湿止泻、明目、祛痰的功效,临床用于治疗热淋涩痛、水肿胀满、暑湿泄泻、目赤肿痛、痰热咳嗽[1]。车前子包含的主要化学成分有多糖、黄酮类、苯乙醇苷类、生物碱类、环烯醚萜类、三萜类等[2-3]。现代药理研究表明,车前子具有利尿、抗氧化、降尿酸、降血糖、调血脂、降血压及抗肝损伤等多种作用,临床应用十分广泛,可用于湿热引起的诸多疾病,如肝炎、肾病、便秘、高尿酸血症、高血压等病症的治疗[4-9]。
车前子的现代炮制方法主要有净制、炒制和盐制[10]。车前子生品性微寒,长于利尿通淋,炮制后寒性减弱,其中炒车前子善于祛痰止咳,盐车前子善于渗湿止泻。中药发挥药效作用的基础是多种有效成分的合理、有机的组合,其模式是多途径作用于机体内与疾病相关的多靶点,发挥对机体的整体调节作用[11]。因此,车前子生品与炮制品的功效不同,可理解为内在化学成分存在差异。目前,关于车前子及其炮制品的研究,多集中于炮制工艺及京尼平苷酸、毛蕊花糖苷等成分的含量测定上,多以单个或多个指标分析车前子炮制前后的差异,不足以作为全面地反映车前子炮制前后差异的主要变量指标[10]。
颜色性状作为中药饮片质量的外在体现,是中药鉴别与质量评价的关键指标之一,采用色度值量化饮片粉末颜色,在中药炮制领域已有较为广泛的应用[12-14]。因此,本研究拟通过UPLC法建立车前子及其不同炮制品的UPLC指纹图谱,结合化学计量学模式识别对三者化学成分进行系统的分析;通过采集饮片粉末的色度值,分析车前子炮制前后饮片粉末的颜色变化;同时测定车前子及其不同炮制品的体外抗氧化活性,进一步分析车前子及其炮制品的药效差异;利用偏最小二乘回归法(partial least squares regression method,PLSR)及灰色关联度法(grey relation analysis,GRA)分析UPLC指纹图谱共有峰与抗氧化活性的谱-效关系,以期为车前子的炮制机制研究提供参考。
1 仪器与材料
1.1 仪器
Waters Acquity型超高效液相色谱系统,美国沃特世公司;Thermo ICAPQ型电感耦合等离子体质谱仪,美国赛默飞公司;ME204E型万分之一天平、XP26型百万分之一天平,瑞士梅特勒-托利多公司;KQ-700DE型数控超声清洗器,昆山市超声仪器有限公司;HWS28型电热恒温水浴锅,上海一恒科技有限公司;111B型二两装高速中药粉碎机,浙江瑞安市永历制药机械有限公司;H22-X3型电陶炉,杭州九阳生活电器有限公司;TS7700型分光测色仪,深圳市三恩时科技有限公司;UV-2600型紫外分光光度计,日本岛津公司;Milli-QDirect超纯水系统,默克股份有限公司。
1.2 材料
对照品京尼平苷酸(批号11828-201805,质量分数98.1%)、阿魏酸(批号110773-201915,质量分数99.4%)、大车前苷(批号111914-202105,质量分数96.0%)、木犀草苷(批号111720-202111,质量分数96.6%)、毛蕊花糖苷(批号111530-201914,质量分数95.2%)、木犀草素(批号111520-202006,质量分数94.4%)、芹菜素(批号111901-202004,质量分数99.4%)、原儿茶酸(批号110809-201906,质量分数97.7%)、野漆树苷(批号111919-201804,质量分数95.5%)、木通苯乙醇苷B(批号111910- 201604,质量分数98.2%),中国食品药品检定研究院;对照品异毛蕊花糖苷,批号FF17B039,质量分数98%,成都普思生物科技有限公司;对照品车前草苷D,批号CFS202101,质量分数98.0%,Chem Faces公司;对照品芹菜素-7--葡萄糖醛酸苷,批号21062901,质量分数98.29%,成都普菲德生物科技有限公司。色谱级甲醇、乙腈,德国默克股份有限公司;色谱纯磷酸,天津市科密欧化学试剂有限公司;水为超纯水,取自实验室Milli-Q超纯水系统,其余试剂均为分析纯;ABTS自由基清除能力检测试剂盒,苏州格锐思生物科技有限公司。
12批车前子药材经广东一方制药有限公司孙冬梅主任中药师鉴定为车前科车前属植物车前L.的干燥成熟种子,12批炒车前子和12批盐车前子为广东一方制药有限公司实验室自制,按照《广东省中药饮片炮制规范》第一册[15]炒车前子炮制项下规定,取净车前子炒至略有爆声并有香气溢出时,取出摊凉,得到炒车前子,按照《中国药典》2020年版一部[1]盐车前子炮制项下规定,取净车前子照盐水炙法(通则0213)炒至起爆裂声时,喷洒盐水,炒干,取出摊凉,得到盐车前子。具体样品信息见表1及图1。
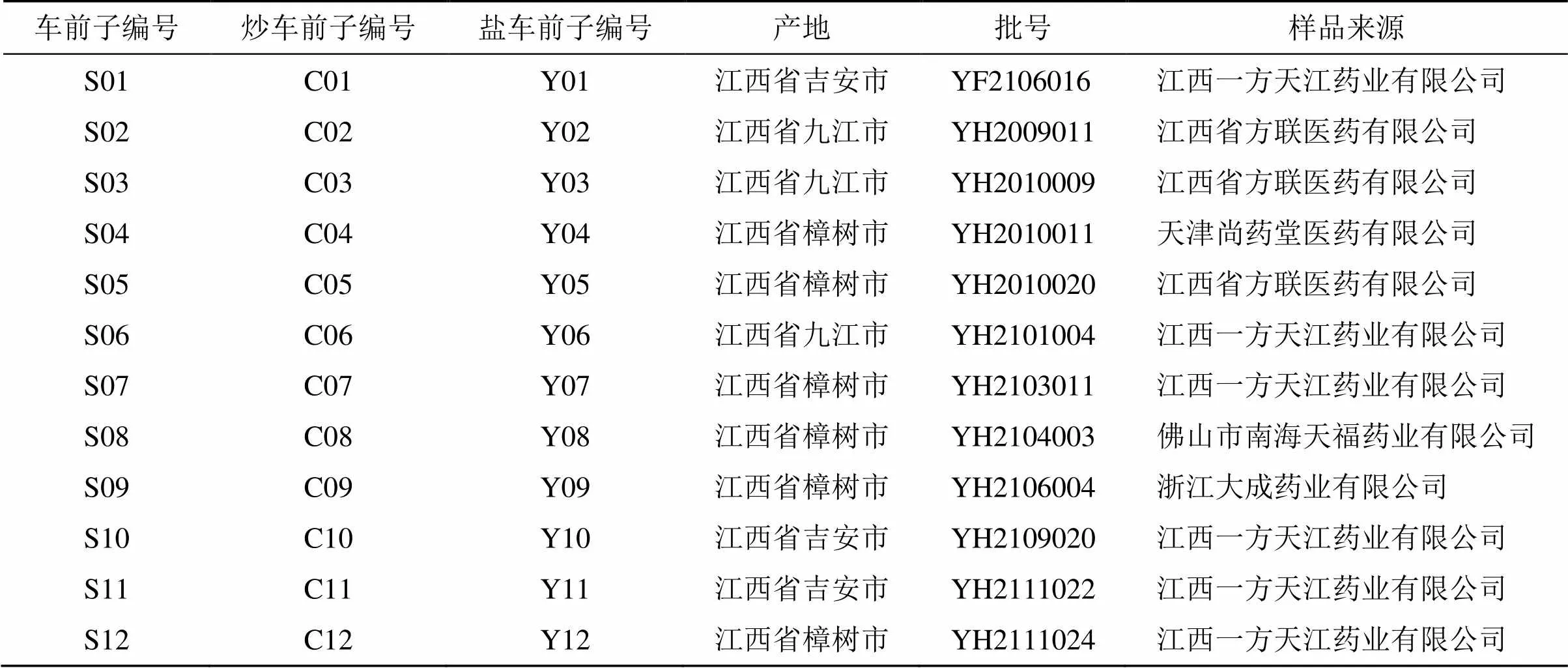
表1 样品来源信息
2 方法与结果
2.1 车前子及其不同炮制品色度值测定与分析
采用分光测色仪对车前子及其不同炮制品饮片粉末进行色度值测定。取12批车前子、炒车前子、盐车前子饮片粉末(过三号筛)适量,均匀平铺于玻片上,压制厚度约1 mm,采用国际照明委员会认可的D65光源,以白色作为背景,测定孔径8 mm,视角选择2度,经白板校正后,采集饮片粉末色彩图像,并测定色度值,平行3次,取平均值,结果见图2及表2。
Lab色彩模式中,L值为明度指数,*、*为色度指数,其中*为红绿轴,*为黄蓝轴,样品粉末颜色用总色度值(*)表示,公式为*=(*2+*2+*2)1/2。Δ*C-S=*C-*S、Δ*Y-S=*Y-*S、Δ*Y-C=*Y-*C、Δ*C-S=*C-*S、Δ*Y-S=*Y-*S、Δ*Y-C=*Y-*C、Δ*C-S=*C-*S、Δ*Y-S=*Y-*S、Δ*Y-C=*Y-*C、色差Δ*C-S=(Δ*C-S2+Δ*C-S2+Δ*C-S2)1/2、Δ*Y-S=(Δ*Y-S2+Δ*Y-S2+Δ*Y-S2)1/2、Δ*Y-C=(Δ*Y-C2+Δ*Y-C2+Δ*Y-C2)1/2,用于表达生品及不同炮制品在明度、红绿、黄蓝、总体的颜色变化情况,计算结果见表3。
当Δ*为6~12时,其色差可被肉眼识别,当Δ*>12时,色差显著[16]。由表3可知,12批车前子与其2种炮制品的色差值均>6.0,即同批次药材中可明显区分生品与炮制品,但炒车前子和盐车前子2种炮制品之间色差值较小,难以用肉眼区分。此外,车前子与炒车前子的Δ*为−14.12~−2.52,均值为−9.54,车前子与盐车前子的Δ*为−15.06~−4.90,均值为−10.87,表明车前子炮制后明度下降,颜色加深;车前子与炒车前子的Δ*为3.97~5.47,均值为4.88,车前子与盐车前子的Δ*为4.48~5.78,均值为5.26,表明车前子炮制后红色加深;车前子与炒车前子、盐车前子Δ*正负均有且数值不大,表明车前子炮制前后在黄蓝轴上颜色变化不大。

图1 车前子、炒车前子及盐车前子样品图

图2 12批车前子(S)、炒车前子(C)及盐车前子(Y)样品粉末色彩图像
2.2 车前子及其不同炮制品指纹图谱的建立
2.2.1 色谱条件 采用Waters Acquity UPLC HSS T3column(150 mm×2.1 mm,1.8 μm)色谱柱;流动相为乙腈-0.1%磷酸水溶液,梯度洗脱:0~5 min,10%乙腈;5~15 min,16%~18%乙腈;15~20 min,18%~25%乙腈;20~25 min,25%~45%乙腈;25~30 min,45%~60%乙腈;30~40 min,60%~70%乙腈;40~41 min,70%~10%乙腈;41~50 min,10%乙腈;程序检测波长:0~10.5 min,245 nm;10.5~35.5 min,330 nm;35.5~50 min,245 nm;体积流量0.3 mL/min;柱温30 ℃;进样量2 μL。

表2 色度值结果
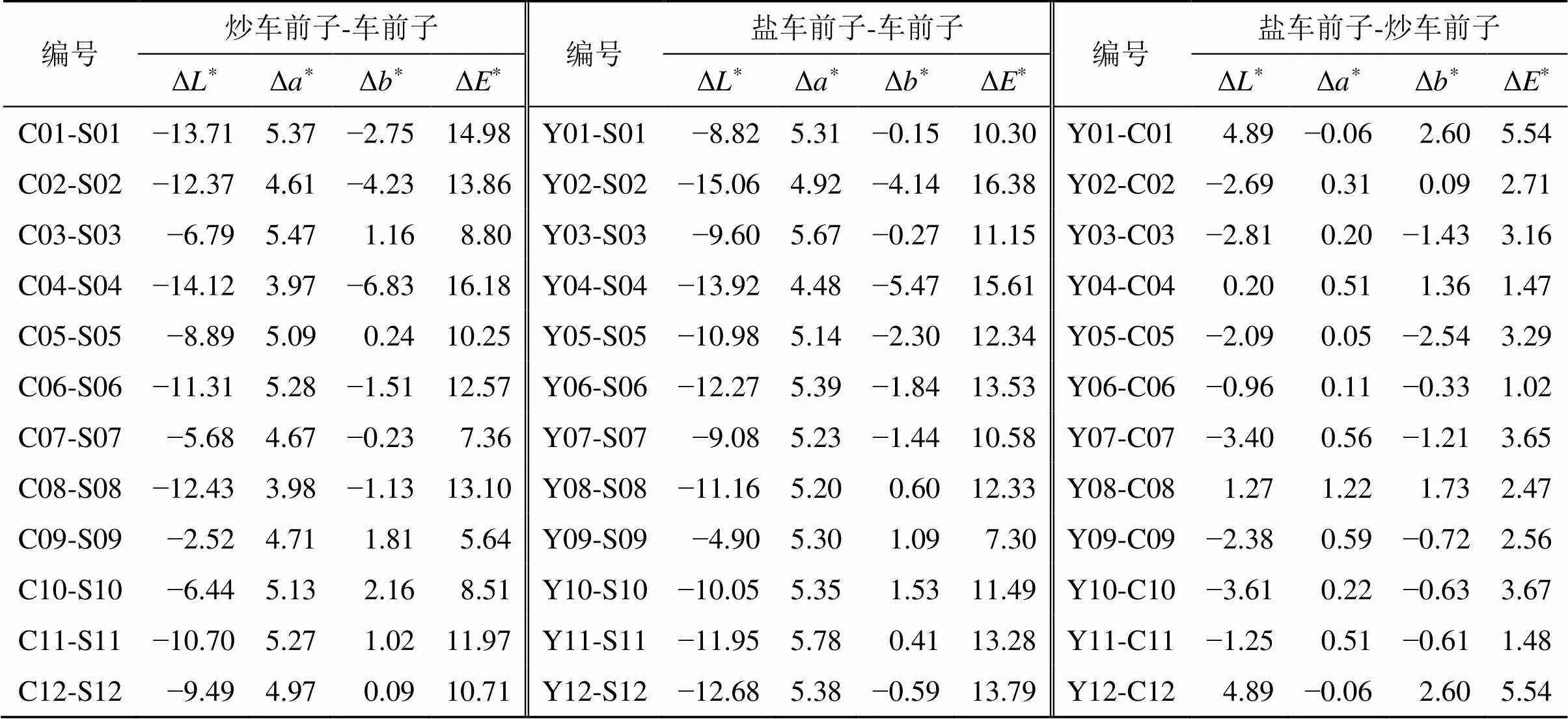
表3 色度值变化结果
2.2.2 质谱条件 氮气作为质谱离子源的雾化、锥孔气;质谱采用HESI离子源,离子源参数为鞘气流速35 arb;辅助气流速10 arb;喷雾电压3.2 kV;射频电压50 V;辅助器加热温度350 ℃;毛细管加热温度350 ℃。质谱扫描参数为正、负离子扫描模式;扫描范围为/150~2000;一级扫描分辨率为70 000 FWHM;二级扫描分辨率为17 500 FWHM;二级碰撞能量为40 eV。
2.2.3 对照品溶液的制备 精密称取京尼平苷酸、原儿茶酸、阿魏酸、大车前苷、木犀草苷、毛蕊花糖苷、木通苯乙醇苷B、车前草苷D、异毛蕊花糖苷、野漆树苷、芹菜素-7--葡萄糖醛酸苷、木犀草素、芹菜素对照品适量,精密称定,加甲醇制成质量浓度分别为53.072 1、84.217 4、86.179 8、40.512 0、42.117 6、158.888 8、69.034 6、44.590 0、57.232 0、49.182 5、48.555 3、38.043 2、62.622 0 μg/mL的混合对照品溶液。
2.2.4 供试品溶液的制备 取饮片粉末(过二号筛)约1.0 g,精密称定,置具塞锥形瓶中,精密加入甲醇25 mL,超声处理(250 W、40 kHz)60 min,离心,滤过,滤液蒸干,残渣加20 mL水使溶解,用醋酸乙酯萃取3次,每次20 mL,合并醋酸乙酯,蒸干,残渣用甲醇溶解,定容到10 mL量瓶,滤过,取续滤液,即得供试品溶液。
2.2.5 精密度试验 取车前子(S04)供试品溶液,按“2.2.1”项下色谱条件连续进样测定6次,以17号毛蕊花糖苷色谱峰为参照峰(S),计算各共有峰相对保留时间的RSD为0.06%~0.96%,相对峰面积的RSD为0.09%~2.89%,结果表明仪器精密度良好。
2.2.6 稳定性试验 取车前子(S04)供试品溶液,按“2.2.1”项下色谱条件,分别在制备后0、2、4、8、16、24 h进样测定,以17号毛蕊花糖苷色谱峰为参照峰(S),计算各共有峰的相对保留时间RSD为0.08%~1.20%,相对峰面积RSD为0.31%~2.53%,结果表明供试品溶液在24 h内稳定性良好。
2.2.7 重复性试验 取车前子样品(S04),按“2.2.3”项下方法制备供试品溶液,平行6份,按“2.2.1”项下色谱条件进样测定,以17号毛蕊花糖苷色谱峰为参照峰(S),计算各共有峰的相对保留时间RSD为0.05%~1.07%,相对峰面积RSD为0.13%~2.52%,结果表明该方法重复性良好。
2.2.8 指纹图谱的建立及色谱峰的指认 取12批车前子、炒车前子及盐车前子样品,按照“2.2.3”项下方法制备供试品溶液,按“2.2.1”项下色谱条件进样检测,采集色谱图。采用“中药色谱指纹图谱相似度评价系统2012版”软件进行数据处理,建立指纹图谱,分别以S01、C01和Y01号图谱作为参照图谱,以“中位数”法作为对照图谱生成方式,分别生成12批车前子、炒车前子及盐车前子的对照指纹图谱。12批车前子共标定了19个共有峰,12批炒车前子和盐车前子均共标定了27个共有峰,结果见图3。通过质谱精确相对分子质量、碎片离子对比分析,再与对照品保留时间及紫外吸收光谱比对,指认出其中13个主要成分,指认结果见图4及表4。
2.2.9 相似度评价 分别以车前子、炒车前子及盐车前子的对照指纹图谱为参照,计算12批车前子(S01~S12)、炒车前子(C01~C12)及盐车前子(Y01~Y12)指纹图谱的相似度,结果分别为0.998、0.998、1.000、0.997、0.999、0.999、0.999、0.972、0.999、0.999、1.000、0.999,0.950、0.955、0.999、0.914、0.999、0.999、0.996、0.991、0.939、0.997、0.998、0.995,0.981、0.965、0.995、0.941、0.959、0.976、0.984、0.984、0.995、0.982、0.987、0.984。结果显示,12批车前子(S01~S12)、炒车前子(C01~C12)及盐车前子(Y01~Y12)的相似度均大于0.9,说明不同批次的车前子样品批间差异较小,且炮制后的样品批间质量也较稳定。分别把车前子、炒车前子及盐车前子生成的对照指纹图谱导入软件,车前子与炒车前子的相似度值为0.388,车前子与盐车前子的相似度值为0.358,炒车前子与盐车前子的相似度值为0.997,说明车前子生品与炮制品之间的化学成分差异性较大,而不同炮制品之间差异较小。
2.3 车前子及其不同炮制品UPLC指纹图谱多元统计分析
2.3.1 单因素方差分析 将车前子及其不同炮制品的峰面积(部分缺失色谱峰峰面积以0计)导入SPSS 26.0进行单因素方差分析,结果见表5。结果表明,车前子经炮制后,色谱峰的变化较为明显。其中,相比于生品,车前子炮制品UPLC指纹图谱中新增了13个色谱峰,分别为峰1~3、6~12、18、20、28,缺失了4个峰,分别为峰14、16、23、31。此外,除峰25外,车前子炮制品各色谱峰的峰面积与车前子生品间的差异均具有统计学意义(<0.05);炒车前子与盐车前子中峰6、8、12、15、17(毛蕊花糖苷)、19(车前草苷D)、21(异毛蕊花糖苷)、22(野漆树苷)、24、26、27、33的峰面积差异均具有统计学意义(<0.05)。
2.3.2 主成分分析(principal component analysis,PCA) 将12批车前子(S01~S12)、炒车前子(C01~C12)及盐车前子(Y01~Y12)的峰面积(部分缺失色谱峰峰面积以0计)导入SIMCA 14.1,进行PCA。以特征值>1为标准,共提取了3个主成分,累积方差贡献率为93.2%,提示模型预测良好,可反映出12批车前子、炒车前子及盐车前子整体的信息,各主成分贡献率见表6。
由前3个主成分建立坐标系,得到的车前子、炒车前子及盐车前子的PCA得分图如图5所示。结果显示,车前子生品与炮制品可明显分为2组,但炒车前子和盐车前子的部分样品相互重叠,无法较好地区分。

图3 12批车前子(S01~S12)、炒车前子(C01~C12)、盐车前子(Y01~Y12)的UPLC指纹图谱及其对照指纹图谱(SR, CR, YR)
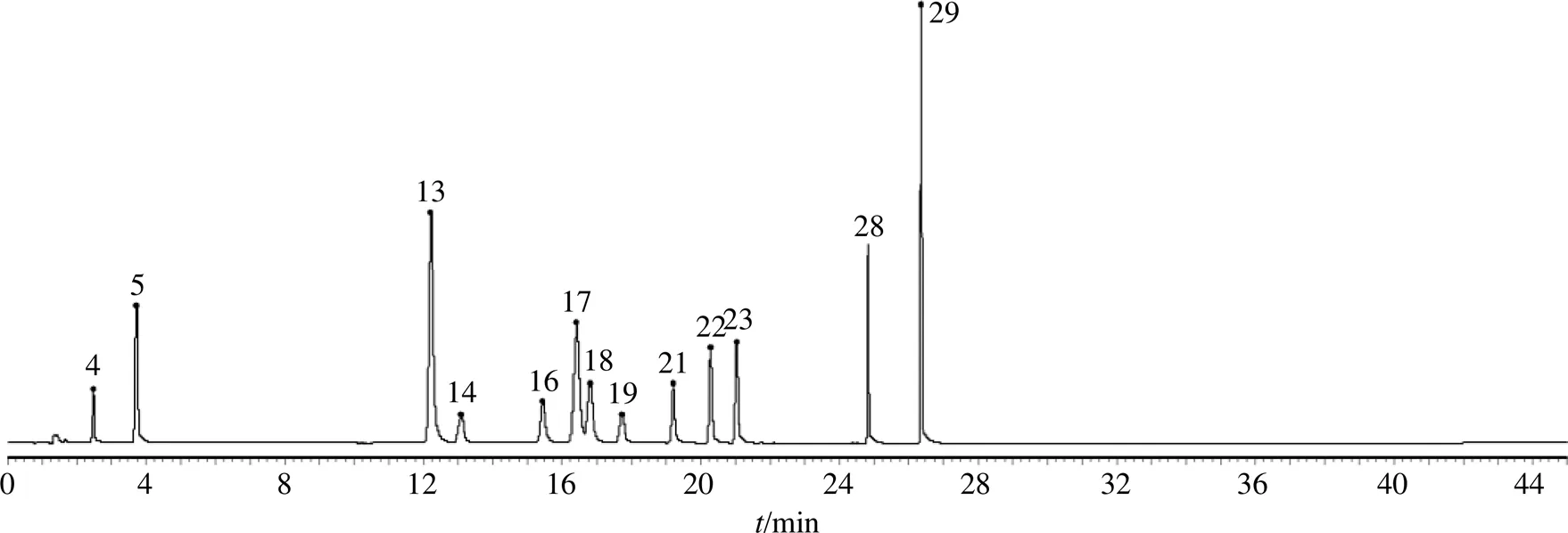
4-京尼平苷酸 5-原儿茶酸 13-阿魏酸 14-大车前苷 16-木犀草苷 17-毛蕊花糖苷 18-木通苯乙醇苷B 19-车前草苷D 21-异毛蕊花糖苷 22-野漆树苷 23-芹菜素-7-O-葡萄糖醛酸苷 28-木犀草素 29-芹菜素
2.3.3 层次聚类分析(hierarchical cluster analysis,HCA) 将12批车前子(S01~S12)、炒车前子(C01~C12)及盐车前子(Y01~Y12)的峰面积(部分缺失色谱峰峰面积以0计)导入SPSS 26.0,采用组间连接法,以平方欧氏距离为分类依据,进行HCA。结果如见图6所示,当聚类距离为5时,车前子生品与炮制品可明显分为2类,但炒车前子和盐车前子无法较好地聚类,其中C09单独聚为一类,其余批次的炒车前子和盐车前子聚为一类,表明炒车前子和盐车前子样品相似度较高,与PCA结果基本一致。
2.3.4 正交偏最小二乘-判别分析(orthogonal partial least squares-discriminant analysis,OPLS-DA) 为筛选车前子、炒车前子及盐车前子成分差异的主要标志性成分,将12批车前子(S01~S12)、炒车前子(C01~C12)及盐车前子(Y01~Y12)的峰面积(部分缺失色谱峰峰面积以0计)导入SIMCA 14.1,进行OPLS-DA。对各指标的变量重要性投影(variable importance for the projection,VIP)值进行大小排列,选择VIP值>1的指标作为区分车前子、炒车前子及盐车前子的主要差异性成分。
建立的车前子、炒车前子及盐车前子的OPLS- DA模型中,自变量累积解释能力参数R2为0.985,因变量累积解释能力参数R2为0.938,预测能力参数2为0.807,均大于0.5,说明所建模型具有较强的解释率和预测率,得到的OPLS-DA得分图见图7,VIP值见图8。由图7可知,车前子、炒车前子及盐车前子呈现明显的分类聚集现象。由图8可知,以VIP值>1为标准共提取10个VIP值,重要程度排名依次为峰21(异毛蕊花糖苷)、24、19(车前草苷D)、26、22(野漆树苷)、8、4(京尼平苷酸)、27、7、15,以上成分可能是车前子、炒车前子与盐车前子的差异性标志物。

表5 指纹图谱峰面积单因素方差分析结果
与车前子比较:*<0.05;与炒车前子比较:#<0.05
*< 0.05PS;#< 0.05fPS
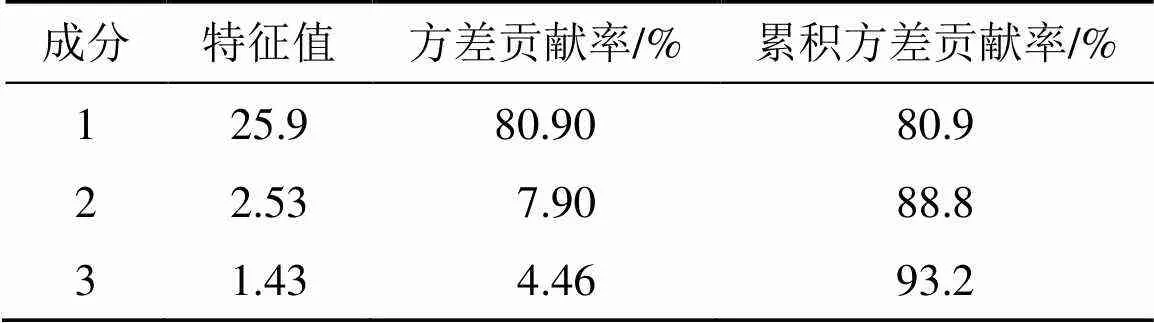
表6 主成分特征值及方差贡献率
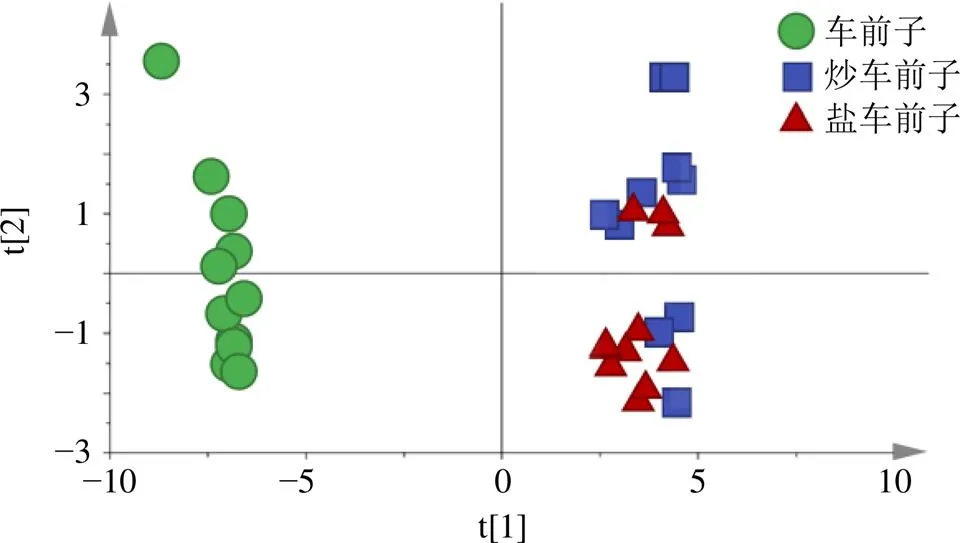
图5 12批车前子及炮制品PCA得分图

图6 12批车前子及炮制品HCA图
2.4 车前子及其不同炮制品体外抗氧化活性测定与分析
2.4.1 测定方法 在预试验的基础上,本研究将供试品溶液的质量浓度稀释成60 μg/mL,按照格锐思试剂盒的规定方法进行测定。
(1)试剂溶液的配制:①试剂1:临用前甩几下使粉剂落入底部,每支加0.49 mL蒸馏水溶解。②试剂2:临用前甩几下使粉剂落入底部,每支加2.86 mL蒸馏水,充分溶解,备用。③ABTS工作液的配制:临用前根据样本量按试剂1-试剂2(1∶1)比例混合,避光反应12 h后(2 d内用完),再用无水乙醇稀释20~30倍备用。

图7 12批车前子及炮制品OPLS-DA图
将上述溶液按照表7设计充分混匀后避光静置6 min,转移至玻璃比色皿(光径1 cm)中,于734nm处读取吸光度()值,分别记为空白、对照和测定,并计算ABTS自由基清除率。
ABTS自由基清除率=1-(测定-对照)/空白
2.4.2 测定结果 12批车前子、炒车前子及盐车前子的抗氧化活性测定结果见表8。可见,12批车前子及其炮制品均具有清除ABTS自由基的能力,其中炒车前子最强,盐车前子与炒车前子差异不大,车前子生品清除能力最弱。
2.5 表-里关联分析
将车前子及其不同炮制品的色度值与峰面积(部分缺失色谱峰峰面积以0计)导入SPSS 26.0进行皮尔逊(Pearson)相关性分析,结果见表9。结果表明,除峰21、24、25外,各共有峰峰面积均与*值、*值及*值呈极显著相关(<0.01);其中峰13、14、16、17、19、22、23、26、27、30~34与*值和*值均呈极显著正相关,其余峰与*值和*值呈极显著负相关;峰1~12、15、18、20、24、28、29与*值呈极显著正相关,其余峰与*值呈极显著负相关;峰19、21、22、25、26与*值呈极显著正相关(<0.01),峰24与*值呈极显著正相关(<0.05),峰5、9、10与*值呈极显著负相关(<0.01),峰1、2、11与*值呈显著负相关(<0.05)。总体而言,各共有峰的峰面积值对色度值均有一定影响,对*值的影响较小,对*值、*值影响较大。
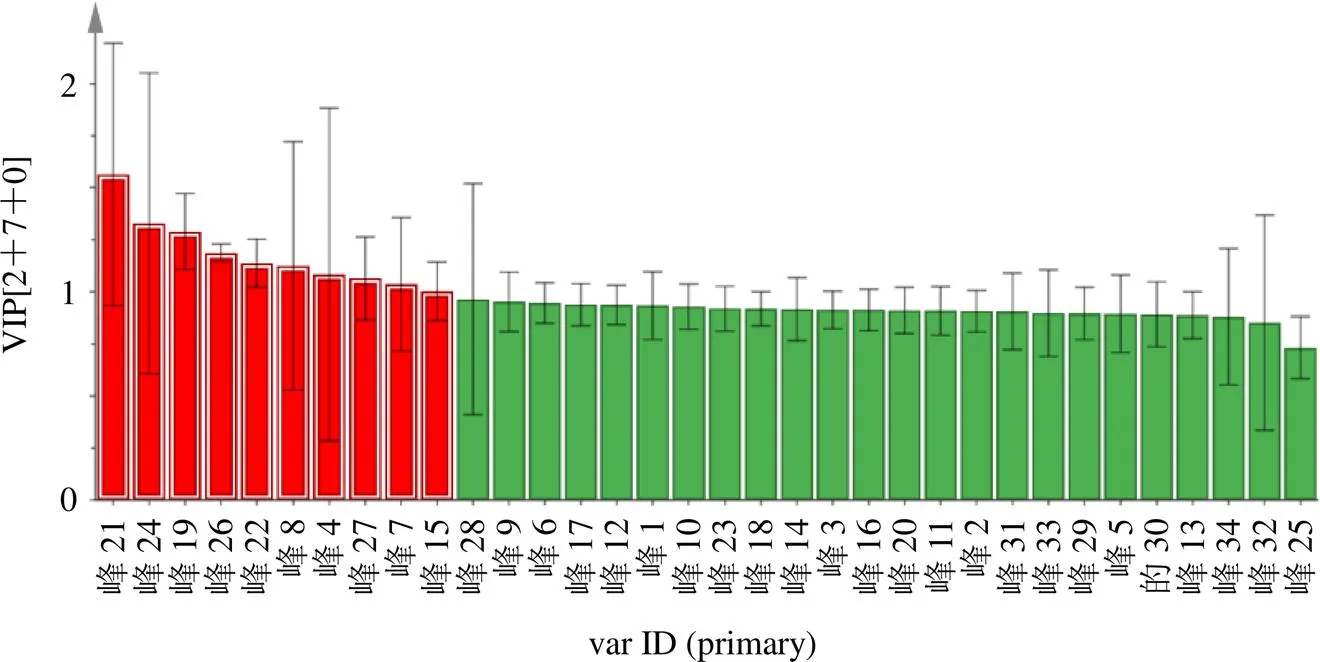
图8 12批车前子及炮制品VIP得分图

表7 ABTS反应体系
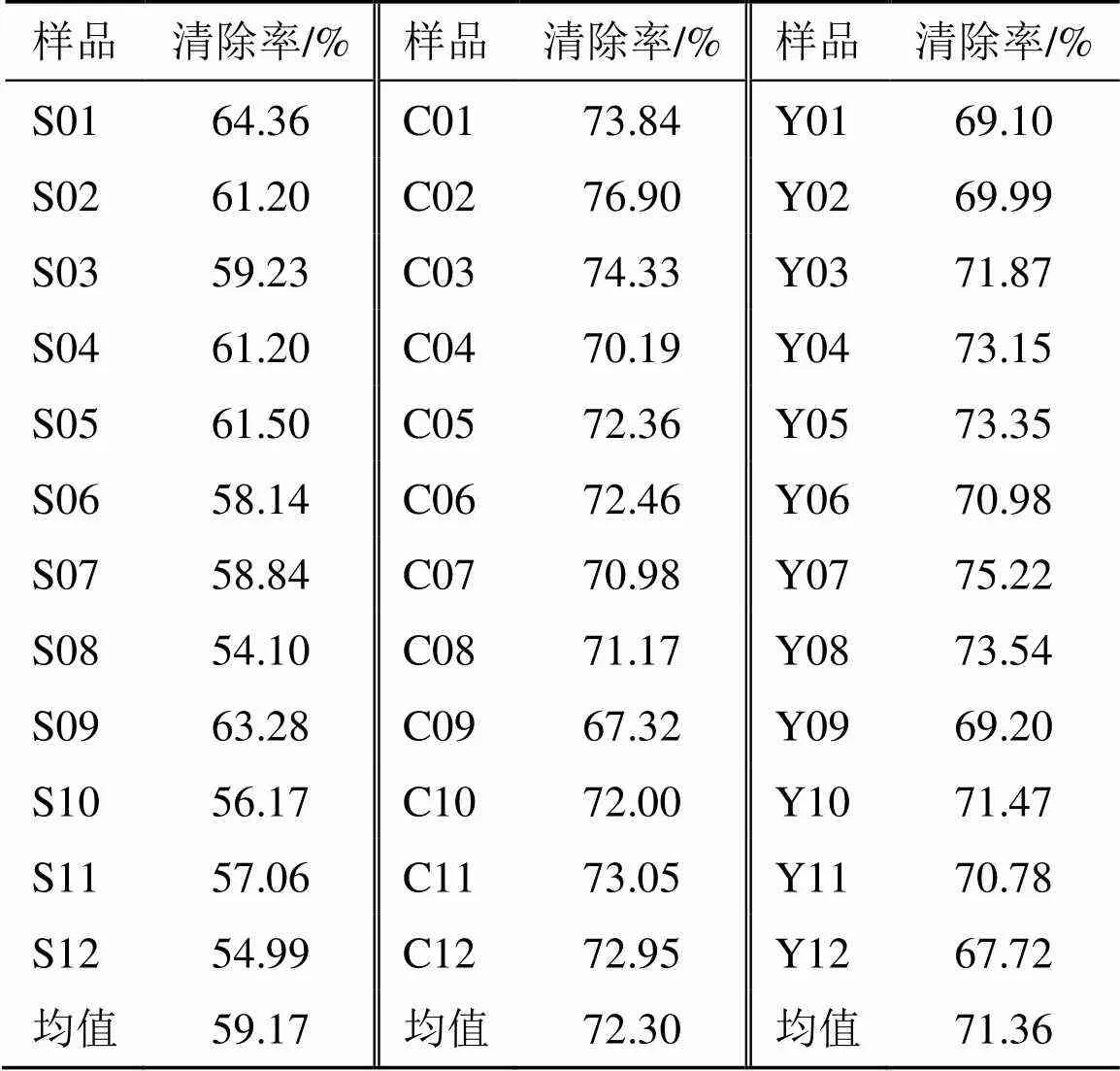
表8 抗氧化活性测定结果
2.6 谱-效关系分析
2.6.1 偏最小二乘回归法(partial least squares regression method,PLSR)分析[17-18]参考文献方法,利用SIMCA 14.1软件,以12批车前子、炒车前子及盐车前子的ABTS清除率为因变量,共有峰的峰面积经折算扣除水分后为自变量(部分缺失色谱峰峰面积以0计),采用PLSR进行相关性分析,建立的回归方程为=0.0591+0.0952+0.0013-0.0164+0.0485+0.0586+0.0307+0.0908-0.0369-0.00710+0.07511+0.06612-0.09513+0.00814+0.06115+0.08416-0.00817+0.04718-0.11219+0.00720-0.05121+0.00522+0.01323+0.08024+0.13125-0.06026-0.01827-0.16428-0.06629-0.05230-0.05531-0.09232-0.11433-0.11434+40 761,得到的标准化回归系数见图9。其中,峰1~3、5~8、11、12、14~16、18、20、22~26的回归系数大于0,表明其与抗氧化活性呈正相关,其余峰的回归系数为负值,与抗氧化活性呈负相关。
2.6.2 灰色关联度(grey correlation degree,GRA)分析[19-21]将车前子、炒车前子及盐车前子共有峰的峰面积(部分缺失色谱峰峰面积以0计)和抗氧化活性数据进行均值化处理。将处理后的抗氧化活性数据设置为母序列0(),峰面积数据为子序列x()(为峰号),根据公式(1)计算母序列与子序列的灰色关联系数。其中为分辨系数,越小,则分辨力越大,一般的取值区间为[0,1],当≤0.546 3时,分辨力最好,通常取=0.5。根据公式(2)计算关联系数的算术平均值,即为关联度,结果见表10。
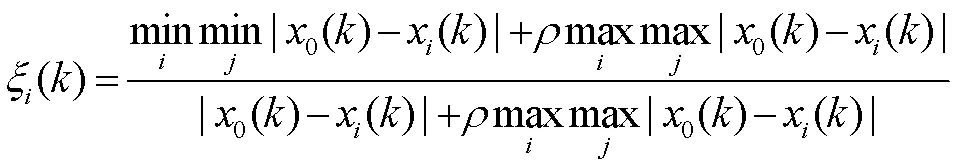
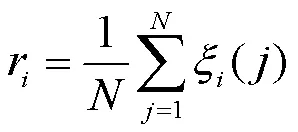
当关联度大于0.8,则表示母序列与子序列关联度较大;当关联度介于0.6~0.8,则表示二者关联度一般;当关联度小于0.6,则表示二者关联度较小。由表10可知,峰1~12、15、18~22、24~26、28、29、34与抗氧化活性贡献作用关联度较大。与PLSR结果结合分析,可综合得出峰1~3、5~8、11、12、15、18、20、22、24~26是与车前子及其炮制品的抗氧化活性关联度较大的正相关色谱峰,即为主要起抗氧化作用的成分,其中峰5为原儿茶酸、峰18为木通苯乙醇苷B、峰22为野漆树苷,其余色谱峰所对应的物质成分还有待进一步探索研究。
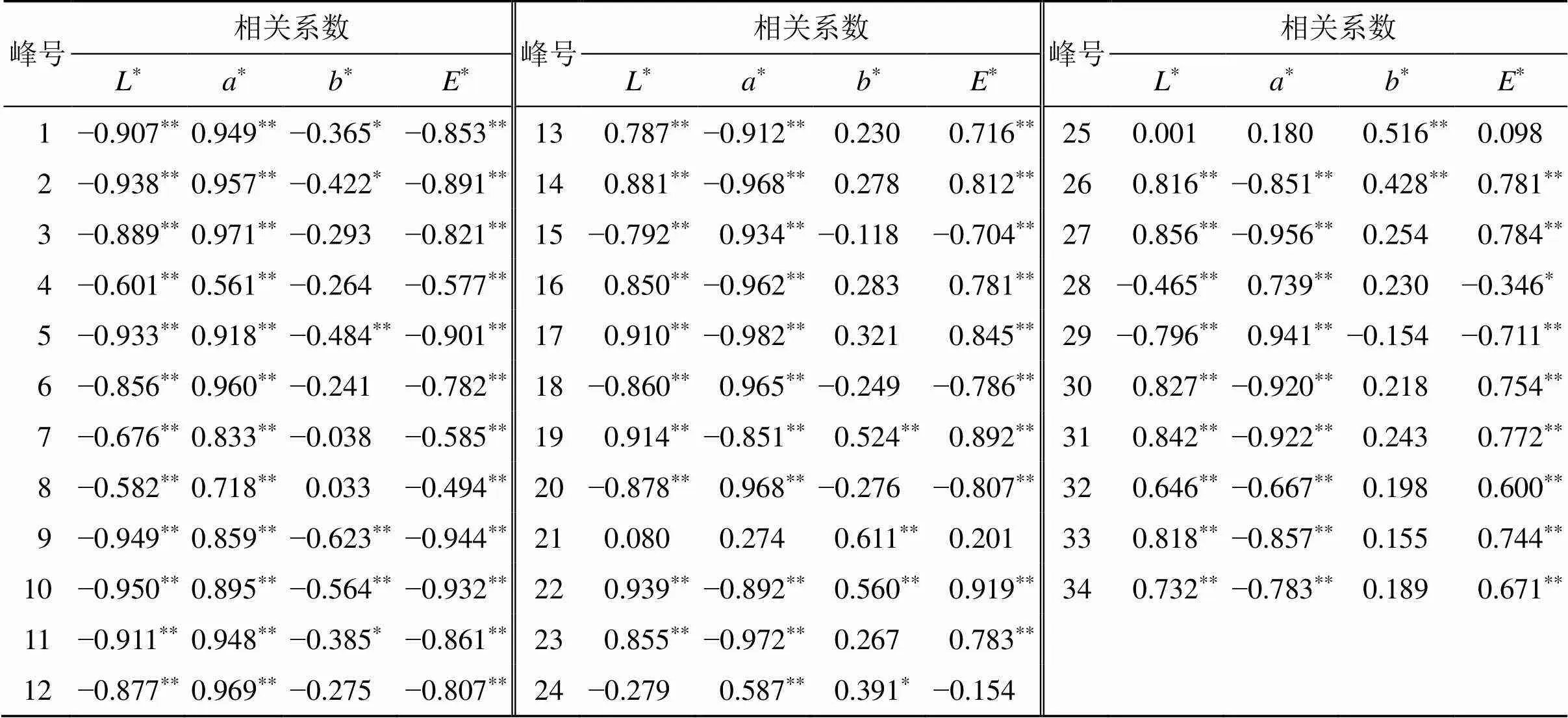
表9 色度值与化学成分(色谱峰)相关性分析
*<0.05**<0.01
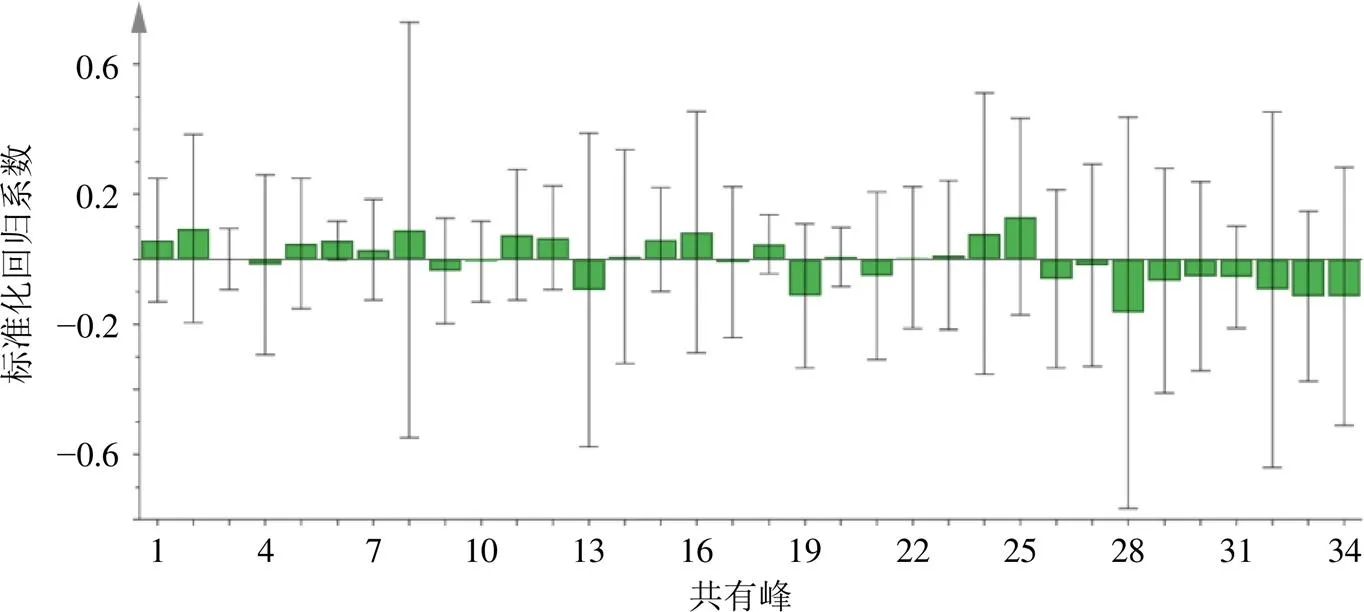
图9 PLSR标准化回归系数图
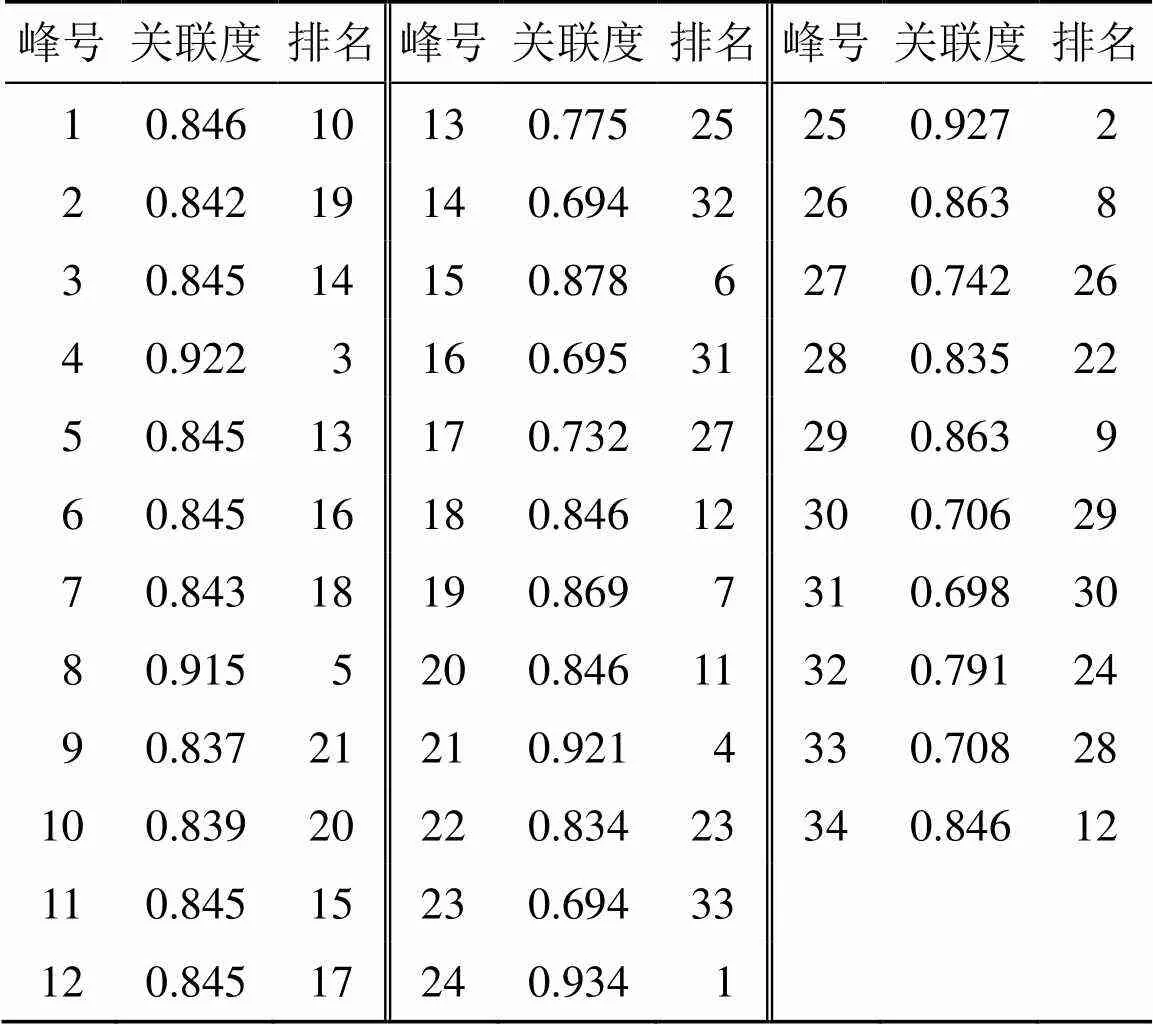
表10 关联度结果
3 讨论
3.1 提取和分析条件优化
本实验分别考察了提取方式(回流、超声)、提取溶剂(60%、80%、100%甲醇)、提取时间(0.5、1.0、1.5、2.0 h)、溶剂用量(25、50 mL)对特征图谱色谱峰的峰型及峰面积的影响,结果显示车前子样品前处理时加入甲醇25 mL超声1.0 h效果整体较佳。同时,本实验采用PDA检测器对车前子及其炮制品中的色谱峰进行全波长扫描,发现京尼平苷酸在238 nm下有最大紫外吸收,原儿茶酸在259 nm有最大紫外吸收,毛蕊花糖苷及的最佳紫外吸收为330 nm,异毛蕊花糖苷、木犀草苷、野漆树苷、芹菜素-7--葡萄糖醛酸苷、芹菜素、木犀草素的最大紫外吸收也在330 nm附近;且0~10.5 min和35.5~50 min时,色谱峰在245 nm下较丰富,紫外吸收较强;10.5~35.5 min时,色谱峰在330 nm下较丰富,紫外吸收较强。因此,本实验最终采用切换波长的方式对车前子及其不同炮制品的UPLC指纹图谱进行检测。
3.2 生品与不同炮制品比较
本研究建立了车前子及其不同炮制品的UPLC指纹图谱,共标定了34个共有峰,其中车前子有19个,炒车前子和盐车前子有27个。共指认出其中13个主要成分,其中车前子指认了10个,炒车前子和盐车前子指认了10个。车前子炮制前后色谱峰变化明显,新增了13个峰,包括原儿茶酸、木通苯乙醇苷B和木犀草素;减少了4个峰,包括大车前苷、木犀草苷和芹菜素-7--葡萄糖醛酸苷,上述色谱峰可作为车前子生品与炮制品的专属性鉴别峰。同时,峰8、15仅在部分批次车前子生品中检出,但在车前子炮制品指纹图谱中均有呈现,且峰面积远高于生品(<0.05),说明峰8、15所表征的化合物亦为受热后新增的成分,生品中检出的原因可能为产地干燥过程中,受热程度稍高产生的。峰27、30、33在所有车前子生品中均有检出,但仅在部分炮制品指纹图谱中呈现,且炮制品中上述3个色谱峰的峰面积远小于生品(<0.05),说明峰27、30、33所表征的化合物为热敏性成分,炮制受热后易分解或转化,部分炮制品中检出峰27、30、33,可能为批间炮制程度差异导致。单因素方差分析结果表明车前子及其炮制品中的部分化学成分具有显著性差异,由PCA、HCA结果可知车前子炮制前后成分含量差异较大,进一步采用OPLS-DA分析可将炒车前子和盐车前子也区分开,同时提取出10个潜在的差异性标志物。粉末外观颜色上,通过色差Δ*>6.0,可辅助识别车前子生品及炮制品。在抗氧化活性研究中,以ABTS自由基的清除率作为抗氧化活性的药效学指标进行分析,结果显示车前子炮制后抗氧化活性较生品明显提高,而不同炮制品间的活性差异不大。
3.3 成分变化分析
车前子炮制后毛蕊花糖苷明显减少,而异毛蕊花糖苷明显增加,同时新产生了木通苯乙醇苷B;芹菜素-7--葡萄糖醛酸苷消失,而芹菜素明显增加,原因可能与炮制时成分相互转化有关[22-23];有研究表明,含有阿魏酸的药材在体外干燥过程中会与阿魏酸松柏酯相互转化,在光照或升温时还会发生降解[24],阿魏酸峰面积在炮制后显著降低可能与此有关;原儿茶酸和木犀草素的增加可能是因为炮制时车前子内部温度升高,药材中含有的苷类化合物在加热条件下不稳定分解而成[25]。此外,还有一些化合物含量升高或降低有待进一步研究。
3.4 谱-效关系分析
中药成分复杂,治疗范围广,副作用小,是多成分、多靶点、多途径协同作用的结果,指纹图谱可以在整体水平阐明中药的化学成分组成,但不能直接对其功效进行评价。中药谱效学[25]是研究中药药效和指纹图谱相互关系的学科,可以将化学成分与中药药效相结合,对中药质量的控制和药效的评价具有重要意义。
PLSR法[24]综合回归分析、相关分析和主成分分析,更加准确可靠,具有较高的预测性,可以通过构建科学的回归模型初步衡量各有效成分对药效的贡献程度;灰色关联分析[25]是研究2个因素变化趋势相关性的一种统计学方法,2个因素之间的关联度高,则表示二者的同向化变化趋势程度高,适合用于分析样本信息量单一但影响因素复杂的图谱,在谱效关系中运用广泛[19,26]。本研究采用PLSR和灰色关联分析相结合的方法,成功建立了车前子及其炮制品UPLC指纹图谱与其抗氧化活性的谱效关系,结果显示有11个峰代表的化学成分与车前子及其炮制品的抗氧化活性关联较大,即主要具有抗氧化作用,其中3个峰分别为原儿茶酸、木通苯乙醇苷B和野漆树苷,文献研究也表明,这3个成分均具有较好的抗氧化活性[27-29],其余峰所代表的化学成分还需要进一步研究。
本研究建立车前子炮制前后的UPLC指纹图谱,并结合色度值和抗氧化活性,明确了车前子生品及其不同炮制品的显著差异点,为车前子及其不同炮制品的鉴别及质量分析提供较科学、全面的判断;同时结合谱效关系研究,明确了车前子及其炮制品抗氧化作用的物质基础,可为车前子的炮制机制研究提供参考。
利益冲突 所有作者均声明不存在利益冲突
[1] 中国药典[S]. 一部. 2020: 70.
[2] 徐硕, 徐文峰, 梁晓丽, 等. 车前子的化学成分及生物活性研究进展 [J]. 西北药学杂志, 2019, 34(4): 567-570.
[3] 彭东辉, 匡海学, 王秋红. 车前子多糖的研究进展 [J]. 广东药科大学学报, 2019, 35(5): 702-706.
[4] 李冲冲, 龚苏晓, 许浚, 等. 车前子化学成分与药理作用研究进展及质量标志物预测分析 [J]. 中草药, 2018, 49(6): 1233-1246.
[5] 崔琳琳, 包永睿, 王帅, 等. 车前草不同药用部位抗炎、抗肿瘤、抗氧化的活性研究 [J]. 世界科学技术—中医药现代化, 2019, 21(3): 395-400.
[6] Li C, Wen R, Liu D W,. Diuretic effect and metabolomics analysis of crude and salt-processed[J]., 2020, 11: 563157.
[7] Yang F, Shi W, Wang L,. Lipidomics study of the therapeutic mechanism ofin potassium oxonate-induced hyperuricemia rat [J]., 2021, 21(1): 175.
[8] 陈浩, 赵威, 俞浩, 等. 基于FXR-MRP2/BSEP通路探究车前子水提物对环磷酰胺致大鼠肝损伤的保护作用及机制研究 [J]. 中药药理与临床, 2018, 34(5): 85-90.
[9] Sun X M, Lan J P, Tong R C,. An integrative investigation on the efficacy ofbased on UPLC-QTOF-MS metabolomics approach in hyperlipidemic mice [J]., 2019, 115: 108907.
[10] 朱盈徽, 杨丹阳, 吴晓莹, 等. 车前子炮制研究进展[J]. 中华中医药学刊, 2023, 41(8): 187-191.
[11] 施繁莉, 吕慧侠, 张振海. 中药药效物质基础的相对动态性研究进展 [J]. 药学进展, 2021, 45(11): 855-861.
[12] 邓李红, 王寿富, 陈仕妍, 等. 基于UPLC特征图谱结合多模式识别和色度值的槐角炮制前后差异研究 [J]. 中草药, 2022, 53(21): 6881-6887.
[13] 郑晓倩, 徐超, 金传山, 等. 基于颜色变化的“九蒸九晒”黄精炮制火候及内外在质量的相关性研究 [J]. 中草药, 2022, 53(6): 1719-1729.
[14] 鲁云, 洪婉敏, 姚晓璇, 等. 麸炒北苍术饮片粉末的色度值与质量指标的相关性分析及其炮制时间研究 [J]. 中国药房, 2021, 32(21): 2605-2612.
[15] 广东省食品药品监督管理局. 广东省中药饮片炮制规范-第一册 [M]. 广州: 广东科技出版社, 2011: 34.
[16] 纪玉华, 洪婉敏, 谢明晏, 等. 基于UPLC特征图谱及色彩图像技术的当归与酒当归差异比较研究 [J]. 中药材, 2022, 45(2): 321-326.
[17] 孙飞, 吴相亲, 戚悦, 等. 基于偏最小二乘算法探究山楂和焦山楂消食健脾功效成分 [J]. 中国中药杂志, 2023, 48(4): 958-965.
[18] 贾毓欣, 刘海帆, 司明东, 等. 知母及其不同炮制品的指纹图谱建立与抗氧化活性的谱-效关系研究 [J]. 中国药房, 2020, 31(22): 2706-2712.
[19] 张萌, 邓家刚, 韦玮, 等. 广山楂HPLC指纹图谱建立及其活血化瘀作用谱效关系研究 [J]. 中草药, 2023, 54(2): 601-607.
[20] 黄潇, 刘婧, 吴建华, 等. 基于灰色关联法分析栀子提取物抗炎作用谱效关系 [J]. 中成药, 2020, 42(1): 233-237.
[21] 孙钰婧, 霍志鹏, 王玉, 等. 基于UPLC-Q-TOF/MSE分析不同炮制时间炒车前子的化学成分变化规律 [J]. 中国实验方剂学杂志, 2022, 28(4): 146-153.
[22] 张姗姗. 亳菊炮制工艺及炮制前后的化学成分和保肝药效初步研究 [D]. 合肥: 安徽中医药大学, 2021.
[23] 王莹, 孙嘉辰, 李霞, 等. 基于建立成分活性权重函数的当归酒炙工艺评价研究 [J]. 中草药, 2022, 53(10): 3014-3021.
[24] 范兰兰, 张姗姗, 姚梦雪, 等. 菊花炒制前后化学成分变化及对CCl4所致小鼠急性肝损伤的影响 [J]. 中国中药杂志, 2020, 45(13): 3144-3154.
[25] 潘杰, 刘德胜, 颜贵明. 数据分析应用于中药谱效关系中的研究进展 [J]. 中医药学报, 2018, 46(4): 119-122.
[26] 杨锡金, 王艳, 陈梓瀚, 等. 基于HPLC-ECD研究景天三七抗氧化活性的谱效关系[J]. 食品工业科技, 2023, 44(16): 15-24.
[27] 张驰, 田富林, 金舟, 等. 酚酸生物活性研究进展 [J]. 粮食与油脂, 2023, 36(5): 4-7.
[28] Kadowaki W, Sugahara Y, Toyoizumi T,. Isolation and identification of antioxidant phenylpropanoids from the fruit peel ofKoidz. [J]., 2023, 29(1): 27-34.
[29] Al-Shalabi E, Abusulieh S, Hammad A M,. Rhoifolin loaded in PLGA nanoparticles alleviates oxidative stress and inflammationand[J]., 2022, 10(19): 5504-5519.
Comparative study on chromaticity value, UPLC fingerprint and antioxidant activityofSemen and its different processed products
CHENG Yu-jie, QIU Cai-yue, HONG Wan-min, LU Peng-xin, WANG Kai-dong, XU Jie, ZHANG Zhi-peng
Guangdong Yifang Pharmaceutical Co., Ltd., Guangdong Provincial Key Laboratory of Traditional Chinese Medicine Formula Granule, Foshan 528244, China
To analyze the difference of fingerprint, chromatic value and antioxidant activity of Cheqianzi (, PS) and its different processed products, and explore the spectrum-effect relationship between the chemical components and antioxidant effects.The chromaticity value were determined by spectrophotometer, the fingerprint of PS and its different processed products were established by UPLC, and the antioxidant activity were determined by ABTS method. The similarity evaluation, variance analysis, principal component analysis (PCA), cluster analysis, and orthogonal partial least squares discriminant analysis (OPLS-DA) were used to analyze the difference of PS and its different processed products; and the partial least-square method regression (PLSR) and grey correlation analysis (GRA) method were used to explore the spectrum-effect relationship between the chemical components and the antioxidant of PS and its different processed products.The established UPLC fingerprint of PS has calibrated 19 common peaks, while 27 common peaks were calibrated in fried PS (fPS) and salt-processed PS (spPS). A total of 34 chromatographic peaks were calibrated and 13 of them were identified. Multivariate statistical analysis showed that there were obvious differences between PS and its different processed products. PCA and HCA divided the raw and processed products of PS into two categories, and OPLS-DA screened 10 differential marker components. The chromaticity value Δ*of PS and its different processed products was greater than 6, making it visually distinguishable, but the color difference among different processed products was not obvious. The results of antioxidant activity showed enhanced antioxidant effect of PS after processing, with no significant difference among different processed products. Correlation analysis indicated that the peak area values of common peaks had a certain impact on chromaticity values, with a smaller impact on*values and a greater impact on*and*values. PLSR and GRA analysis showed that the chemical constituents represented by 11 peaks were significantly related to the antioxidant of PS and its different processed products, including protocatechuate, calceorioside B and rhoifolin.The UPLC fingerprint established in this study, as well as the determination method of chromaticity value and antioxidant activity, can be used for the identification and quality analysis of PS and its different processed productsThe study of the spectrum-effect relationship between fingerprint and antioxidant activitycan provide a reference for the study of the processing mechanism of PS
; processing; UPLC; fingerprint; chromatic value; antioxidant activity; spectrum-effect relationship; ABTS method; principal component analysis; hierarchical cluster analysis; orthogonal partial least squares-discriminant analysis; grey relation analysis; isoacteoside; plantainoside D; rhoifolin; geniposidic acid
R283.6
A
0253 - 2670(2023)20 - 6657 - 14
10.7501/j.issn.0253-2670.2023.20.010
2023-04-28
国家工信部2022年产业技术基础公共服务平台项目——中药全产业链质量技术服务平台(2022-230-221)
程钰洁(1998—),女,汉族,学士,初级中药师,从事中药及中药配方颗粒质量标准研究。Tel: 13226546740 E-mail: 2496773973@qq.com
通信作者:张志鹏(1990—),男,汉族,硕士,副主任中药师,从事中药及中药配方颗粒质量标准研究。Tel: 15919328456 E-mail: zhangzp0909@163.com
[责任编辑 郑礼胜]
