红花八角叶中1个新的酚酸类化合物
2023-10-19王振中耿剑亮
沈 浪,李 旭,曹 亮,王振中,肖 伟*,耿剑亮*
红花八角叶中1个新的酚酸类化合物
沈 浪1,李 旭2,曹 亮2,王振中2,肖 伟2*,耿剑亮1*
1. 广东药科大学中药学院,广东 广州 510006 2. 中药制药过程控制与智能制造技术全国重点实验室,江苏康缘药业股份有限公司,江苏 连云港 222001
对红花八角的干燥叶进行化学成分研究。综合应用各种现代色谱分离技术进行系统的分离纯化,根据化合物的理化性质和核磁共振波谱数据进行结构鉴定。从红花八角叶50%乙醇提取物经HP-20大孔吸附树脂30%乙醇洗脱部位中共分离鉴定5个化合物,分别为7---甲氧基苄基莽草酸(1)、黑麦草内酯(2)、去氢催吐萝芙木醇(3)、蚱蜢酮(4)、chakyunglupulin A(5)。化合物1为新的酚酸类化合物,2~5为首次从该属植物中分离得到。
红花八角;7---甲氧基苄基莽草酸;黑麦草内酯;去氢催吐萝芙木醇;蚱蜢酮;chakyunglupulin A
红花八角Tutcher为五味子科(Schisandraceae)八角属Linn.植物,别名山八角、野八角[1-2]。味苦、辛,性温,由于其具有散瘀消肿、祛风除湿、止痛的功效,民间常用其根和树皮入药,外用治疗风湿骨痛、跌打损伤、挫伤骨折[3-4]。文献报道红花八角中主要含有苯丙素类[5-9]、倍半萜类[9-13]、酚苷类[14]、黄酮类[15-17]、三萜[5]、挥发油[18]及其他类成分,现代药理学研究表明红花八角提取物及部分化合物具有多种生物活性,包括抗炎镇痛和解痉作用[17,19]、调节免疫功能[20]、抗抑郁[8]等。
目前对红花八角的研究大多集中在根与树皮,而对其叶的研究鲜有报道。而药理实验研究表明红花八角叶的醇提液具有中枢及外周镇痛作用,对多种疼痛及急性软组织损伤具有较好的止痛和消肿作用,此外还能解除胃肠平滑肌的痉挛以及具有抗炎作用[20]。以红花八角叶入药的中成药金红片对于治疗慢性浅表性胃炎具有较好疗效[21-23]。为了全面揭示红花八角叶的药效物质基础,为其进一步的合理开发利用奠定基础,本课题组对红花八角叶开展了系统的化学成分研究,前期本课题组已经从红花八角叶50%乙醇提取物经大孔吸附树脂50%乙醇洗脱部分中分离鉴定了24个木脂素类成分(包括9个新化合物)[24];1个新的酚酸苷和1个新的苯并呋喃衍生物[25]以及14个酚酸类成分(包括8个新化合物)[26]。为了进一步丰富其化学多样性,对红花八角叶50%乙醇提取物经HP-20大孔吸附树脂30%乙醇洗脱部位进行化学成分研究,从中分离鉴定5个化合物,分别鉴定为7---甲氧基苄基莽草酸(7---methoxybenzyl shikimic acid,1)、黑麦草内酯(loliolide,2)、去氢催吐萝芙木醇(dehydrovomifoliol,3)、蚱蜢酮(grasshopper ketone,4)、chakyunglupulin A(5),其中化合物1为新的酚酸类化合物,2~5为首次从该属植物中分离得到。
1 仪器与材料
Brucker AVANCE 400型核磁共振仪,Finni-gan LCQ Advantage MAX质谱仪,Waters Snapt G2 mass spectrometer高分辨质谱仪,Shimadzu分析高效液相色谱(Shimadzu LC-6AD series pump,配置UV检测器),Shimadzu制备型高效液相色谱,P2000旋光测定仪、FT/IR-480 plus红外光谱仪(KBr压片)、JASCOV-550型紫外-可见光谱仪(日本Jasco公司)。分析高效液相色谱柱为Phenomenex Gemini(C18,250 mm×4.6 mm,5 μm),制备高效液相色谱柱为C18柱(250 mm×20 mm,5 μm,Nacalai tesque Inc.,日本)。薄层硅胶GF254和柱色谱硅胶(青岛海洋化工厂),HP-20型大孔树脂(Mitsubishi-Chemical,日本),反相ODS填料(Merck公司),Sephadex LH-20填料(Amersham Biosciences公司),Toyo-pearl HW-40填料(Toyo Soda MFG)。
红花八角叶于2018年从江西吉安药材市场购买,并由江苏康缘药业股份有限公司的生药鉴定学专家吴舟教授鉴定为五味子科八角属植物红花八角Tutcher,药材标本(2018ID101)保存于暨南大学中药及天然药物研究所。
2 提取与分离
取干燥的红花八角叶15.5 kg,用8~10倍量50%乙醇回流提取3次,每次2 h,合并提取液,减压回收乙醇,喷雾干燥得红花八角叶干膏粉2 kg。将得到的总提取物用适量水分散后,经HP-20大孔吸附树脂柱色谱,用水及30%、50%和95%乙醇梯度洗脱,得到4个洗脱部位:水洗脱部位(ID-1,1.28 kg)、30%乙醇洗脱部位(ID-2,326.1 g)、50%乙醇洗脱部位(ID-3,203.5 g)和95%乙醇洗脱部位(ID-4,107.8 g)。取30%乙醇水洗脱部分ID-2(300 g)进行硅胶柱色谱分离,二氯甲烷-甲醇梯度洗脱得到6个流分Fr. 2A~2F。再经过硅胶柱色谱、ODS柱色谱、Sephadex LH-20、Toyopearl HW-40、半制备HPLC以及重结晶等方法分离纯化。从Fr. 2B中得到化合物1(8.5 mg)、2(52.6 mg)、3(15.5 mg)、4(24.9 mg)和5(36.4 mg)。
3 结构鉴定

化合物1的1H-NMR (400 MHz, CD3OD) 图谱中显示2组相互偶合的芳香质子信号 [H7.31 (2H, d,= 8.5 Hz, H-2′, 6′), 6.91 (2H, d,= 8.5 Hz, H-3′, 5′)],表明结构中含有1个对位取代苯环;1个甲氧基氢信号 [H3.79 (3H, s, 4′-OCH3)];1个连氧的亚甲基氢信号 [H5.14 (1H, d,= 12.2 Hz, H-7′a), 5.11 (1H, d,= 12.2 Hz, H-7′b)];1个烯烃质子信号 [H6.80 (1H, t,= 1.4 Hz, H-2)] 和3个连氧次甲基氢信号 [H4.36 (1H, brs, H-3), 3.68 (1H, dd,= 7.1, 4.2 Hz, H-4), 3.99 (1H, dd,= 12.0, 5.1 Hz, H-5)];13C-NMR (100 MHz, CD3OD) 结合DEPT-135谱可观察到15个碳信号,包括4个季碳信号 (C129.6, 130.4, 161.2, 168.0)、8个次甲基碳信号 (C67.3, 68.4, 72.5, 114.9×2, 131.1×2, 139.2)、2个亚甲基碳信号 (C31.4, 67.4) 和1个甲氧基碳信号 (C55.7)。
在1H-1H COSY谱中(图1)可观察到H-2/H-3/H-4/H-5/H2-6相关,结合HMBC谱中H-2/C-4,6,7;H-4/C-2,6;H-5/C-1以及 H-6/C-2,4的远程相关可构建一个莽草酸结构片段。莽草酸结构片段的绝对构型主要通过与文献进行了光谱数据的比对[27]。最后,在HMBC谱中还可以观察到H-7′/C-1′,2′,6′,7的远程相关,确定结构中含有-甲氧基苯甲醇结构片段与莽草酸片段的C-7位羧酸成酯,因此确定了化合物1的结构。
化合物1的碳氢信号归属见表1,经SciFinder网络检索,化合物1为新的酚酸类化合物,命名为7---甲氧基苄基莽草酸,化合物结构见图1。
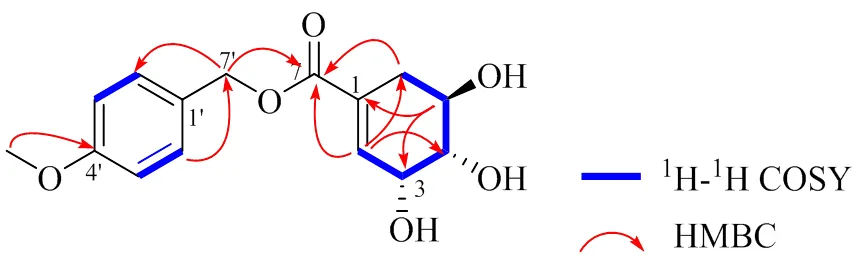
图1 化合物1的主要1H-1H COSY () 和HMBC ()相关
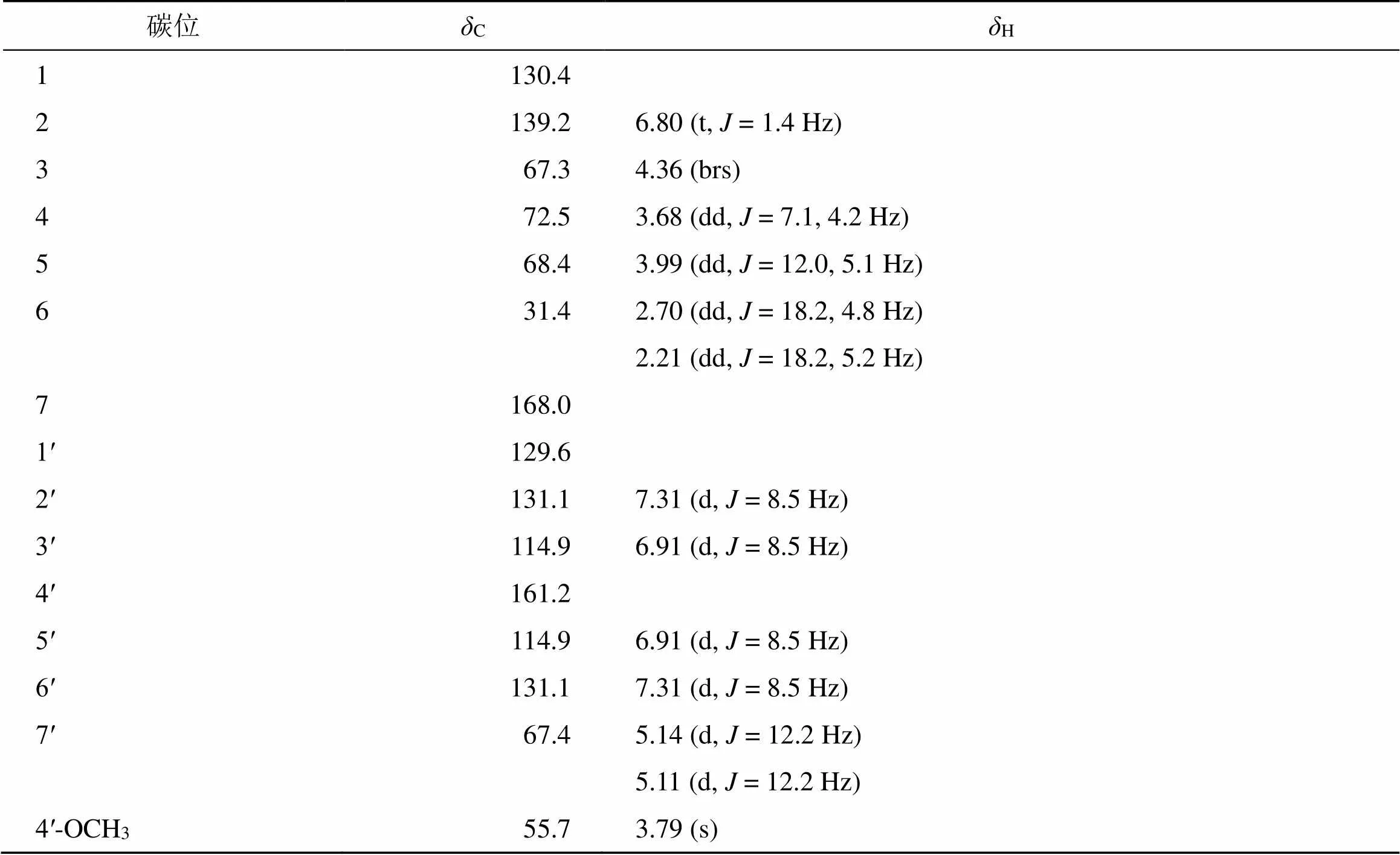
表1 化合物1的核磁数据 (400/100 MHz, CD3OD)
化合物2:白色粉末,HR-ESI-MS给出/219.099 9 [M+Na]+(计算值219.099 7),确定化合物分子式为C11H16O3,不饱和度为4。1H-NMR (400 MHz, CD3OD): 5.74 (1H, s, H-7), 2.43 (1H, dt,= 13.2, 2.6 Hz, H-4a), 1.99 (1H, dt,= 15.0, 2.6 Hz, H-2a), 1.76 (3H, s, CH3-11), 1.75 (1H, dd,= 13.2, 4.0 Hz, H-4b), 1.54 (1H, dd,= 15.0, 4.0 Hz, H-2b), 1.46 (3H, s, 9-CH3), 1.27 (3H, s, 10-CH3);13C-NMR (100 MHz, CD3OD): 185.7 (C-8), 174.4 (C-6), 113.3 (C-7), 89.0 (C-5), 67.3 (C-3), 48.0 (C-2), 46.4 (C-4), 37.2 (C-1), 31.0 (C-10), 27.4 (C-11), 27.0 (C-9)。氢谱、碳谱数据与文献报道一致[28],故鉴定化合物2为黑麦草内酯。
化合物3:黄色油状物,HR-ESI-MS给出/245.115 8 [M+Na]+(计算值245.115 4),确定化合物分子式为C13H18O3,不饱和度为5。1H-NMR (400 MHz, CD3OD): 7.00 (1H, d,= 15.8 Hz, H-7), 6.44 (1H, d,= 15.8 Hz, H-8), 5.94 (1H, s, H-4), 2.61 (1H, d,= 17.2 Hz, H-2a), 2.31 (3H, s, CH3-10), 2.27 (1H, d,= 17.2 Hz, H-2b), 1.91 (3H, s, CH3-13), 1.07 (3H, s, CH3-12), 1.03 (3H, s, CH3-11);13C-NMR (100 MHz, CD3OD): 200.7 (C-9), 200.4 (C-3), 164.6 (C-5), 148.4 (C-7), 131.7 (C-8), 128.0 (C-4), 80.0 (C-6), 50.5 (C-2), 42.7 (C-1), 27.6 (C-10), 24.7 (C-12), 23.5 (C-11), 19.2 (C-13)。氢谱、碳谱数据与文献报道一致[29],故鉴定化合物3 (+)-去氢催吐萝芙木醇。
化合物4:黄色油状物,HR-ESI-MS给出/247.131 2 [M+Na]+(计算值247.131 0),确定化合物分子式为C13H20O3,不饱和度为4。1H-NMR (400 MHz, CD3OD): 5.82 (1H, s, H-8), 4.20 (1H, m, H-3), 2.19 (1H, m, H-4a), 2.18 (3H, s, CH3-10), 1.92 (1H, m H-2a), 1.41 (1H, m, H-2b), 1.37 (6H, s, CH3-12, 13), 1.35 (1H, m, H-4b), 1.15 (3H, s, CH3-11);13C-NMR (100 MHz, CD3OD): 211.5 (C-7), 200.8 (C-9), 119.9 (C-6), 101.1 (C-8), 72.4 (C-5), 64.4 (C-3), 49.9 (C-2), 49.7 (C-4), 37.0 (C-1), 32.3 (C-12), 30.8 (C-13), 29.3 (C-11), 26.5 (C-10)。氢谱、碳谱数据与文献报道一致[30],故鉴定化合物4为蚱蜢酮。
化合物5:无色油状物,HR-ESI-MS给出/237.110 7 [M+Na]+(计算值237.110 3),确定化合物分子式为C11H18O4,不饱和度为3。1H-NMR (400 MHz, CD3OD): 5.79 (1H, s, H-2), 4.11 (1H, m, H-6), 2.48 (1H, ddd,= 11.7, 4.1, 2.2 Hz, H-5a), 2.02 (1H, ddd,= 13.0, 4.4, 2.2 Hz, H-7a), 1.60 (3H, s, CH3-11), 1.41 (1H, t,= 12.3 Hz, H-5b), 1.32 (3H, s, CH3-10), 1.30 (3H, s, CH3-9), 1.28 (1H, overlapped, H-17b);13C-NMR (100 MHz, CD3OD): 183.9 (C-1), 174.0 (C-3), 113.7 (C-2), 88.6 (C-4), 65.3 (C-6), 50.7 (C-7), 48.8 (C-5), 36.2 (C-8), 30.3 (C-10), 25.8 (C-11), 25.3 (C-9)。氢谱、碳谱数据与文献报道一致[31],故鉴定化合物5为chakyunglupulin A。
利益冲突 所有作者均声明不存在利益冲突
[1] WFO.Tutcher [DB/OL]. [2023-04-11]. http://www.worldfloraonline.org/taxon/wfo- 0001219855.
[2] 中国科学院中国植物志编辑委员会. 中国植物志 (第二十七卷) [M]. 北京: 科学出版社, 1979: 222.
[3] 林祁. 八角属药用植物资源 [J]. 中草药, 2002, 33(7): 654-657.
[4] 张连富, 林开中, 杨武德, 等. 红花八角原植物及易混品的鉴别 [J]. 中国中药杂志, 1995, 20(12): 717-718.
[5] Sy L K, Saunders R M K, Brown G D. Phytochemistry ofand the systematic position of the Illiciaceae [J]., 1997, 44(6): 1099-1108.
[6] Lai-King S, Brown G D. A sesquilignan from[J]., 1996, 43(6): 1417-1419.
[7] Kouno I, Morisaki T, Hara Y,. Two new sesquineolignans from the bark of[J]., 1991, 39(10): 2606-2608.
[8] Li J, Geng D, Xu J,. Antidepressant-like effect of macranthol isolated fromtutch in mice [J]., 2013, 707(1/2/3): 112-119.
[9] Bai J, Chen H, Fang Z F,. Sesquiterpenes and neolignans from the roots of[J]., 2012, 14(10): 940-949.
[10] Huang J M, Wang J L, Yang C S. Sesquiterpene lactones from the pericarp of[J]., 1997, 46(4): 777-780.
[11] Bai J, Chen H, Fang Z F,. Sesquiterpenes from the roots of[J]., 2012, 80: 137-147.
[12] Kouno I, Kawano N, Yang C S. New pseudoanisatin-like sesquiterpene lactones from the bark of[J]., 1988, 19(40):1537-1539.
[13] Brown G D. A sesquiterpene class from[J]., 1998, 47(2): 301-302.
[14] Bai J, Fang Z F, Chen H,. Antioxidant phenolic glycosides from the roots of[J]., 2012, 361: 206-211.
[15] Geng D, Weng L J, Han Y Y,. Flavonoids from[J]., 2012, 610/613: 3375-3377.
[16] Geng D, Weng L J, Han Y Y,. Chemical constituents from[J]., 2012, 550-553: 1586-1589.
[17] 张俊巍. 红花八角茎叶化学成分的研究 [J]. 中国中药杂志, 1989, 14(1): 36-37.
[18] 张俊巍, 张连富, 张水国. 红花八角精油化学成分的研究 [J]. 贵阳中医学院学报, 1988, 10(4): 57-59.
[19] 方玉珍, 宋杰云, 岑燕飞, 等. 毒八角酸的镇痛作用研究 [J]. 贵阳中医学院学报, 1989, 11(1): 59-62.
[20] 曾万玲, 宋杰云, 岑燕飞, 等. 红花八角醇提液对小鼠免疫功能的影响 [J]. 贵阳中医学院学报, 1992, 14(2): 60-62.
[21] 张俊巍, 宋洁云, 张连富, 等. 金红片治疗肝胃不和型慢性浅表性胃炎325例疗效观察 [J]. 中国中医药科技, 1998, 5(4): 251.
[22] 韦虹, 黄泰基, 苟忠萍, 等. 金红片治疗肝胃不和型胃脘痛临床观察 [J]. 现代中西医结合杂志, 2000, 9(5): 385.
[23] 陈峰. 金红片联合雷尼替丁治疗慢性浅表性胃炎临床观察 [J]. 临床合理用药杂志, 2010, 3(20): 69.
[24] Ma S J, Li H B, Li T,. Illiciumlignans G-O from the leaves ofand their anti-inflammatory activities [J]., 2021, 11(49): 30725-30733.
[25] Shao J R, Ma S J, Li T,. Two new chemical constituents from the leaves of[J]., 2023, 37(8): 1233-1240.
[26] Li H B, Ma S J, Shan Y X,. Eight new phenolic acids from the leaves ofand their osteoprotective activities [J]., 2022, 12(33): 21655-21661.
[27] Adam K P. Phenolic constituents of the fern[J]., 1999, 52(5): 929-934.
[28] Yang C S, Zhou T, Han S Q,. Alkaloids and terpenoids fromand their potential antiproliferative activity [J]., 2020, 56(4): 763-766.
[29] Kim I, Chin Y W, Lim S W,. Norisoprenoids and hepatoprotective flavone glycosides from the aerial parts ofvar.[J]., 2004, 27(6): 600-603.
[30] 李海波, 黄玉欣, 秦大鹏, 等. 青蒿中1个新的生物碱类化合物 [J]. 中草药, 2021, 52(2): 327-330.
[31] Kim K H, Clardy J, Senger D,. Chakyunglupulins A and B, two novel 4, 8, 8-trimethylcyclooct-2-enone derivatives from[J]., 2015, 56(21): 2732-2734.
A new phenolic acid from leaves of
SHEN Lang1, LI Xu2, CAO Liang2, WANG Zhen-zhong2, XIAO Wei2, GENG Jian-liang1
1. School of Traditional Chinese Medicine Guangdong Pharmaceutical University, Guangzhou 510006, China 2. National Key Laboratory on Technologies for Chinese Medicine Pharmaceutical Process Control and Intelligent Manufacture, Kanion Pharmaceutical Co., Ltd., Lianyungang 222001, China
To study the constituents from the dried leaves of.The chemical constituents were isolated by various chromatographic techniques and their structures were identified by physicochemical properties and nuclear magnetic resonance spectroscopic data of the compounds.Five compounds were obtained from ID-2 and characterized as 7---methoxybenzyl shikimic acid (1), loliolide (2), dehydrovomifoliol (3), grasshopper ketone (4), chakyunglupulin A (5), respectively.Compound 1 is a new phenolic acid, and compounds 2—5 are identified fromfor the first time.
Tutcher; 7--pmethoxybenzyl shikimic acid; loliolide; dehydrovomifoliol; grasshopper ketone; chakyunglupulin A
R284.1
A
0253 - 2670(2023)20 - 6592 - 04
10.7501/j.issn.0253-2670.2023.20.004
2023-05-18
2021年国家中医药管理局岐黄学者项目(国中医药人教函[2022]6号)
沈 浪,男,在读本科生。E-mail: 905154412@qq.com
通信作者:肖 伟,中国工程院院士,博士生导师,研究方向为中药新剂型研究与开发。E-mail: xw_kanion@163.com
耿剑亮,博士,研究方向为代谢组学,中药及天然药物活性成分研究。E-mail: gengjianliang8521@126.com
[责任编辑 王文倩]
