荞麦麸皮黄酮稳定性和抗氧化活性分析及其壳聚糖共混膜的制备
2023-10-19郭佩佩金丽娜
郭佩佩,李 琳,金丽娜,章 中,傅 婧
(宁夏大学食品科学与工程学院,宁夏银川 750021)
荞麦(Fagopyrum esculentumMoench.)是一年生草本植物,是药食同源食物[1],主要生产地有中国、俄罗斯、乌克兰、法国和波兰等地[2]。荞麦通常分为普通荞麦(甜荞)和苦荞。普通荞麦味甜,种子大,易于脱壳,消量高;苦荞味苦,种子小,皮包裹紧,不易脱壳。荞麦粉在加工过程中会产生大量的副产物荞麦麸皮,其中含有多种类黄酮,但因其口感较差,且不易被人体消化吸收,常被用作饲料或直接丢弃,致其浪费且污染环境。
黄酮类化合物是由三原子碳单元C6-C3-C6 连接而成的碳骨架[3],可分为花青素、黄烷酮、黄酮、异黄酮、黄酮醇和查耳酮[4],其具有重要的生物学特性,包括降血糖、降血压、降血脂、增强免疫力、抗炎[5]、抗癌[6]及抗病毒等生物活性。此外,黄酮类化合物作为抗氧化剂可以有效地清除自由基,从而维持体内的氧化平衡,并减弱自由基对机体的损害[7]。刘东旭[8]研究发现荞麦壳、荞麦麸皮及荞麦面粉中黄酮含量最高的是荞麦麸皮。因此,提取荞麦麸皮中的黄酮类化合物加以利用,可减少资源浪费提高经济价值。
壳聚糖(chitosan,CS)是甲壳素的衍生物,成膜性能良好,因此常被用作制备生物活性薄膜[9],但因其易溶于酸且分子量高,导致其抗氧化及抗菌活性弱,纯CS 膜不足以保护食品的氧化变质,从而限制了其在各种食品应用中的使用[10]。因此,将具有抗氧化性的生物活性物质掺入CS 薄膜中是改善CS 薄膜物理和生物学特性的有效途径。目前,通过添加具有抗氧化或抗菌活性的不同天然产物,例如细菌素、精油、植物提取物和酚类化合物,已经开发出许多基于CS 的共混膜[11]。在CS 膜中加入黄酮类化合物可提高共混膜的整体机械性能,减少壳聚糖分子内和分子间的氢键,从而增强共混膜的抗氧化及抗菌活性。何惠利等[12]发现蒲公英黄酮-壳聚糖共混膜能抑制微生物繁殖,延缓脂肪氧化,保持鸡胸肉的风味品质。
本研究以荞麦麸皮为研究对象,通过使用超声辅助提取法从荞麦麸皮中提取黄酮类化合物,对其稳定性及体外抗氧化活性进行研究,并制备荞麦麸皮黄酮-壳聚糖共混膜(BBF-CS),探究荞麦麸皮黄酮(buckwheat bran flavonoids,BBF)的添加量对共混膜性能的影响,以期制得性能较好的BBF-CS 共混膜,提高荞麦麸皮的经济价值及综合利用率,对促进荞麦麸皮的发展具有重要意义,同时可为BBF-CS共混膜在食品包装和保鲜中的应用提供更多参考。
1 材料与方法
1.1 材料与仪器
荞麦麸皮 陕西定边县(市场购买);芦丁标准品 上海源叶生物科技有限公司;壳聚糖、无水乙醇、乙酸、氢氧化钠、硝酸铝、铁氰化钾、三氯化铁、亚硝酸钠、丙三醇 分析纯,山东利尔康医疗科技股份有限公司。
SE-750 型高速粉碎机 圣象电器有限公司;BSA223S 型分析天平 赛多利斯科学仪器(北京)有限公司;TDL-5-A 型离心机 上海安亭科学仪器厂;V-5100 型可见分光光度计 上海元析仪器有限公司;SHZ-Ⅲ型循环水真空泵 郑州长城科工贸有限公司;RE-2000A 型旋转蒸发器 上海亚荣生化仪器厂;FD-1A-50 型真空冷冻干燥机 北京博医康仪器有限公司;BXH-280H 精密可程式烘箱 上海新黄医疗器械制造有限公司。
1.2 实验方法
1.2.1 BBF 提取 BBF 提取方法参考王昱儒等[13]方法稍作修改,将荞麦麸皮粉碎,过60 目筛,保存备用。称取荞麦麸皮粉与50%的乙醇溶液1:50 混匀,置于70 ℃超声波中超声80 min,离心(20 min,5000 r/min)后将上清液旋转蒸发,除去乙醇和水,置于-80 ℃冰箱,冷冻干燥得到BBF,置于干燥器内保存备用。
1.2.2 BBF 稳定性研究
1.2.2.1 pH 对BBF 的影响 称取一定质量纯化后的BBF 粉末用蒸馏水复溶,每支试管中放入等体积黄酮溶液,用氢氧化钠溶液和盐酸溶液调节pH 分别为1、3、5、7、9、11,做三组平行试验,将各试管中的黄酮溶液避光保存3 h,测定各试管中的黄酮含量,测定pH 对BBF 稳定性的影响。
1.2.2.2 温度对BBF 的影响 称取一定质量纯化后的BBF 粉末用蒸馏水复溶,每支试管中放入等体积黄酮溶液,将各试管分别置于4、25、50、70、90 ℃的温度条件下,做三组平行试验,将各试管中的黄酮溶液避光保存3 h,测定各试管中的黄酮含量,测定温度对BBF 稳定性的影响。
1.2.2.3 光照对BBF 的影响 称取一定质量纯化后的BBF 粉末用蒸馏水复溶,每支试管中放入等体积黄酮溶液,将各试管分别置于室外太阳光、室内自然光和室内避光条件下(10 月,宁夏大学农学院三楼)保存3 h,做三组平行试验,测定各试管中的黄酮含量,测定光照对BBF 稳定性的影响。
1.2.2.4 金属离子对BBF 的影响 称取一定质量纯化后的BBF 粉末用蒸馏水复溶,每支试管中放入等体积黄酮溶液,各添加0.1%的Na+、K+、Ca2+、Zn2+、Fe3+、Cu2+,做三组平行试验,将各试管中的黄酮溶液避光保存3 h,测定各试管中的黄酮含量,测定pH对BBF 稳定性的影响。
1.2.3 BBF 体外抗氧化活性分析
1.2.3.1 DPPH 自由基清除能力 参考盛丹丹[14]方法稍作修改,分别制备0.2、0.4、0.6、0.8、1.0 mg/mL的黄酮样液。在517 nm 下测定各反应吸光值,计算公式如下:
式中:A1表示DPPH 与黄酮反应的吸光值;A0表示无水乙醇与DPPH 反应的吸光值;A2表示无水乙醇与黄酮反应的吸光值。
1.2.3.2 铁还原力清除能力 参考陆庆[15]方法,分别制备2.0、4.0、6.0、8.0、10 mg/mL 的黄酮样液。在700 nm 下测定各反应吸光值,吸光值的高低反映了还原力的强弱。
1.2.3.3 ABTS+自由基清除能力 参考Wang 等[16]方法稍作调整,分别制备0.2、0.4、0.6、0.8、1.0 mg/mL的黄酮样液。在734 nm 下测定各反应吸光值,计算公式如下:
式中:A1表示ABTS+·溶液与黄酮反应的吸光值;A0表示ABTS+·溶液与蒸馏水反应的吸光值。
1.2.3.4 超氧阴离子自由基清除能力 参考李颖等[17]方法,分别制备0.2、0.4、0.6、0.8、1.0 mg/mL 的黄酮样液。在299 nm 下测定各反应吸光值,计算公式如下:
式中:A1表示Tris-HCL 缓冲溶液+黄酮+邻苯三酚+盐酸反应的吸光值;A0表示蒸馏水作为空白对照反应的吸光值;A2表示蒸馏水代替邻苯三酚反应的吸光值。
1.2.4 BBF-CS 共混膜制备 参考姜雪等[18]方法制作共混膜。2%乙酸35 mL+1 g 壳聚糖+0.3 g 甘油,50 ℃水浴30 min 搅拌,5%样液(0、5、10、15、20 mL),50 ℃水浴30 min 搅拌,室温超声20 min除气泡,20 mL 共混膜液倒入10 cm 平板,50 ℃烘干。
1.2.5 共混膜指标测定
1.2.5.1 共混膜厚度测量 共混膜厚度使用塑料薄膜测厚仪进行测量。在膜上随机选取几个位置重复测量,计算平均值。
1.2.5.2 共混膜透明度的测定 选取光滑、平整、洁净且无瑕疵的膜,将共混膜(1 cm×4 cm 样条)置于紫外分光光度计中,在600 nm 处测定试样膜的吸光度。未放置膜的单元作为参照样。试样膜的透明度以不透明度表示,计算公式如下:
式中:O 表示不透明度;Abs600表示试样在600 nm 下的吸光度;d 表示试样的厚度,mm。
1.2.5.3 共混膜颜色的测定 用色差仪测量膜的颜色,L*表示明亮度,它的值越大表明膜越亮白。a*表示红绿色,当a*的值大于0 时表示所占比重较大的颜色为红色,当a*的值小于0 时表示所占比重较大的为绿色;b*表示黄蓝色,当b*的值大于0 时表示所占比重较大的颜色为黄色,当b*的值小于0 时表示所占比重较大的颜色为蓝色。裁取大概8 cm×8 cm的待测膜,用色差计进行测定与记录数据。以标准白板为色差参比,总色差值△E按照以下公式计算。
式中:∆L*=L*-L0,∆a=a*-a0,∆b=b*-b0;L*,a*,b*表示实际测得的待测样品的数值;L0,a0,b0表示标准白板的数值。
1.2.5.4 共混膜含水率和水溶解性的测定 将完好无损的复合保鲜膜剪成2 cm×2 cm 大小。称重,并于105 ℃下干燥4 h,称重,放入装有40 mL 蒸馏水的锥形瓶中,室温下浸泡24 h,取出后于105 ℃下干燥4 h,称重,按下式计算膜的含水率与水溶性。
式中,MC 表示含水率,%;WS 表示溶解性,%;W0表示共混膜的质量,g;Wd表示共混膜干燥后的质量,g;Wt表示浸泡后再干燥共混膜的质量,g。
1.2.5.5 力学性能测定 共混膜力学性能测定参考李昊珍[19]方法。共混膜的力学性能通过测定抗拉强度和断裂伸长率来表示。将共混膜均匀裁减,使用电子万能试验机进行测定,初始距离为20 mm。
1.3 数据处理
使用Excel 2016 软件进行数据统计,Origin 2021b 软件进行绘图,SPSS 17.0 软件对数据进行显著性分析,以P<0.05 为差异具有统计学意义。所有试验均重复三次,结果以“平均值±标准差”表示。
2 结果与分析
2.1 BBF 稳定性研究
pH 对BBF 稳定性影响如图1a 可知,pH<7 时,BBF 含量随pH 的上升而显著升高(P<0.05),pH 大于7 时,BBF 含量随pH 的上升而降低。当pH=1或pH=11 时,BBF 含量较低,说明BBF 不适宜在过酸或过碱的环境中储存。pH 在5~7 时,黄酮含量最高。李慧等[20]发现从桑葚黄酮更适宜在弱酸性条件下贮藏,与此研究结果一致。这主要是因为BBF 分子的酚羟基结构,在碱性条件下酚羟基醚化[21],使得含量降低。因此,BBF 更适宜弱酸或中性环境,避免强酸强碱环境。
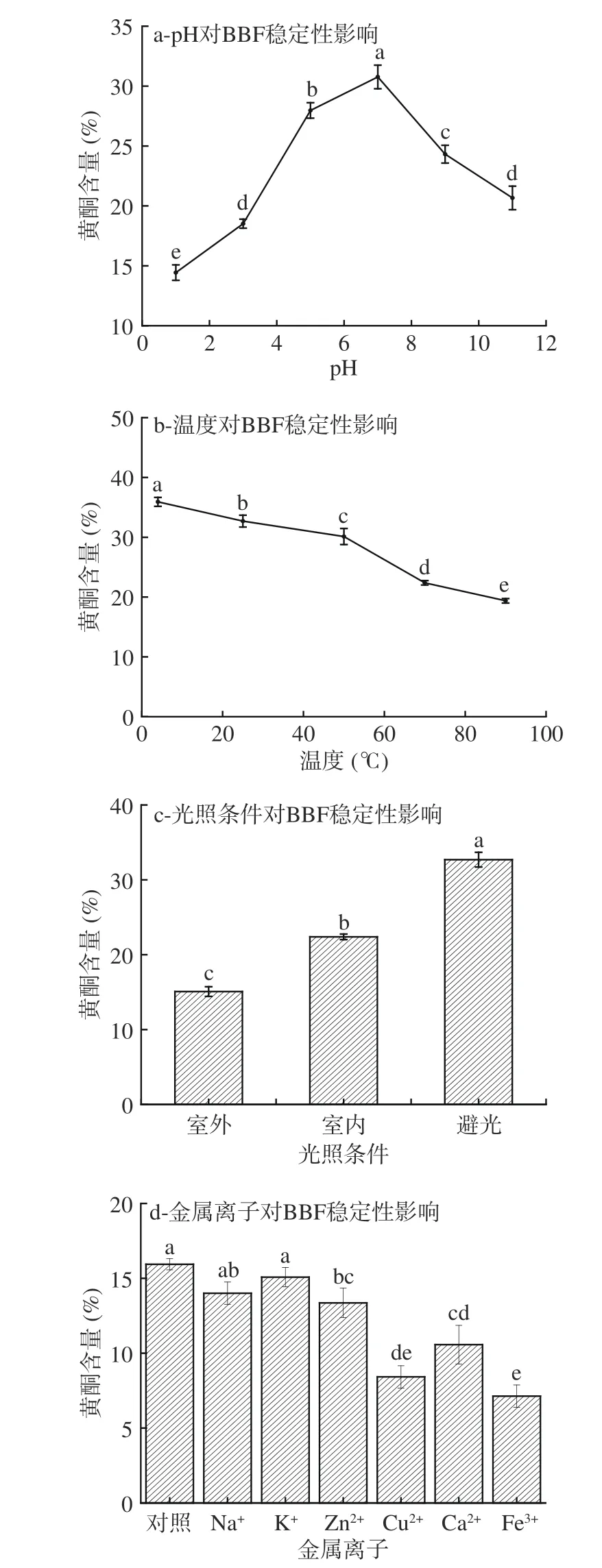
图1 pH、温度、光照条件以及金属离子对荞麦麸皮黄酮稳定性影响Fig.1 Effects of pH,temperature,light conditions and metal ions on the stability of buckwheat bran flavonoids
温度对BBF 稳定性影响如图1b 可知,随着温度的上升BBF 含量逐渐降低。4 ℃时黄酮含量最高,常温条件下黄酮含量无明显变化,大于50 ℃时,随着温度的持续升高黄酮含量下降显著(P<0.05)。由于温度的升高会加快分子间的运动,使得BBF 氧化分解速率加快。因此BBF 应在4 ℃或常温下贮藏加工,温度不宜超过50 ℃。
光照条件对BBF 稳定性影响如图1c 可知,不同光照条件会影响BBF 的稳定性。室外自然光保存时黄酮含量最低,而避光保存可以使BBF 保持稳定。这与黄琼等[22]对洛神花黄酮的稳定性试验结果一致,避光保存稳定性最好。这主要是因为黄酮对紫外线敏感,具有一定光敏性,自然光照射会加速黄酮分解[23],破坏黄酮结构。因此BBF 在贮藏加工过程中应尽可能避光保存。
金属离子对BBF 稳定性影响如图1d 可知,以对照组为参比,部分金属离子影响了BBF 的稳定性。在加入Na+、K+、Zn2+时,BBF 含量相对保持稳定,而Ca2+、Fe3+、Cu2+加入后,黄酮含量显著下降。这主要是因为这些金属离子会与黄酮类化合物的邻二酚羟基发生络合反应[24],破坏黄酮结构,且金属离子本身具有一定颜色,用吸光度法测定时也会造成影响。因此BBF 在加工过程中应该避免Ca2+、Fe3+、Cu2+的接触。
2.2 体外抗氧化活性分析
DPPH 自由基存在单电子,在乙醇溶液中呈现紫色,可与黄酮类化合物中的氧原子配对,使DPPH 自由基清除到稳定状态,其颜色变为黄色,在517 nm处存在特征吸收[25]。由图2a 可知,在一定浓度范围内,清除率与其浓度呈正相关。当浓度为1.0 mg/mL时,BBF(92.1%)和VC(98.7%)对DPPH 自由基清除率都达到最高。这与盛丹丹[14]从黄金茶提取黄酮对DPPH 的抗氧化效果一致,黄金茶黄酮和VC对DPPH 自由基清除率都达到了90%以上,抗氧化效果显著。由此可见BBF 是有效的抗氧化剂。
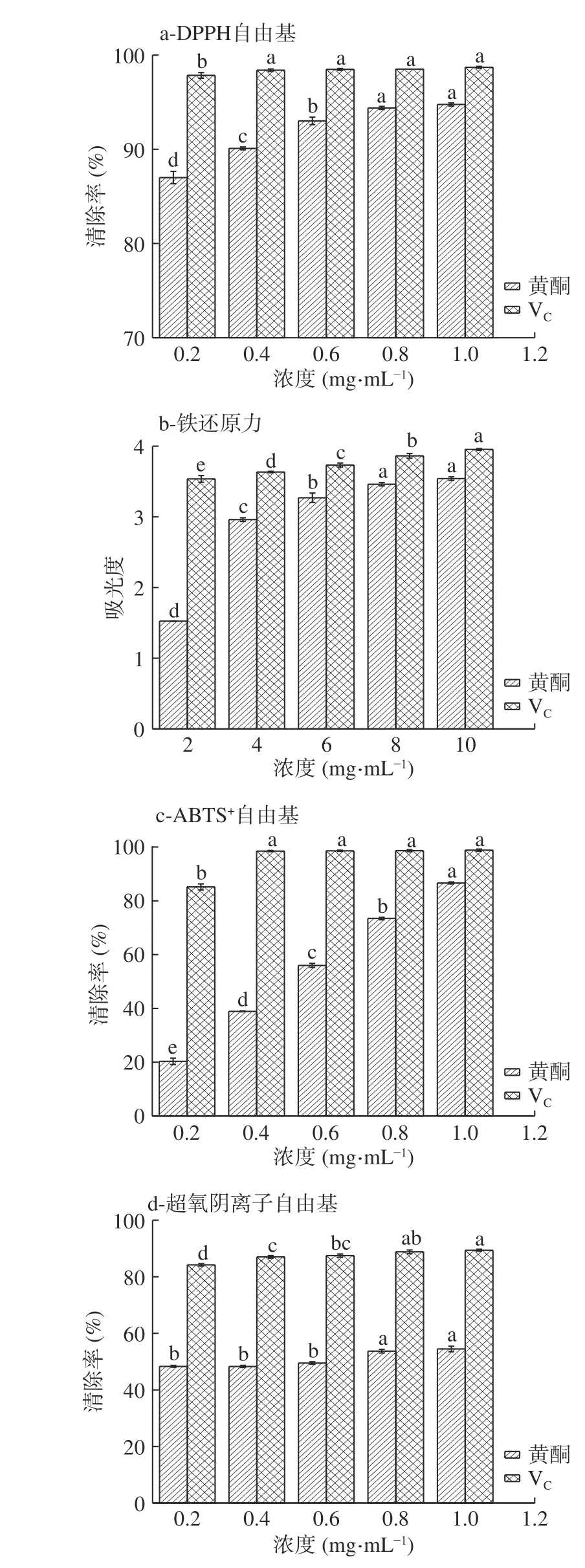
图2 BBF 与VC 清除自由基能力Fig.2 Free radical scavenging ability of buckwheat bran flavonoids and VC
铁氰化钾反应后结合生成普鲁士蓝,在700 nm下存在特征吸收。由图2b 可知,BBF 和VC在一定浓度范围内,其吸光度呈上升趋势。当浓度为10.0 mg/mL时,BBF 和VC还原力都达到最高,其吸光值分别为3.54、3.95。这与陆庆[15]从桃花提取黄酮对铁还原力的能力相同,随着浓度的升高,桃花黄酮和VC吸光值也升高,还原力提高,抗氧化活性增强。由此可见BBF 具备铁离子还原能力。
ABTS 氧化生成ABTS+自由基,呈蓝绿色,在734 nm 处具有特征吸收,与黄酮反应后,抑制了ABTS+自由基的生成,吸光度在其最大波长下降低[26]。由图2c 可知,BBF 和VC在一定浓度范围内,其ABTS+自由基清除率逐渐升高。当浓度为1.0 mg/mL 时,BBF(87.7%)和VC(98.84%)对ABTS+自由基清除率都达到最高。这与Wang 等[16]从黄花菜叶提取黄酮对ABTS+自由基的抗氧化效果一致,当类黄酮浓度达到0.35 mg/mL 时,类黄酮对ABTS+自由基清除率达到95.60%,接近了抗坏血酸的清除率。由此可见BBF 可以有效地清除ABTS+自由基,是良好的抗氧化剂。
邻苯三酚在碱性条件下与黄酮反应会抑制其自动氧化而生成超氧阴离子,从而达到抗氧化效果。由图2d 可知,BBF 和VC在一定浓度范围内,对超氧阴离子自由基清除率缓慢升高。当浓度为1.0 mg/mL时,荞麦麸皮(53.81%)和VC(89.41%)对超氧阴离子自由基清除率都达到最高。这与李颖等[17]分析黄晶果皮黄酮对超氧阴离子的抗氧化效果一致,黄晶果皮黄酮对超氧阴离子自由基的清除率与浓度呈正相关,有抑制作用。由此可见BBF 可以有效的清除超氧阴离子自由基。
2.3 BBF-CS 共混膜性能测定
2.3.1 BBF-CS 共混膜厚度及不透明度 薄膜的厚度是评价食品包装性能的一个重要指标,过厚或过薄都不适宜用作包装材料。由表1 可知,随着BBF 添加量的增加,薄膜厚度逐渐增加,呈正比例趋势。当BBF 添加量达到20 mL 后,薄膜厚度从0.0684 mm增加到0.0953 mm。由于薄膜在制作过程中,倒平板的膜液质量和烘干时间都相同,但共混膜厚度不同,因此BBF 的添加量会影响薄膜分子之间的排列结构。这主要是因为CS 中存在大量的羟基物质,BBF可增加交联与CS 结合,从而导致CS 与BBF 之间的距离变短,薄膜表面形成堆积[27],使得薄膜厚度增加。此外,BBF 的存在破坏了CS 聚合链的有序排列,分子以更松散的方式排列,使BBF-CS 共混膜表面形成致密突出的结构[28],且共混膜的固形物含量也随之增加,使得薄膜厚度增加[29]。
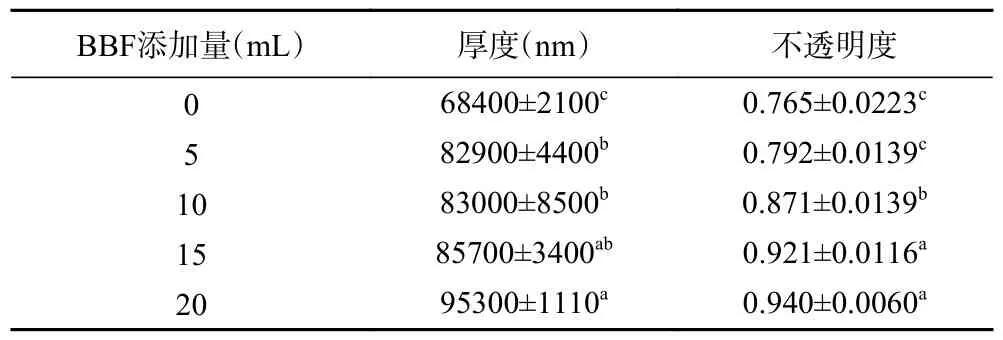
表1 BBF 添加量对共混膜厚度及不透明度影响Table 1 Effects of BBF addition on the thickness and opacity of composite film
对于易受光照影响的食品,包装材料的不透明度也是保障食品营养品质的重要特性,薄膜包装食品暴露在紫外可见光下时,很容易被氧化,导致食品营养损失、变色和产生异味。在可见光和紫外线的作用下,氧气能迅速从基态转变为激发态,导致包装食品氧化变质[30]。BBF-CS 共混膜的不透明度如表1可知,BBF 的加入增加了薄膜的不透明度。当BBF添加量达到20 mL 后,薄膜不透明度由0.765 增加到0.940。CS 共混膜的不透明度低是由于缺乏紫外可见吸收基团,而BBF 分子中的芳香基团对紫外光、可见光以及一些低能辐射表现出优异的紫外阻隔性能。此外,BBF 与CS 之间的交联会增加薄膜的致密性,从而对紫外线和可见光产生抵抗力,防止薄膜包装食品的氧化变质。
2.3.2 BBF-CS 共混膜色度 薄膜的颜色通常会影响薄膜包装食品对消费者的接受程度,CS 膜与BBFCS 共混膜的L*、a*、b*、∆E如表2 所示。添加BBF后,薄膜的L*和 ∆E值显著降低(P<0.05),表明BBF 的添加使得薄膜亮度降低,逐渐变暗;a*代表的是薄膜的红度,无显著变化;b*代表薄膜的黄度,薄膜黄度逐渐增加,这是因为BBF 存在有色化合物,呈现为淡黄色,添加后会使薄膜黄度增加。这与平雪丽对山奈提取物改性壳聚糖膜的颜色变化结果一致。

表2 BBF 添加量对L*、a*、b*及 ∆E值影响Table 2 Effects of BBF addition on L*,a*,b* and ∆E values
2.3.3 BBF-CS 共混膜含水率、水溶解性 水分含量反映了潮湿环境中薄膜的吸湿特性。CS 膜与BBFCS 共混膜的含水量如图3 所示。CS 膜的含水量最高,这是由于水分子与壳聚糖官能团之间的强氢键相互作用导致的。随着BBF 的加入,共混膜的含水量由28.37%降至20.35%。这是因为BBF 分子中的羟基和羧基可以与CS 中的亲水基团相互作用,使得薄膜更致密,从而阻碍了壳聚糖与水分形成分子间氢键,限制了薄膜的吸水能力,使得水分含量降低。当苹果皮多酚与壳聚糖复配时,也可观察到类似的结果[31]。
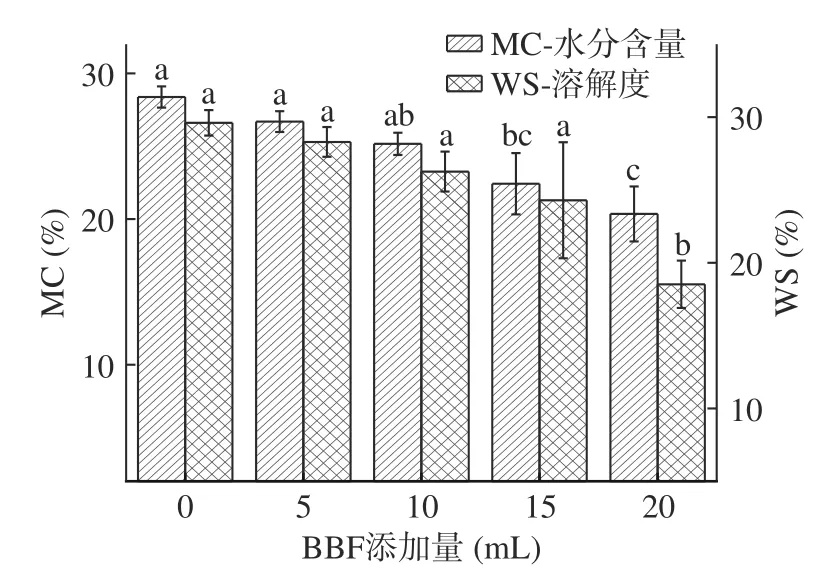
图3 BBF 添加量对水分含量及溶解度影响Fig.3 Effect of BBF addition on water content and solubility
溶解度用于反映天然包装薄膜的耐水性,其主要与薄膜的亲水性和疏水性有关,溶解度越低,表明薄膜的水溶性越好。CS 膜与BBF-CS 共混膜的溶解度如图3 所示。CS 膜的溶解度最高,这主要是因为CS 膜自身含有氨基等亲水性基团。薄膜的溶解度随BBF 的添加逐渐降低(P<0.05),这主要是因为BBF 中存在大量的疏水性基团苯环,与CS 分子中的亲水性基团相互作用,发挥作用的亲水基团减少,且增加了共混膜的疏水性,提高了生物聚合物的界面结合特性,从而使得薄膜溶解度降低[32]。
2.3.4 BBF-CS 共混膜力学性能 力学性能是描述薄膜在食品包装、运输及贮藏过程中承受应力的能力,包括抗拉强度和断裂伸长率,其反映了共混膜的强度和柔韧性。通常,薄膜的力学性能取决于加入的活性化合物的类型和含量,聚合物基质的种类以及不同组分之间的特定相互作用。CS 膜与BBF-CS 共混膜的抗拉强度和断裂伸长率如图4 所示。随着BBF 的添加,薄膜的抗拉强度呈下降趋势(P<0.05),这主要是因为BBF 对CS 薄膜内部结构的破坏力强于两者的氢键结合力,使其变形抗力减弱,最终加入BBF 的共混膜的拉伸强度低于CS 膜。并且,酯类可以打乱聚合物结构中的结晶顺序,降低CS 的结晶度,从而削弱分子间相互作用并降低拉伸强度[33]。此外,薄膜表面也会出现少量的不溶性颗粒,从而影响了薄膜的致密性,使得抗拉强度下降。薄膜的断裂伸长率也受BBF 含量的影响。随着BBF 含量的增加,BBF-CS 共混膜的断裂伸长率呈下降趋势,从71.63%降至44.75%,降低了薄膜的柔韧性,提高了刚性。这表明CS 膜在BBF 的加入后运动受到很大的限制,BBF 会在共混膜中发生聚集导致分子间氢键弱化,阻碍BBF-CS 链的相互作用,影响薄膜致密稳定结构的形成,造成膜的机械性能下降[34]。

图4 BBF 添加量对抗拉强度及断裂伸长率影响Fig.4 Effect of BBF addition on tensile strength and elongation at break
3 结论
本研究以荞麦麸皮为原料,采用超声辅助提取法提取BBF,通过稳定性研究表明,BBF 应贮藏于弱酸(pH5~7)环境中避光常温保存,且不易与Ca2+、Fe3+、Cu2+的接触。BBF 对DPPH 自由基(92.1%)、铁还原力(3.54)、ABTS+自由基(87.7%)和超氧阴离子自由基(53.81%)的清除能力良好,在体外具有很强的抗氧化活性,是一种天然的抗氧化剂。通过测定BBF-CS 共混膜的性能,表明BBF 的加入会显著增加薄膜的厚度、不透明度和黄度值,而含水率、溶解度、抗拉强度及断裂伸长率显著降低(P<0.05)。因此BBF 的加入可提高共混膜的性能,但共混膜的柔韧性等方面还需进一步优化。该实验结果表明BBF与CS 复合成膜,提高CS 膜的抗氧化性及其机械性能,为CS 膜在食品包装方面的应用提供了数据支撑。
