靓竹彩叶形成的细胞学以及光合色素*
2023-10-19徐薪璐赵婉琪姚文静林树燕
徐薪璐 蔡 鸥 赵婉琪 吕 卓 姚文静 李 龙 林树燕
(1. 南京林业大学 南方现代林业协同创新中心 南京 210037;2. 南京林业大学竹类研究所 南京 210037;3. 南京林业大学生物与环境学院 南京 210037)
叶是植物进行光合作用的重要器官。彩叶植物是长时间内叶片呈现如紫色、金色、红色、条纹等非绿色的植物(何冰,2006),彩叶植物在叶片生长过程的某个阶段会出现变色期,这种叶色变化与叶绿素含量、叶绿体发育程度有关。叶绿素代谢是一个复杂的过程,中间任何一个过程受抑制均会引起叶绿素的大量累积或降解从而引起叶色变异。目前,关于彩叶植物叶色呈色机制的研究多集中于银杏(Ginkgo biloba)(王改萍等, 2020)、 紫叶李(Prunus cerasifera)(高艳等,2014)、金叶女贞(Ligustrum vicaryi)(郑健等,2012)、鸡爪槭(Acer palmatum)(蔡雪雁等,2015)、槭树(Acer pseudosieboldianum)(姜楠南等,2013)等较为常见的彩叶植物上,也有一些研究从分子水平研究彩叶产生的机制,如杨树(Populus)中AP3的过表达诱导叶片衰老并降低叶绿素含量(Duet al.,2022)。Zhou等(2022)在绿白叶观赏羽衣甘蓝(Brassica oleracea)中鉴定出PSBQ、LHCB1.3、LHCB2.4和HSP70是叶绿体形成的关键基因(Zhouet al.,2022)。
许多观赏彩叶竹种特点为全绿色叶片上出现黄色或白色条纹。 杨海芸(2015)在花叶矢竹(Pseudosasa japonicaf.akebonosuji)中发现ELIPs基因参与调控叶绿体发育,抑制色素合成。黄滔等(2016)对 白 纹 阴 阳 竹(Hibanobambusa tranquillans‘Shiroshima’)、 鼓 节 竹 (Bambusa tuldoides‘Swolleninternode’)、花秆早竹(Phyllostachys violascens‘Viridisulcata’)和美丽箬竹 (Indocalamus decorus)4 个观赏竹种的光合特性进行了比较研究,探究各竹种叶片的光合能力。陈凌艳等(2017)对银丝竹(Bambusa multiplex‘Silverstripe’)不同叶色叶片的光合色素含量、叶绿素合成前体相对含量及叶片显微和超微结构研究发现,叶绿素合成受阻、叶绿体发育异常是叶色变异产生的原因。徐胤(2020)在白化类型的绿竹(Bambusa oldhamii)中发现PIFs 通过抑制PEP 的转录活性,下调参与叶绿素生物合成相关基因,导致绿竹中的叶绿体发育异常,进而叶绿素合成受阻。
靓竹(Sasaella glabra‘Albostriata’)为禾本科(Poaceae)竹亚科((Bambusoideae))东笆竹属竹种,高度20~40 cm,直径0.1~0.2 cm,叶片具3~5 条黄色条纹,为优良地被类观赏植物。1984 年周芳纯从日本引至南京林业大学,目前已广泛分布在我国华东、华北地区。该种可作为竹坪、林下绿化或作为盆栽观赏竹,还可用于矿区土壤修复,山坡绿化,避免水土流失。靓竹叶色在叶片发育过程中形成,且能够稳定遗传。目前,对于彩叶竹种叶色形成原因的研究都集中在成熟功能叶,而对于叶片发育过程中叶色形成的研究尚未见报道。鉴于此,本研究以不同发育阶段的靓竹叶片为材料,通过比较各时期叶片显微结构、超微结构、光合色素以及叶绿素合成前体物质,同时对成熟功能叶的黄区和绿区的表皮结构、细胞内部结构、光合色素进行比较,分析竹叶内部结构形态及光合色素合成在不同时期及不同叶色分区的差异,为探讨靓竹彩叶形成机制提供基础依据。
1 材料与方法
1.1 试验材料
试验所需靓竹叶片于2022 年4—5 月采自南京林业大学白马苗圃繁育基地(119°10'35″ E,31°36'19″ N)。叶片按照生长发育及叶色变化特征分为S1、S2、S3和S4 4 个时期(表1,图1),成熟功能叶根据叶色分为黄区(yellow stripe,YS)和绿区(green stripe,GS)。靓竹集中于4—6 月抽枝展叶。

图1 靓竹不同发育时期叶片发育过程中形态Fig. 1 Appearance of morphological characteristics at different developmental stages of S. glabra ‘Albostriata’

表1 靓竹叶片不同发育时期特征描述Tab. 1 Description of leaf characteristics at different developmental stages of S. glabra ‘Albostriata’
1.2 试验方法
1.2.1 靓叶片发育过程中内部结构观察 1)光学显微镜观察显微结构:分别取靓竹叶片4 个发育时期各15 片, 选取S1、 S2 时期的叶片放入50% FAA(formaldehyde-acetic acid-alcohol)固定液中,S3、S4 时期的叶片放入70% FAA 固定液中,固定2 天以上,待用,每个时期样品至少3 个生物学重复。固定后取S1、S2 时期的叶片中段、S3、S4 时期的叶片及S4 时期叶片YS、GS 区切取中部以主脉为中轴10 mm×5 mm 大小区域,置于25% HF(氢氟酸)中软化48~72 h。采用常规石蜡切片技术(李正理,1987)切片,乙醇梯度脱水,二甲苯透明,石蜡包埋,Leica RM 2255 自动切片机切片(厚度为 8 µm) ,番红—固绿双重染色法染色,中性树胶封片,Leica DM 2500 光学显微镜选取成熟叶片沿主脉左右对称视野拍照观察。Leica LAS X 软件对叶片厚度、上表皮厚度、下表皮厚度、梅花状细胞长度、指状臂细胞长度、梭形细胞空隙长度、泡状细胞长度、主脉面积、侧脉(1 级脉、2 级脉)面积进行测量。每个时期的叶片选取10 个切片,每个切片选取10 个视野观测,每个时期测量至少50 个数据。此外,将靓竹S4 时期叶片的黄绿条纹区域分开分别放入PBS 溶液中固定,制作方法参考张书敏等(2015),将制作好的徒手切片置于Leica DM 2500 光学显微镜下观察,利用Leica LAS X 软件拍照,黄绿两区各选取10 个视野观测。
2)透射电镜观察超微结构:分别取靓竹的4 个时期叶片各3 片,其中已经出现条纹叶色的S2、S3、S4时期要将黄区和绿区分开取样,避开叶脉切取叶片的三角形叶块(2 mm×2 mm,底×高),置于2%戊二醛混合固定液(pH 7.0) 中,抽气使叶片下沉,4 ℃下固定24 h,每个样品至少设置3 个重复。固定后参考 Hall等(1991)的方法,磷酸缓冲液冲洗 3 次后,乙醇逐级脱水,丙酮置换,LR. white 树脂包埋,Leica EM UC6 超薄切片机切片(切片厚度约为 90 nm),醋酸双氧铀和柠檬酸铅双重染色,在电子透射电镜 JEM-1400 下拍照观察。
3)扫描电镜观察超微结构:取新鲜S4 时期叶片洗净,将叶片区别YS 和GS 区修剪成0.5 cm × 0.5 cm的小块于FAA 固定液中固定24 h,脱水后真空镀膜,在PHILIPS XL30 ESEM 扫描电镜下观察表皮系统。
1.2.2 光合色素含量的测定 对各发育时期叶片及S4 时期叶片的YS、GS 区进行光合色素含量测定。提取方法参考 Hodgins 等(1986)的方法,每个样品3个重复。按照下列公式计算叶绿素a、叶绿素b、总叶绿素和类胡萝卜素的含量。
式中:Ca、Cb、C(x+c)分别代表叶绿素a、叶绿素b、类胡萝卜素含量(mg·g-1),A为吸光值,V为提取液总体积(mL),若稀释则乘以相应的倍数,W为叶片鲜质量(g)。
1.2.3 叶绿素合成前体物质的测定 5-氨基乙酰丙酸(5-aminolevulinic acid, ALA)含量的测定:根据Dei(1985)的方法稍加改动,取混合液2 mL 加入2 mL显色液(Ehrlich-Hg 试剂),黑暗处理15 min 后测定553 nm 处的OD 值。并按下述公式计算ALA 摩尔浓度:A=ε·C·L,其中A为吸光值,ε 为摩尔消光系数(ALA 的含量以553 nm 处的摩尔消光系数7.2×104L·mol-1cm-1计算),C为摩尔浓度,L为测试液的液层厚度。
卟啉原(porphobilinogen, PBG)含量的测定参照Bogorad(1962)的方法稍加改动,取混合液2 mL,加入2 mL 显色液(Ehrlich-Hg 试剂),黑暗中放置15 min 后,测定553 nm 处的OD 值。
按下述公式计算PBG 摩尔浓度:A=ε·C·L,其中A为吸光值,ε 为摩尔消光系数(PBG 的含量以553 nm处的摩尔消光系数6.1×104L·mol-1cm-1计算),C为摩尔浓度,L为测试液的液层厚度。
尿卟啉原III(UrogenIII)和粪卟啉原III(CoprogenIII)含量的测定参照Bogorad(1962)的方法稍加改动,按下述公式计算摩尔浓度:A=ε·C·L,其中A为吸光值,ε为摩尔消光系数(UrogenIII 含量以405.05 nm 处的摩尔消光系数5.48×105L·mol-1cm-1计算;CoprogenIII 含量以399.5 nm 处的摩尔消光系数4.89×105L·mol-1cm-1计算),C为摩尔浓度,L为测试液的液层厚度。
原卟啉IX(ProtoIX)、镁原卟啉IX(Mg-ProtoIX)和原脱植基叶绿素(Pchlide)的测定参照Hodgins 等(1986)的方法,根据下列公示计算原卟啉IX(ProtoIX)和原脱植基叶绿素(Pchlide)的含量:
式中,E、F分别为摩尔消光系数、OD 值,下标为nm 值。
镁原卟啉IX(Mg-ProtoIX)的相对含量以E400F595值直接表示。
1.3 数据处理
使用SPSS 19.0 进行数据统计和方差分析,利用Graphpad Prism 9 作图,Microsoft PowerPoint 作表,图表中所有数据值均为重复测定的平均值。
2 结果与分析
2.1 靓竹不同发育时期叶片内部细胞结构观察
靓竹叶片各发育时期内部细胞显微结构变化如图2a–e 所示。不同发育时期的叶片内部显微结构差异较大。S1 时期叶片卷曲未露出叶鞘,因此整个叶片嫩黄白色,此时期的叶片内部细胞界限不清晰,细胞核大,组织分化程度低,维管系统初步分化但无明显的主侧脉之分,上下表皮无明显差异(图2a)。S2 时期叶片卷曲、刚露出叶鞘,初步出现条纹叶色,此时期的叶片内部细胞相对清晰,细胞壁加厚,细胞核近似圆形,组织分化程度较明显,维管系统分化出明显的1 级侧脉和2 级侧脉,主脉和1 级侧脉的差异不显著,下表皮出现乳突结构,上下表皮差异显著(图2b)。S3 时期叶片由卷曲逐渐展平,叶片出现稳定的条纹叶色,此时期叶片内部细胞界限清晰,细胞壁加厚,组织分化程度高,可观察到明显的梅花状细胞、指状臂细胞、泡状细胞和梭形细胞,维管束完整,有清晰的主侧脉之分,上下表皮差异显著,下表皮乳突结构清晰(图2c)。S4 时期为功能叶,叶片展平,细胞结构与S3 时期类似(图2d–e)。功能叶绿区(图2d)和黄区(图2e)叶片显微结构差异较大,区别在于绿区上表皮附近的指状臂细胞有2~3 层且结构清晰、排列紧密;而黄区叶肉细胞中仅有1 层清晰可见的指状壁细胞紧贴上表皮,其余叶肉细胞无明显指状臂细胞和梅花状细胞的区别。叶片黄区和绿区着色程度不同,绿区细胞较易染色。随着发育过程的推进,叶片厚度、上下表皮、叶肉厚度均不断增厚(表2),叶脉面积不断增加,前期主脉和1 级侧脉差异较小,S3 到S4 时期主脉发育速度最快(表3)。

图2 靓竹叶片不同发育时期内部细胞结构观察Fig. 2 Microstructure comparison of S. glabra ‘Albostriata’ in different stages
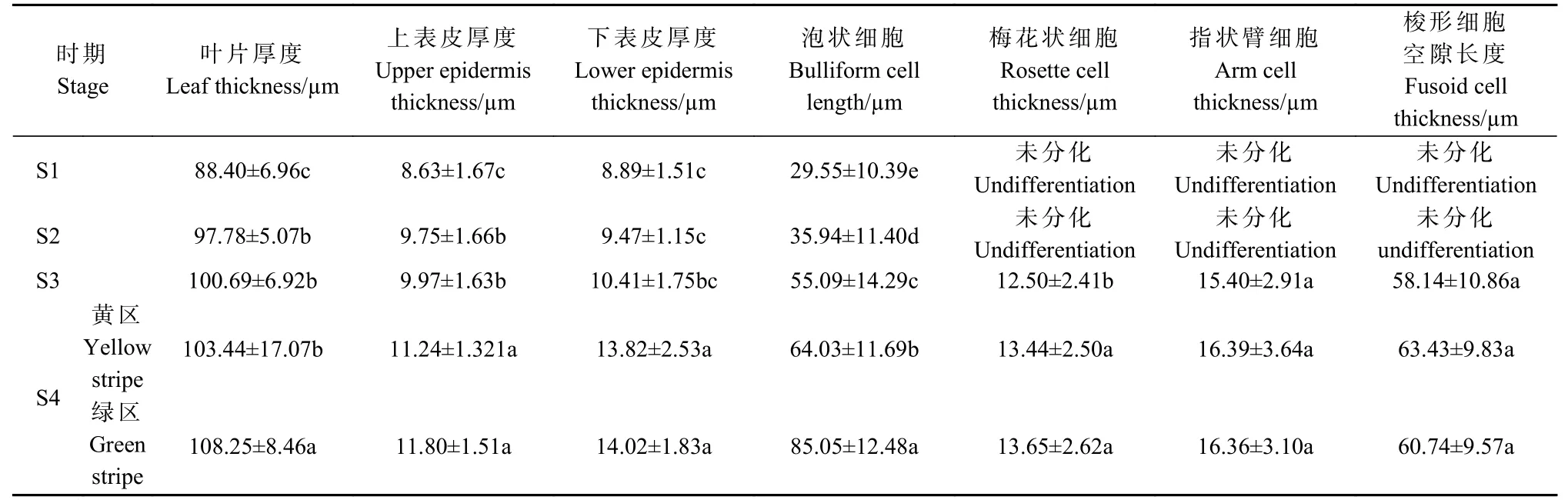
表2 靓竹叶片不同生长阶段显微结构指标(一)①Tab. 2 Leaves microstructure parameters in S. glabra ‘Albostriata’

表3 靓竹叶片不同生长阶段显微结构指标(二)①Tab. 3 Leaves microstructure parameters in S. glabra ‘Albostriata’
2.2 靓竹不同发育时期叶片超微结构观察
靓竹S1 时期叶肉细胞较小,形状相对规则,细胞排列紧密,未出现梅花细胞和指状臂细胞的分化(图3a1);细胞壁薄;细胞核大质浓,成分生细胞状态(图3a2);线粒体数目较多,多靠近细胞壁分布;细胞质中散布核糖体和高尔基体等细胞器(图3a3);未出现明显的叶绿体结构,有较大的淀粉粒出现在原质体中(图3a4)。
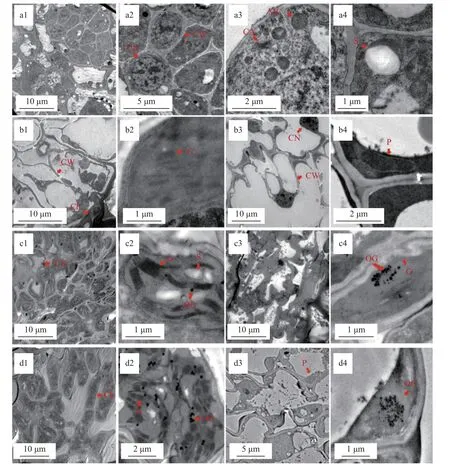
图3 靓竹不同发育时期叶片超微结构观察Fig. 3 Ultrastructure comparison of S. glabra ‘Albostriata’ in different stages
靓竹叶片S2 期初步出现条纹,绿区各类型细胞壁较S1 时期加厚;叶肉细胞开始出现梅花状细胞和指状臂细胞的初步分化(图3b1);多数细胞内有较大面积的空洞,部分发育中的细胞内部细胞核大质浓;细胞器较少;原质体开始向叶绿体转化,靠近细胞壁分布,但叶绿体数量较少且内部结构不清晰,少数类囊体片层垛堞成基粒,基粒数量少且分散(图3b2)。同时期黄区细胞结构如图3b3,此时期细胞壁较S1 时期加厚;叶肉细胞开始出现梅花状细胞和指状臂细胞的初步分化;相较于绿区,更多细胞内有较大面积的空洞,部分发育中的细胞内部细胞核大质浓;线粒体饱满;原质体靠近细胞壁分布,无明显叶绿体结构(图3b4)。
靓竹叶片S3 期绿区叶肉细胞多分化为梅花状,细胞壁加厚,细胞核不明显,细胞空腔面积小,无明显细胞器(图3c1);质体靠近细胞壁附近分布,叶绿体数量多且内部结构清晰,内部有小型淀粉粒和嗜饿颗粒,嗜饿颗粒分散分布,类囊体垛叠层数多,基粒间距大、片层多(图3c2)。同时期黄区细胞如图3c3 所示,同样观察到细胞壁加厚、细胞核不明显的现象,相较于S2 时期黄区细胞空腔面积缩小,细胞器减少,叶绿体数量少且发育不完全,内部有嗜饿颗粒集中分布(图3c4)。
如图3d1 所示,S4 绿区的叶肉细胞形状清晰,完全分化为梅花状结构和指状臂结构,细胞内无明显空腔,细胞壁加厚,细胞核不明显,无明显细胞器;质体靠近细胞壁附近分布,叶绿体数量多且面积大,基粒数量多且排列密集,内部有嗜饿颗粒分散分布(图3d2)。黄区细胞中可观察到大面积空腔,与绿区相似,同样出现细胞壁加厚,细胞核不明显,无明显细胞器的现象(图3d3);质体靠近细胞壁分布,无清晰叶绿体结构,淀粉粒大且数量多,嗜饿颗粒集中分布(图3d4)。
2.3 靓竹叶片YS 和GS 的徒手切片及扫描电镜观察
通过徒手切片可以看出黄区YS 及绿区GS 的叶绿体数量以及分布有明显差别。黄区的叶绿体数量明显少于绿区。绿区的叶绿体在上下表皮间叶肉细胞中均有分布(图4a),黄绿交界区域的叶绿体主要集中分布在下表皮附近的梅花状细胞中,靠近上表皮的指状壁细胞中叶绿体分布很少(图4b),而黄区(图4c)叶肉细胞呈黄色,无明显叶绿体分布。

图4 靓竹分区徒手切片观察Fig. 4 Microscopic structure of hand sectioning of different stripes of S. glabra ‘Albostriata’
显微结构观察(图5),与石蜡切片类似,靓竹叶片的黄区(图5i、l)及绿区(图5c、f)的叶表皮及横切面结构差异明显,绿区叶片厚于黄区叶片,且绿区叶片内部细胞排列紧密。二者上表皮(图5a、g)均较为平整,能够清晰地分辨出叶脉部分和脉间部分,少有附属物;下表皮(图5b、h)均着生密集的乳突,绿区的乳突密度较黄区的乳突密度大;乳突有大乳突和小乳突两种类型,大乳突为三角状,小乳突为颗粒状,大乳突体积约为小乳突的10 倍,少数区域有须状刺挠着生(图5d、j);二者在下表皮的颗粒状乳突中有气孔分布(图5e、k),且气孔形状类似,均为狭长椭圆形,气孔两端各有2 个小乳突,区别在于绿区气孔数目较黄区多。
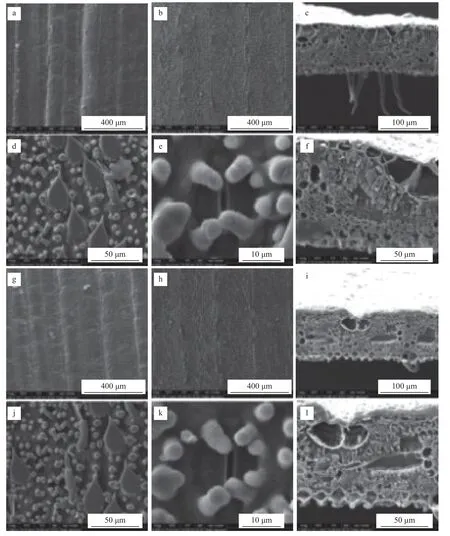
图5 靓竹叶片分区的表皮及叶片横切面的超显微结构观察Fig. 5 Ultrastructure of epidermis and transsections of S. glabra ‘Albostriata’ in different stripes
2.4 靓竹叶片光合色素的测定
光合色素是导致叶色变化的重要因素,提取靓竹不同时期叶片的叶绿素a、叶绿素b、叶绿素、类胡萝卜素,由表4 可知,叶绿素a、叶绿素b、叶绿素、类胡萝卜素的含量均随着发育而逐渐增加。S1、S2 期叶绿素a、叶绿素b、叶绿素、类胡萝卜素含量较低,且差异不显著(P>0.05),发育到功能叶差异较为显著(P<0.05)。

表4 靓竹不同时期叶片光合色素含量变化①Tab. 4 Changes of leaves photosynthetic pigment content during different stages of S. glabra ‘Albostriata’
将靓竹叶片分为黄区和绿区分别测定各区光合色素,并与靓竹完整叶片进行比较分析,由表5 可知,叶片黄区及绿区各光合色素均存在显著差异(P<0.05)。绿区的各光合色素含量均高于黄区,绿区的叶绿素含量是黄区叶绿素的10 倍左右,类胡萝卜素是叶绿素的9 倍左右,绿区中叶绿素和类胡萝卜素的比例为3.542,高于黄区的2.952,说明绿区中影响叶色的主要原因是叶绿素的积累。

表5 靓竹S4 时期叶片光合色素含量分区对比①Tab. 5 Photosynthetic pigment content comparision in different stripes at S4 stage of S. glabra ‘Albostriata’
2.5 靓竹叶片叶绿素合成前体物质的测定
对靓竹叶片不同时期的前体物质相对含量进行比较,以功能叶S4 时期为标准,结果如图6 所示,除尿卟啉原III(UrogenIII)之外的物质都是随着发育过程推进逐渐积累的。UrogenIII 在靓竹叶片发育前期(S1、S2)显著高于叶色稳定的后期(S3、S4),并且相较于粪卟啉原III(CoprogenIII)的相对含量,原卟啉IX(Proto IX)各时期相对含量骤减。以上结果说明,随着靓竹叶片条纹的出现,UrogenIII 向CoprogenIII 的转化增加,CoprogenIII 向Proto IX 的转化过程受阻从而造成CoprogenIII 的大量积累。由此推测,UrogenIII和CoprogenIII 是靓竹叶片发育过程中叶绿素合成途径中的关键物质。
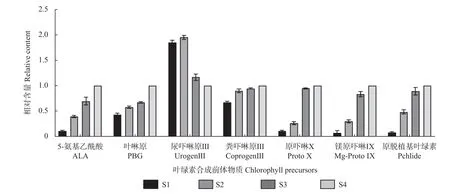
图6 靓竹叶片不同前体物质在不同发育阶段的相对含量Fig. 6 Relative concentration of different precursor material of chlorophyll during different stages of S. glabra ‘Albostriata’
3 讨论
3.1 解剖结构与彩叶形成的关系
Hara(1957)认为彩叶叶片表面具有不同颜色,形成规则图案或不规则斑点或斑块。Sheue 等(2012)将彩叶分为5 种类型:叶绿素型、色素型、表皮型、空腔型和附属物类型,而其中表皮型、空腔型和附属物类型的彩叶属于结构型彩叶。叶片结构很大程度上会引起彩叶的形成,影响因素主要是叶片的表皮形态和叶肉细胞排列方式具有差异。叶肉细胞排列疏松,细胞间隙大导致光反射,从而影响叶色。银色叶片叶色变异归因于表皮细胞和栅栏细胞之间存在广泛的细胞间隙(Burgeret al.,1998;Hochet al.,1980)。Tsukaya等(2004)发现广西落檐(Schismatoglottis calyptrata)叶片的斑块叶色是由于叶肉细胞松散、表皮和栅栏组织之间有不规则的细胞间隙造成;王振兴等(2016)的研究认为狗枣猕猴桃(Actinidia kolomikt)这种彩叶变异与彩叶叶肉细胞结构更为疏松从而导致的光反射有关;尖萼报春苣苔(Primulina pungentisepala)白叶类型叶肉细胞的栅栏组织细胞呈白色球形且排列松散(Chenet al.,2022)。在本研究中,通过对靓竹不同发育时期及成熟功能叶分区的叶片显微结构观察中发现,随着发育过程不断推进,各细胞及叶脉面积不断增大,细胞界限逐渐清晰;叶片绿区的表皮细胞与叶肉细胞、叶肉细胞间均排列紧密,黄区叶肉细胞内部不易被染色,且分化程度低,黄区指状臂细胞层数少于绿区,因此,靓竹彩叶的形成与指状臂细胞的分化和排列方式有关。
由于表皮细胞的形状可将光聚焦到色素上(Zhanget al.,2009)以及叶片表皮上的腺毛和蜡质等附属结构,从而来影响叶色(Reicoskyet al.,1978;Karabourniotiset al.,1999)。禾本科植物的叶表皮形态结构被认为在研究种的分类和系统关系方面具有重要的价值(陈志强等,1987;Bothmeret al.,1993),稻型叶片表皮系统具有上表皮有长短细胞之分、叶脉带常有微毛或兼有刺毛、下表皮乳突密集等特征(张志耘等,1998)。靓竹叶片属于稻型叶片表皮系统,本研究在对靓竹不同叶色分区进行扫描电镜观察,可以观察到靓竹叶片上表皮均较为平整、叶脉清晰、下表皮均着生密集的乳突,乳突有三角状和颗粒状两种,气孔两端各附着2 个小乳突。但是不同叶色之间的表皮结构差异不显著,说明靓竹叶色变异受到表皮的影响较小。
植物组织的质地和颜色可能受到组织中色素浓度和分布的影响(Neillet al.,1999;Gouldet al.,2000)。通过对不同叶色区域的叶片进行徒手切片,观察到绿区叶片叶绿体在靠近上下表皮的叶肉细胞中均有分布,而黄区叶片叶绿体靠近下表皮分布。综上,可以推断在靓竹叶片中,叶绿体在叶肉细胞中的分布情况会对叶色产生影响,而表皮、叶片内部细胞排列方式并非决定叶色变异的因素。
3.2 彩叶形成过程中叶绿体发育与叶绿素合成的变化
叶色变异与光合色素有着密切联系,光合色素的含量及组成均会对叶色的形成产生影响(陈星旭,2009; 邱义兰等,2010)。光合色素主要包括叶绿素和类胡萝卜素,叶绿素又包括叶绿素a 和叶绿素b,其中叶绿素a 呈黄绿色,叶绿素b 呈蓝绿色。叶绿素位于叶绿体上,叶绿体发育异常或结果受损均会引起叶色变异(Yuet al.,2016)。叶绿体发育进程与叶片发育大致同步,叶片发育的过程也是叶色逐渐加深的过程。王啸晨(2012)在对4 种彩叶竹种叶片研究中发现,白纹阴阳竹和白纹椎谷笹的叶肉细胞则呈现基粒片层降解、产生大量嗜锇颗粒等不同程度的叶绿体变异。白纹阴阳竹、白纹椎谷笹、菲黄竹和黄条金刚竹叶片呈现不同颜色可能由光合色素合成途径受抑制引起;成敏敏(2018)研究花叶矢竹不同复绿阶段叶片叶绿体超微结构和光合色素,确定叶绿素累积是使花叶矢竹白叶复绿的原因,并且可观察到复绿过程中叶绿体内膜系统由无序泡状到有序的片层和基粒类囊体排列;苏佳露等(2020)研究了6 个彩叶竹种在不同分区的叶色与光合色素,以及与细胞显微超微结构之间的关系,证明彩叶叶片不同叶色的呈现与部分细胞内叶绿体发育异常和光合色素含量较低有关。本研究中,靓竹叶片黄区细胞及叶绿体发育异常,表现为细胞空腔大、叶绿体数量少且内部结构不清晰;绿区叶肉细胞中的叶绿体随发育进程不断趋于成熟,这与苏佳露等(2020)的研究结果类似。在光合色素上,各时期光合色素的含量随着发育而逐渐积累,功能叶的黄区及绿区在光合色素的含量上也有显著差异,这也与苏佳露等(2020)的研究结果类似。说明叶色是光合色素含量的直观呈现,且叶片在发育过程中,光合色素处于不断积累的状态,叶绿素的积累是影响叶色的最主要原因。
在高等植物叶片中,叶绿素是由L-谷氨酸-tRNA经过一系列复杂的反应合成的。这一过程中ALA 的合成和镁原卟啉IX 的合成对于叶绿素合成速度有限制作用,属于叶绿素合成途径中的关键步骤。叶绿素合成途径中需要20 多个基因编码的15 种酶的参与(Beale, 2005)。在合成过程中,其中任何一个基因发生突变都会导致合成途径中的中间产物大量积累,阻碍叶绿素的合成。目前有一些对于发生叶色变异的叶片其叶绿素合成途径的研究,陈凌艳等(2017)的研究中证明银丝竹叶片呈现出白色性状的原因在于其叶片叶绿素生物合成过程受阻,受阻点位于CoprogenIII至ProtoIX 的转化过程中;杨荧等(2019)推测安吉白茶(Camellia sinensis‘Baiyel 1’)由于叶绿素合成阶段中Mg-proto IX 合成叶绿素a 时受阻,使Mg-proto IX在白化叶片中积累,使白化叶中Mg-proto IX 含量高于返绿叶;徐胤(2020)在对绿竹白化叶片的研究中证明,绿竹白化变异类型的叶绿素合成途径在合成ALA 之前就可能受到了阻碍;黄婧等(2021)证明复绿期黄金枸骨(Ilex×attenuata‘Sunny Foster’)叶片的叶绿素积累可能起始于UrogenIII 的增加。在对叶片光合色素的研究中发现了靓竹叶片中光合色素的含量是随着发育进程不断积累的。为了探究这一现象出现的原因,寻找叶绿素合成途径中的差异,故对于叶绿素合成途径中的前体物质进行测定,并发现靓竹叶片多个发育时期在CoprogenIII 向Proto IX 转化过程中受到阻碍,出现了CoprogenIII 的大量积累,另外在彩叶功能叶中除UrogenIII 之外的物质都是随着发育过程推进逐渐积累,可推测UrogenIII 和CoprogenIII 对于靓竹叶片发育进程中的叶色变异有重要影响,CoprogenIII 的合成受阻或CoprogenIII 至ProtoIX 的转化受阻均会导致叶色变异,这与陈凌艳等(2017)的研究结果一致。
3.3 类胡萝卜素含量对于叶色的影响
除叶绿素之外,类胡萝卜素及叶黄素的大量积累也可以引起叶色变黄。叶片通过合成类胡萝卜素和叶黄素来实现保护作用。之前研究中一些金叶植物叶片黄化与类胡萝卜素的含量增加有关。Li 等(2018)在银杏中发现上调基因ZISO、ZDS和LCYE促进类胡萝卜素的积累,类胡萝卜素与叶绿素比率的变化是导致突变株叶片呈金色的主要因素(Liet al.,2018)。但在Tian 等(2021)的研究中发现金叶杨突变体JHY 的叶绿素和类胡萝卜素含量低于原种L22025,但类胡萝卜素/叶绿素比值高于L22025。这两种色素之间的差异是叶片颜色变化的原因之一。本研究经对比黄区及绿区的光合色素含量,未观察到黄区类胡萝卜素含量增高,黄、绿两区的叶绿素:类胡萝卜素比例基本在3∶1 左右浮动,绿区比值高于黄区,这与Tian 等(2021)的研究结果类似。说明在靓竹叶色变异中,叶绿素的含量更具有决定性,而非类胡萝卜素。
4 结论
靓竹叶片发育过程中,叶片厚度逐渐增大,叶片表皮细胞、叶肉细胞、叶脉均不断增大。光合色素含量逐渐积累,UrogenIII 和CoprogenIII 是靓竹叶片发育过程中叶绿素合成途径中的关键物质。黄区叶片叶肉细胞空腔大且叶绿体发育异常,指状臂细胞层数少,绿区叶片随发育程度叶绿体数量逐渐增加,叶绿素含量积累。靓竹条纹叶色的出现与指状臂细胞分化程度低、叶绿体发育异常以及叶绿素合成受阻有关。
