不同剂量1.5%氯普鲁卡因缓解分娩镇痛爆发痛的效果
2023-10-15计天珍徐成刘红霞李国防李锐朱海娟
计天珍,徐成,刘红霞,李国防,李锐,朱海娟△
目前硬膜外镇痛是公认的安全有效的分娩镇痛方式,但约25%的产妇会经历爆发痛,需额外追加镇痛药物[1]。目前临床常用于缓解爆发痛的方法为0.15%罗哌卡因硬膜外注射,而罗哌卡因起效时间较长,扩散效果不佳[2]。氯普鲁卡因属苯甲酯类局麻药,麻醉效能强、扩散好、起效快、胎盘通过率低、毒性低、不良反应较少[3-4]。Zhu 等[5]采用1.5%氯普鲁卡因6 mL、1.2%氯普鲁卡因7.5 mL作为首剂量用于分娩镇痛,结果显示1.5%氯普鲁卡因6 mL 效果更优,且对运动功能、子宫收缩及母儿无不良影响。本课题组既往采用1.5%氯普鲁卡因6 mL 用于缓解分娩时爆发痛,结果显示起效时间和产妇满意度均优于0.15%罗哌卡因6 mL[2],但该研究仅涉及一个剂量,是否为缓解爆发痛的最佳有效剂量尚不清楚,需进一步探索。本研究使用1.5%氯普鲁卡因6、8、10 mL 硬膜外注射治疗分娩爆发痛,观察其疗效和不良反应情况,旨在寻找1.5%氯普鲁卡因缓解分娩爆发痛的最佳用量。
1 对象与方法
1.1 研究对象 本研究为前瞻性研究。选取安徽省妇幼保健院2022年2—12月拟经阴道分娩,行硬膜外镇痛且镇痛后出现爆发痛的单胎、足月、胎位正常初产妇,年龄20~36岁,平均(26.2±3.4)岁,体质量指数(BMI)21.0~35.0 kg/m2,美国麻醉医师协会(ASA)Ⅰ或Ⅱ级。排除标准:妊娠合并症(胎盘早剥、重度子痫前期、前置胎盘等高危妊娠),椎管内穿刺禁忌证,已知胎儿异常,慢性疼痛病史,产前使用精神类药物史或精神异常不能很好配合,对阿片类、酯类或酰胺类局麻药过敏者,镇痛后1 h 内分娩者。本研究获本院伦理委员会批准(YYLL2021-02-13-01),产妇或其委托人均签署知情同意书。
1.2 分组 使用计算机生成随机数字列表,按照1∶1∶1∶1的比例对硬膜外分娩镇痛后产程出现爆发痛的产妇进行随机分配,根据爆发痛处理的方法不同,分为R 组(0.15%罗哌卡因6 mL)、C1组(1.5%氯普鲁卡因6 mL)、C2组(1.5%氯普鲁卡因8 mL)和C3组(1.5%氯普鲁卡因10 mL)。组别分配被隐藏在密封的不透明信封中。在子宫收缩期间,患者主诉疼痛难忍需要额外硬膜外镇痛的情况下,由1位不参与研究的分组执行者打开信封来进行分组分配。采用PASS v11.0 进行样本量估算。在对40 例患者(每组10 例)进行的预试验研究中,R组、C1组、C2组和C3组产妇爆发痛给药后的成功率分别为50%、60%、70%和90%。在检验效能(1-β)为0.8,α为0.05的情况下,每组最小样本量为25例,共100例,考虑到20%失访率,最终每组纳入32例,共128例。
1.3 分娩镇痛方案 产妇进入分娩镇痛间后,开放上肢静脉通路,输入平衡液6~8 mL/(kg·h),持续监测宫缩、胎心率(FHR)及产妇心率(HR)、血压(BP)、血氧饱和度(SpO2)等生命体征。宫颈口扩张至2~3 cm 时,实施硬膜外穿刺置管。产妇取左侧卧位,选取L2—3间隙,消毒铺巾后行硬膜外穿刺,向头侧置入多孔钢丝加强硬膜外导管4~5 cm,弹力胶布妥善固定后嘱产妇平卧。回抽无脑脊液或血液,给予硬膜外试验剂量1%利多卡因5 mL,观察5 min,无误入蛛网膜下腔或血管内征象,硬膜外注射负荷剂量0.09%罗哌卡因+0.4 mg/L舒芬太尼10 mL,10 min后冰块测试双侧感觉阻滞平面达T10且产妇的疼痛视觉模拟评分(VAS)≤3 分,则为镇痛满意,若疼痛VAS>3分,则被剔除,以排除神经阻滞不全的病例。此时,连接硬膜外脉冲泵(型号:ZZB-100,江苏爱朋医疗科技股份有限公司),泵内药液:0.09%罗哌卡因+0.4 mg/L舒芬太尼100 mL。设置硬膜外程控间歇式输注(programmed intermittent epidural bolus,PIEB)方案:脉冲剂量7 mL/h,限制剂量30 mL/h。完成镇痛后,每次子宫收缩期间以盲法进行疼痛VAS。通过胎儿监护仪描记宫缩强度来确认宫缩。
胎儿娩出后,用两把血管钳钳夹住近胎儿端的一段脐带,用肝素化的2 mL注射器抽取脐动脉血行血气分析(血气分析仪型号:ABL9,Radiometer Medical ApS),检测pH、动脉血二氧化碳分压[p(O2)]、动脉血氧分压[p(O2)]。
1.4 爆发痛处理方案 产妇硬膜外分娩镇痛后自觉阵痛难忍,自诉要求额外硬膜外镇痛治疗定义为爆发痛[6]。发生爆发痛时,麻醉医生评估硬膜外导管位置未发生移位、脱落等,产妇无单侧阻滞等阻滞不全现象,4 组经硬膜外分别注射0.15%罗哌卡因6 mL、1.5%氯普鲁卡因6、8、10 mL。每隔3 min 对产妇进行1 次疼痛VAS 评估镇痛效果。若15 min 内疼痛VAS下降≥4分,则定义为爆发痛治疗“成功”,否则定义为“失败”[7]。“失败”者给予硬膜外注射1%利多卡因5 mL补救镇痛[8]。若15 min内疼痛VAS下降仍不满意,由麻醉医生进行评估,并给予相应处理(重新穿刺或静脉镇痛药等)。
1.5 观察指标及相关定义 一般资料:产妇年龄、BMI、孕龄、宫颈口直径、ASA 分级、基线FHR、基础平均动脉压(MAP)。主要观察指标:爆发痛治疗起效时间和爆发痛治疗的成功率。爆发痛治疗起效时间指给药后达充分镇痛的时间(VAS 评分下降≥4 分)。次要观察指标:补救镇痛率;产妇满意度(爆发痛给药后5 min、胎儿娩出后24 h);爆发痛发生次数;首次爆发痛发生时间;首次爆发痛发生时宫颈口直径;首次爆发痛发生时(T0)、给药后3 min(T1)、6 min(T2)、9 min(T3)、12 min(T4)、15 min(T5)、18 min(T6)的疼痛VAS、改良Bromage评分、FHR;爆发痛时、给药后第2、4、6、8、10、12次宫缩的间隔和持续时间;第一产程、第二产程、第三产程时间;镇痛泵罗哌卡因用量和舒芬太尼用量;1、5 min 时Apgar 评分;新生儿体质量;分娩方式(自然分娩、产钳助产、剖宫产);不良反应(皮肤瘙痒、恶心、尿潴留、寒战、仰卧位低血压、产程停滞、宫缩乏力、爆发痛给药30 min 内出现胎儿心动过缓、爆发痛给药30 min内出现下肢麻木感等)发生率。
疼痛VAS:分值0~10分,0分代表无痛,分值越高疼痛越明显,10分为不能忍受的剧痛。产妇对分娩镇痛的满意度采用0~10 分数字评分量表:0 分,无效果,非常不满意;1~3 分,未达到镇痛期望,不满意;4~6分,基本达到镇痛需求,一般满意;7~9分,比较满意;10分,非常满意。改良Bromage评分:1分:完全阻滞,无法背屈脚踝;2分:几乎完全阻滞,仅能背屈脚踝;3分:部分阻滞,只能弯曲膝盖;4分:双下肢可活动,但出现一定程度麻木;5分:无运动神经阻滞,双下肢活动自如。
仰卧位低血压:收缩压<90 mmHg(1 mmHg=0.133 kPa)或比基线降低>20%,予以加快输液和(或)静脉注射去甲肾上腺素8 μg,产妇左侧卧位或借助楔形体位垫左倾15°;胎儿心动过缓:FHR<110 次/min 超过2 min,由产科医生根据产科管理指南进行相应处理。宫缩乏力诊断由产科医生进行评估,并依照产科方案处理。
1.6 统计学方法 采用SPSS 22.0 软件进行数据分析,GraphPad Prism 8软件进行绘图。定量数据采用Shapiro-wilk法进行正态性检验,正态分布的计量资料以表示,组间比较采用单因素方差分析,组间多重比较采用Dunnett-t检验。重复测量数据比较采用重复测量资料的方差分析。偏态分布的计量资料以M(P25,P75)表示,组间比较使用Kruskal-WallisH检验,组间多重比较采用Bonfferroni 法。计数资料以例或例(%)表示,组间比较采用χ2检验或Fisher 确切概率法,组间多重比较采用Bonfferroni 法。采用Kaplan-Meier 曲线计算各组镇痛起效时间。P<0.05为差异有统计学意义。
2 结果
2.1 一般资料比较 128 例产妇中有11 例中途要求退出试验,3 例神经阻滞不全而重新置管,2 例硬脊膜意外穿破,镇痛后1 h 内分娩者1 例,最终纳入111例。4组产妇年龄、BMI、孕龄、宫颈口直径、ASA分级、基线FHR、基础MAP 比较差异均无统计学意义,见表1。
2.2 爆发痛给药起效时间的比较 Kaplan-Meier结果显示,R组、C1组、C2组、C3组爆发痛给药后的中位起效时间(95%CI)分别为14.3(13.4~15.2)min、6.6(5.6~7.6)min、5.9(5.0~6.8)min 和4.7(3.9~5.4)min,C3组爆发痛给药起效时间明显快于C1组和C2组(Log-rankχ2分别为9.852和5.325,P<0.05),C2组与C1组起效时间差异无统计学意义(Log-rankχ2=0.921,P=0.337),见图1。
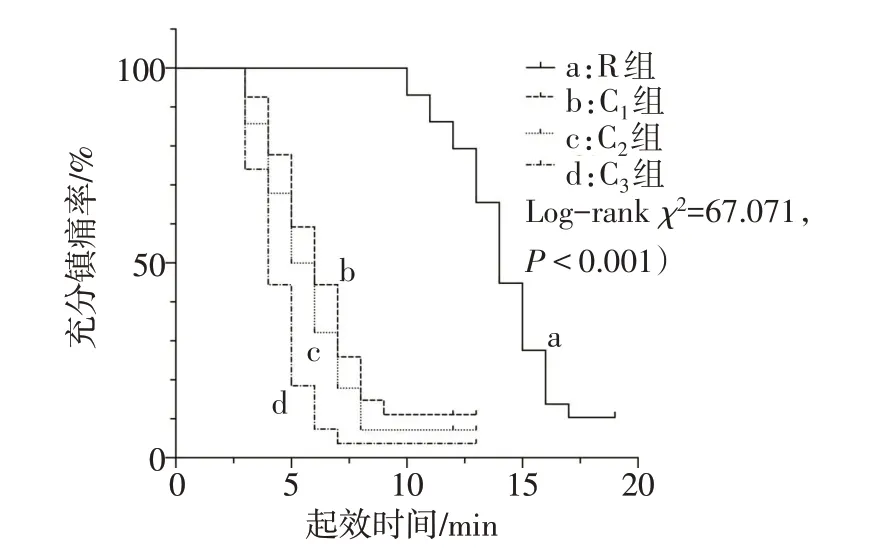
Fig.1 Kaplan-Meier curves of onset time of effective analgesia for breakthrough pain in the four groups图1 4组产妇爆发痛有效镇痛起效时间的kaplan-Meier曲线
2.3 爆发痛相关指标比较 与R组比,C2、C3组爆发痛治疗成功率、爆发痛给药后5 min 和胎儿娩出后24 h 的产妇满意度升高,C3组补救镇痛率下降(P<0.05);与C1组比,C3组爆发痛治疗成功率升高,补救镇痛率下降,C2、C3组爆发痛给药后5 min 和胎儿娩出后24 h的产妇满意度提高(P<0.05)。4组爆发痛发生次数、首次爆发痛发生时间、首次爆发痛发生时宫颈口直径比较差异无统计学意义,见表2。
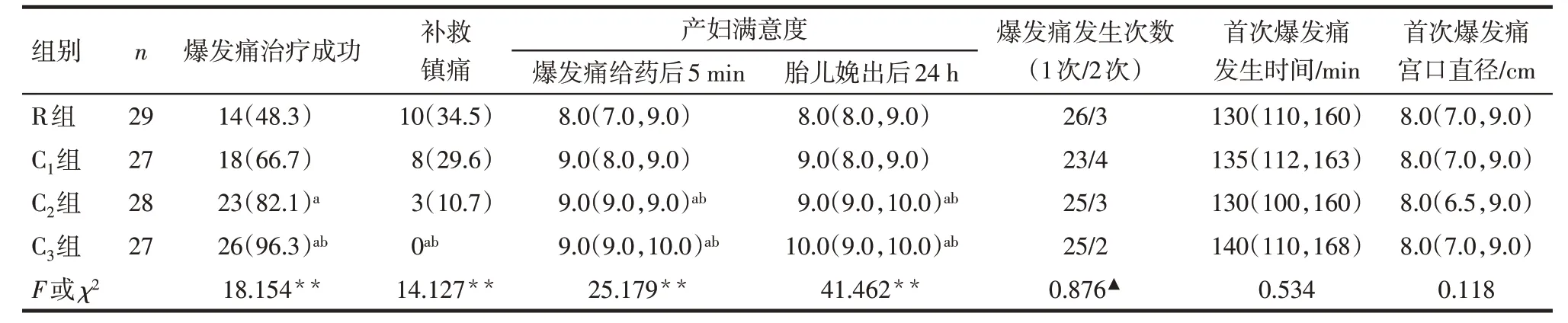
Tab.2 Comparison of the breakthrough pain related indicators between the four groups表2 4组爆发痛相关指标的比较
2.4 爆发痛给药前后疼痛VAS、改良Bromage 评分和FHR 比较 见表3。4 组产妇T0时疼痛VAS 差异无统计学意义。时间和处理因素对疼痛VAS的影响存在交互作用,与T0时比较,R 组爆发痛给药后T2—6疼痛VAS 降低,C1、C2、C3组爆发痛给药后T1—6疼痛VAS 降低(P<0.05);组间比较:T1时,C2、C3组疼痛VAS低于R组,C3组低于C1组(P<0.05);T2—5时,C1、C2、C3组疼痛VAS 低于R 组,C2、C3组疼痛VAS 低于C1组(P<0.05);T6时,C2、C3组疼痛VAS 低于R 和C1组(P<0.05)。时间和处理因素对改良Bromage评分的影响不存在交互作用,与T0和T1时比较,爆发痛给药后T2—6改良Bromage 评分降低(P<0.05)。4 组间改良Bromage评分和爆发痛给药前后不同时点FHR差异无统计学意义(P>0.05)。
Tab.3 Comparison of VAS,modified Bromage score and FHR before and after administration of breakthrough pain between the four groups表3 4组爆发痛给药前后疼痛VAS、改良Bromage评分和FHR的比较()
*P<0.05,**P<0.01;组内比较:A与T0比较,P<0.05;B与T1比较,P<0.05;组间比较:a与R组比较,P<0.05;b与C1组比较,P<0.05。VAS评分:F组间=18.213**,F时间=559.370**,F交互=11.243**;改良Bromage 评分:F组间=2.197,F时间=2.203*,F交互=0.678;FHR:F组间=0.230,F时间=1.428,F交互=1.311。
?
2.5 爆发痛给药前后宫缩间隔和持续时间 时间和处理因素对宫缩间隔时间和宫缩持续时间的影响不存在交互作用。4 组间爆发痛时宫缩间隔时间、宫缩持续时间比较差异无统计学意义(P>0.05),见表4。
Tab.4 Comparison of the interval and duration of uterine contraction before and after administration of breakthrough pain between the four groups表4 4组爆发痛给药前后宫缩间隔时间和持续时间的比较()
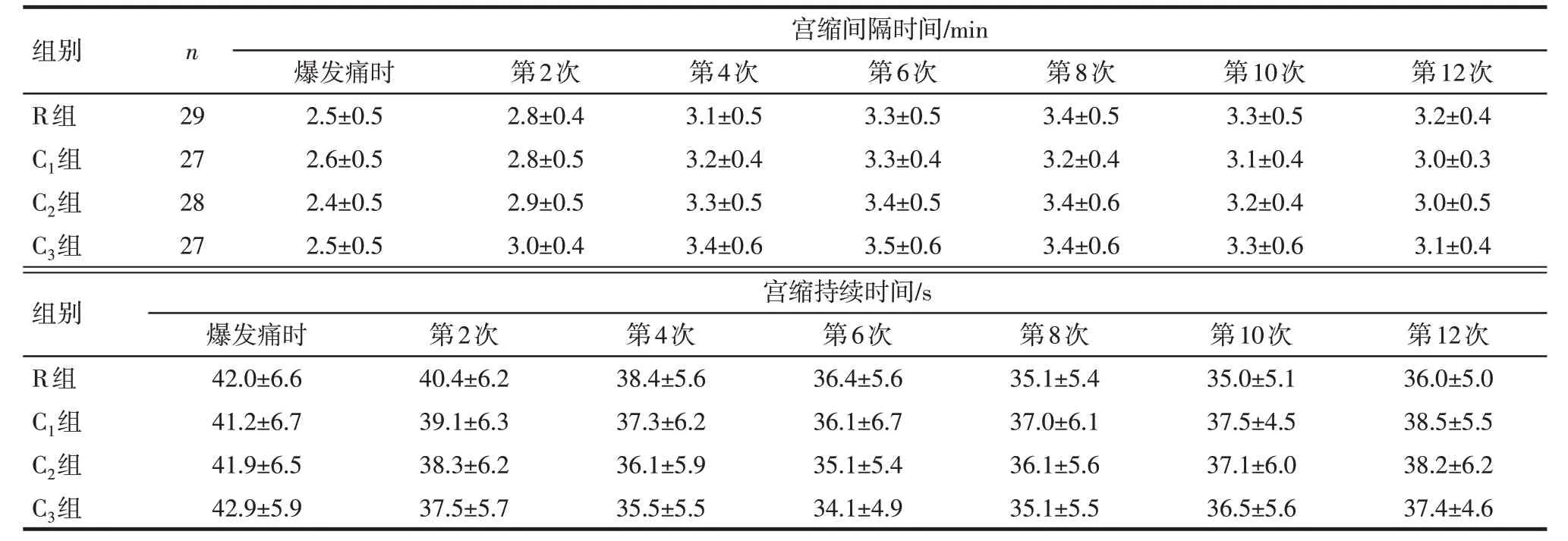
Tab.4 Comparison of the interval and duration of uterine contraction before and after administration of breakthrough pain between the four groups表4 4组爆发痛给药前后宫缩间隔时间和持续时间的比较()
**P<0.01;宫缩间隔时间:F组间=1.056,F时间=69.694**,F交互=1.383;宫缩持续时间:F组间=0.179,F时间=123.395**,F交互=1.693。
?
2.6 分娩情况、新生儿指标、不良反应的比较 与R组和C1组相比,C3组爆发痛给药30 min 内下肢麻木发生率升高(P<0.05)。4组间第一、第二、第三产程时间,镇痛泵罗哌卡因和舒芬太尼用量,脐动脉血pH、p(CO2)、p(O2),1 min 和5 min 时Apgar 评分,新生儿体质量,分娩方式,皮肤瘙痒、恶心、寒战、仰卧位低血压、产程停滞、宫缩乏力、爆发痛给药30 min内出现胎儿心动过缓差异均无统计学意义,见表5。4组均未发生尿潴留、仰卧位低血压、产程停滞和宫缩乏力。C2、C3组的下肢麻木感为轻度,均可抬双腿或下床活动。
3 讨论
本研究选择不同剂量的1.5%氯普鲁卡因硬膜外注射治疗分娩镇痛中爆发痛,结果显示,爆发痛时硬膜外注射1.5%氯普鲁卡因8 mL 起效快、成功率高、镇痛效果好、产妇满意度高、并发症少,且对母婴无不良影响。硬膜外镇痛是当前国内外应用较广泛的分娩镇痛方式,但其骶尾部阻滞相对不完善,爆发痛的发生率高于腰硬联合和硬脊膜穿破硬膜外阻滞镇痛模式[1]。出现爆发痛时给予及时有效的治疗是关键,罗哌卡因虽能有效缓解爆发痛,但起效较慢,扩散差,快速降低疼痛评分程度有限[2]。氯普鲁卡因是快速起效的局麻药,已在许多门诊手术和急诊剖宫产术中用于硬膜外麻醉[3,9-10]。研究显示,氯普鲁卡因用于急诊剖宫产术硬膜外麻醉起效时间明显快于罗哌卡因和利多卡因[11],且其局部麻醉毒性罕见,胎盘通过率低,低浓度具有感觉和运动阻滞分离作用,无快速耐药性和蓄积作用,通过血浆胆碱酯酶代谢,这些特性均优于利多卡因[9,12],而利多卡因和罗哌卡因依赖肝微粒体酶代谢,肝微粒体酶在新生儿出生后1年才能完全发育成熟[13]。
在分娩镇痛实施过程中,局麻药的应用原则为选择最低有效浓度和容量,从而把局麻药的不良反应降到最低,然而随着产程进展,疼痛级别增加,往往需要相对高浓度的局麻药才能有效缓解爆发痛[14]。如李冰等[15]采用罗哌卡因浓度递增的方式维持分娩镇痛,0.075%或0.1%罗哌卡因+0.5 mg/L舒芬太尼用于潜伏期镇痛,0.125%罗哌卡因+0.5 mg/L舒芬太尼用于活跃期镇痛,镇痛效果确切,对母婴无不良影响。马丽等[16]使用0.08%罗哌卡因+0.4 mg/L 舒芬太尼维持分娩镇痛,而硬膜外推注0.15%罗哌卡因治疗爆发痛,效果显著优于推注维持药物组。研究显示1.2%的氯普鲁卡因可以达到运动与感觉阻滞分离的作用[9],但Zhu等[5]比较了1.5%氯普鲁卡因6 mL和1.2%氯普鲁卡因7.5 mL用于启动分娩镇痛的效果,发现1.5%氯普鲁卡因6 mL获得了更快的分娩镇痛起效且无明显抑制宫缩等不良反应。因此,结合既往研究和临床经验,本研究采用1.5%氯普鲁卡因缓解爆发痛。
本研究探索1.5%氯普鲁卡因的最佳有效容量,结果显示,爆发痛给予6、8、10 mL1.5%氯普鲁卡因后VAS 评分下降≥4 分的中位时间(95%CI)分别为6.6(5.6~7.6)min、5.9(5.0~6.8)min、4.7(3.9~5.4)min。Zhu 等[5]采用1.2%氯普鲁卡因7.5 mL、1.5%氯普鲁卡因6 mL,作为首剂量用于分娩镇痛,起效时间分别为8.0(7.5~8.5)min、7.0(6.2~7.8)min。许兰兰等[17]在分娩镇痛中转剖宫产术中,硬膜外推注3%氯普鲁卡因12~13 mL,温觉阻滞起效时间为(5.4±1.9)min。Yang等[10]在门诊膝关节镜检查中使用3%氯普鲁卡因10 mL 硬膜外阻滞,感觉阻滞起效时间为(4.7±1.4)min。阻滞起效时间的差异可能与不同药物浓度、剂量、手术类型、阻滞节段、测试阻滞起效时间的方法等有关。
与罗哌卡因对感觉和运动功能阻滞分离作用不同,氯普鲁卡因可能会导致一定程度的运动阻滞效果。本课题组既往的研究采用1.5%氯普鲁卡因6 mL硬膜外注射用于分娩镇痛的爆发痛,对运动功能无明显影响[2]。Lee 等[18]报道了1 例对酰胺类局麻药过敏史的产妇分娩镇痛,采用1.5%氯普鲁卡因连续硬膜外镇痛,运动功能受到轻微影响,但不影响下肢活动,运动和感觉功能在停止硬膜外泵注2 h以后完全恢复,这可能与给药剂量较大有关,该产妇给予试验剂量1.5%氯普鲁卡因3 mL,负荷量12 mL,随后以10 mL/h 的速度持续泵注。而本研究在爆发痛发生时,单次给予1.5%氯普鲁卡因6、8或10 mL,未出现明显运动神经阻滞作用,且1.5%氯普鲁卡因10 mL组相比于8 mL组,不能进一步增加疗效,双下肢麻木感发生率增加。因此,本研究认为1.5%氯普鲁卡因8 mL 可能为氯普鲁卡因缓解爆发痛的最佳用量。
既往有研究表明,硬膜外输注氯普鲁卡因会造成术后硬膜外阿片类药物的镇痛效果减低,即患者术后疼痛评分可增高以及阿片类药物需求增加[19-20]。但是对于这一观点目前仍存在争议,这可能与硬膜外氯普鲁卡因作用消退与硬膜外吗啡达到峰值作用之间存在镇痛窗口期有关[21-22];可以使用长效局部麻醉剂(罗哌卡因或布比卡因)或中效局部麻醉剂利多卡因的镇痛桥接剂量来填补此镇痛窗口期[21]。本研究没有观察到爆发痛镇痛窗口期,这可能是由于镇痛泵内低浓度罗哌卡因的桥接作用,并且阿片类药物被用作小剂量的佐剂。
本研究结果显示,4 组的FHR、宫缩间隔时间、宫缩持续时间、产程时间、分娩方式、镇痛泵药物用量、首次爆发痛发生时间、首次爆发痛发生时宫口直径、爆发痛发生次数、新生儿脐动脉血pH、p(CO2)、p(O2),1、5 min 时Apgar 评分无明显差异,表明本研究中不同剂量的硬膜外氯普鲁卡因不会对宫缩间隔时间、宫缩持续时间产生影响,这与Zhu 等[5]的研究结果一致。本研究中Apgar 评分与脐动脉血气分析值均在正常范围内,可见硬膜外氯普鲁卡因对新生儿转归无不良影响,与既往研究结果一致[23-24]。
综上所述,产妇在接受硬膜外分娩镇痛过程中出现爆发痛时,硬膜外给予1.5%氯普鲁卡因治疗的最佳用量为8 mL。本研究的局限性:采用单盲法,不能排除研究者带来的主观偏倚;纳入样本量较少;未纳入经产妇;未观察胎头位置,这些需要在未来的研究中进一步探讨。
