慢性阻塞性肺疾病患者血嗜酸粒细胞分布及临床特征分析
2023-10-07李龙胡振红刘海潮吴妍雯夏飞秦少文
李龙 胡振红 刘海潮 吴妍雯 夏飞 秦少文
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)简称慢阻肺,是一种常见的,可防可治的以持续的呼吸道症状和气流受限为特征的气道慢性炎症性疾病[1]。2018年我国发布的慢阻肺流行病学调查研究显示,40岁以上人群中慢阻肺患病率为13.7%[2]。以往研究报道中性粒细胞、T淋巴细胞、巨噬细胞参与了慢阻肺的发病过程,但近期一项研究显示约40%左右稳定期慢阻肺患者气道中存在嗜酸粒细胞(eosinophil,EOS)浸润,EOS在慢阻肺的发生发展中发挥重要作用[3]。高EOS慢阻肺患者在急性加重期使用全身激素可迅速缓解症状,表现出与正常EOS患者不同的临床特征[4]。血嗜酸粒细胞计数同样能反应气道嗜酸粒细胞浸润水平。目前我国慢阻肺患者血EOS分布特点不清,针对相关表型患者临床特征研究较少,本研究回顾性分析我院呼吸科门诊慢阻肺患者EOS增高的比例及临床特征。
资料与方法
一、研究对象
收集2018年7月1日至2020年7月1日我院呼吸科门诊稳定期慢阻肺患者226例,均规范使用吸入制剂(噻托溴铵18μg、沙美特罗氟替卡松50μg/500μg、布地奈德福莫特罗320μg/9μg),没有口服或静脉使用激素,其中男性患者173例,女性患者53例,年龄56~74岁,中位年龄66岁,所有患者均满足慢性阻塞性肺疾病全球倡议(global initiative for chronic obstructive lung disease,GOLD)2021诊断标准,即在吸入支气管舒张剂如沙丁胺醇后,肺功能指标FEV1/FVC<70%。稳定期指6周内咳嗽、咳痰、气短、呼吸困难症状未见加重。排除标准包括:(1)年龄<40岁。(2)合并过敏性疾病如过敏性鼻炎。(3)合并其他肺部疾病如肺结核、支气管扩张、支气管哮喘、肺栓塞、特发性肺纤维化、泛细支气管炎合并间质性肺炎、特发性肺纤维化等。(4)近1月内患有急性泌尿系感染、急性肠炎、胆囊炎等其他感染性疾病。(5)肺功能检查无法配合完成。本研究已获得我院伦理委员会批准[(2023)029-01]。
二、方法
临床资料:收集患者的年龄、性别、吸烟指数、体重指数、慢阻肺评估测试评分(COPD assessment test,CAT)、改良英国医学研究委员会呼吸困难量表(modified British medical research council,mMRC)、稳定期药物使用情况、近1年急性加重次数及因急性加重导致住院次数。职业暴露定义为职业暴露有害气体、粉尘或过敏原超过3个月。慢阻肺急性加重期定义为慢阻肺患者咳嗽、咳痰、呼吸困难症状在原有基础上出现加重,或咳黄痰,治疗用药需要进行调整。依据慢阻肺GOLD 2020指南将患者进行分组,A组指上一年急性加重次数≤1次,mMRC 0~1级或CAT评分<10分;B组指上一年急性加重期次数≤1次,mMRC≥2级或CAT评分≥10分;C组指上一年急性加重次数≥2次或因急性加重导致住院1次及以上,mMRC 0~1级或CAT评分<10分;D组指上一年急性加重次数≥2次或因急性加重导致住院1次及以上,mMRC≥2级或CAT评分≥10分。
实验室检查:抽取患者肘部静脉血,检查血常规、快速C-反应蛋白、凝血功能8项、总IgE等。
肺功能检查:患者于上诉检查7 d内完善肺功能及支气管舒张试验检查(使用肺功能仪,支气管舒张剂均为万托林气雾剂400μg),根据患者吸入支气管舒张剂后FEV1占预计值百分比,气流受限分为4级(GOLD分级):1级(轻度)为FEV1占预计值百分比≥80%;2级(中度)为50%≤FEV1占预计值百分比<80%;3级(重度)为30%≤FEV1占预计值百分比<50%;4级(极重度)为FEV1占预计值百分比<30%。
三、分组
根据血EOS计数以0.1×109/L为临界值[1],分为高血EOS慢阻肺组及低血EOS慢阻肺组。
四、统计学分析
结 果
一、慢阻肺患者血EOS分布情况
92例患者EOS≥100个/μL,占比40.7%,24例患者血EOS≥300个/μL,占比10.7%,134例患者血EOS<100个/μL,占比59.3%,所有患者血EOS中位数为114个/μL。
二、高EOS慢阻肺组患者临床特征
高EOS组男性患者78例,占比84.8%,明显高于低EOS慢阻肺组(95例,70.9%),差异具有统计学差异(χ2=5.86,P=0.015),高EOS组过去1年急性加重次数(0.6±0.3)次,因急性加重导致住院次数(0.3±0.1)次,低EOS组过去1年急性加重次数(0.3±0.2)次,因急性加重导致住院次数(0.1±0.1)次,均高于低EOS组,差异有统计学意义(均P<0.05)。年龄、吸烟指数、GOLD分组、药物治疗情况等其他临床特征(表1)均无统计学差异(均P>0.05)。

表1 以血EOS计数100个/μL为分界值分组基本情况比较
三、高EOS慢阻肺组与低EOS慢阻肺组患者肺功能比较
高EOS组FEV1占预计值百分比在用药前为(54±17)%,在用药后为(57±15)%,均较低EOS慢阻肺组低,但差异不具备统计学意义(均P>0.05)。以用药后FEV1进行GOLD分级,高EOS组GOLD 3级患者有52例(56.5%),GOLD4级患者有12例(13.0%),占比均较低EOS慢阻肺组更高(表2),均具有统计学意义(均P<0.05)。高、低EOS慢阻肺组其他肺功能指标均无统计学差异(均P>0.05)。
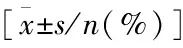
表2 以血EOS计数100个/μL为分界值分组肺功能比较
四、高EOS慢阻肺组与低EOS慢阻肺组患者实验室检查结果比较
高EOS慢阻肺组中性粒细胞百分比为(63.4±10.8)%,低EOS慢阻肺组中性粒细胞百分比为(65.5±10.5)%,高EOS组中性粒细胞占比较低(表3),差异具有统计学意义(χ2=161.23,P=0.015),其他指标如D-二聚体、血红蛋白、淋巴细胞百分比、C-反应蛋白、免疫球蛋白E等均无统计学差异(均P>0.05)。
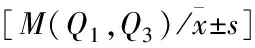
表3 以血EOS计数100个/μL为分界值分组慢阻肺患者化验检查结果比较
五、多因素回归分析
将单因素研究中P<0.05的因素如性别、中性粒细胞百分比、过去1年急性加重次数及GOLD分级纳入多因素Logistic回归方程,由于急性加重住院次数与急性加重次数存在相关性,因此前者没有纳入,该Logitic回归方程模型具有统计学差异(χ2=28.233,P=0.012),高EOS慢阻肺组与较低中性粒细胞百分比、较重气流受限及过去1年较多急性加重次数相关,与性别无相关(表4)。

表4 血EOS计数100个/μL为分界值分组慢阻肺患者与临床特征回归分析
讨 论
慢阻肺患者血EOS水平可预测急性加重风险,在指导ICS应用中发挥重要作用。多项研究发现[5-7]高EOS慢阻肺患者有更高的急性加重风险,但该类人群可从ICS中获益,减少急性加重风险,改善症状、肺功能及生活质量。本研究中高EOS组慢阻肺患者过去一年急性加重次数及因急性加重导致住院次数均较低EOS组增加(均P<0.05),进一步证实血EOS水平可预测急性加重风险。GOLD 2020提出将EOS水平分为100个/μL、300个/μL两个阈值,血EOS低于100个/μL水平慢阻肺患者无法从ICS中获益,在两阈值之间时,ICS作用效果随着EOS水平增高而加大,高于后者时,ICS作用效果不再继续加强[1]。美国胸科学会(American Thoracic Society,ATS)关于慢阻肺2020年治疗指南推荐血EOS≥150个/μL且过去一年中存在一次及以上急性加重史的慢阻肺患者建议加用ICS[8]。欧洲呼吸协会(European Respiratory Society,ERS)推荐血EOS≥300个/μL慢阻肺患者持续使用ICS[9]。高EOS作为慢阻肺独特表型目前受到广大研究者关注,已成为慢阻肺研究热点,但国内对于该表型EOS分布研究十分有限,该表型慢阻肺人群的年龄、性别、肺功能、炎症指标等特征暂未明确。
本研究将血EOS以100个/μL为阈值,高EOS患者占比为40.7%,与既往研究报道相符[3]。ECLIPSE研究[10]表明在血EOS≥2%慢阻肺群体中,男性比例较高;SPIROMICS研究[11]以血EOS≥200个/μL为界将慢阻肺分为两组,高EOS组慢阻肺患者男性占比同样偏高。本研究同样发现高EOS组男性占比高的特点(χ2=5.86,P=0.015)。有文献报道[12],正常肺功能组人群中血EOS占比≥2%人群相对于<2%人群同样具有男性占比高特点,但其男性占比均较同时研究的慢阻肺人群低,提示EOS多寡不仅与性别密切相关,同时与慢阻肺疾病进程相关。
1999年首次有研究者在慢阻肺人群中发现血EOS、嗜酸粒细胞过氧化物酶、特异性碱性蛋白及嗜酸粒细胞阳离子蛋白表达水平均与FEV1占预计值百分比及FEV1FVC呈负相关[13]。本研究通过将P<0.05的因素如性别、中性粒细胞百分比、过去1年急性加重次数及GOLD分级进行多因素二元Logistic分析,发现高EOS慢阻肺患者与较低中性粒细胞百分比、较重气流受限、频繁急性加重相关。高EOS慢阻肺组患者肺功能较差、GOLD分级较重,近1年急性加重次数增多,该结论与大多数研究相符。高EOS慢阻肺组患者中性粒细胞百分比较低,这可能与慢阻肺表型相关。Balzano等[13-14]研究发现,中性粒细胞及EOS在外周血的分布差异与慢阻肺不同症状表型密切相关,在呼吸困难为主要症状表型的慢阻肺人群中血EOS相对较高,中性粒细胞百分比相对较低,以咳嗽、咳痰为主要症状表型的慢阻肺人群则相反。
本研究采用血EOS≥100个/μL为分界值相比其他研究的高界值得出了同样的结论,因该界值可以囊括更多的慢阻肺人群,更能反映EOS对慢阻肺的临床特征影响。同时本研究存在诸多不足,如该研究为横断面研究,纳入的血EOS为单次结果,血EOS存在一定波动性,有研究报道[15],以血EOS≥100个/μL为界,6个月和1年的稳定性分别为91%及85%。
高EOS作为慢阻肺独特表型已受到越来越多研究者广泛关注。该表型患者急性加重风险相对较高,但稳定期及急性加重期均可从激素规范治疗中获益。今后应着手于EOS与慢阻肺气道慢性炎性反应的相互作用机制以及针对该表型的炎性反应特有通路的生物治疗研究当中,为今后以EOS表型的个体化治疗奠定理论基础,为慢阻肺患者带来生存获益。
