厦门地区3~17岁儿童及青少年醛固酮、肾素活性化学发光法参考区间的建立*
2023-09-28肖秀香林淑雯詹伟武徐锦林建成厦门市儿童医院检验科福建厦门36006复旦大学附属儿科医院临床检验中心上海00
肖秀香,林淑雯,詹伟武,徐锦,林建成(.厦门市儿童医院检验科,福建厦门36006;.复旦大学附属儿科医院临床检验中心,上海00)
高血压是导致全球死亡和致残的主要危险因素,2010年全国学生体质调研报告[1]显示我国中小学生高血压患病率为14.5%,且在儿童、青少年以继发性高血压为主[2]。原发性醛固酮增多症(primary hyperaldosteronism,PA)是继发性高血压最常见的类型,以高血压、醛固酮(aldehyde ketones,ALD)增多、肾素(renin activity,PRA)抑制为主要特征,因此血浆ALD、PRA是诊断和鉴别儿童、青少年高血压是遗传性还是继发性的重要指标。1981年Hiramatsu等[3]首次采用ALD和PRA比值(aldosterone renin activity ratio,ARR)作为PA指标筛查高血压患者人群后,Mulatero等[4]利用ARR对正常血钾水平的高血压人群筛查,证实了ARR提高PA检出率,中华医学会内分泌学分会制定PA诊断治疗的专家共识(2020版)也推荐ARR作为PA的首选筛查指标[5]。
目前,血浆ALD、PRA的参考区间基本来自行业指南或试剂说明书。本研究按照美国临床和实验室标准协会(Clinical and Laboratory Standards Institute,CLSI)及国际临床化学和检验医学联合会(International Federation of Clinicial Chemistry and Laboratory Medicine,IFCC)联合发布的C28-A3文件标准,通过收集厦门地区健康儿童及青少年人群样本,初步建立化学发光法检测厦门地区3~17岁健康儿童及青少年血浆ALD、PRA及ARR的参考区间。
1 材料与方法
1.1研究对象 选取2019年1月至2022年1月厦门市儿童医院儿童保健中心体检表观健康3~17岁儿童及青少年人群。身高、体重、腰围、臀围、血压测量均由专人进行,高血压判断标准按照2018年中国3~17岁儿童和青少年高血压诊断标准[6]。共纳入满足上述条件的915例健康志愿者,分3组:3~7岁:男152例、女142例;8~12岁:男139例、女158例;13~17岁:男184例、女140例。排除标准:(1)有以下疾病者:高血压、冠心病、心肌炎、心力衰竭、肿瘤、中枢神经系统疾病、内分泌代谢性疾病、自身免疫病;肝功能(丙氨酸氨基转移酶、天门冬氨酸氨基转移酶、总蛋白、清蛋白、总胆红素、直接胆红素)、肾功能(肌酐、尿素、尿酸)、血脂(总胆固醇、三酰甘油、高密度脂蛋白胆固醇、低密度脂蛋白胆固醇)、电解质(钾、钠、氯、钙)及C反应蛋白异常人群;(2)身体发育异常者;(3)30 d内使用过可能引起血压波动的药物如止痛药、中药、生长激素、血管紧张素转换酶抑制剂、血管紧张素受体拮抗剂、钙离子拮抗剂、促红细胞生成素、类固醇激素等;(4)近一个月作息欠规则的个体以及近一周作息明显紊乱的个体;(5)2周内发热、感冒或用抗生素者;(6)男性:收缩压<100+2×年龄(岁)且舒张压<65+年龄(岁),女性:收缩压<100+1.5×年龄(岁)且舒张压<65+年龄(岁)[7];(7)BMI≥25 kg/m2或≤18.5 kg/m2;BMI=体重(kg)/身高(m)的平方[8]。本研究经厦门市儿童医院伦理委员会批准(批准文号:厦儿科伦审[2021]36号),由接诊医生当面告知儿童家长本研究的相关情况并签署知情同意书。
1.2仪器与试剂 日立7600-010全自动生化分析仪)(日本日立公司)及肝功能、电解质、血糖试剂(和光纯药工业株式会社),肾功能、血脂试剂(瑞正善达科技公司);Autolumo A2000plus分析仪及配套ALD试剂(郑州安图公司),PETECK96-I化学发光免疫分析仪及配套PRA试剂(博奥赛斯公司)。
1.3方法
1.3.1标本采集与处理 研究对象或其家属填写的问卷调查表核对无误后,采集研究对象清晨空腹立位肘静脉血,采血及量血压前避免情绪紧张或激动,血液标本采集后充分混匀,室温静置10~15 min,20 ℃以下离心10 min(离心力1 000×g),离心后肉眼观察有溶血、脂血或黄疸为不合格标本,分离血浆于-80 ℃保存,避免反复冻融[9]。
1.3.2指标检测 严格按照标准操作规程进行操作,在质控在控情况下检测样本。仪器每年进行一次校准,同时试剂更换批号或仪器校准后进行留样复查及质控品检测。ARR用计算法。
1.4统计学分析 用SPSS 26. 0统计软件进行。按照CLSI C28-A3文件,将各项目数据先按性别,再按年龄从小到大排列后,将数据与相邻值的差值(D)和数据全距(R)相除,若D/R≥1/3则判定为离群值,予以剔除处理。采用K-S检验进行正态性检验,判断数据不符合正态分布,数据采用M(P25,P75)表示。数据经过转换后,组间比较采用单因素方差分析,若方差齐,采用Bonferroni法:若方差不齐,采用Dunette-t法,以P<0.05表示差异有统计学意义。采用百分位数法确定P2.5~P97.5作为参考区间。
2 结果
2.1不同性别组之间ALD、PRA检测结果比较 见表1。不同性别组ALD水平差异有统计学意义(P<0.05),女性组整体高于男性组,PRA差异无统计学意义(P>0.05),ARR水平差异有统计学意义(P<0.05),女性组略高于男性组。
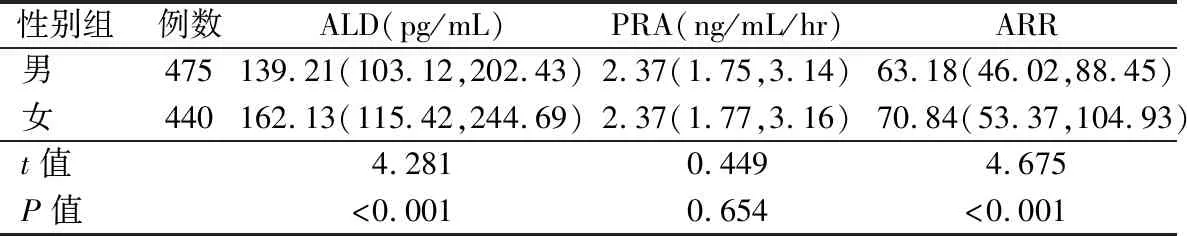
表1 不同性别组之间ALD、PRA水平比较[M(P25,P75)]
2.2不同性别不同年龄段之间ALD、PRA检测结果比较 见表2。男性组中,8~12岁和13~17岁组ALD差异有统计学意义(P<0.05),各年龄组PRA、ARR差异均无统计学意义。女性组中,3~7岁和8~12岁、13~17岁组ALD差异有统计学意义(P<0.05),8~12岁组和13~17岁组ALD差异无统计学意义(P>0.05),各年龄组间PRA、ARR差异无统计学意义。
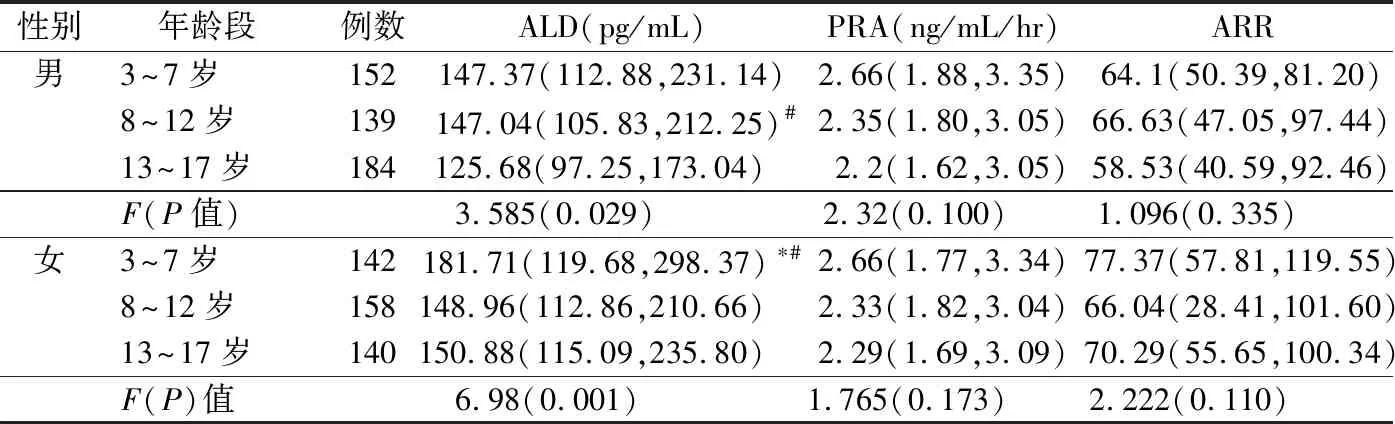
表2 不同性别儿童中不同年龄段之间ALD、PRA水平的比较[M(P25,P75)]
表1数据显示PRA男性和女性整体无显著差异,但整体年龄段是否有差异还需要验证,故再分析整体分年龄段的PRA数据见表3。3~7岁组和8~12岁组差异不显著(P>0.05),8~12岁组和13~17岁组差异不显著(P>0.05),但3~7岁组和8~12岁组有显著差异(P<0.05)。
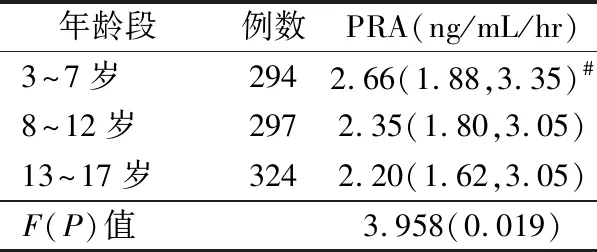
表3 不同年龄段之间PRA水平的比较[M(P25,P75)]
2.3ALD、PRA、ARR项目的参考区间 综合上述数据分析,差异无统计学意义组别汇总统计,男性组3~7岁和8~12岁ALD差异无统计学意义,女性组8~12岁和13~17岁ALD差异无统计学意义;PRA项目男性和女性整体差异无统计学意义,不同年龄段中,相邻年龄段差异无统计学意义,但低龄组(3~7岁)和高龄组(13~17岁)差异有统计学意义,故PRA区分年龄段进行参考区间统计。ARR男性组和女性组中,不同年龄段差异均无统计学意义,故ARR参考区间只区分男性组和女性组。采用百分位数法确定P2.5和P97.5得到3~17岁儿童和青少年血清ALD、PRA、ARR化学发光法的参考区间,见表4。
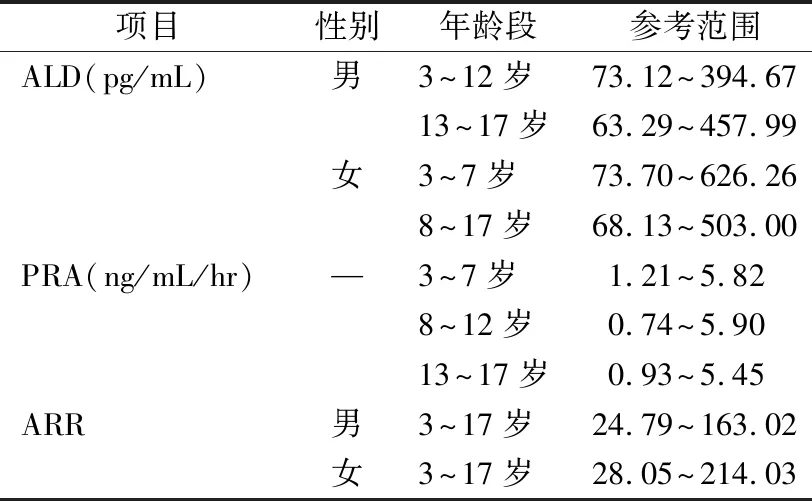
表4 3~17岁儿童及青少年血清ALD、PRA、ARR化学发光法的参考区间
3 讨论
肾素-血管紧张素-醛固酮系统(RASS)是人体内分布最广泛的内分泌调节系统,RASS与继发性高血压疾病密切相关[10]。成人原发性高血压多起源于青少年时期,血压处于高百分位值的儿童易发展为成人高血压,是儿童高血压发展的“轨迹现象”[6,11]。与原发性高血压相比,原发性醛固酮增多症(PA)患者心脏、肾脏和脑等高血压靶器官损害更为严重[12],损害靶器官及死亡风险明显高于原发性高血压[13-14]。因此早期诊断及时治疗PA具有重要意义。
目前各临床实验室检测ALD、PRA有多种不同方法,主要包括免疫分析法(RIA)、化学发光免疫分析法(CLIA)、高效液相色谱法(HPLC)和质谱分析法(LC-MS/MS)[15]。其中,RIA法难于自动化、影响因素多、对环境有污染,HPLC法检测费时、工作量大,该两种方法很少在临床应用。LC-MS/MS法具有灵敏度高、特异性强、测量范围宽等优势,是检测的金标准[16],但该法需要用到的仪器价格昂贵,也很难在实验室普遍应用。CLIA法目前在各实验室已普及使用,以其灵敏度高、重复性好及自动化、快速等优点已被指南推荐运用[17]。
由于不同检测系统检测结果之间存在差异,仍需要系统研究并建立满足ISO15189性能要求的测量方法[15]。Yin等[18]采用Autolumo A2000plus与LC-MS/MS检测ALD斯皮尔曼相关系数(spearman′s coefficient)为0.934,证实了两种平台检测方法相关性良好。杨超一等[19]建立CLIA法检测AngⅠ并计算肾素活性,经方法学评价符合免疫分析的基本要求。赖凤华等[20]采用CLIA与RIA两种方法检测ALD、PRA,具有良好相关性。杜超等[21]报道,4种品牌CLIA法检测系统结果一致性亟待提高,各实验室建立一个合理的参考区间十分必要。本实验室严格依据ISO15189性能要求进行了验证,对使用试剂盒的精密度、正确度、线性范围进行评价,均符合国家卫健委临床检验中心NCCL-C-39-2021醛固酮和肾素计划能力验证报告(2021)评价指标要求。本研究建立3~17岁儿童及青少年人群外周血ALD、PRA、ARR参考区间,主要供本院及其他相同检测系统使用,以帮助临床对PA筛查的判定,但不同实验室采用相同的检测系统使用该参考区间前需要进行验证。
