{[La(PCPA)3(H2O)2]∙DMF∙(H2O)2}n配合物的合成、晶体结构及性质研究
2023-09-27李勇辉
李 波,沈 红,李勇辉
宜宾职业技术学院新能源电池学院,四川 宜宾 644000
由于稀土元素原子具有特别的电子层结构,使其构筑的配合物拥有特殊物理、化学性质,因此,稀土配合物的合成制备、结构和性质研究是无机化学一个重点研究领域,已经受到越来越多的关注[1]。稀土配合物不仅展示出丰富多彩的结构,还在发光性质、强顺磁性、染料溶液催化降解、气体吸附等方面表现出良好的效果[2-5]。在众多稀土金属配合物中,特别是以芳香酸为配体的稀土配合物,因芳香酸具有较大的共轭刚性平面,可以形成配位丰富、结构稳定的配合物,其中的羧基能以单齿螯合、双齿螯合、双齿桥联以及螯合-三齿桥联等模式进行配位,构筑的配合物常以单核、双核、多聚等方式存在,从而形成一维链状、二维层状和三维网状等多种特殊结构[6]。镧系金属中La 原子的最外层电子结构为5s25p6,其4f 电子层具有不同的填充形式,能够产生多种跃迁发射和吸收[7],并可以发射出从紫外光、可见光到红外光的各种波长的电磁辐射[8]。因此,由镧离子构筑的配合物在荧光材料领域具有重要作用,已经受到越来越多的关注。
本文采用镧离子为中心离子、对氯苯乙酸为有机配体,水热合成了镧系稀土配合物,并对其结构和性质进行了测试,丰富了镧配合物的种类,为其后期应用于荧光材料奠定基础。
1 实验部分
1.1 主要仪器与试剂
Bruker APEX-Ⅲ D8 VENTURE X 线单晶衍射仪,德国Bruker 公司;Hitachi F-4600 型荧光光谱仪,株式会社日立制作所;TGA Q500 型热重分析仪,美国TA 公司;X 线衍射仪,日本理学株式会社;DHG 型鼓风干燥箱,上海一恒科学仪器有限公司;Nicoletiz10 型傅里叶变换显微红外光谱仪,赛默飞世尔科技(中国)有限公司;UV2700型紫外分光光度计,日本岛津公司;SHZ-D 型水循环真空泵、DF-101S型集热式磁力搅拌水浴锅,浙江巩义予华仪器有限责任公司。
对氯苯乙酸(PCPA)、N,N-二甲基甲酰胺(DMF)、六水合硝酸镧,分析纯,上海阿拉丁生化科技股份有限公司。
1.2 配合物{[La(PCPA)3(H2O)2]∙DMF ∙(H2O)2}n的合成
将La(NO3)3·6H2O(0.5 mmoL,0.217 mg)、对氯苯乙酸(2 mmoL,0.34 mg)在25 mL 聚四氟乙烯不锈钢的反应釜中混合,反应釜中含有18 mL 蒸馏水和5 mLN,N-二甲基甲酰胺,在170 ℃下反应3 d,然后以5 ℃/h 的冷却速率冷却至室温,分离出白色晶体,用蒸馏水清洗后干燥即得配合物。
1.3 晶体结构测试
选取单晶大小尺寸为0.18 mm×0.16 mm×0.14 mm 的晶体进行XRD 表征,用石墨单色化的Mo Kα线(λ=0.071 073 nm),在2.213°≤θ≤28.266°、168 K 下,采用ω-scan 技术收集衍射数据,所有衍射数据还原和结构解析工作使用晶体学软件SHELXT-2014、SHELXL-2014 完成,所有非氢原子坐标用直接法解出,然后采用全矩阵最小二乘法进行修正,氢原子坐标通过Fourier 法和理论加氢确定[9]。
配合物最后的残差因子R1=0.024 1,wR2=0.045 8,配合物的主要晶体学特征如表1 所示,主要键长和键角如表2所示,氢键键长和键角如表3所示。配合物的编号为CCDC:2179596。
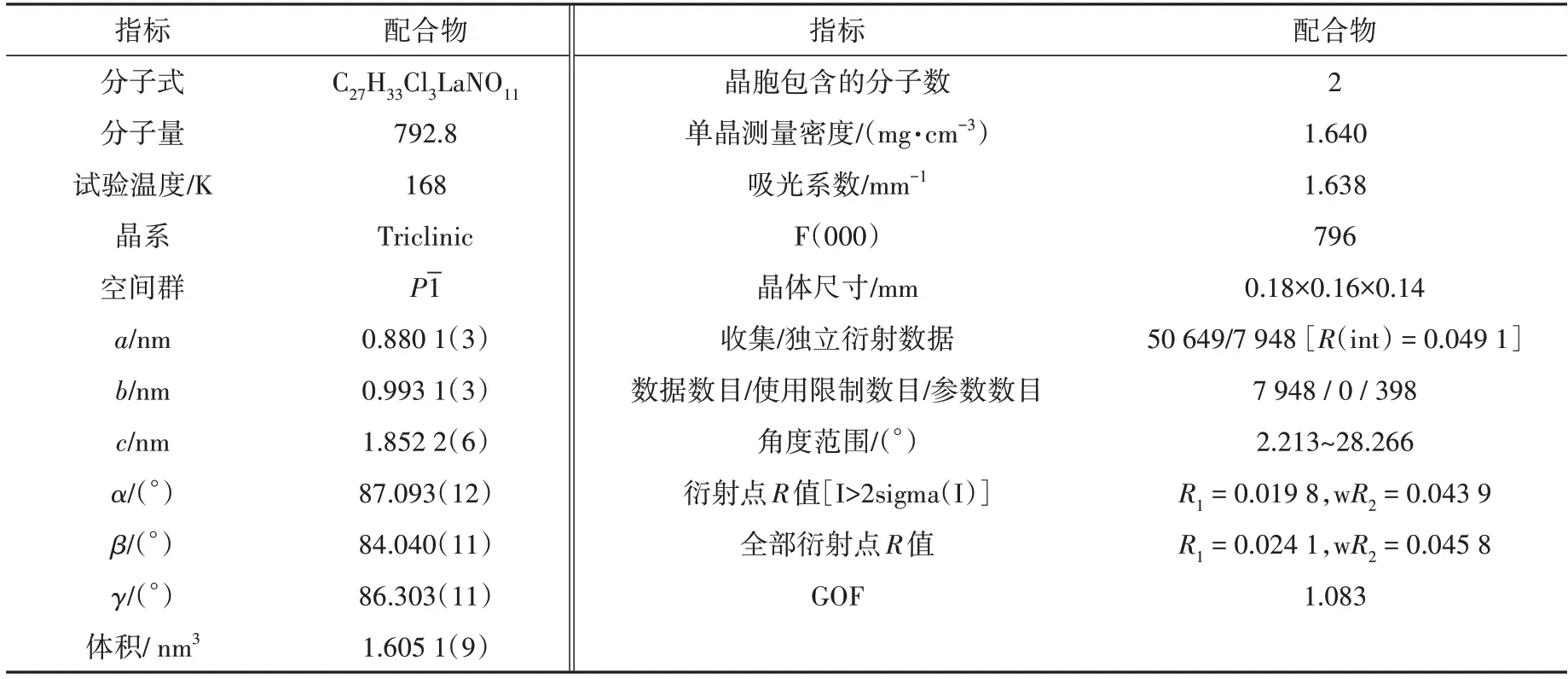
表1 配合物的晶体学特征

表2 配合物的主要键长和键角
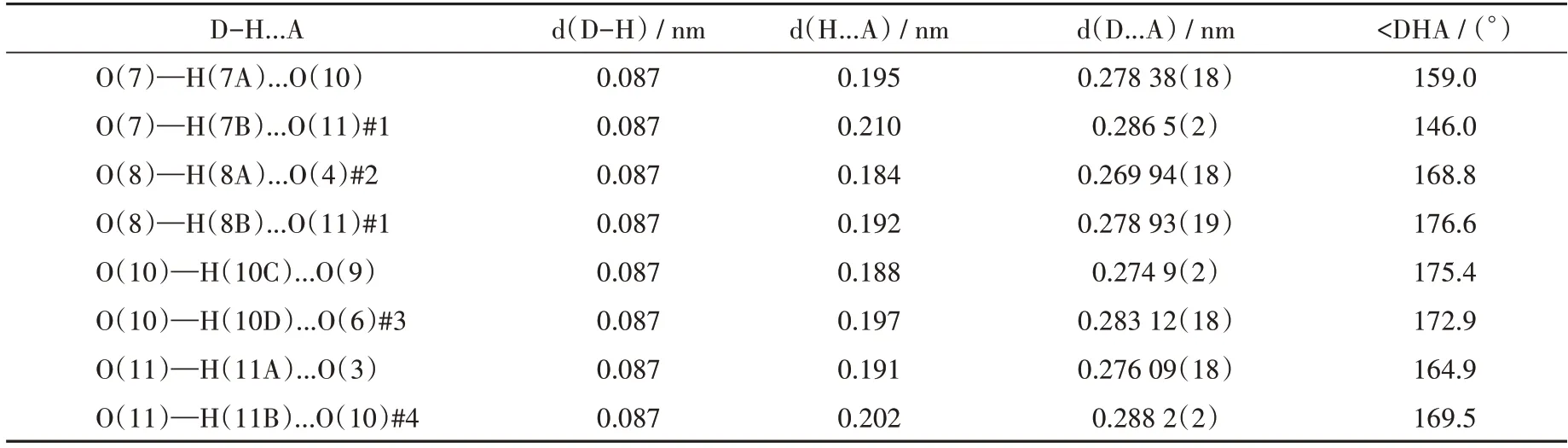
表3 配合物的氢键键长和键角
2 结果与讨论
2.1 配合物的晶体结构分析
图1 为配合物中心La(Ⅲ)离子的配位环境,晶体结构分析结果表明,配合物晶体结构属于三斜晶系、P1空间群,每个不对称结构单元包括1个La(Ⅲ)离子、3 个脱去活泼氢的对氯苯乙酸配体、2 个配位水分子、1 个游离N,N-二甲基甲酰胺分子和2 个游离的水分子。以金属La1 离子为例,La(Ⅲ)离子同时与10 个O 原子配位,形成了配位数为10 的配合物,其中,O10、O11 分别来自于两个结晶水分子;O9 来自于结晶物中的N,N-二甲基甲酰胺分子;O7、O8 分别来自于两个配位水分子,直接与La1 离子配位;来自第一个对氯苯乙酸配体中的O3、O4 以螯合的方式配位到La1 离子上;其余的O 原子来自对氯苯乙酸配体,即O6i、O1 直接与La1 离子配位,O2、O2i以桥联方式连接La2 和La1 离子,O5、O5i 以桥联方式连接La1 和La3 离子。在这种配位键作用下形成了一维链状结构,结果见图2,其中,La—O 的键长为0.250 5~0.266 2 nm,与已报道的La 离子配合物La—O 的键长(0.241 7~0.259 4 nm)大体一致[10-11]。形成的一维链再通过配体上的羧基氧原子与配位水分子中的氧原子形成氢键,彼此进一步连接,在平面上形成了二维网络结构层[12]。

图1 配合物中镧(Ⅲ)离子的配位环境

图2 配合物的一维链状结构
2.2 配合物的红外分析
室温下测定了配合物的红外光谱,结果见图3。由图3 可知:IR 谱图的主要吸收峰(cm-1)位于:3 414(m)、1 658(s)、1 564(s)、1 542(s)、1 494(m)、1 424(s)、1 396(s)、1 286(w)、1 202(w)、1 158(w)、1 090(m)、1 018(w)、1 018(w)、940(w)、809(m)、766(m)、680(m)、591(w)、502(w)、456(w)。
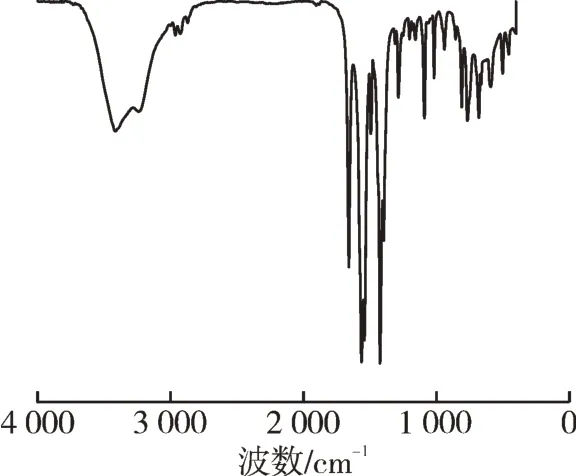
图3 配合物的红外光谱
2.3 配合物的衍射分析
图4 为室温下配合物的粉末衍射测试结果。由图4 可知:实验测定的粉末衍射图谱与Mercury软件基于晶体结构模拟得到的衍射峰角度基本吻合,说明配合物为纯相。
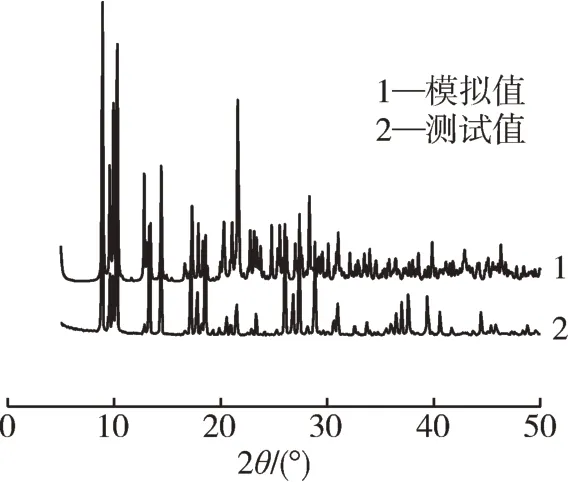
图4 配合物的衍射图谱
2.4 配合物的热重分析
在测试温度30~800 ℃、N2氛围、升温速率15 ℃/ min 的条件下,使用热重分析仪测试配合物的热重曲线,结果如图5 所示。由图5 可知:配合物的失重主要分为4步,第1步从131 ℃到150 ℃,质量损失率为4.56%,失去的是配合物中的2个结晶水分子(理论质量损失率为4.54%);第2 步从206 ℃到330 ℃,质量损失率为20.7%,失去的是配合物中的N,N-二甲基甲酰胺、2 个配位水分子和部分对氯苯乙酸配体;第3 步从458 ℃到499 ℃,质量损失率为21.67%,失去的是配合物中的1 个对氯苯乙酸配体(理论质量损失率为21.32%);第4步从688 ℃到788 ℃,质量损失率为11.93%,失去的是剩余的对氯苯乙酸配体,最终残留41.14%,与La2O341.10%相符。由此可知该配合物在室温下稳定。

图5 配合物的热重曲线
2.5 配合物的紫外光谱分析
以甲醇为空白溶剂,在波长200~400 nm 范围内,测定了1×10-4mol/L 配合物和对氯苯乙酸配体的紫外吸收光谱,结果见图6。由图6 可知:配合物在紫外区有较强吸收,主要是配体吸收引起的。这是因为对氯苯乙酸对位取代基团供电子效应引起苯环电子云分布发生改变[13-16],苯环产生π-π*跃迁,引起配合物吸收波长发生位移;配合物的最大吸收峰蓝移至225 nm 处,也表明对氯苯乙酸与La(Ⅲ)离子发生了配位。

图6 对氯苯乙酸配体和配合物的紫外吸收光谱
2.6 配合物的荧光光谱分析
图7 是对氯苯乙酸配体和配合物的荧光光谱分析结果。由图7 可知:对氯苯乙酸配体的最强激发峰(ex)在395 nm,在491 nm 有最强发射峰(em);配合物的最强激发峰在376 nm,最强发射峰在468 nm。与配体相比,配合物荧光强度增加,可能是配合物结构刚性增强和电子跃迁的原因[17-19]。由此可见,该配合物有较好的荧光性能。

图7 对氯苯乙酸配体和配合物的荧光光谱
3 结论
以对氯苯乙酸为配体,与六水合硝酸镧通过水热法合成了镧系配合物。X 线单晶衍射分析结果表明配合物属于三斜晶系、P1 空间群;热重分析结果表明配合物在室温下稳定;紫外可见光谱和荧光光谱分析结果表明配合物具有很好的荧光性,在紫外区有强的吸收,最大吸收峰位于225 nm 处,最强激发峰和发射峰分别在376 nm 和468 nm。研究结果丰富了镧配合物的种类,为其后期应用于荧光材料奠定基础。
