基于网络药理学结合正交设计优化复方降脂口服液的提取工艺
2023-09-27曹蕾邹明慧秦雪莹闫占宽冯静高珣秦昆明
曹蕾, 邹明慧, 秦雪莹, 闫占宽, 冯静, 高珣*, 秦昆明
(1.江苏海洋大学药学院, 连云港 222005; 2. 江苏原创药物研发有限公司, 连云港 222000; 3.辽宁省疾病预防控制中心, 沈阳 110000)
单纯性肥胖是一种由于长期摄入过多热量及消耗不充分,使得脂肪积累、脂质代谢紊乱的慢性代谢性疾病[1-3]。肥胖伴随有糖尿病、高血压以及心血管和肾脏疾病的发生,为了倡导全球各国关注超重和肥胖人群的预防控制,世界肥胖联盟(World Obesity Federation, WOF)2020年宣布每年3月4日为“世界肥胖日”,根据《中国居民营养与慢性病状况报告(2020年)》的最新数据显示,目前中国的成人中已经有超过半数的人超重或肥胖,全国已经有6 亿人超重和肥胖[4]。目前,最常见的是药物治疗,如氯卡色林、利拉鲁肽、奥利司他等,然而这类化学药物常出现消化道不良等副作用,中药有望在该领域取得一席之地。中医对肥胖的认识最早起源于《黄帝内经》,认为主要是因脾胃失调从而导致超重等。
依据中医药理论基础,复方降脂口服液由焦山楂、赤小豆、决明子、荷叶、茯苓、薏苡仁、玫瑰花、陈皮、枸杞子9 味中药组成。以焦山楂为君药,现代药理研究表明焦山楂及其焦香味可促进单纯性肥胖大鼠胃动力,调节干细胞因子-受体酪氨酸激酶信号通路从而达到减肥作用[5-6];荷叶、决明子为臣药,荷叶中的生物碱类、黄酮类以及决明子中蒽醌类、萘并吡喃酮类物质能够调控mTOR信号通路、抑制3T3-L1前脂肪细胞的增殖,介导脂肪代谢相关酶的表达[7-9];配赤小豆、茯苓、薏苡仁利水消肿,陈皮、玫瑰花、枸杞子理气调中、行气解郁、滋补肝肾,诸药合用,能够针对单纯性肥胖患者达到减肥降脂的效果[10]。为探究复方降脂口服液的最佳提取工艺,现基于网络药理学探究复方中治疗单纯性肥胖的活性成分、作用靶点以及信号通路[11],并筛选活性成分与作用靶点进行分子对接以阐明成分-靶点之间具有良好活性,同时分析处方中治疗肥胖症的主要活性成分,以此为测定指标进行单因素及正交设计优化工艺参数,为复方口服液后续生产提供试验依据。
1 仪器与材料
1.1 仪器
UV-TU-1901型紫外-可见分光光度计(上海元析仪器有限公司);MS105DU型十万分之一电子分析天平(梅特勒托利多仪器上海有限公司,精度为0.01 mg);BSM-120.4万分之一电子天平(上海卓精电子科技有限公司);DZTW型加热套、RE-52AA旋转蒸发仪(上海力辰邦西仪器有限公司);DHG-9080A鼓风干燥箱(上海博珍仪器设备制造厂)。
1.2 药材与试剂
焦山楂(批号:20050604)、赤小豆(批号:210801)、决明子(批号:210701)、茯苓(批号:22012002-1)、陈皮(批号:21032601)以及荷叶(批号:210601)均购自连云港市北京同仁堂药房;枸杞子(批号:220424)、薏苡仁(批号:210524)及玫瑰花(批号:200628)均购自南京海源中药饮片有限公司;芦丁对照品(批号:PU001-0025,纯度为99.0%)购自成都普思生物科技股份有限公司);无水乙醇、硝酸铝[Al(NO3)3]、亚硝酸钠(NaNO2)、氢氧化钠(NaOH)均为分析级;水为实验室自制超纯水。
2 方法与结果
2.1 复方降脂口服液网络药理学研究
2.1.1 复方降脂口服液的活性成分及作用靶点筛选
通过TCMSP(http: //tcmspw.com)检索复方降脂口服液的活性成分,以类药性(DL)≥0.18和口服生物利用度(OB)≥30%为条件,以及相关文献总结焦山楂中的活性成分[12-14]。将活性成分在Pubchem(https://pubchem.ncbi.nlm.nih.gov/)转成SMILES格式,并导入SwissTargetPrediction[11](http://www.swisstargetprediction.ch/)收集Probability≥0.12的作用靶点。最终筛选出复方中8味中药的活性成分共有116种活性成分(去除重复),舍去未有靶点的活性成分,共得到390个作用靶点,结果如表1所示。

表1 复方降脂口服液的主要活性成分Table 1 Main active components of compound lipid-lowering oral liquid
2.1.2 单纯性肥胖疾病靶点筛选
在Genecards(https://www.genecards.org/)数据库中分别输入关键词“simple obesity”“obesity”“hyperlipidemia”获得疾病靶点,并设定Relevance score≥10筛选疾病靶点207 个。将活性成分的作用靶点与肥胖症疾病靶点导入Venny(https://bioinfogp.cnb.csic.es/ tools/venny/)在线平台进行靶点交集,得到27 个交集靶点。
2.1.3 “中药-活性成分-作用靶点”网络构建与分析
将药材中活性成分进行ID编号,其中含有9 个重复成分,以A1、B1、B2、C1、D1、E1、E2、G1、G2表示,分别代表的是槲皮素、豆甾醇、CLR、谷甾醇、环阿屯醇、α1-谷甾醇、亚油酸乙酯、β-谷甾醇、花青苷。将“中药-活性成分-作用靶点”的网络文件和属性文件导入Cytoscape3.7.1软件中构建网络图,如图1所示。结果数据分析得出,该网络共有490个节点,共有1 665条边,其中Degree≥20的活性成分有24 种,分别来自焦山楂、荷叶、茯苓、玫瑰花、枸杞子这5味药材,其中作用较强的化合物是槲皮素、维生素-E、山柰酚、异鼠李素等;Degree≥20的作用靶点有9 个,分别是CYP19A1、AR、PTPN1、ESR2、SHBG、ESR1、NR1H3、HMGCR、RORC。

绿色三角形表示中药名称,蓝色菱形表示作用靶点,所有圆形表示中药活性成分;JSZ为焦山楂;CXD为赤小豆;JMZ为决明子;HY为荷叶;FL为茯苓;YYR为薏苡仁;MGH为玫瑰花;CP为陈皮;GQZ为枸杞子图1 “中药-有效成分-作用靶点”网络图Fig.1 “Medicinal material-component-target” network diagram
2.1.4 PPI网络的构建与分析
将27个交集靶点导入STRING(https: //string-db.org/)数据库分析,构建PPI网络如图2所示。节点所显示的形状越大、颜色越深,说明该靶点的度(degree)就越高;边的粗细反映连接评分(combined score)大小变化,边越粗combined score越大。由可视化结果分析可知,得到27个节点和138条边,平均节点值为10.2,其中AKT1、IL6、PPARG、TNF是在PPI网络中有较高程度的节点,可能是肥胖症的核心候选靶点。

图2 PPI网络图Fig.2 PPI network diagram
2.1.5 GO功能富集和KEGG通路富集分析
将交集靶点导入Metascape数据库(https://metascape.org/)进行GO功能和KEGG通路富集分析,且采用微生信平台(http://www.bioinformatics.com.cn)绘制富集图。GO富集得到所有功能条目563 条,包括522 条生物过程条目(biological process,BP),31条分子功能条目(molecular function,MF)以及10 条细胞组成条目(cellular composition,CC)。其中生物过程主要包括防御反应的调节(regulation of defense response)、蛋白质磷酸化的正向调节(positive regulation of protein phosphorylation)、炎症反应的调节(regulation of inflammatory response)、蛋白质激酶活性的调节(regulation of protein kinase activity)等,分子功能主要包括核受体活性、配体激活的转录因子活性、核类固醇受体活性、脂质结合、类固醇结合等,细胞组分主要包括受体复合体、质膜外侧、神经元细胞体等,如图3所示。
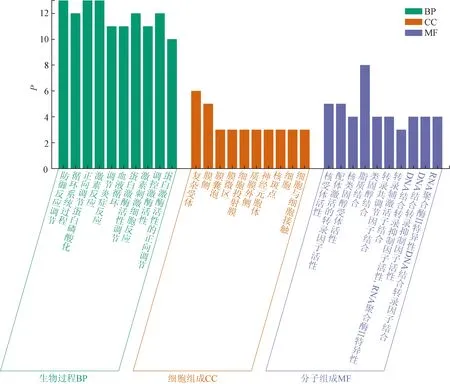
图3 GO功能富集分析网络图Fig.3 Network diagram of GO functional enrichment analysis
KEGG通路富集得到87 条信号通路,以富集程度(enrichment)、显著性(lgP)值高于均值为标准,筛选出前10 条信号通路进行可视化分析,主要包括胰岛素抵抗、糖尿病并发症中的AGE-RAGE信号通路、脂肪分解调节、TNF信号通路、AMPK信号通路[15-18]等,如图4所示。
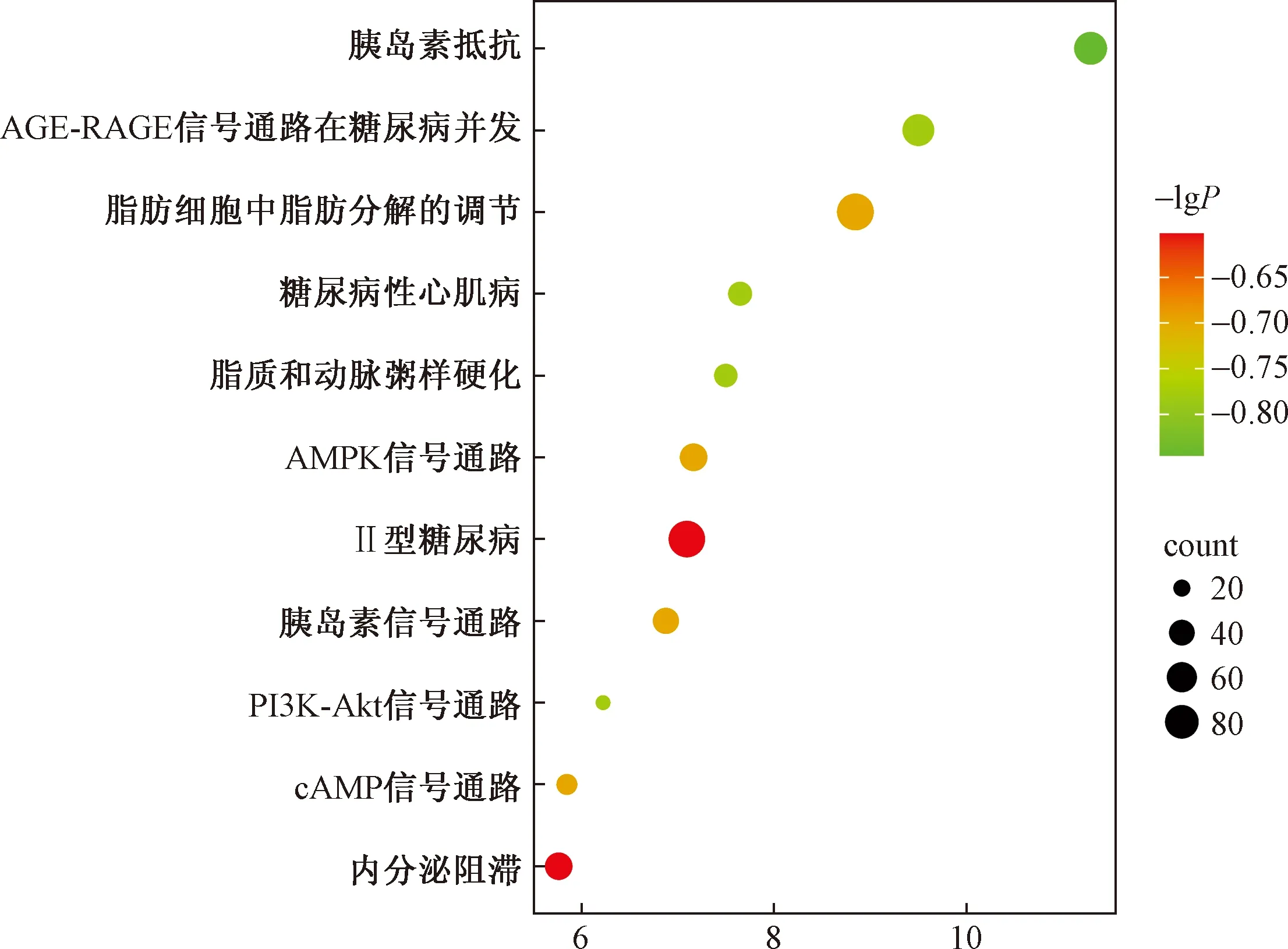
图4 KEGG通路分析图Fig.4 KEGG pathway analysis diagram
2.1.6 “活性成分-作用靶点-信号通路”网络构建与分析
为进一步探究中药活性成分、作用靶点与信号通路之间的相互联系,从KEGG通路富集分析数据中进行筛选,将各信号通路导入KEGG(https://www.kegg.jp/)中查询信号通路与肥胖症的联系,获得20 条与肥胖密切相关的关键信号通路,构建“活性成分-作用靶点-信号通路”网络图并进行拓扑分析, 如图5所示。结果分析显示,3β-羟基-羊毛甾-24-亚甲基-21-酸、槲皮素、山柰酚、异鼠李素为核心成分。
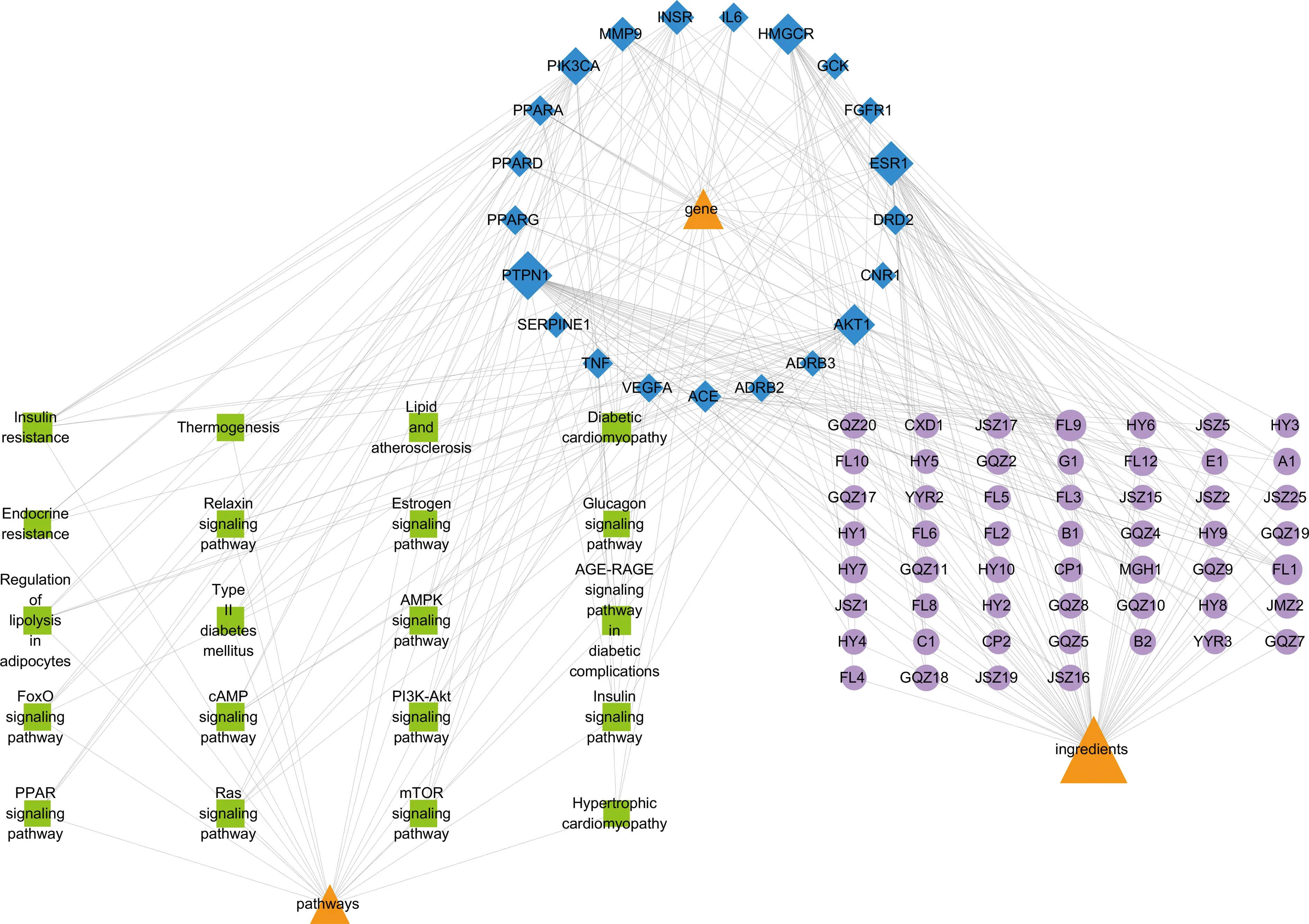
菱形表示作用靶点;长方形表示信号通路;圆形表示复方活性成分图5 有效成分-关键靶点-主要通路网络图Fig.5 Components-key targets-main pathway network diagram
2.1.7 分子对接验证
以PPI网络图中Degree值高低进行排序,选择前3 个关键靶点(AKT1、IL6、PPARG)分别与“中药-活性成分-作用靶点”网络数据中3 个关键成分(4-羟基肉桂酸、异鼠李素、山柰酚)进行分子对接,从表2中分析发现与3 个核心靶点对接最低结合能的活性成分为异鼠李素,能与AKT1、IL6、PPARG可以较好结合,如图6所示,分别是异鼠李素与AKT1、IL6、PPARG分子对接的2D、3D图。
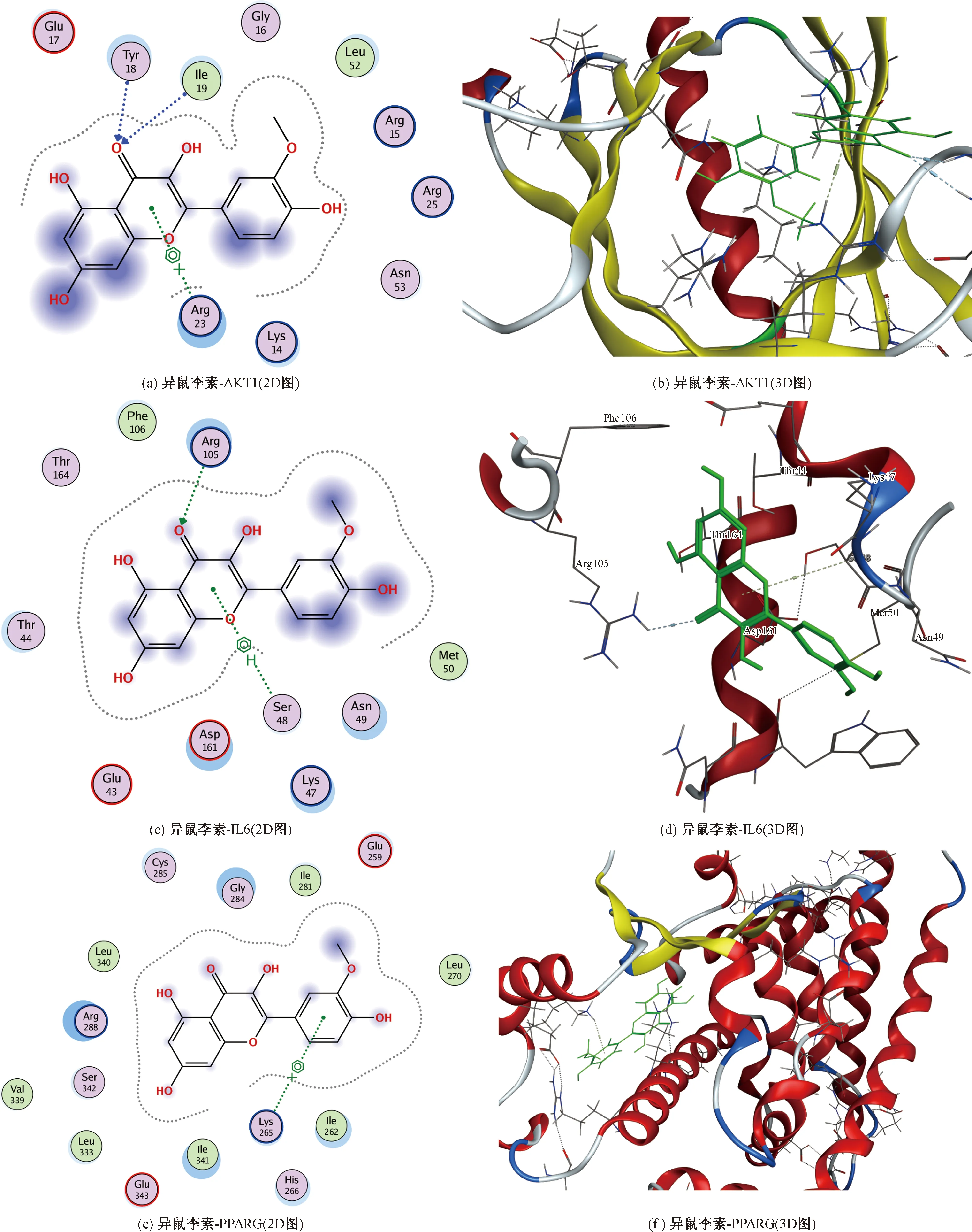
图6 异鼠李素与AKT1、IL6、PPARG受体-配体相互作用2D、3D图Fig.6 2D and 3D images of the interaction of isorhamnetin with AKT1, IL6 and PPARG receptor-ligand

表2 关键活性成分与核心靶点分子对接的分子结合力Table 2 Molecular binding force of key active ingredients for docking with core target molecules
2.2 总黄酮含量测定
2.2.1 溶液的配制
取芦丁对照品约10 mg,精密称定,置于25 mL容量瓶中,加入60%乙醇溶解稀释定容至刻度,摇匀,即得芦丁对照品溶液(400 μg/mL)。按处方称取药材125 g,加入1 500 mL量水,浸泡60 min后煎煮45 min,后下荷叶、玫瑰花、陈皮,共煎25 min,过滤浓缩至约200 mL,加水定容至250 mL。精密移取1 mL浓缩液,置于10 mL容量瓶中,加60%乙醇混合均匀,并定容至刻度,摇匀后过0.45 μm滤膜,即得供试品溶液。
2.2.2 检测波长的选择
精密移取适量2.2.1节下对照品溶液和供试品溶液,分别加入5% NaNO20.3 mL,摇匀放置6 min,再加入10% Al(NO3)30.3 mL,摇匀放置6 min,最后加入4% NaOH 4.0 mL,60%乙醇定容至10 mL,摇匀放置10 min[19]。以60%乙醇溶液作为空白,在400~900 nm波长范围内进行全扫描。结果测得芦丁对照品溶液最大吸收在509 nm处。
2.2.3 方法学考察
线性关系:精密移取对照品溶液0、0.4、0.8、1.2、1.6、2.0 mL,置于不同10 mL具塞比色管内,按照2.2.2节方法操作测定线性溶液的吸光度。以吸光度(Abs)作为纵坐标,溶液浓度C作为横坐标进行线性绘图,得到线性方程为A=0.011 6C-0.002 1(r2=0.999 7,n=5),表明芦丁对照品溶液在0~96 μg/mL范围内线性关系良好。
精密度试验:分别精密移取芦丁对照品溶液1.2 mL、供试品溶液1 mL,置于不同的10 mL具塞比色管中,连续测定6次,RSD分别为0.07%、0.26%,表明该方法仪器精密度、重复性良好。
稳定性试验:精密移取芦丁对照品溶液1.2 mL,在室温下分别静置0、10、20、30、40、50、60 min后进行测定。结果表明在室温下显色后60 min内稳定性良好,相对标准偏差(relative standard deviation,RSD)为0.83%,因此检测应在显色后60 min内进行测定。
加样回收率试验:精密移取已知总黄酮含量的供试品溶液0.5 mL和芦丁对照品溶液(400 μg/mL)0.6 mL置于10 mL比色管中,平行制备6份,测定吸光度并计算总黄酮含量(total flavonoid content,TFC)。结果得平均加样回收率为104.89%,表明该方法的准确度良好。
2.3 干膏得率的测定
精密移取10 mL水提浓缩液置于蒸发皿(已干燥至恒重)中,水浴蒸干,置于105 ℃烘箱中干燥3 h后,于干燥器冷却30 min,迅速称定质量,再于105 ℃干燥1 h,冷却称定质量,反复干燥至恒定质量,计算干膏率。
2.4 复方降脂口服液提取工艺优化
2.4.1 单因素试验结果分析
以不同的加水量A(500、750、1 000、1 250、1 500 mL)、浸泡时间B(20、30、40、60、70 min)、先煎时间C(30、45、60、75、90 min)、后下共煎时间D(5、15、25、35、45 min)为考察因素,进行加热回流提取,以总黄酮含量和干膏得率为评价指标,确定各因素三水平[20],如表3所示。
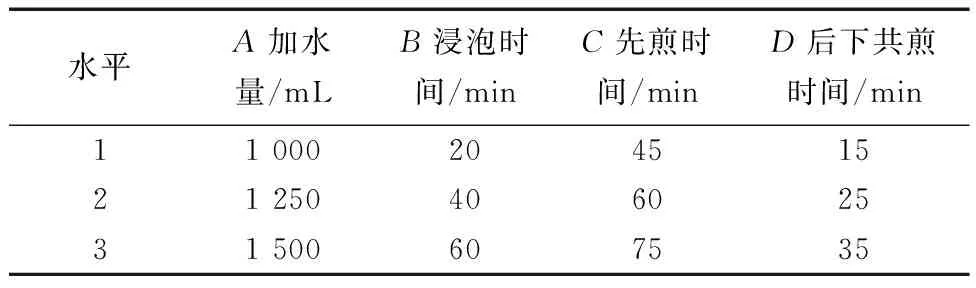
表3 提取工艺正交试验因素水平表Table 3 Levels and factors of the orthogonal of water extraction
2.4.2 正交设计试验
在单因素试验的基础上,采用L9(34)正交试验设计,以总黄酮含和干膏率为综合评价指标(C),优化复方降脂口服液的提取工艺参数。

(1)
式(1)中:TFCi为测得总黄酮含量;TFCmax为测得最大总黄酮含量;Gi为测得干膏率;Gmax为测得最大干膏率。
如表4所示,直观分析各因素对复方降脂口服液的提取工艺的影响依次为A>B>D>C。如表5所示,加水量对提取效果的影响具有显著性(P<0.05)。最佳提取条件为A3B3C1D2,即加水量为1 500 mL、浸泡时间为60 min、先煎时间为45 min、后下共煎时间为25 min。

表4 正交实验直观分析表Table 4 Results of orthogonal test
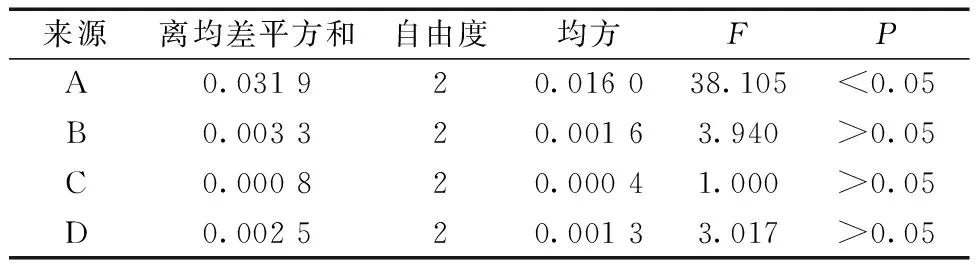
表5 水提工艺试验方差分析表Table 5 Analysis of variance of water extraction
2.4.3 工艺验证
对优选的最佳工艺参数A3B3C1D2,进行工艺验证,平行制备3份样品,测定总黄酮含量及干膏率,如表6所示。在最佳提取工艺条件下,总黄酮含量和干膏率的RSD分别为1.26%和0.59%。

表6 工艺验证结果Table 6 Results of process validation
3 讨论与结论
肥胖是一种由遗传、环境等多因素而引起能量代谢紊乱的慢性炎症,中医认为该症与脾胃功能失调有关。复方降脂口服液依据中医药理论组成,能够综合调节机体以实现减肥降脂的功效,但药理作用机制尚不明确。采用网络药理学方法,构建了“中药-活性成分-作用靶点”和“活性成分-作用靶点-信号通路”调控网络图,筛选得到116种活性成分,其中大多数化合物归属于焦山楂、荷叶、决明子、茯苓、枸杞子这5味药材,与中医药治疗肥胖组方的用药频次一致[21-22];活性成分的作用靶点与单纯性肥胖疾病靶点映射得到24个交集靶点,PPI网络拓扑分析发现AKT1、IL6、PPARG、TNF是治疗肥胖症的关键靶点,且GO功能富集及KEGG通路富集分析得出本品治疗单纯性肥胖,主要作用于AKT1、IL6、PPARs、TNF、VEGFA等靶点,调控胰岛素抵抗、AGE-RAGE信号通路、脂肪分解、AMPK、PI3K-Akt等信号通路,也有研究表明通过刺激肿瘤坏死因子(TNF-α)、白细胞介素(IL6、IL20)等的释放激活胰岛素抵抗、炎症反应,从而缓解代谢综合征[23];分子对接结果表明:异鼠李素、山柰酚与PPARG的结合力较好,且异李鼠素对AKT1、IL6、PPARG的结合能力均强于4-羟基肉桂酸、山柰酚;由此可见,该口服液通过多成分-多靶点-多通路-多生物途径,实现治疗单纯性肥胖[24-26]。
通过网络药理学及分子对接技术对复方降脂口服液治疗单纯性肥胖的作用机制进行了预测,并筛选出其治疗肥胖的活性成分如黄酮类、有机酸类、甾醇类化合物,其中绝大多数物质为黄酮类化合物。基于此,以总黄酮含量及干膏得率作为评价指标,采用先煎后下的提取方式考察加水量、浸泡时间、先煎时间、后下共煎时间对提取工艺的影响,确定最佳提取工艺条件为加水量1 500 mL、浸泡60 min后煎煮45 min,后下荷叶、陈皮、玫瑰花共煎25 min,并工艺验证该提取条件稳定可靠,可为后续进行工业生产奠定理论基础。
