吉非替尼联合顺铂治疗晚期非小细胞肺癌的临床研究
2023-09-26董竞瑾倪荣萍刘靖丰
董竞瑾,倪荣萍,刘靖丰
淮南东方医院集团总医院 呼吸内科,安徽 淮南 476005
肺癌是临床发病率较高的恶性肿瘤之一,其发病率及死亡率在临床中均排名第1,其中非小细胞肺癌最为常见[1],患者早期没有显著的典型症状,难以及时检测出,导致较多患者发展至中晚期,因此很难通过胸腔镜手术根除[2-3]。临床常用广谱抗肿瘤药物顺铂,是一种金属铂类络合物,通过与细胞核内DNA 的碱基结合,形成3 种形式的交联,造成DNA 损伤,破坏DNA 复制和转录。顺铂抗癌谱广、作用性强,常用与联合靶向药物治疗非小细胞肺癌[4]。晚期非小细胞肺癌患者的治疗方式多为多靶点药物联合化疗治疗,如培美曲塞等多靶点化疗药物,但其在免疫系统等方面不良反应明显。吉非替尼是一种表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI),其对晚期非小细胞肺癌患者有较好的治疗效果,其靶向抑制表皮生长因子受体酪氨酸激酶,对肿瘤生长、转移以及血管生成可进行有效抑制,同时诱导肿瘤细胞的凋亡,且不良反应较少[5-6]。本研究旨在回顾性分析吉非替尼联合顺铂治疗晚期非小细胞肺癌患者的疗效、不良反应及对免疫功能的影响,为吉非替尼临床应用提供研究基础。
1 资料和方法
1.1 一般资料
采用回顾性分析方法,严格按照纳排标准筛选出2017 年2 月—2020 年4 月淮南东方医院集团总医院收治的60 例晚期非小细胞肺癌患者的临床资料作为研究对象,其中男性33 例,女性27 例;Ⅲ期36,Ⅳ期24 例。
本次研究上报备案至本院伦理委员会,通过并批准,同时纳入研究所有患者均签订知情同意书。
纳入标准:参照《中华医学会肺癌临床诊疗指南》确诊非小细胞肺癌者[6];临床分期为Ⅲ期、Ⅳ期者;符合采用吉非替尼靶向治疗;患者自愿参与,签订知情同意书。
排除标准:严重重要脏器如肝、肾、心功能异常;已知对该活性物质或该产品任一赋形剂有严重超敏反应者;接受过手术、化疗及放疗等综合治疗。
1.2 药物
吉非替尼片由齐鲁制药(海南)有限公司生产,规格0.2 5g/片,产品批号DC1B0082、DC1B0083;顺铂注射液由江苏豪森药业集团有限公司生产,规格6 mL∶30 mg,产品批号601200401、601 200402;注射用培美曲塞二钠由齐鲁制药有限公司生产,规格0.2 g/支,产品批号9M0116B05、9M0116B06。
1.3 分组和治疗方法
根据用药方案不同将患者分为对照组和治疗组,每组各30 例。其中对照组男性16 例,女性14例;平均年龄(59.85±7.39)岁;Ⅲ期19 例,Ⅳ期11 例。治疗组男性17 例,女性13 例;平均年龄(59.67±7.40)岁;Ⅲ期17 例,Ⅳ期13 例。两组患者性别构成、年龄、临床分期等资料比较差异均无统计学意义,可以进行临床回顾性分析比较。
对照组患者化疗第1 天静脉滴注注射用培美曲塞二钠,500 mg/m2,注射时间大于10 min,化疗第1~3 天静脉滴注顺铂注射液,75 mg/m2,给药前2~16 h 和给药后至少6 h 内必需进行充分的水化治疗。治疗组从化疗第1 天开始口服吉非替尼片,250 mg/d。同时化疗第1~3 天静脉滴注顺铂注射液,用法用量同对照组。两组均以3 周为1 个疗程,治疗2 个疗程。
1.4 临床疗效判断标准[8-9]
完全缓解(CR):肿瘤全部消失,维持4 周以上;部分缓解(PR):肿瘤减少大于50%,并维持4周以上;疾病稳定(SD):肿瘤减少不超过50%;肿瘤进展(RD):肿瘤增大20%及以上。
客观缓解率(ORR)=(CR 例数+PR 例数)/总例数
疾病控制率(DCR)=(CR 例数+PR 例数+SD 例数)/总例数
DEA方法的一个重要功能在于,可以通过找出投入要素的冗余和产出的不足,进而有针对性地为战略决策和发展路径提供转变的方向和程度。该研究更加注重投入最小和最小投入下高新技术企业利益最大化,所以分析中采用CCR模型。DMU4企业的纯技术效率<1,说明该企业的投入存在一定的冗余,可通过投影分析比较发现投入无效率的要素,从而更好的为高新技术企业发展提供量化的参考依据。在此,借助软件(DEA-SLOVER3.0)对DMU4高新技术企业进行超效率DEA分析,运行后的结果显示如表4。
1.5 观察指标
1.5.1 生活质量评价 中国癌症化疗患者生活质量量表评分包括患者躯体如睡眠、乏力、食欲等;心理如医护态度、焦虑、配合治疗情绪等;社会如经济、交往等[10]。卡氏功能状态量表(KPS)评分:对两组患者治疗前后功能状态进行评价,80 分以上为非依赖级,即生活自理;50~70 分为半依赖级,即生活半自理;50 分以下为依赖级,即生活需要别人帮助[7]。
1.5.2 实验室免疫指标 收集所有患者治疗前后血液,Ficoll 密度梯度离心得到PBMC,标记CD4+、CD8+等流式抗体(ThermoFisher Scientific),采用赛默飞Attune NxT 流式细胞仪检测CD4细胞(CD4+)、CD8 细胞(CD8+)。
1.5.3 肿瘤标志物 治疗前后抽取患者空腹静脉血,使用酶联免疫吸附法测定血清肿标瘤志物,包括癌胚抗原(CEA)、神经元特异性烯醇化酶(NSE)、血管内皮生长因子(VEGF)。
1.5.4 血清细胞因子水平 治疗前后抽取患者空腹静脉血,使用酶联免疫吸附法测定血清白细胞介素-2(IL-2)、白细胞介素-4(IL-4)、白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)、干扰素-γ(INF-γ)。
1.5.5 总生存率(OS)和无进展生存率(PFS)随访两组患者3 年,观察两组患者OS、PFS。OS 生存率:随访日期时存活例数占开始随访总例数的比值。PFS 生存率:随访日期时未发生肿瘤进展或肿瘤相关死亡的病例数占开始随访总例数的比值。
1.6 不良反应观察
观察两组不良反应发生率及类型,如肝肾功能、皮肤系统、消化道系统等方面的不良反应。
1.7 统计学方法
2 结果
2.1 两组临床疗效比较

表1 两组临床疗效比较Table 1 Comparison on clinical efficacy between two groups
2.2 两组生活质量相关评分比较
治疗后,对照组躯体、心理、社会、总分均显著低于治疗前(P<0.05),两组KPS 评分显著高于治疗前(P<0.05)。治疗后治疗组患者躯体、心理、社会、总分及KPS 评分均显著高于对照组(P<0.05),见表2。
表2 两组生活质量相关评分比较()Table 2 Comparison on life quality related scores between two groups ()
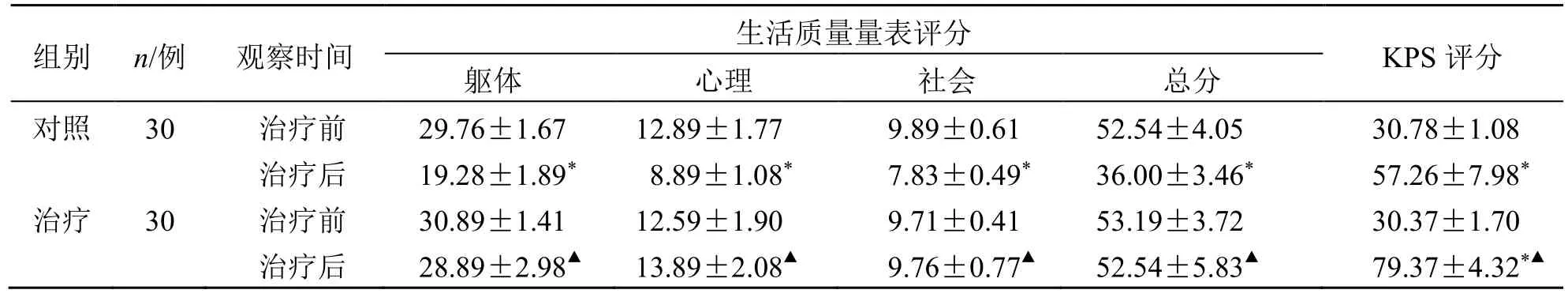
表2 两组生活质量相关评分比较()Table 2 Comparison on life quality related scores between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05*P <0.05 vs same group before treatment;▲P <0.05 vs control group after treatment
2.3 两组免疫指标比较
治疗后,治疗组患者CD4+和CD4+/CD8+均显著上升,CD8+下降(P<0.05);对照组 CD4+和CD4+/CD8+均显著下降(P<0.05),CD8+有上升趋势但无统计学意义。治疗后,治疗组患者CD4+和CD4+/CD8+显著高于对照组,CD8+低于对照组(P<0.05),见表3。
表3 两组免疫指标比较()Table 3 Comparison on immune indexes between two groups ()
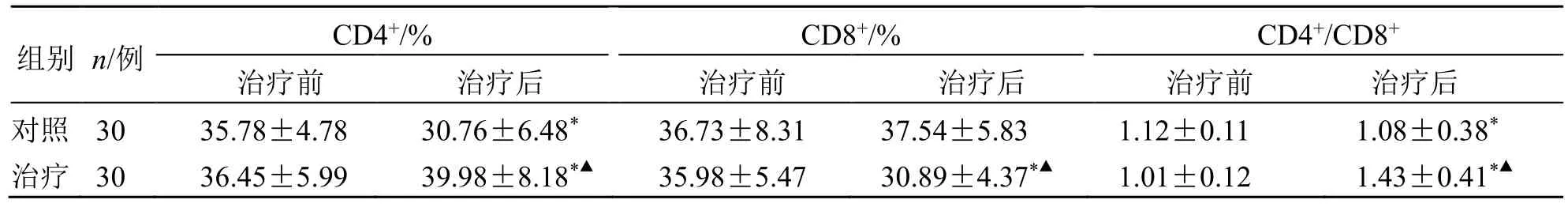
表3 两组免疫指标比较()Table 3 Comparison on immune indexes between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05*P <0.05 vs same group before treatment;▲P <0.05 vs control group after treatment
2.4 两组肿瘤标志物比较
治疗后,两组CEA、NSE、VEGF 均显著下降(P<0.05);且治疗后治疗组CEA、NSE、VEGF 水平显著低于对照组(P<0.05),见表4。
表4 两组肿瘤标志物比较()Table 4 Comparison on tumor markers between two groups ()

表4 两组肿瘤标志物比较()Table 4 Comparison on tumor markers between two groups ()
与同组治疗前比较:*P<0.05;与对照组治疗后比较:▲P<0.05*P <0.05 vs same group before treatment;▲P <0.05 vs control group after treatment
2.5 两组血清细胞因子比较
治疗后,两组患者IL-2、IL-6、TNF-α 和INFγ 显著升高,而IL-4 显著降低(P<0.01);且治疗后,治疗组IL-6 和INF-γ显著高于对照组(P<0.05),见表5。
表5 两组血清细胞因子比较()Table 5 Comparison on serum cytokines between two groups ()

表5 两组血清细胞因子比较()Table 5 Comparison on serum cytokines between two groups ()
与同组治疗前比较:**P<0.01;与对照组治疗后比较:▲P<0.05**P <0.01 vs same group before treatment;▲P <0.05 vs control group after treatment
2.6 两组OS 和PFS 比较
随访发现,治疗组OS、PFS 中位生存时间分别为20.6、28 个月,对照组为16、19 个月。Log-rank(Mantel-Cox) test 结果显示,治疗组PFS 显著优于对照组(P<0.05),而OS 虽有一定趋势但无显著性差异,见图1。

图1 两组OS 和PFSFig.1 OS and PFS of two groups
2.7 治疗期间两组不良反应比较
对照组发生腹泻1 例,皮疹2 例,肝功能异常2 例,恶心呕吐4 例,不良反应发生率是30.0%;治疗组发生腹泻2 例,皮疹4 例,肝功能异常2 例,恶心呕吐5 例,不良反应发生率是43.3%,两组不良反应发生率比较差异无统计学意义,见表6。

表6 两组不良反应比较Table 6 Comparison on adverse reactions between two groups
3 讨论
目前,晚期非小细胞肺癌患者的治疗方式多采用顺铂类药物化疗,但化疗所引起的不良反应如免疫功能严重下降始终是化疗无法逾越的沟壑[11]。尤其是肺癌多发病于老年人群,患者免疫功能本就脆弱,导致其对化疗的耐受性不足[12]。甚者可能会打断化疗计划。近年来,随着肿瘤分子生物学技术的不断发展,靶向治疗药物的应用愈发广泛,如吉非替尼是晚期非小细胞肺癌患者的主要药物选择[13-14]。
本研究发现,吉非替尼联合顺铂能有效治疗晚期非小细胞肺癌患者,客观缓解率、疾病控制率显著高于对照组。可见对于晚期非小细胞肺癌患者,吉非替尼联合顺铂治疗能有效改善患者病情,对于患者携瘤生存,患者自身免疫系统是一个主要的方面。研究发现,治疗组CD4+和CD4+/CD8+细胞显著高于对照组,CD8+显著低于对照组,治疗组患者自身免疫系统明显改善[15-16]。两组治疗后,治疗组CD4+和CD4+/CD8+均显著上升,CD8+显著下降,差异有统计学意义(P<0.05);对照组 CD4+和CD4+/CD8+均显著下降,CD8+有上升趋势但无统计学意义。治疗后,治疗组患者CD4+和CD4+/CD8+显著高于对照组(P<0.05),表明吉非替尼联合顺铂能有效改善患者的免疫功能。Th1 亚群分泌IL-2、INF-γ 并介导免疫功能,影响IL-4、IL-6 和IL-10 等细胞因子的分泌,对体液免疫功能起着重要的介导作用[17-20]。TNF-α 对免疫功能有调节作用,且可增强杀伤肿瘤细胞的作用,其在体内、体外均能杀死肿瘤细胞,或抑制其增殖[21-22]。两组患者治疗后IL-2、IL-6、TNF-α 和INF-γ 显著升高,而IL-4 显著降低,差异有统计学意义(P<0.01)。且治疗组IL-6和INF-γ 显著高于对照组(P<0.05),表明吉非替尼联合顺铂对患者治疗后炎症及免疫功能有显著改善作用[22]。VEGF 促进血管内皮细胞的增殖,加快肿瘤发展,CEA、NSE 可用于肿瘤鉴别诊断、疗效评价、病情监测,是重要的肿瘤标志物[24-25]。治疗前两组相关肿瘤标志物差异无统计学意义。治疗后,两组CEA、NSE、VEGF 水平均显著下降,差异有统计学意义(P<0.05);且治疗组低于对照组,差异有统计学意义(P<0.05),说明吉非替尼联合顺铂治疗时,患者体液免疫状况优于化疗及多靶点药物治疗。监测患者不良反应发现,两组患者均出现不同的不良反应,但组间比较差异无显著性,提示吉非替尼在有效治疗晚期非小细胞肺癌患者,改善自身免疫的状况下,无显著不良反应。3 种药物药理作用机制中,培美曲塞抑制叶酸合成必须酶,破坏细胞叶酸依赖性代谢,抑制肿瘤生长;顺铂通过与细胞核内DNA 的碱基结合,形成3 种形式的交联,造成DNA 损伤,破坏DNA 复制和转录;靶向药物吉非替尼塞主要作用于癌细胞S 期,而吉非替尼主要作用于癌细胞G0/G1期,可使细胞阻滞于G0~G1 期,从而发挥抗癌机制。临床对于肿瘤患者多采用联合用药治疗方式,减少不良反应,改善患者耐受,提高治疗效果[26-28]。
治疗组无进展生存率显著优于对照组(P<0.05),表明吉非替尼治疗能有效延缓晚期癌症患者的癌症恶化进展,表明吉非替尼是现代治疗晚期非小细胞肺癌患者的优选药物。
值得关注的是,治疗结局为部分缓解治疗组有15 例,显著高于对照组的8 例;但治疗结局为完全缓解治疗组为3 例、对照组为2 例,两组基本无差异。且治疗后治疗组患者躯体、心里、社会及总分,以及KPS 评分均显著高于对照组(P<0.05);结果表明,接受吉非替尼治疗的患者生活质量明显改善,可以非依赖自主生活;躯体、心理和社会评分都得到有效改善。总之,吉非替尼能有效改善携瘤生存状态,实体瘤体积明显缩小,可以改善患者携瘤生存时的生活质量、延长生存时间及提高患者的治疗信心。
综上所述,吉非替尼联合顺铂可有效治疗晚期非小细胞肺癌患者,能提高ORR、DCR,改善患者携瘤生活质量,提高无进展生存率,且无显著不良反应。
利益冲突所有作者均声明不存在利益冲突
