褪黑素对早发性卵巢功能不全的临床疗效及机制研究
2023-09-25王晓红
杨 婷, 王晓红, 李 怡
(中国人民解放军空军军医大学第二附属医院 妇产科, 陕西 西安, 710038)
早发性卵巢功能不全(POI)是指女性40岁之前由于卵巢中的卵泡破坏或耗尽而发生卵巢功能衰竭,可表现出一系列症状,例如月经紊乱和性欲减退[1-2]。当年龄小于40岁的女性出现停经或稀发月经4个月,且间隔4周连续2次卵泡刺激素(FSH)水平高于25 U/L, 即可诊断为POI[3]。POI发病机制复杂,可能与遗传因素、免疫疾病、医源性因素(放疗、化疗等)、不良生活习惯和特发性因素有关[4-5]。既往研究[6]显示, POI在普通女性人群中的发病率为1%~2%, 近年来呈上升趋势。褪黑素是一种主要由大脑松果体合成的神经激素,但生殖腺器官(如睾丸和卵巢)也能合成褪黑素[7]。研究[8]显示,褪黑素可以延缓卵巢衰老,调节卵巢生物节律,促进卵泡形成,提高卵细胞质量和受精率。作为卵巢卵泡中的自由基清除剂,褪黑素有助于卵母细胞成熟、胚胎发育和颗粒细胞黄体化[9-10]。本研究基于前瞻性随机对照研究方法探讨褪黑素对POI的临床疗效及其相关机制,现报告如下。
1 资料与方法
1.1 一般资料
选取2021年1月—2022年6月中国人民解放军空军军医大学第二附属医院妇科门诊收治的100例POI患者作为研究对象,POI的诊断参照2016年欧洲人类生殖和胚胎学学会发布的指南[3]。纳入标准: ① 首次诊断时年龄<40岁者; ② 月经过少或闭经至少4个月者; ③ 间隔4周以上的2次测量中,FSH>25 U/L者。排除标准: ① 已知或怀疑妊娠女性,哺乳期女性; ② 合并自身免疫性疾病者; ③ 合并慢性疾病(肾脏疾病、肝脏疾病、高血压病、充血性心力衰竭、脑血管或心血管疾病)者; ④ 患有乳腺癌或性激素依赖性恶性肿瘤者; ⑤ 先天性生殖器官发育异常者,治疗史包括卵巢切除术、子宫切除术、放疗、化疗等; ⑥ 正在接受可能影响月经周期或卵巢功能的药物治疗或针灸治疗等,或过去3个月内参加过可能影响生殖系统的其他临床试验者; ⑦ 对研究药物过敏者; ⑧ 抽烟或饮酒者。根据随机对照原则将入选患者分为对照组和试验组,每组50例。本研究经医院伦理委员会审核批准,所有患者已签署知情同意书。
1.2 治疗方法
对照组采用常规激素替代疗法: 患者于月经第5天(月经未来潮者于彩超监测子宫内膜厚度<5 mm时)开始口服戊酸雌二醇片(Bayer拜耳), 2 mg/d, 连续21 d, 并于服用戊酸雌二醇片的第12天时开始加服地屈孕酮片(Abbott雅培), 10 mg/d, 连续10 d。试验组在对照组治疗基础上联合应用褪黑素,患者每晚睡前口服褪黑素片(汤臣倍健), 2 mg/d。2组患者均连续用药3个月经周期,为1个疗程。
1.3 采血和血清性激素、氧化应激指标水平检测方法
治疗前的采血日为患者月经后2~4 d(自然月经周期或药物辅助月经来潮周期),治疗后的采血日要求子宫内膜厚度<5 mm, 卵泡直径<10 mm, 不符合要求者将被剔除。对照组有5例患者不符合要求被剔除,试验组有3例患者不符合要求被剔除。早晨9点前采集患者空腹肘部静脉血5 mL, 室温静置1 h或4 ℃过夜,之后将样品4 ℃下离心分离血清,通过罗氏自动化模块分析系统检测血清中FSH、黄体生成素(LH)、雌二醇(E2)和抗米勒管激素(AMH)的基础水平。若不能当天上机检测,血清应保存于-20 ℃(不超过30 d)或-80 ℃(不超过60 d)环境,禁止反复冻融。分别使用活性氧(ROS)检测试剂盒(化学荧光法)、总抗氧化能力(T-AOC)检测试剂盒(比色法)检测血清ROS、T-AOC水平,试剂盒均购自南京建成生物工程研究所,检测时严格按照说明书要求进行操作。
1.4 观察指标
① 主要观察指标: 治疗前和治疗1、3、6个月后血清FSH水平。② 次要观察指标: 治疗前和治疗1、3、6个月后血清LH、E2、AMH、ROS、T-AOC水平,月经改善情况。③ 安全性指标: 血常规、尿常规、肝肾功能,不良反应发生率。④ 月经改善情况: 治疗6个月后(从开始服药治疗时计算),对患者月经情况进行电话随访或当面沟通。参照既往研究[11]制订月经改善的评估标准: 无效,指月经量、持续时间、月经周期均无改善; 有效,指月经量、持续时间、月经周期有所改善; 显效,指月经量、持续时间基本正常,月经周期恢复正常; 痊愈,指月经量、持续时间、月经周期均正常。有效率=(有效+显效+痊愈)/总例数×100%。
1.5 统计学分析

2 结 果
2.1 基本资料比较
2组患者年龄、BMI、月经周期和生育要求比较,差异无统计学意义(P>0.05), 具有可比性,见表1。

表1 2组患者基线资料比较
2.2 治疗前后血清性激素水平比较
治疗前、治疗1个月后, 2组FSH、LH、E2、AMH 水平比较,差异无统计学意义(P<0.05); 治疗3、6个月后,试验组FSH水平低于对照组, E2和AMH水平高于对照组,差异有统计学意义(P<0.05); 治疗后, 2组患者FSH、LH、E2、AMH 水平均表现为时间依赖性改善,差异有统计学意义(P<0.05), 见表2。

表2 2组患者治疗前后性激素水平比较
2.3 治疗前后血清氧化应激指标水平比较
治疗3、6个月后,试验组ROS水平低于对照组,差异有统计学意义(P<0.05); 治疗1、3、6个月后,试验组T-AOC水平高于对照组,差异有统计学意义(P<0.05); 治疗后,试验组ROS、T-AOC水平均表现为时间依赖性改善,差异有统计学意义(P<0.05); 治疗后不同时点,对照组ROS、T-AOC水平比较,差异无统计学意义(P>0.05), 见表3。

表3 2组患者治疗前后血清氧化应激指标水平比较
2.4 治疗后月经改善情况比较
治疗6个月后,对照组、试验组患者月经改善有效率分别高达96.00%、98.00%, 差异无统计学意义(P>0.05), 见表4。
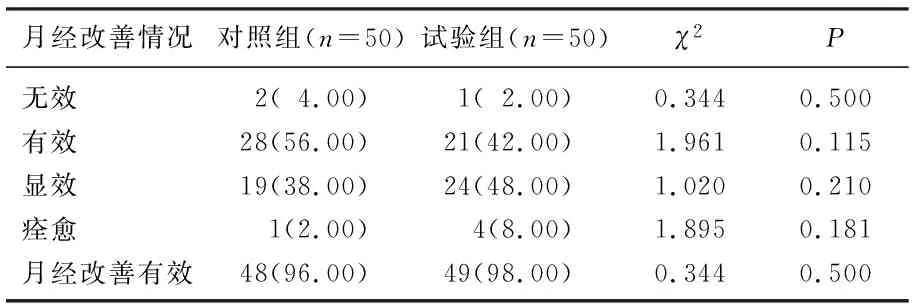
表4 2组患者治疗6个月后月经改善情况比较[n(%)]
2.5 安全性评价
与治疗前比较, 2组患者治疗6个月后的血常规、尿常规、肝肾功能检测结果均无明显改变。治疗过程中, 2例患者出现服药后乳房胀痛(对照组和试验组各1例),停药后症状均可逐渐缓解。2组不良反应发生率比较,差异无统计学意义(P>0.05)。
3 讨 论
POI是一种少见的妇科疾病,其特征是卵巢卵泡减少,激素分泌过多[2]。相关研究[12]称POI的患病率为0.9%~1.2%, 而瑞典一项全国性登记研究[13]显示POI的总患病率约为1.9%。一项荟萃分析[14]估计,全球有3.7%的女性受到该疾病的影响。POI患者往往伴随长期并发症,如骨质疏松、骨折、心血管疾病和抑郁[15]。POI是一种由遗传因素、自身免疫性疾病、线粒体异常、医源性因素(包括化疗、放疗、外科手术)和环境因素引起的异质性疾病[16], 且另有一些是特发性的,病因不明。长期以来,激素替代疗法均是POI的首选治疗方法,但并不能恢复卵巢功能,目前可选用的新治疗策略有体外激活、线粒体激活、干细胞和外泌体治疗等[17]。研究[18]发现, POI患者的ROS水平明显更高。ROS的过度产生可能会抑制细胞的抗氧化防御系统,导致氧化应激和线粒体功能障碍,进而诱发卵巢过早衰老[19]。
近年来,研究人员专注于应用药理学方法恢复线粒体的活力,目前可用的线粒体营养素包括辅酶Q10、白藜芦醇、褪黑素和雷帕霉素等[12]。褪黑素是一种针对线粒体的抗氧化剂,研究[20]表明,褪黑激素可通过增强抗氧化能力、维持端粒酶活性和激活sirtuin1而延迟小鼠的卵巢衰老。一项研究[21]探讨了褪黑素预处理的自体脂肪来源性干细胞在POI小鼠治疗中的优越性,发现褪黑素预处理组POI小鼠的血清激素水平和生殖功能明显恢复,原始卵泡平均计数增加,治疗效果更加显著。另有研究[22-23]显示,褪黑素可以激活PI3K/Akt/mTOR通路,进而抑制POI患者颗粒细胞的自噬作用,有效减轻卵巢损伤。此外,褪黑素以多种方式参与调控Hippo信号通路,并与卵巢功能恢复相关[10]。
本研究发现,激素替代疗法与褪黑素联合治疗3个月,可以有效改善POI患者的血清性激素水平和生殖功能, FSH水平显著降低, E2和AMH水平则显著升高,且治疗效果表现为时间依赖性改善。本研究还发现,激素替代疗法与褪黑素联合治疗3个月后患者血清ROS水平显著降低,治疗1个月后T-AOC水平显著升高,但对照组治疗前后ROS、T-AOC水平无显著差异,提示褪黑素治疗可以提升POI患者的抗氧化能力。本研究结果显示,治疗后, 2组患者月经情况均显著改善,且联合使用褪黑素对血常规、尿常规、肝肾功能均无显著影响,提示褪黑素治疗是安全的。
综上所述,激素替代疗法联合褪黑素治疗POI安全且有效,可降低患者氧化应激水平,改善血清性激素水平和月经情况,且不会增加不良反应发生风险。但本研究为单中心随机对照研究,观察时间有效,样本量较小,且未分析褪黑素治疗POI的具体分子机制,故未来还需开展多中心的大样本量临床试验进一步深入探讨。
